2014-11-16
Okresowość właściwości chemicznych
pierwiastków
Układ okresowy pierwiastków
1. Konfiguracje elektronowe pierwiastków
w
ó
ł
.G
3. Budowa układu okresowego
4. Historyczny rozwój układu okresowego
Okresowy charakter zmian właściwości pierwiastków wynika z
okresowych zmian w liczbie elektronów na ich zewnętrznych
(walencyjnych w sensie energetycznym a niekoniecznie według
rosnących liczb kwantowych) powłokach
M
,
a
k
z
d
5. Efektywna liczba atomowa
6. Elektroujemność
7. Właściwości pierwiastków a układ okresowy
3.1
e
t
i
l
o
P
a
k
Układ okresowy jest tablicą pierwiastków chemicznych, uszeregowanych
według wzrastających liczb atomowych, w której pierwiastki o podobnych
konfiguracjach elektronowych (i w rezultacie właściwościach chemicznych)
znajdują się w pionowych kolumnach
2. Konfiguracje a układ okresowy
a
k
i
n
Łó
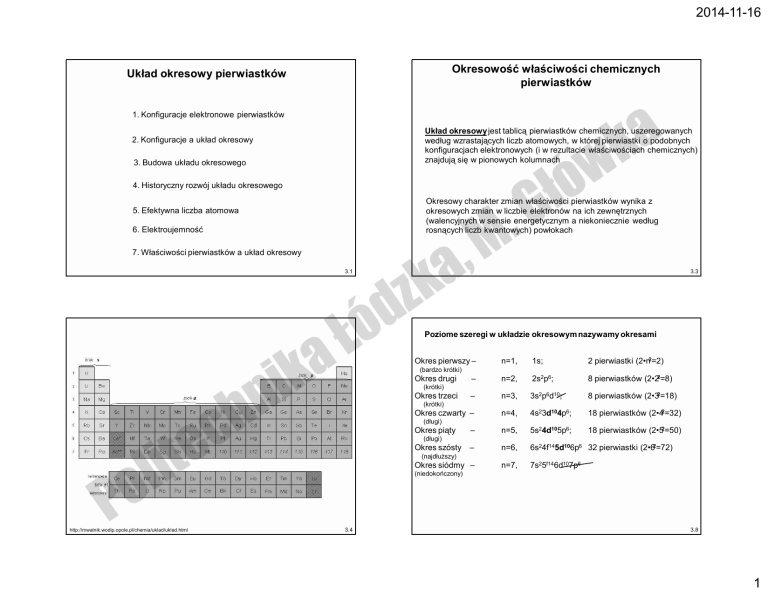
Poziome szeregi w układzie okresowym nazywamy okresami
n=1,
1s;
2 pierwiastki (2•n2=2)
–
n=2,
2s2p6;
8 pierwiastków (2•22=8)
–
n=3,
3s2p6d10;
8 pierwiastków (2•32=18)
Okres czwarty –
n=4,
4s23d104p6;
18 pierwiastków (2•42=32)
–
n=5,
5s24d105p6;
18 pierwiastków (2•52=50)
–
n=6,
6s24f145d106p6 32 pierwiastki (2•62=72)
Okres siódmy –
n=7,
7s25f146d107p6
Okres pierwszy –
(bardzo krótki)
Okres drugi
h
c
3.3
(krótki)
Okres trzeci
(krótki)
(długi)
Okres piąty
(długi)
Okres szósty
(najdłuższy)
(niedokończony)
3.4
3.8
http://mwalnik.wodip.opole.pl/chemia/uklad/uklad.html
1
2014-11-16
Okresowość właściwości fizycznych
Pionowe kolumny w układzie okresowym nazywamy grupami
Energia jonizacji energia potrzebna do oderwania 1 elektronu od atomu
Grupę (rodzinę) tworzą pierwiastki o analogicznych konfiguracjach
elektronowych na zewnętrznych powłokach
Pierwsza energia jonizacji
w
ó
ł
.G
Elektrony walencyjne – elektrony powłok zewnętrznych
Gdy atomy stykają się ze sobą, np. w reakcji, następuje oddziaływanie
między elektronami ich zewnętrznych powłok (elektronami walencyjnymi)
Dlatego właściwościchemiczne atomów zależą od liczby
i rozmieszczenia elektronów walencyjnych czyli ich konfiguracji
a
k
M
,
a
k
z
d
Czyli pierwiastki tej samej grupy mają podobne właściwościchemiczne
3.7
3.9
A. Korczyński „Repetytorium z chemii ogólnej i nieorganicznej”
a
k
i
n
Objętość atomowa
e
t
i
l
o
P
Łó
h
c
Początki układu okresowego
Prawa okresowości w chemii
Triady (Döbereiner -1816)
Mśr
MCa MBa
88,5
2
Ca
40
Mśr
127 35
81
2
Sr
88
Ba
137
Cl
Br
I
35
80
127
Prawo oktaw (Newlands – 1864)
Jeśli uszeregować pierwiastki wg rosnących ciężarów atomowych,
co ósmy pierwiastek ma podobne właściwości
3.10
Na(9)
K(17)
a) Nie znano wszystkich pierwiastków
C(5)
Si(12)
b) Nie umiano wyznaczać mas (ciężarów)
tylko równoważniki chemiczne
3.11
A. Bielański „Chemia ogólna i nieorganiczna”
2
2014-11-16
Układ okresowy według Mendelejewa (1869)
Prawo okresowości (Mendelejew – 1869
Meyer – 1870)
Właściwości chemiczne i fizyczne zmieniają
okresowo w miarę wzrostu ciężarów atomowych
się
w
ó
ł
.G
Helowce nieznane do 1892 roku (Argon– Ramsay),
hel w widmie Słońca 1868
H
Li
Be
B
C
N
O
F
Na
Mg
Al
Si
P
S
Cl
V
a
k
http://www.meta-synthesis.com/
K
Ca
ekabor
Ti
Cu
Zn
ekaglin
ekakrzem As
ekaglin 1875 (Ga – Lecoq de Boisbaudran)
ekabor 1881 (Sc – Nilsson)
ekakrzem 1875 (Ge – Winkler)
Cr
Mn
Se
Br
Fe
Co
M
,
a
k
z
d
Ni
- Ga
- Sc
- Ge
3.13
a
k
i
n
Zalety i wady układu okresowego
(Mendelejewa)
Zalety:
- ujawnienie podobieństw (Cd i Hg, Sn i Pb, B i Al)
Łó
h
c
e
t
i
l
o
- przewidywanie istnienia pierwiastków jeszcze nieznanych
Wady:
-…
- łączenie pierwiastków grup głównych i pobocznych
P
Właściwości pierwiastków
Atomowe (swoiste):
Zależą od budowy atomów
- Masa atomowa
- Promień atomu
- Ładunek jądra
- Energia jonizacji
- Powinowactwo elektronowe
- Elektroujemność
- Podatność magnetyczna
- prawidłowe określenie ciężarów atomowych
np. uważano Be za trójwartościowy (BeCl3)
równoważniki Be 4,5x3=13,5 ??
4,5x2=9 (BeCl2)
- 3 pierwiastki w VII grupie
- nie wiadomo co zrobić z lantanowcamii aktynowcami
3.14
Zespołowe (koligatywne):
Zależą od sposobu powiązania
atomów i oddziaływań między nimi
- Gęstość
- Stan skupienia
- Temperatura topnienia
- Temperatura wrzenia
- Współczynnik załamania światła
- Przewodnictwo cieplne
- Przewodnictwo elektryczne
- Objętość molowa
- Barwa
- Ciepło właściwe
-…
- wartościowośćCu i Au nie odpowiadały numerowi grupy
- kolejność pierwiastków niezgodna z ciężarami (Ar i K, Co i Ni, Te i I)
3.14
3.15
3
2014-11-16
Energia jonizacji
Energia anionizacji –
energia potrzebna do utworzenia anionu
(energia przyłączenie elektronu– może
być ujemna i dodatnia)
1
Energia powinowactwa elektronowego–
energia uwalniana (dla nas dodatnia) podczas przyłączania
dodatkowego elektronu do atomu, z którego powstaje anion
A + 1eAH-
Jon
Energia 71
anioniz.
F-
Cl-
Br-
I-
O-
OH-
333
350
330
300
140
175
O2-
S2-
1
H
1310
2
Li
519
Be
900
3
Na
494
Mg
736
4
K
418
Ca
590
[kJ/mol]
Energia jonizacji (kationizacji) –
- pierwsza energia jonizacji
M M 2 1e
- druga energia jonizacji
3.16
Atom
1
2
He
2370
5250
Ne
2080
3952
3
4
a
k
i
n
Ar
Li
519
7298
Na
494
4562
K
418
3051
Be
900
1757
Mg
736
1451
Ca
590
1145
B
799
2430
Al
577
1817
Ga
577
1979
Si
786
1577
Ge
784
1557
C
o
P
e
t
li
N
1400
2856
P
1011
1903
As
947
1798
O
1310
3388
S
1000
2251
Se
941
2044
F
1680
3374
Cl
1255
2297
Br
1140
2104
h
c
4910
3660
2744
2963
13
Łó
5
Rb
402
Sr
548
6
Cs
376
Ba
502
14
15
B
799
C
1090
Al
577
Si
786
Ga
577
N
1400
a
k
16
w
ó
ł
.G
M
,
a
k
z
d
energia potrzebna do odebrania
elektronu najsłabiej związanego
M M 1e
2
17
18
He
2370
O
1310
F
1680
Ne
2080
P
1011
S
1000
Cl
1255
Ar
1520
Ge
784
As
947
Se
941
Br
1140
Kr
1350
In
556
Sn
707
Sb
834
Te
870
I
1008
Xe
1170
Tl
590
Pb
716
Bi
812
Po
812
At
1037
Rn
1036
3.18
Energia jonizacji zależy od:
–
–
–
–
–
Promienia atomu (wielkości powłoki walencyjnej),
Ładunku atomu (0) lub jonu (+ lub-)
Efektywnej liczby atomowej
Typu orbitalu walencyjnego, z którego usuwamy elektron (energii orbitalu)
Liczby elektronów na orbitalu walencyjnym, z którego usuwany jest elektron
25000
3302
2912
3.19
3.20
A. Korczyński „Repetytorium z chemii ogólnej i nieorganicznej”
4
2014-11-16
Efektywna liczba atomowa. Efekt ekranowania
Efektywna liczba atomowa. Efekt ekranowania
–0,35 dla każdego elektronus i p na powłoce n (dla 1s tylko -0,3)
Z 2 me e 4
Energia elektronu E
2
8 o h 2 n 2
–0,85 dla każdego z elektronów na powłoce (n
-1)
Z - liczba atomowa
a
k
–1,0 dla każdego z elektronów n
-2 lub jeszcze bliżej jądra
w
ó
ł
.G
Każdy elektron jestnie tylko przyciągany przez jądro ale teżodpychany
przez elektrony, zwłaszcza powłok wewnętrznych w stosunku do niego
Przykład:
Ekranowanie dla elektronów walencyjnych tlenu
-0,35x5=-1,75
-0,85x2=-1,70
-3,45
Efektywna liczba atomowa jestmniejsza od liczby protonów w jądrze, co
wynika z ekranowania (osłabiania) oddziaływania elektronów
walencyjnych z jądrem przez inne elektrony.
Ekranowanie (zmniejszanie liczby atomowej) wynosi dla elektronów s i p:
M
,
a
k
z
d
Efektywna liczba atomowa tlenu wynosi:
–0,35 dla każdego elektronus i p na rozpatrywanej powłocen
(dla 1s tylko -0,3)
–0,85 dla każdego z elektronów na powłocen-1)
(
–1,0 dla każdego z elektronów powłokin-2 lub jeszcze bliżej jądra
3.21
a
k
i
n
Elektroujemność (X)
Gdy myślimy ogólnie o charakterze (właściwości) atomu:
Zdolność przyciągania elektronów w wiązaniu kowalencyjnym
Zdolność atomu do przyciągania elektronów
Łó
h
c
o
P
8,00
-3,45
4,55
3.22
Elektroujemność (X)
Skala Paulinga – dobrana tak, aby różnica elektroujemnościatomów
tworzących wiązanie była równa momentowi
dipolowemu wiązania (w debajach)
Skala Millikena – elektroujemność pierwiastka jest wprost proporcjonalna
do sumy jego powinowactwa elektronowego i
energii pierwszej jonizacji.
Duża elektroujemność, gdy obie energie duże
Gd y chcemy określić ją liczbowo:
Miara przyciągania elektronów przez dany atom
Miara dążenia atomu w związku chemicznym do przyciągania
do siebie elektronów
Miara tendencji atomu znajdującego się w cząsteczce do
przyciągania ku sobie elektronów
e
t
li
1s22s2p4
Skala Allreda i Rochowa- elektroujemność jest miara sił, z jaką jądro
o ładunku Ze działa na elektrony walencyjne
X 0,359
Z S
0,744
r2
S – stała ekranowania (Z-S=Ze), r – promień atomu
Standardowa elektroujemność wynosi około 2,2 dla wodoru
we wszystkich trzech skalach.
3.23
3.24
5
2014-11-16
Elektroujemność w układzie okresowym
Porównanie skal elektroujemności
Atom
P
M
AR
F
3,98
3,90
4,10
O
3,44
3,04
3,50
N
3,04
2,28
3,07
Cl
3,16
2,95
2,83
Br
2,96
2,62
2,74
C
2,55
1,75
2,50
Se
2,55
2,18
2,48
S
2,58
2,28
2,44
I
2,66
2,52
2,21
As
2,18
1,59
2,20
H
2,20
2,21
2,20
P
2,19
1,84
2,06
B
2,04
1,81
2,01
Si
1,90
2,25
1,74
Al
1,61
1,64
1,47
Be
1,57
1,40
1,47
Mg
1,31
1,17
1,23
Ca
1,00
0,99
1,04
Na
0,93
0,74
1,01
Li
0,98
0,84
0,97
Rb
0,82
0,50
0,89
w
ó
ł
.G
M
,
a
k
z
d
3.25
a
k
3.26
http://pl.wikipedia.org/wiki/Elektroujemno%C5%9B%C4%87
Fr
0,7
-
0,86
a
k
i
n
Wielkość atomów (Promienie atomowe)
Czy można wyznaczyć wielkość atomu doświadczalnie?
•Czy jest to możliwe dla izolowanegoatomu?
•W jakim stanie skupienia to zrobić?
Łó
Wielkość atomów bloku s i p
h
c
Promień atomowy (kowalencyjny)
- połowa długości wiązania kowalencyjnegoniespolaryzowanego
e
t
i
l
o
Promień jonowy
- zależy od liczby koordynacyjnej i stopnia utlenienia
- można wyznaczyć sumę dwu promieni jonowych
Promień metaliczny
- połowa odległości międzyjądrowej stykających się atomów
w krysztale danego metalu
P
Promień van der Waalsa
-połowa odległości międzyjądrowej dla dwu jednakowych
atomów nie związanych ze sobą
3.27
3.28
http://intro.chem.okstate.edu/1314F00/Lecture/Chapter7/Lec111300.html
6
2014-11-16
Wielkość atomów i jonów
Wielkość atomów i jonów
1. Promienie atomowe i jonowe [podano wartości w
Å]
pierwiastków tej samej grupy rosną wraz z numerem okresu
Li+
0,70
Na+
0,98
F
0,58
Cl
0,99
0,28
Cl-
1,81
1,33
Br
1,49
0,15
1,14
Br-
1,96
I-
2,20
0,19
I
w
ó
ł
.G
3. Promienie kationów [w Å] izoelektronowychmaleją
ze wzrostem ładunku
Na+ Mg2+ Al3+
Si4+
P5+
S6+
Cl7+
0,98 0,78 0,57
0,39
0,35
0,34
0,26
0,48
0,15
0,16
Rb+
1,33
0,41
0,35
K+
F-
0,24
1,33
M
,
a
k
z
d
4. Aniony są na ogół większe niż kationy,
np. przy tej samej liczbie elektronów.
N3O2FNe
Na+
Mg2+ Al3+
1,71
1,32
1,33
1,60
0,98
0,78
0,57
v.d.W.
0,21
Cs+
1,70
3.29
a
k
i
n
Wielkość atomów i jonów
5. Promienie van der Waalsa a promienie atomowe
Atom
Promień
atomowy [Å]
H
0,31
N
0,70
O
0,66
S
F
Cl
He
o
P
Ne
Ar
a
k
2. Promienie atomowe [w Å] pierwiastków tego samego okresu maleją
w miarę wzrostu liczby atomowej
B
C
N
O
F
Ne
0,88 0,77 0,70 0,66 0,64
0,70
e
t
li
1,04
0,64
0,99
-
Promień van
der Waalsa [Å]
h
c
1,20
1,50
1,40
1,85
1,35
1,80
Δ
Łó
Wielkość atomów i jonów
6. Kationy pierwiastków leżących na przekątnej
(z lewego rogu w dół na prawo)
mają zbliżone promienie jonowe
0,89
0,80
0,74
0,81
Li+
Na+
1,60
-
1,91
K+
0,71
Mg2+
Ca2+
Sr2+
0,81
Sc3+
0,93
-
3.30
0,70
3.31
0,78
0,83
Y3+
0,98
1,06
1,06
La3+
1,33
1,27
1,22
3.31
7
2014-11-16
Pytania i tematy egzaminacyjne
1. Dlaczego miejsce pierwiastka w układzie okresowym decyduje
o jego właściwościach?
2. Wyjaśnij brak monotoniczności zmian właściwości fizycznych
atomów (np. objętości atomowej i energii jonizacji) w okresach
3. Wymień główne zalety i wady układu okresowego pierwiastków
w wersji zaproponowanej przez Mendelejewa
4. Od czego zależy i o czym decyduje wielkość energii jonizacji?
5. Co to jest efektywna liczba atomowa?
6. Jak się określa elektroujemność i do czego ona służy?
7. Dlaczego elektroujemność na ogółmaleje dla kolejnych
pierwiastków danej grupy układu okresowego arośnie dla
kolejnych pierwiastków bloków s i p w danym okresie?
8. Od czego zależy wielkość atomów i jak się zmienia w grupach
(rodzinach) i okresach?
e
t
i
l
o
w
ó
ł
.G
a
k
M
,
a
k
z
d
ó
Ł
a
k
i
n
h
c
P
8











