Znak postępowania: ZP/PN-33/13
Załącznik nr 3 do SIWZ
(wzór)
po zmianach z dnia 01.08.2013 r.
Specyfikacja oferowanego przedmiotu zamówienia
Część 1 – sukcesywne dostawy zestawów do redukcji wirusów w jednej jednostce osocza
uzyskanego w krwi pełnej
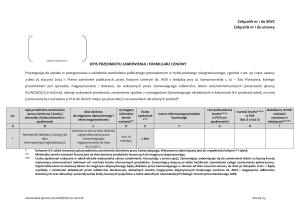
1) Zestawy do redukcji wirusów w jednej jednostce osocza uzyskanego w krwi pełnej:
Lp.
1.
2.
3.
4.
5.
6.
7.
8.
9.
Wymagania minimalne Zamawiającego
Zestawy do redukcji wirusów w osoczu
przeznaczonym
do
użytku
klinicznego
otrzymywanym z krwi pełnej muszą być jałowe,
apirogenne
Zestawy muszą zapewnić redukcję wirusów
w jednej (1) jednostce osocza z krwi pełnej
w przedziale objętości od 240 ml do 310 ml
i cechować się skutecznością redukcji wirusów
do poziomu bezpiecznego
Zestawy muszą umożliwiać redukcję wirusów w
osoczu przed jego szokowym zamrażaniem jak i
osocza świeżo mrożonego tuż po rozmrożeniu
a bezpośrednio przed wydaniem
W przypadku, gdy tego wymaga metoda,
zestawy winne posiadać skuteczny system
oczyszczania osocza z dodawanego w danej
procedurze czynnika fotouczulającego, należy
usunąć nie mniej niż 90% wartości początkowej
substancji fotouczulającej
Pojemnik do przechowywania osocza po
redukcji
wirusów
powinien
zapewniać
możliwość
zamrażania
szokowego
w
temperaturze, minimum (-)60 °C i bezpiecznego
przechowywania osocza w temperaturze poniżej
(-)25 °C z zachowaniem jałowości pojemnika
Zestawy muszą gwarantować małe straty
objętości osocza (max do 15%), utrzymanie
klinicznej skuteczności FFP – średnie stężenie
białka całkowitego – nie mniej niż niż 50 g/l
oraz średnia zawartość czynnika VIII – nie
mniej niż 70 IU w 100 ml
Średnica drenów zestawu powinna mieć
wymiary
zapewniające
wzajemną
kompatybilność drenów zestawu i różnych
pojemników do pobierania i preparatyki krwi,
aby umożliwić ich połączenia w układzie
otwartym i zamkniętym
Wszystkie dreny muszą być elastyczne,
umożliwiające łatwe rolowanie i skuteczne
wykonywanie zgrzewów
Materiał pojemników zestawów musi być
przejrzysty, umożliwiający wizualną ocenę
pojemnika i składnika znajdującego się w
pojemniku
Charakterystyka
proponowanego przez
Wykonawcę wyrobu
Uwagi
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
zaoferowane zestawy nie
wymagają oczyszczani osocza
*) / zaoferowane zestawy
wymagają oczyszczania
osocza, a zastosowana metoda
usuwa .... % wartości
początkowej substancji
fotouczulającej *)
zamrażanie
szokowe
w
temperaturze, min. - … °C
bezpieczne przechowywanie
osocza w temperaturze poniżej
-… °C z zachowaniem
jałowości pojemnika
średnie
stężenie
białka
całkowitego – nie mniej niż
niż
…
g/l
średnia zawartość czynnika
VIII – nie mniej niż … IU w
100 ml
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
1
Znak postępowania: ZP/PN-33/13
10.
11.
12.
13.
14.
15.
16.
17.
Na pojemniku do przechowywania osocza po
redukcji wirusów musi być trwale umocowana
etykieta, która nie może ulegać uszkodzeniom
ani odklejeniu w czasie preparatyki i
przechowywania oraz, której nie może zerwać
użytkownik. Etykieta robocza winna mieć
odpowiednie
wymiary
umożliwiające
przyklejanie na nich etykiety głównej zgodnej z
wymaganiami ISBT
Etykieta macierzysta pojemnika na osocze
redukowane musi posiadać znak CE oraz
zawierać następujące dane:
1) nazwę firmy i nazwę pojemnika w postaci
numeru referencyjnego
2) miejsce na datę i numer donacji
3) numer serii w postaci literowo-cyfrowej i
kodu kreskowego
4) datę ważności
Pojemniki na osocze redukowane winne
zawierać co najmniej 2 porty zabezpieczone
wewnątrz oraz odpowiednią ochroną z zewnątrz
zapewniającą jałowość, umożliwiające łatwy
dostęp do podłączenia zestawu do przetoczenia
Na dolnej krawędzi pojemnika na osocze
redukowane, centralnie, winno znajdowac się
podłużne nacięcie materiału pojemnika o
długości
około
2
cm,
umożliwiajace
zawieszanie
pojemników
na
haczykach
statywów transfuzyjnych
W odpowiednich pojemnika lub drenach
zestawu winne znajdować się kominy z łatwo
łamiącą się w czasie preparatyki membraną tak,
aby osocze w trakcie kolejnych etapów
związanych z redukcja wirusów znajdowało się
we właściwym pojemniku
Zestawy do redukcji wirusów muszą być
zamknięte w indywidualnych opakowaniach
zabezpieczających, w jednym opakowaniu
mogą być zabezpieczone maksymalnie dwa
zestawy do redukcji wirusów. Po zużyciu
jednego z nich drugi może być wykorzystany w
ciągu 7 dni. Opakowanie zabezpieczające
zapewnia odpowiednią wilgotność w czasie
przechowywania. Zestawy w opakowaniach
zabezpieczających muszą być zapakowane w
odporne na uszkodzenia zbiorcze opakowania
kartonowe. Jedne opakowanie zbiorcze może
zawierać zestawy tylko jednej serii
termin ważności min. 12 miesięcy od daty
dostawy do Zamawiającego.
zestawy winny współpracować z posiadanymi
przez Zamawiającego dwoma iluminatorami
Mirasol BCT z prawidłową transmisją danych
do systemu informatycznego posiadanego przez
Zamawiającego IBS 32, które umożliwiają
łącznie redukcję minimum sześciu jednostek
osocza w ciągu 1 godziny oraz redukują wirusy
w pojedynczych jednostkach osocza uzyskanych
z 450 ml krwi pełnej
lub
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
…
porty
wewnątrz
zabezpieczone
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
termin ważności (w
miesiącach) .............
zestawy do posiadanych przez
Zamawiającego iluminatorów
Mirasol BCT * ) /
zestawy wraz z dzierżawą
urządzeń i prawidłową
transmisją danych do systemu
informatycznego posiadanego
przez Zamawiającego IBS 32,
w ilości zapewniającej łącznie
redukcję minimum sześciu
jednostek osocza w ciągu 1
2
Znak postępowania: ZP/PN-33/13
zestawy wraz z dzierżawą urządzeń i
prawidłową transmisją danych do systemu
informatycznego wykorzystywanego przez
Zamawiającego IBS 32, w ilości zapewniającej
łącznie redukcję minimum sześciu jednostek
osocza w ciągu 1 godziny oraz redukcję
wirusów w pojedynczych jednostkach osocza
uzyskanych z 450 ml krwi pełnej
*)
godziny oraz redukcję
wirusów w pojedynczych
jednostkach osocza
uzyskanych z 450 ml krwi
pełnej * )
- niepotrzebne skreślić
2) Dzierżawa urządzenia przeznaczonego do obsługiwanych zestawów do redukcji osocza
uzyskanego z krwi pełnej **:
Lp.
1.
2.
Wymagania minimalne Zamawiającego
Charakterystyka
proponowanego przez
Wykonawcę wyrobu
Urządzenie (aparatura) przeznaczone do
obsługi zamawianych zestawów do redukcji
wirusów w osoczu ma zapewniać pełną kontrolę
przebiegu procesu dla każdej jednostki osocza,
pełną identyfikację każdej jednostki osocza oraz
zapewnić
zbieranie,
analizowanie
i
archiwizowanie informacji dotyczącej procesu
redukcji
TAK / NIE * )
Zaoferowana ilość urządzeń winna zapewniać
prawidłową transmisją danych do systemu
informatycznego wykorzystywanego przez
Zamawiającego IBS 32 oraz łącznie redukcję
minimum sześciu jednostek osocza w ciągu 1
godziny
Urządzenie musi zapewniać skuteczną redukcję
wirusów w pojedynczych jednostkach osocza,
uzyskanych z 450 ml krwi pełnej
Urządzenie musi zapewniać przekazywanie
4.
danych do posiadanego przez RCKiK systemu
informatycznego IBS 32
Urządzenie musi posiadać system drukowania
5.
etykiety roboczej wskazującej na poprawnie
wykonaną redukcję wirusów
W przypadku awarii urządzenia Wykonawca
6.
udostępni urządzenie zastępcze w terminie
24 godzin od zgłoszenia awarii
*)
- niepotrzebne skreślić
3.
TAK / NIE * )
Uwagi
Oferujemy ...... szt. urządzeń
zapewniających prawidłową
transmisją danych do systemu
informatycznego
wykorzystywanego przez
Zamawiającego IBS 32 oraz
łącznie redukcję minimum
sześć jednostek osocza w ciągu
1 godziny
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
** Wykonawca oferuje dzierżawę urządzeń w przypadku zaoferowania zestawów, które nie są kompatybilne z systemem
redukcji wirusów Mirasol BCT
………………………………………
/Miejscowość i data/
………………………………………………………………….........…………
/Podpis osoby/osób upoważnionej do występowania w imieniu wykonawcy/
(pożądany czytelny podpis albo podpis i pieczątka z imieniem i nazwiskiem)
3
Znak postępowania: ZP/PN-33/13
Część 2 – Sukcesywna dostawa zestawów do pobierania dwóch jednostek KKCz na separatorze
komórkowym MCS+ Haemonetics oraz płynów CPD i SAGM
1. Zestawy do pobierania dwóch jednostek KKCz na separatorze komórkowym MCS+
Haemonetics:
Charakterystyka
proponowanego przez
Wykonawcę wyrobu
Uwagi
1.
Zestawy jednorazowego użytku do pobierania
dwóch jednostek KKCz na separatorze
komórkowym MCS+ Haemonetics winne być
być wyposażone w:
1) Igłę 16 G, poddaną obróbce zwiększającej
poślizg
2) Pojemnik
próbkowy,
umożliwiający
pobieranie krwi z pierwszej porcji krwi
przed donacją o pojemności min. 30 ml
3) Port typu Luer żeński, umożliwiający
podłączenie płynu antykoagulacyjnego CPD
4) Port typu Luer męski, umożliwiający
podłączenie płynu wzbogacającego SAGM
5) Coupler – przebijak do podłączenia płynu
kompensującego objętość krwi krążącej –
0,9% NaCl
TAK / NIE * )
2) Pojemnik próbkowy,
umożliwiający pobieranie krwi
z pierwszej porcji krwi przed
donacją o pojemności ..............
ml
2.
Termin ważności uzyskanych KKCz winien
wynosić 42 dni
TAK / NIE * )
…. dni
Lp.
3.
4.
5.
6.
Wymagania minimalne Zamawiającego
Każdy zestaw musi być zamknięty w
indywidualnym opakowaniu zabezpieczającym,
zapewniającym odpowiednią wilgotność w
czasie przechowywania.
Pojedyncze zestawy muszą być zapakowane w
odporne na uszkodzenia, oznakowane (nazwa,
symbol, numer serii zestawów, nazwę i adres
producenta,
informacja
o
warunkach
przechowywania) opakowanie zbiorcze. Jedno
opakowanie zbiorcze może zawierać zestawy
tylko jednej serii.
Na pojemnikach do przechowywania KKCz/
RW Af muszą być trwale umocowane etykiety,
które nie mogą ulegać uszkodzeniom ani
odklejeniu
w
czasie
preparatyki
i
przechowywania. Etykieta robocza winna mieć
odpowiednie
wymiary
umożliwiające
przyklejenie na niej etykiety głównej zgodnej z
wymaganiami ISBT
Etykieta macierzysta musi posiadać znak CE
oraz kody odpowiadające standardom ISBT 128
(EAN 128). Etykiety muszą zawierać
następujące dane:
1) nazwę i adres producenta
2) numer serii w postaci literowo- cyfrowej
i kodu kreskowego
3) datę ważności zestawu w postaci
literowo- cyfrowej lub kodu kreskowego
Pojemniki do przechowywania KKCz/ RW Af
powinny zawierać co najmniej 2 porty,
zabezpieczone membraną od wewnątrz oraz
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
TAK / NIE * )
4
Znak postępowania: ZP/PN-33/13
odpowiednią ochroną z zewnątrz zapewniającą
jałowość, umożliwiające łatwy dostęp do
podłączenia zestawu do przetoczenia
Centralnie na dolnej krawędzi pojemników do
przechowywania KKCz/ RW Af, powinno
znajdować się podłużne nacięcie materiału
pojemnika o długości około 2 cm,
umożliwiające zawieszanie pojemników na
haczykach statywów transfuzyjnych
termin ważności min. 24 miesiące od daty
dostawy do Zamawiającego
7.
8.
*)
TAK / NIE * )
TAK / NIE * )
termin ważności (w
miesiącach) .............
- niepotrzebne skreślić
2. Płyn antykoagulacyjny CPD50:
Lp.
Pakowany po 150 ml w plastikowym worku z
poretm typu Luer męski i blokadą wypływu
termin ważności min. 12 miesięcy od daty
dostawy do Zamawiającego
1.
2.
*)
Wymagania minimalne Zamawiającego
Charakterystyka
proponowanego przez
Wykonawcę wyrobu
Uwagi
TAK / NIE * )
pakowany po …. ml
TAK / NIE * )
termin ważności (w
miesiącach) .............
- niepotrzebne skreślić
3. Płyn wzbogacający SAGM:
Lp.
1.
2.
*)
Wymagania minimalne Zamawiającego
Pakowany po 350 ml w plastikowym worku z
poretm typu Luer żeński i blokadą wypływu
termin ważności min. 12 miesięcy od daty
dostawy do Zamawiającego
Charakterystyka
proponowanego przez
Wykonawcę wyrobu
Uwagi
TAK / NIE * )
pakowany po …. ml
TAK / NIE * )
termin ważności (w
miesiącach) .............
- niepotrzebne skreślić
………………………………………
/miejscowość i data/
………………………………………………………………….........…………
/podpis osoby/osób upoważnionej do występowania w imieniu wykonawcy/
(pożądany czytelny podpis albo podpis i pieczątka z imieniem i nazwiskiem)
5