AMINOKWASY
1. Wielofunkcyjne pochodne węglowodorów
związki, których cząsteczki zawierają co najmniej dwie grupy funkcyjne połączone z
grupą węglowodorową
grupy funkcyjne mają wpływ na właściwości chemiczne i fizyczne związków, w których
skład wchodzą
grupy funkcyjne mogą wzajemnie na siebie oddziaływać
2. Aminokwasy należą do wielofunkcyjnych pochodnych węglowodorów
Zawierają dwie grupy funkcyjne:
Karboksylową: –COOH
Aminową: –NH2
Aminokwasy występują w roztworze w jednej z trzech postaci: jonu obojnaczego,
formy kwasowej (anionowej) lub formy zasadowej (kationowej).
To, która z form dominuje, zależy od pH roztworu.
3. Wzór ogólny aminokwasów:
4. Przykłady aminokwasów:
W nazewnictwie zwyczajowym atomy węgla w łańcuchu głównym oznacza się
kolejnymi literami alfabetu greckiego (α, β ....) zaczynając od atomu węgla położonego
najbliżej grupy karboksylowej
5. Najprostszy aminokwas to glicyna – kwas aminooctowy
Substancja stała, tworzy kryształy, dobrze rozpuszcza się w wodzie, ma odczyn obojętny
Obecne w cząsteczce glicyny grupy: aminowa i karboksylowa ulegają w roztworze
wodnym wzajemnemu zobojętnianiu wskutek przeniesienia kationu H + z grupy
karboksylowej –COOH do grupy aminowej –NH2.
Powstaje wówczas sól wewnętrzna czyli tzw. jon obojnaczy
Jon obojnaczy powstaje tylko przy określonej wartości pH, wartość ta nazywana
jest punktem izoelektrycznym lub punktem izojonowym.
W roztworze wodnym glicyny ustala się stan równowagi, w którym istnieją
trzy formy jonowe:
W środowisku silnie kwasowym równowaga reakcji przesuwa się w kierunku
tworzenia kationów,
W środowisku silnie zasadowym – w kierunku tworzenia się anionów.
Na tym polega amfoteryczność aminokwasów.
Glicyna jest związkiem amfoterycznym – reaguje z kwasami jak i z zasadami
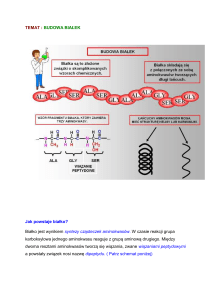
6. Wiązanie peptydowe:
Jest to wiązanie charakterystyczne dla peptydów oraz białek
Wiązanie to powstaje w wyniku połączenia grupy karboksylowej jednego
aminokwasu z grupą aminową drugiego aminokwasu
Tworzenie peptydów jest przykładem reakcji polikondensacji ponieważ podczas
reakcji wydziela się produkt uboczny – woda.
Kolejność uszeregowania aminokwasów w łańcuchu peptydowym nazywa się
sekwencją aminokwasów
7. Aminokwasy białkowe
Wchodzą w skład białek naturalnych
Organizm ludzki może samodzielnie syntetyzować jedynie część spośród 20
niezbędnych aminokwasów – są to aminokwasy endogenne. Pozostałe
aminokwasy muszą być dostarczane do organizmu w postaci gotowej – są to
aminokwasy egzogenne.
Aminokwasy, oprócz glicyny, mogą tworzyć izomery optyczne typu L lub D
We wszystkich współczesnych organizmach białkowych występują
aminokwasy
Ze względu na liczbę reszt aminokwasów peptydy dzielimy na:
L–
PRZYKŁADY α AMINOKWASÓW:
Wśród aminokwasów białkowych tylko dwa: treonina i izoleucyna zawierają dwa chiralne atomy węgla