Aminokwasy, peptydy, białka
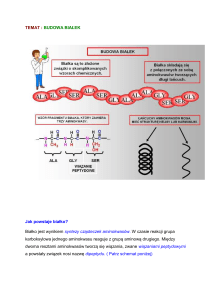
Aminokwasy
KWAS 1-AMINOCYKLOPROPANOKARBOKSYLOWY
α AMINOKWAS
KWAS 3-AMINOPROPANOWY
β AMINOKWAS
KWAS 4-AMINOPROPANOWY
γ AMINOKWAS
KWAS 2-AMINOETANOSULFONOWY
β AMINOKWAS
Aminokwasy
Ponad 700 aminokwasów zidentyfikowanych w przyrodzie.
Większość z nich to α aminokwasy.
20 aminokwasów (19 α-aminokwasów i jeden α-iminokwas) buduje białka.
Aminokwasy
WSZYSTKIE AMINOKWASY BIAŁKOWE TO α AMINOKWASY
AMINOKWASY BIAŁKOWE, Z WYJĄTKIEM GLICYNY, NALEŻĄ DO SZEREGU KONFIGURACYJNEGO L
Aminokwasy
AMINOKWASY BIAŁKOWE, Z WYJĄTKIEM GLICYNY, NALEŻĄ DO SZEREGU KONFIGURACYJNEGO L
D-AMINOKWAS
ALDEHYD D-GLICERYNOWY
L-AMINOKWAS
ALDEHYD L-GLICERYNOWY
Aminokwasy
WSZYSTKIE AMINOKWASY BIAŁKOWE TO α AMINOKWASY
GLICYNA
AMINOKWAS
CHIRALNY
AMINOKWAS
ACHIRALNY (PROJEKCJA FOSCHERA)
Charakter kwasowo-zasadowy aminokwasów
OHR
COOH
R
NH2
H3O+
R
H2N
R
H3N
C
C
R
COO
R
NH3
H
COOH
H3O+
H
OH-
OH-
COOH
H3O+
R
H3N
C
H
COO
H2N
R
C
H
COO
Charakter kwasowo-zasadowy aminokwasów
Charakter kwasowo-zasadowy aminokwasów
FORMY ZJONIZOWANIA AMINOKWASÓW W ZALEŻNOŚCI OD pH ROZTWORU
KATION
KATION
JON OBOJNACZY
ANION
DWA ŁADUNKI
DODATNIE
DWA ŁADUNKI
DODATNIE
I ŁADUNEK UJEMNY
ŁADUNEK
DODATNI
I ŁADUNEK UJEMNY
ŁADUNEK
UJEMNY
Charakter kwasowo-zasadowy aminokwasów
MIARECZKOWANIE AMINOKWASÓW OBOJĘTNYCH
JON OBOJNACZY
PUNKT IZOELEKTRYCZNY (pI) – WARTOŚĆ pH PRZY KTÓREJ AMINOKWAS WYSTĘPUJE
W POSTACI JONU OBOJNACZEGO
PUNKT IZOELEKTRYCZNY DLA AMINOKWASÓW OBOJĘTNYCH – OKOŁO 6
PUNKT IZOELEKTRYCZNY DLA AMINOKWASÓW ZASADOWYCH – OKOŁO 10
PUNKT IZOELEKTRYCZNY DLA AMINOKWASÓW KWAŚNYCH – OKOŁO 3
Charakter kwasowo-zasadowy aminokwasów
PUNKT IZOELEKTRYCZNY (pI) – WARTOŚĆ pH PRZY KTÓREJ AMINOKWAS WYSTĘPUJE
W POSTACI JONU OBOJNACZEGO
OBLICZENIE pI DLA AMINOKWASÓW OBOJĘTNYCH
Charakter kwasowo-zasadowy aminokwasów
PUNKT IZOELEKTRYCZNY (pI) – WARTOŚĆ pH PRZY KTÓREJ AMINOKWAS WYSTĘPUJE
W POSTACI JONU OBOJNACZEGO
OBLICZENIE pI DLA AMINOKWASÓW ZASADOWYCH I KWASNYCH
SUMA pKa GRUP AMINOWYCH
2
SUMA pKa GRUP KARBOKSYLOWYCH
2
Charakter kwasowo-zasadowy aminokwasów
MIARECZKOWANIE AMINOKWASÓW OBOJĘTNYCH
Charakter kwasowo-zasadowy aminokwasów
MIARECZKOWANIE AMINOKWASÓW ZASADOWYCH
Charakter kwasowo-zasadowy aminokwasów
MIARECZKOWANIE AMINOKWASÓW KWASOWYCH
Charakter kwasowo-zasadowy aminokwasów
MIARECZKOWANIE AMINOKWASÓW – PORÓWNANIE CHARAKTERU KRZYWYCH
AMINOKWAS
OBOJĘTNY
AMINOKWAS
KWAŚNY
AMINOKWAS
ZASADOWY
Charakter kwasowo-zasadowy aminokwasów
ROZDZIAŁ AMINOKWASÓW W POLU
ELEKTRYCZNYM - ELEKTROFOREZA
Charakter kwasowo-zasadowy aminokwasów
ROZDZIAŁ AMINOKWASÓW W POLU
ELEKTRYCZNYM - ELEKTROFOREZA
AMINOKWASY POSIADAJĄCE ŁADUNEK DODATNI WĘDRUJĄ DO ELEKTRODY O ŁADUNKU UJEMNYM
AMINOKWASY POSIADAJĄCE ŁADUNEK UJEMNY WĘDRUJĄ DO ELEKTRODY O ŁADUNKU DODATNIM
Podział aminokwasów
AMINOKWASY
NATURALNE (D, L)
BIAŁKOWE (L)
PIERWSZORZĘDOWE
(KODOWANE)
ENDOGENNE
DRUGORZĘDOWE
EGZOGENNE
SYNTETYCZNE
NIEBIAŁKOWE (D, L)
TRZECIORZĘDOWE
Aminokwasy
BIAŁKOWE (L)
PIERWSZORZĘDOWE
(KODOWANE)
DRUGORZĘDOWE
AMINOKWASY BIAŁKOWE
TO AMINOKWASY
TWORZĄCE BIAŁKA
TRZECIORZĘDOWE
RZĘDOWOŚĆ NIE JEST ZWIĄZANA Z RZĘDOWOŚCIĄ GRUPY AMONOWEJ,
TYLKO Z PROCESEM BIOSYNTEZY BIAŁKA
Aminokwasy
AMINOKWASY PIERWSZORZĘDOWE
STANOWIĄ SUBSTRATY
W RYBOSOMALNEJ SYNTEZIE BIAŁKA
PIERWSZORZĘDOWE
(KODOWANE)
BIAŁKOWE (L)
DRUGORZĘDOWE
AMINOKWASY
DRUGORZĘDOWE
POWSTAJĄ W WYNIKU
POSTRYBOSOMALNEJ
MODYFIKACJI AMINOKWASÓW
PIERWSZORZĘDOWYCH
(METYLOWANIE,
HYDROKSYLOWANIE,
HALOGENOWANIE)
TRZECIORZĘDOWE
AMINOKWASY TRZECIORZĘDOWE
POWSTAJĄ W WYNIKU POSTRYBOSOMALNEJ MODYFIKACJI PROWADZĄCEJ DO UTWORZENIA
NIETYPOWYCH WIĄZAŃ KOWALENVYJNYCH MIĘDZY RESZTAMI AMINOKWASOWYMI
(WIĄZANIA DISULFIDOWE)
Aminokwasy
AMINOKWASY ENDOGENNE
NIE MUSZĄ BYĆ DOSTARCZANE WRAZ
Z PPOŻYWIENIEM, MOGĄ BYĆ
SYNTEZOWANE W ORGANIZMACH Z
INNYCH SUBSTRATÓW
ENDOGENNE
PIERWSZORZĘDOWE
(KODOWANE)
AMINOKWASY EGZOGENNE
TO AMINOKWASY NIEZBĘDNE,
NIESYNTEZOWANE PRZEZ
ORGANIZM, KTÓRE MUSZĄ BYĆ
DOSTARCZANE WRAZ
Z POŻYWIENIEM W CELU
PRAWIDŁOWEGO
FUNKCJONOWANIA
ORGANIZMU
EGZOGENNE
Aminokwasy
AMINOKWASY EGZOGENNE
LISTA AMINOKWASÓW
EGZOGENNYCH JEST RÓŻNA
DLA RÓZNYCH ORGANIZMÓW
U PTAKÓW GLICYNA JEST
EGZOGENNA
ARGININA
HISTYDYNA
LIZYNA
LEUCYNA
IZOLEUCYNA
METIONINA
TREONINA
WALINA
FENYLOALANINA
TRYPTOFAN
ZAPOTRZEBOWANIE NA
AMINOKWASY EGZOGENNE
WZRASTA W OKRESIE
KRWAWIEŃ, REGENERACJI
TKANEK
I REKONWALESCJENCJI
ARGININA I HISTYDANA
SĄ NIEZBĘDNE W
PRAWIDŁOWYM
ROZWOJU ORGANIZMÓW
MŁODYCH
ZAPOTRZEBOWANIE NA
LIZYNĘ I TRYPTOFAN JEST
WIĘKSZE U KOBIET W CIĄŻY I
W OKRESIE KARMIENIA
Aminokwasy
GLICYNA
ASPARAGINA
ALANINA
GLUTAMINA
WALINA
SERYNA
LEUCYNA
TREONINA
IZOLEUCYNA
TYROZYNA
METIONINA
PROLINA
CYSTEINA
FENYLOALANINA
AMINOKWASY OBOJĘTNE
TRYPTOFAN
Aminokwasy
AMINOKWASY KWAŚNE
KWAS ASPARAGIONOWY
KWAS GLUTAMINOWY
Aminokwasy
AMINOKWASY ZASADOWE
LIZYNA
ARGININA
HISTYDYNA
Aminokwasy
AMINOKWASY ZASADOWE
SILNIE ZASADOWA
GRUPA GUANIDYNOWA
Właściwości fizykochemiczne aminokwasów
AMINOKWASY TO ZWIĄZKI AMFOTERYCZNE – POSIADAJĄ GRUPĘ O CHARAKTERZE KWAŚNYM
I ZASADOWYM
TWORZĄ SOLE WEWNĘTRZNE, TAK ZWANE JONY OBEJNACZE (ZWITTERION)
WIĘKSZOŚĆ AMINOKWASÓW JEST ROZPUSZCZALNA W WODZIE
TRUDNO ROZPUSZCZALNE A NAWET NIEROZPUSZCZALNE W ROZPUSZCZALNIKACH ORGANICZNYCH
SUBSTANCJE KRYSTALICZNE O WYSOKICH TEMPERATURACH TOPNIENIA
Właściwości fizykochemiczne aminokwasów
ZAPACH
W WIĘKSZOŚCI SĄ BEZZAPACHOWE
CYSTEINA I METIONINA MAJĄ NIEPRZYJEMNY ZAPACH
KWAS GLUTAMINOWY MA ZAPACH HYDROLIZATU BIAŁKOWEGO – ROSOŁU (DODATEK DO PRZYPRAW)
SMAK
GORZKI LUB SŁODKI
GLICYNA, ALANINA, SERYNA, TREONINA SĄ SŁODKIE
BEZ SMAKU SĄ LIZYNA, TRYPTOFAN, KWAS ASPARAGINOWY, ASPARAGINA, CYSTEINA
GORZKIE SĄ TYROZYNA, LEUCYNA I IZOLEUCYNA
ZMIANA KONFIGURACJI Z L NA D MOŻE ZMIENIC SMAK SŁODKI NA GORZKI I ODWROTNIE, LUB NA OBOJĘTNY
Właściwości fizykochemiczne aminokwasów
TOKSYCZNOŚĆ
NADMIAR LEUCYNY PRZY JEDNOCZESNYM NIEDOBORZE
TRYPTOFANU POWODUJE PELAGRE (RUIEŃ LOMBARDZKI)
DUŻE DAWKI TYROZYNY MOGĄ POWODOWAĆ ZMIANY SKÓRNE, UBYTKI WAGI, MARKOSĆ WĄTROBY
A NAWET PROWADZIĆ DO ŚMIERCI.
NADMIAR FENYLOALANINY MOŻE POWODOWAĆ FENYLOKETONURIĘ – NASTĘPUJE GROMADZENIE
FENYLOALANINY W PŁYNACH USTROJOWYCH, WYDZIELANIE DUŻYCH ILOSCI ACETONU,
ZAHAMOWANIE SYNTEZY TYROZYNY
NADMIAR TRYPTOFANU MOŻE WYWOŁYWAĆ DEPRESJĘ (KIEDYŚ STOSOWANY JAKO LEK NA DEPRESJĘ)
AMINOKWASY O CHARAKTERZE HYDROFOBOWYM MOGĄ DZIAŁAĆ SZKODLIWIE
AMINOKWASY O CHARAKTERZE HYDROFILOWYM SĄ ZWYKLE NIESZKODLIWE
WYJĄTEK STANOWI GLUTAMINIAN SODU !
Właściwości fizykochemiczne aminokwasów
TOKSYCZNOŚĆ
GLUTAMINIAN SODU !
ODPOWIEDZIALNY ZA ODCZUWANIE SMAKU MIĘSNEGO (UMAMI)
PORCJA WIELKOŚCI 5 g MOŻE PROWADZIĆ DO ZABURZENIA KONCENTRACJI, KOŁATANIA SERCA,
DEPRESJI, NADMIERNEJ POBUDLIWOŚCI I BÓLU GŁOWY (SYNDROM CHIŃSKIEJ KUCHNI)
Zastosowanie aminokwasów
KWAS GLUTAMNOWY – DODATEK DO PRZYPRAW (W POSTACI GLUTAMINIANU SODU)
LIZYNA – DODATEK ZWIĘKSZAJĄCY WARTOŚĆ ODRZYWCZĄ PRODUKTÓW MĄCZNYCH
METIONINA – AMINOKWAS NIEZBĘDNY, DODATEK DO PASZ DLA ZWIERZĄT HODOWLANYCH
DODATEK METIONINY DO LEKÓW PRZECIWBULOWYCH ZAWIERAJĄCYCH PARACETAMOL
ZMNIEJSZA SKUTKI UBOCZNE
LIZYNA BUFORUJE SOK ŻOŁĄDKOWY DO PRAWIDŁOWEJ KWASOWOŚCI – STOSOWANA W LECZENIU
NADKWAŚNOŚCI I NIEDOKWAŚNOŚCI ŻOŁĄDKA
KWAS ASPARAGINOWY I FENYLOALANINA SŁUŻĄ DO PRODUKCJI ASPARTAMU (SŁODZIK)
KWAS ASPARAGINOWY BIERZE UDZIAŁ W METABOLIZMIE TKANKI NERWOWEJ, DZIAŁA ANABOLICZNIE
Zastosowanie aminokwasów
TYROZYNA PRZYSPIERZA BRĄZOWIENIE SKÓRY – KREMY DO OPALANIA
3,4 – DIHYDROKSY-L-FENYLOALANINA (DOPA) – ŁAGODZI SKUTKI CHOROBY PARKINSONA,
STOSOWANA PRZY ZATRUCIACH MANGANEM
POWODZENIA NA EGZAMINIE !!!