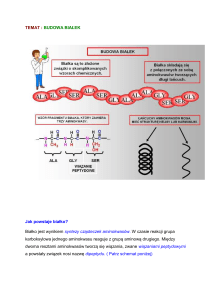
ĆWICZENIE 3
REAKCJE CHARAKTERYSTYCZNE
AMINOKWASÓW I BIAŁEK
Celem ćwiczenia jest zapoznanie się z charakterystycznymi reakcjami aminokwasów
i białek przy zastosowaniu jako materiału ćwiczeniowego czystych roztworów tych związków.
Reakcje te umożliwiają odróżnianie aminokwasów i białek od innych związków organicznych,
białek od wolnych aminokwasów, wykrycie aminokwasów zawierających atomy siarki oraz
aminokwasów aromatycznych. Należy także dokonać identyfikacji otrzymanej próbki
aminokwasu.
Sprzęt i odczynniki:
statyw z probówkami, pipety
1% r-ry aminokwasów: alanina, leucyna, cystyna, tyrozyna, tryptofan, wodny r-r białka,
alkohol etylowy, nieznany aminokwas
0,1% acetonowy r-r ninhydryny,
0,5% r-r siarczanu miedziowego,
6n NaOH, stęż. kwas azotowy,
stęż. kwas siarkowy,
odczynnik Millona,
2% r-r octanu ołowiawego
Wykonanie ćwiczenia:
Dla wymienionych powyżej roztworów aminokwasów i białka wykonać szereg reakcji
charakterystycznych wg schematu zamieszczonego poniżej. Wyniki zamieścić w tabelach:
ZWIĄZEK
REAKCJA
Próba ninhydrynowa
WYNIK
WNIOSEK
zw. organiczny
alanina
leucyna
cystyna
cysteina
tryptofan
tyrozyna
białko
nieznana próbka
Próba biuretowa
Próba ksantoproteinowa
Próba Millona
Próba z octanem ołowiu
WYNIKI DOŚWIADCZEŃ Z BADANĄ PRÓBKĄ:
PRÓBA
Próba ninhydrynowa
Próba biuretowa
Próba ksantoproteinowa
Próba Millona
Próba z octanem ołowiu
Nieznanym aminokwasem jest
WYNIK
WNIOSEK
PRÓBA NINHYDRYNOWA - odróżnianie aminokwasów i białek od innych związków
organicznych
Do probówek odmierzyć po 1 ml badanych roztworów, dodać po 1 ml r-r ninhydryny
i ogrzewać przez 3 min w łaźni wodnej. Powinno pojawić się fioletowe zabarwienie
(aminokwas) lub niebieskie (białko).
PRÓBA BIURETOWA - odróżnianie białek od wolnych aminokwasów
Do probówek wprowadzić po 1 ml badanych roztworów dodać po 2 ml 6n NaOH oraz po
1 kropli 0,5 % r-ru siarczanu miedzi dobrze wymieszać i dodać jeszcze raz 0,5 ml r-ru
miedzi. W obecności białka pojawia się fioletowe zabarwienie, a aminokwasy dają
barwę jasnoniebieską.
PRÓBA KSANTOPROTEINOWA - wykrywanie aminokwasów aromatycznych
Do probówek odmierzyć po 1 ml badanych r-rów, dodać po 1 ml stęż kwasu azotowego
i ogrzewać na łaźni wodnej przez 5 min. Po ochłodzeniu dodać małymi porcjami, ciągle
mieszając 3 ml 6n NaOH. W obecności aminokwasu aromatycznego pojawia się czerwone
zabarwienie.
PRÓBA MILLONA - wykrywanie tyrozyny
Do probówek odmierzyć po 1 ml badanych r-rów, dodać 4 krople odczynnika Miliona
i ogrzewać ostrożnie do wrzenia nad płomieniem palnika. W obecności tyrozyny powinno
pojawić się ceglastoczerwone zabarwienie.
WYKRYWANIE AMINOKWASÓW ZAWIERAJĄCYCH SIARKĘ (próba z octanem
ołowiu)
Do probówek odmierzyć po 1 ml badanych r-rów, dodać po 2 ml 6n NaOH oraz 1,0 ml r-ru
octanu ołowiu i ogrzewać przez 5 min w łaźni wodnej. W obecności aminokwasu
zawierającego siarkę pojawi się brunatno czarny osad lub szare zmętnienie.
START
Wykonaj próbę
ninhydronową
inny związek
NIE
Czy próba
pozytywna?
TAK
aminokwas
lub białko
Wykonaj próbę
biuretową
NIE
Czy próba
pozytywna?
TAK
białko
aminokwas
Wykonaj próbę
ksantoproteinową
Czy próba
pozytywna?
TAK
NIE
aminokwas
niearomatyczny
aminokwas
aromatyczny
Wykonaj reakcję
z octanem ołowiu
Wykonaj próbę
Millona
Wykonaj próbę
Adamkiewicza
NIE
Czy próba
pozytywna?
Czy próba
pozytywna?
TAK
TAK
Czy próba
pozytywna?
TAK
tryptofan
tyrozyna
cystyna
cysteina
NIE
inny
aminokwas