Wymagania programowe dla klasy III o rozszerzeniu biologiczno-chemicznym dla działu:
Wielofunkcyjne pochodne węglowodorów.
Wymagania na ocenę dopuszczającą.
Uczeń powinien :
posługiwać się nazewnictwem systematycznym hydroksykwasów i aminokwasów oraz nazwą
zwyczajową dla kwasu 2-hydroksypropanowego (kwas mlekowy), kwasu aminooctowego (glicyna),
kwasu 2-aminopropanowego (alanina), cukrów prostych, dwucukrów i wielocukrów,
rozumieć i definiować pojęcia: związki wielofunkcyjne, hydroksykwasy, asymetryczny atom węgla,
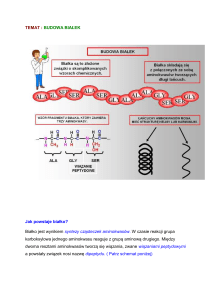
chiralność, enancjomery, izomeria optyczna, kondensacja, aminokwasy, peptydy, polipeptydy, białka,
cukry (mono-, di-, polisacharydy), aldoza, ketoza, pentoza, heksoza,
podzielić cukry na mono-, di- i polisacharydy,
dokonać podziału cukrów prostych ze względu na:
liczbę atomów węgla,
obecność grup funkcyjnych (aldehydowej lub ketonowej),
podać wzory sumaryczne: glukozy, fruktozy, sacharozy, skrobi, celulozy,
wskazać i nazwać grupy funkcyjne występujące w glicynie i glukozie,
omówić właściwości fizyczne glicyny, alaniny, glukozy, fruktozy, sacharozy, skrobi i celulozy (stan
skupienia, rozpuszczalność w wodzie, odczyn roztworu wodnego),
podać przykłady występowania w przyrodzie typowych przedstawicieli sacharydów ( glukozy,
fruktozy, laktozy, maltozy, skrobi, glikogenu, celulozy).
Wymagania na ocenę dostateczną:
Uczeń powinien wykazać się znajomością zagadnień na ocenę dopuszczającą oraz:
zapisywać równania reakcji, jakim ulegają pochodne dwufunkcyjne ze względu na posiadanie
określonych grup funkcyjnych:
- glicyny i alaniny z HCl i NaOH,
- kondensacji aminokwasów (glicyny, alaniny, cysteiny) do dipeptydów i tripeptydów,
- hydrolizy podanego dipeptydu,
- za pomocą wzorów ogólnych i nazw równania hydrolizy disacharydów (sacharoza, maltoza, laktoza)
oraz polisacharydów (skrobia, celuloza),
podać sposoby wykrywania białek w roztworach (reakcja ksantoproteinowa, reakcja biuretowa),
opisać właściwości fizyczna białek (stan skupienia, rozpuszczalność w wodzie, charakter wodnych
roztworów),
wymienić produkty bogate w białka,
wymienić czynniki powodujące proces wysalania i denaturacji białek,
omówić właściwości chemiczne glukozy (spalanie, karmelizacja, fermentacja, utlenianie – zapisać
równania reakcji tych procesów),
podać równanie procesu fotosyntezy,
zapisać wzory Fischera glukozy i fruktozy (forma łańcuchowa),
wymienić znaczenie cukrów,
dokonać podziału polisacharydów na budulcowe (celuloza) i zapasowe (skrobia i glikogen).
Wymagania na ocenę dobrą:
Uczeń powinien wykazać się znajomością zagadnień na ocenę dostateczną oraz potrafi:
za pomocą odpowiednich równań reakcji wykazać kwasowo-zasadowy charakter aminokwasów,
zapisywać równania kondensacji dwóch lub trzech podanych za pomocą wzorów aminokwasów,
zapisywać równania hydrolizy tripeptydów,
omówić punkt izoelektryczny aminokwasów oraz zapisywać tworzenie jonu obojnaczego dowolnego
aminokwasu w roztworze wodnym,
przedstawić biologiczne znaczenie białek,
wyjaśniać przyczyny i sposób tworzenia wiązań wodorowych w białkach,
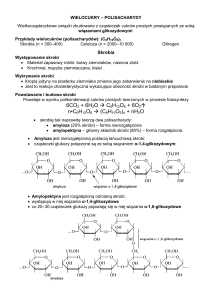
podać wzory Hawortha - i -glukozy oraz - i -fruktozy,
podać w formie pierścieniowej wzory disacharydów (maltoza, sacharoza) oraz fragmentu łańcucha
skrobi i celulozy,
wykazać różnicę pomiędzy skrobią i celulozą (związkami wielkocząsteczkowymi o takim samym
wzorze sumarycznym),
wykryć skrobię w produktach spożywczych,
rozróżniać z podanych wzorów związków, związki optycznie czynne,
omówić i przedstawić za pomocą równań reakcji właściwości hydroksykwasów (kwas mlekowy i
salicylowy).
Wymagania na ocenę bardzo dobrą:
Uczeń powinien wykazać się znajomością zagadnień na ocenę dobrą oraz potrafi:
projektować wzory stereochemiczne związków optycznie czynnych,
na przykładzie kwasu winowego rozróżniać enancjomery od diastereoizomerów,
przewidzieć i zapisać za pomocą równań reakcji zachowanie jonu obojnaczego w środowisku
zasadowym i kwasowym,
analizując wzory podanych aminokwasów określić ich przynależność do szeregu L lub D,
omówić strukturę białek oraz wiązania odpowiedzialne za utrwalanie struktury I, II i III rzędowej,
ocenić rolę DNA w procesie biosyntezy białka,
omówić na podstawie budowy właściwości redukujące monosacharydów (np. glukoza, fruktoza) oraz
niektórych disacharydów (np. maltoza, laktoza) lub ich brak na przykładzie sacharozy, skrobi i
celulozy,
projektować doświadczenia dla typowych reakcji aminokwasów (właściwości kwasowo-zasadowe),
odróżniania cukrów redukujących od nieredukujących (np. próba Tollensa, Trommera) oraz
pozwalające na odróżnienie związków w roztworach (np. glukozę od glicerolu, sacharozy od acetonu
itp.)
rozwiązywać zadania stechiometryczne z wykorzystaniem budowy i właściwości aminokwasów i
cukrów.
Wymagania na ocenę celującą:
Uczeń powinien wykazać się znajomością zagadnień na ocenę bardzo dobrą oraz potrafi:
przedstawić budowę oraz omówić właściwości biologiczne kwasów nukleinowych,
określić współzależność pomiędzy budową a właściwościami fizycznymi, chemicznymi i
biologicznymi związków.