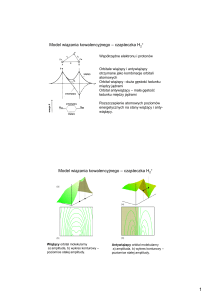
Temat 11: Wiązania w cząsteczkach.
Aby, przypomnieć sobie podstawowe wiadomości przeglądnij załączoną prezentację :
Wiązania w cząsteczkach. Wiązania w czasteczkach.pps
Na czy polega istota wiązania kowalencyjnego dowiesz się z poniższej strony.
http://wapedia.mobi/pl/Wi%C4%85zanie_kowalencyjne
Wiązanie atomowe (kowalencyjne) występuje w cząsteczkach homoatomowych tzn
zbudowanych z atomów tego samego pierwiastka
Istotą wiązania atomowego jest uwspólnienie elektronów
W wyniku uwspólnienia elektronów każdy atom osiąga trwałą konfigurację najbliższego gazu
szlachetnego.
Warunkiem powstawania wiązań chemicznych jest nakładanie się orbitali na których znajdują
się niesparowane elektrony
Wiązanie atomowe spolaryzowane występuje w cząsteczkach heteroatomowych tzn
zbudowanych z atomów różnych pierwiastków.
Istotą istnienia wiązania atomowego spolaryzowanego jest przesunięcie wspólnej pary
elektronów w stronę bardziej elektroujemnego pierwiastka.
Elektroujemność - zdolność doprzyciągania ( przyjmowania ) elektronów
Polaryzacja wiązań -przejście pary elektronów w stronę bardziej ujemnego pierwiastka
Wiązanie jonowe
Istotą wiązania jonowego jest oddziaływanie różnoimienne naładowanych jonów (kationów i
anionów)
Substancje jonowe to;
-ciała stałe, krystaliczne
-dobrze rozpuszczalne w wodzie
-posiadają wysokie t topnienia
-zarówno w roztworze jak i w stanie stopionym => przewodzą prąd elektryczny
Wiązanie metaliczne występuje w kryształach metali i ich stopach. Kryształ metalu
zbudowany jest z uporządkowanych przestrzennie kationów i swobodnie poruszających się
między nimi elektronów. Zlokalizowane elektrony tworzą tzw. gaz elektronowy.
Istotą wiązania metalicznego jest elektrostatyczne oddziaływanie gazu elektronowego z
kationami danego metalu. Budowa wewnętrzna. metali wpływa na ich właściwości fizyczne
Wiązanie wodorowe tworzy się między cząsteczkami w których atom H połączony jest z
silnie elektroujemnym pierwiastkiem. Wiązanie wodorowe ma charakter oddziaływania dipoldipol.
Wiązania wodorowe mogą tworzyć się zarówno między cząsteczkami organicznymi a
nieorganicznymi.
Wiązania H odgrywają dużą rolę biologiczną. Obecność wiązania wodorowego powoduje
podwyższenie temp. topnienia oraz wrzenia substancji
Zapoznaj się z konfiguracją elektronową pierwiastków grupy 17.
Zobacz jak zmieniają się długości promieni atomowych i jonowych pierwiastków grupy 17,
Zaobserwuj związki pomiędzy budową atomów a właściwościami fizycznymi pierwiastków,
http://www.scholaris.pl/cms/index.php/resources/lekcja_pierwiastki_grupy_17_495.html
Przykład 1
Ilu elektronów brakuje do oktetu podanym atomom:
a) chlor
b) siarka
Rozwiązanie:
Odp. a) Chlor leży w 17 grupie układu okresowego, na powłoce walencyjnej ma 7
elektronów, a więc do oktetu brakuje mu jednego elektronu.
Odp. b) Siarka leży w 16 grupie układu okresowego, na powłoce walencyjnej ma 6
elektronów, a więc do oktetu brakuje jej dwóch elektronów.
Przykład 2
Oblicz ilość protonów, neutronów i elektronów w podanych jonach.
Ilość protonów
11
Ilość elektronów
10
Ilość neutronów
12
Ca 2
20
18
20
S 2
16
18
16
Jon
23
11 Na
40
20
32
16
Rozwiąż zadania
Zad. 1 (2p )
Ilu elektronów brakuje do oktetu podanym atomom:
c) azot
d) tlen
Zad. 2 (2p
Oblicz ilość protonów, neutronów i elektronów w podanych jonach.
Jon
35
17 Cl
39
19
K
27
13
Al 3
Ilość protonów
Ilość elektronów
Ilość neutronów
Zad.3 (1p)
Podaj wzór sumaryczny związku chemicznego złożonego z jonów:
Ba2+, Cl
opracowanie: Elżbieta Pozorska
konsultant: Anna Jońska- Choinka