Model wiązania kowalencyjnego – cząsteczka H2+
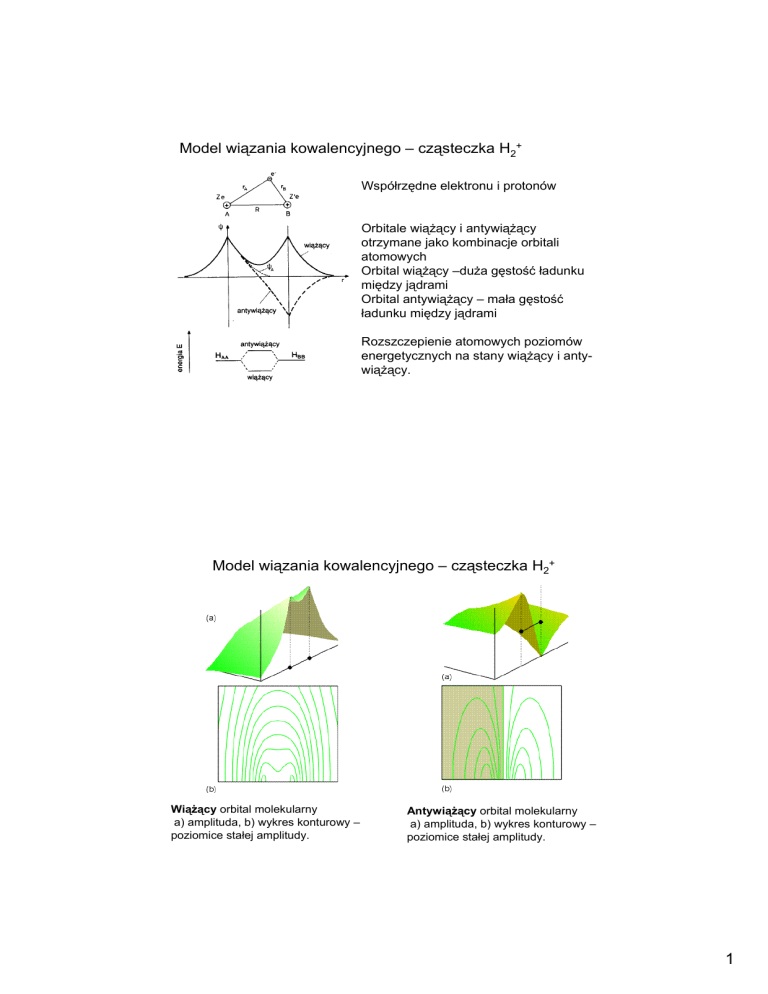
Współrzędne elektronu i protonów
Orbitale wiążący i antywiążący
otrzymane jako kombinacje orbitali
atomowych
Orbital wiążący –duża gęstość ładunku
między jądrami
Orbital antywiążący – mała gęstość
ładunku między jądrami
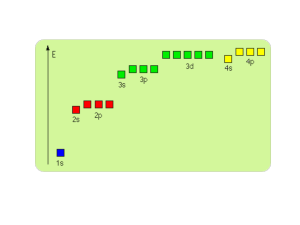
Rozszczepienie atomowych poziomów
energetycznych na stany wiążący i antywiążący.
Model wiązania kowalencyjnego – cząsteczka H2+
Wiążący orbital molekularny
a) amplituda, b) wykres konturowy –
poziomice stałej amplitudy.
Antywiążący orbital molekularny
a) amplituda, b) wykres konturowy –
poziomice stałej amplitudy.
1
Wiązanie kowalencyjne
Tworzenie się wiązania w
cząsteczce wodoru H2
Cząsteczki dwuatomowe – jednakowe atomy
Nałożenie dwu orbitali atomowych p o
kierunku osi cząsteczki – wiązanie σ.
Wiązanie potrójne w cząsteczce azotu N2 –
jedno wiązanie σ i dwa wiązania π.
2
Cząsteczka wody H2O
Wiązania σ z nałożenia orbitali atomowych
H 1s i O 2p. Dwie wolne pary elektronów
walencyjnych pozostają przy atomie tlenu.
Kierunkowość wiązań kowalencyjnych
Przekrywanie się orbitali „wodorowych” s i
p sąsiednich atomów: a) oddziaływanie
znosi się, b) efektywne przekrywanie s i py
Fulleren C60
3
Hybrydyzacje
W kryształach uzyskuje się obniżenie energii dla przekrywania się
większej ilości orbitali - hybrydyzacja
Kształty orbitali po
hybrydyzacji muszą być
jednakowe !
Hybrydyzacja sp3
Metan CH4
Diament
kąt 109.5°
4
Hybrydyzacja sp2
Grafit
kąt 120°
Hybrydyzacja sp
Cząsteczki o budowie liniowej
Acetylen C2H2
kąt 180°
5
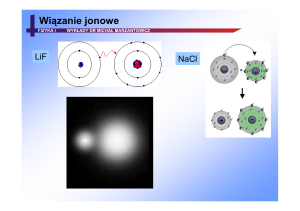
Wiązanie jonowe
LiF
NaCl
6
Wiązanie jonowe
energia jonizacji
powinowactwo elektronowe
siły odpychania
siły kulombowskie
Siły i energia potencjalna w zależności od odległości między jonami o
przeciwnych ładunkach
Siła przyciągania elektrostatycznego
Fattr ~ -r-2
Siła odpychania przy przekrywaniu
powłok elektronowych Frep~ r-n
Wartość wykładnika n zależy od
rdzenia jonu: [He] n=5, [Ne] n=7,
[Ar] n=9, [Kr] n=10, [Xe] n=12
Minimum energii sieciowej:
E min = −
N A AZ + Z − e 2 ⎛ 1 ⎞
⎜1 − ⎟
4πε 0 a 0 ⎝ n ⎠
równanie Borna-Landé
7
Kryształy jonowe
Sól kuchenna – chlorek sodu
NaCl
CsCl
Struktura ciasnego upakowania
Kryształy jonowe są kruche – pękają pod wpływem naprężeń
Wiązanie wodorowe
-Atom wodoru wiąże się z dwoma innymi atomami
-Elektron z wodoru prawie całkowicie przeniesiony
na silnie elektroujemny atom
-Proton może przyciągnąć kolejny ujemnie
naładowany atom
Symetryczne: A-H-A
Antysymetryczne: A-H...B
8
Wiązanie wodorowe:
¾ oddziaływanie między spolaryzowany wiązaniem A__H a
centrum protono-akceptorowym B: δ− δ+
A___H.....B
¾ donorem protonu A__H może być OH, NH, SH, CH ....
¾silne wiązanie, gdy B jest elektroujemnym atomem (O, N, F, S) i
ma wolną parę elektronową (energia wiązania około 0,3 eV)
¾ atom wodoru pozbawiony elektronu jest gołym protonem
¾ następuje nakrywanie chmur elektronowych A i B ściąganych
przez proton mostkowy pozbawiony elektronu
¾ odległość między jądrami atomów A i B jest mniejsza od sumy
promieni van der Waalsa tych atomów nawet o 0,06 nm
¾ potencjał odpychania narasta mniej stromo niż w innych
wiązaniach
¾ może pojawić się drugie minimum potencjału dla protonu
¾ możliwe przeniesienie protonu w wiązaniu od A do B
Wiązanie wodorowe
9
Wiązanie Van der Waalsa
-Występuje zawsze
-Źródło: fluktuacje ładunku w atomach, moment
dipolowy atomów i cząsteczek
-Wiąże atomy o zamkniętych powłokach,
nasycone cząsteczki (kryształy molekularne)
-Duży promień atomowy.
Kształt potencjału w wiązaniu Van
der Waalsa może być przybliżony
potencjałem Lennarda-Jonesa
Wiązanie Van der Waalsa
Przykład: atom helu
Oscylacje ładunku
10
Wiązanie metaliczne
-Funkcje falowe zewnętrznych elektronów
ulegają przekrywaniu
-Konsekwencją przekrywania się jest
rozszczepienie poziomów i utworzenie
pasma
-Chmura elektronowa rozkłada się na cały
kryształ poprzez przyciąganie elektronów do
kolejnych jąder atomowych
-Nie ma wyróżnionego kierunku wiązania
(struktura krystaliczna związana z
upakowaniem w przestrzeni)
„Morze” swobodnych elektronów pomiędzy „rdzeniami” atomowymi o ładunku dodatnim
Wiązanie metaliczne
Metale grupy 1 wnoszą do wiązania tylko po
jednym elektronie – niska temperatura
topnienia (np. sód Na 98°C)
Im więcej elektronów bierze udział w
wiązaniu, tym silniejsze wiązanie (np.
magnez Mg – 2 elektrony - 650°C)
Własności metali:
-dobre przewodnictwo elektryczne
-dobre przewodnictwo cieplne
-własności mechaniczne (twardość,
wytrzymałość itp.)
11
Klasyfikacja ciał stałych na podstawie typu wiązań
Rozkład przestrzenny elektronów walencyjnych
12
Korelacja między
energią spójności
(kohezji) a temperaturą
topnienia ciał stałych
Temperatury topnienia
ciał stałych o różnych
rodzajach wiązań
13