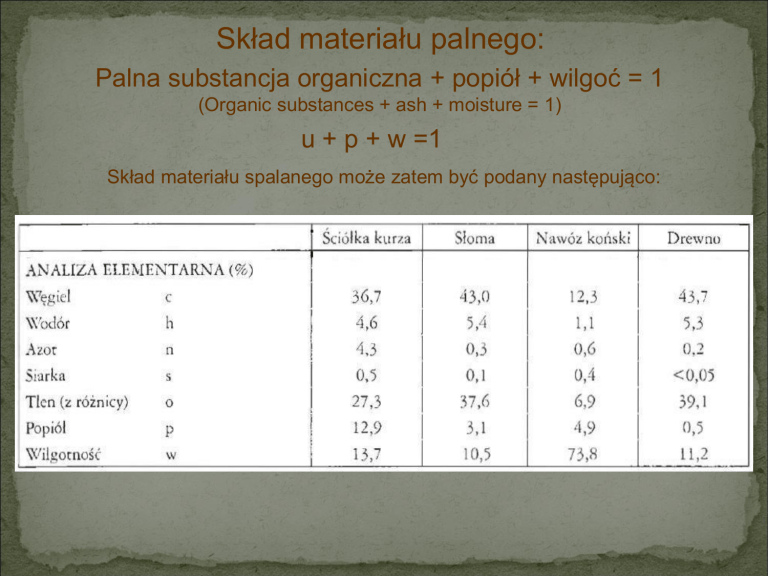
Skład materiału palnego:
Palna substancja organiczna + popiół + wilgoć = 1
(Organic substances + ash + moisture = 1)
u + p + w =1
Skład materiału spalanego może zatem być podany następująco:
Skład elementarny organicznej substancji palnej
c
hsn
o
p
Składniki palne
um.s.b
um.s
w
Transport materiału do miejsca spalania może powodować
zmianę zawartości wilgoci, dlatego skład takiego materiału
wygodniej jest podawać w przeliczeniu na masę suchą:
um . s
składnik
u
1 w
kg/kg m.w. kg/kg m.s.
c
0,367
0,4253
h
0,046
0,0533
n
0,043
0,0498
s
0,005
0,0058
o
0,273
0,3163
p
0,129
0,1495
w
0,137
suma:
1,000
1,000
Skład materiału spalanego podaje się często w
przeliczeniu na masę suchą, bezpopiołową. Wtedy:
um. s.b
składnik
u
1 w p
% m.w.
% m.s.
% m.s.b
c
36,7
42,53
50,00
h
4,6
5,33
6,27
n
4,3
4,98
5,86
s
0,5
0,58
0,68
o
27,3
31,63
37,19
p
12,9
14,95
-
w
13,7
-
-
suma:
100,0
100,00
100,00
Skład substancji palnej może być określony za pomocą
udziału masowego części lotnych (volatiles V), wilgoci
(moisture M), popiołu (ash A) oraz węgla związanego
(fixed carbon FC) następująco:
FC V A M 1
lub odniesiony do masy suchej:
FCs Vs As 1
Spalanie palnej substancji organicznej
C
CO2,(CO)
H
H2O
S
SO2
N
N2, (NO)
P
P2O5
Cl
HCl
O
Zużywany jako utleniacz
Skład elementarny drewna odpadów komunalnych, %
(Wood from municipal waste, %)
c
h
o
n
s
33,22
3,80
27,06
0,97
0,07
c 33,22 kg 100kgm. w.
cs
c
48,01 kg 100kgm. s
1 w
cm.s.b.
c
51,01 kg 100kgm.s.b.
1 w p
p
w
(ash)
(moisture)
4,08
30,80
Skład elementarny drewna odpadów komunalnych, %m.s
(Wood from municipal waste, % dry mass)
c
h
o
n
s
48,01
5,49
39,10
1,40
0,10
Wilgoć: 30,80%m.w
cm. s.
cm. w.
33,22%
48,01%
1 w 1 30,80%
cm. s.b.
cm. s.
51,01%
1 p
p
(ash)
5,90
Skład elementarny drewna odpadów komunalnych, %
(Wood from municipal waste, %)
c
h
o
n
s
p (ash)
w (moisture)
suma:
m.w.
33,22
3,80
27,06
0,97
0,07
4,08
30,80
100,00
m.s.
48,00
5,50
39,10
1,40
0,10
5,90
100,00
m.s.b.
51,01
5,84
41,55
1,49
0,11
100,00
Minimalne zapotrzebowanie na tlen (1)
nO2 ,C nC
m pal c
MC
nO2 , H 0,25 nH
nO2 , S nS
0,25 m pal h
m pal s
MS
MH
Minimalne zapotrzebowanie na tlen (2)
CCO
nO2 ,C 0,5 n 'C
NNO
nO2 , N 0,5 n ' N
0,5 m pal c '
MC
0,5 m pal n '
MN
Całkowite zapotrzebowanie na tlen
nO2 ,min nO2 ,C nO2 , H nO2 ,S ...
0,5 m pal o
MO
nO2 nO2 ,min
100 nO2 R T0
V pow
21
p0
J
R 8314
kmol K
T0 273K
p0 101325Pa
Współczynniki nadmiaru powietrza
Współcz. nadmiaru
Rodzaj spalania
powietrza
Spalanie węgla na ruszcie z ręcznym przegarnianiem
1,6 - 2
Spalanie węgla na ruszcie mechanicznym
1,3 – 1,6
Spalanie pyłu węglowego i paliw ciekłych
1,2 – 1,4
Spalanie gazu
Spalanie fluidalne
1,05 – 1,2
2
Efekt cieplny procesu spalania
Wartość opałowa Wd to ilość ciepła jaką uzyskuje się w
procesie spalania całkowitego i zupełnego jednostki
(liczności, masy lub objętości) paliwa, przy czym produkty
zostają ochłodzone do temperatury substratów, a zawarta
w spalinach para wodna pozostaje w fazie gazowej.
Dla wielu substancji stałych wartość opałową ustala się na
podstawie ciepła spalania Wg (entalpii spalania), tj. ilości
ciepła powstałego w warunkach określonych wartością
opałową powiększonej o ciepło całkowitego wykroplenia
pary wodnej.
Wg Wd xw, sp H par
Jeśli znana jest wartość opałowa suchej masy
bezpopiołowej Wd,s,p to wartość opałową masy
wilgotnej oblicza się zgodnie z zależnością:
Wd Wd , s , p (1 p w) w H par
Wartość opałowa Wd niektórych paliw
Rodzaj paliwa
Wartość
opałowa,
MJ/kg
węgiel kamienny – orzech
węgiel kamienny – miał
węgiel brunatny
koks
drewno opałowe suche
brykiety
pelety
słoma zbożowa sucha
24–28
19–26
7 5-21
27
16-19
17-20
17-21
14-15
Ustalić zapotrzebowanie na powietrze niezbędne do
spalenia biomasy i paliwa wspomagającego
Zebrać dane niezbędne do przeprowadzenia bilansu
ciepła (ciepła właściwe, ciepło parowania wody)
Obliczyć strumienie części palnych, niepalnych, wody
Qspal Qogrz, such Qogrz, wody H par, wody Qogrz, pary 0
T2
Q m c p T
Q m c p (T ) dT
T1
Pojemność cieplna:
c p ,O2
c p,N2
J
36,21 8,46 10 T 4,315 10 T ,
mol K
4
5
2
J
27,86 4,19 10 T ,
mol K
3
,,Poradnik fizykochemiczny"- praca zbiorowa- wydanie 2 - rok wydania 1974