Analiza własności utleniających AgF2 w stosunku do rozmaitych
organicznych grup funkcyjnych i próby syntezy adduktów AgF2
ze związkami o wysokim stopniu sfluoryzowania.
Dorota Grzybowska
Promotor i opiekun pracy: dr hab. Wojciech Grochala
Pracownia Oddziaływań Międzycząsteczkowych
WPROWADZENIE
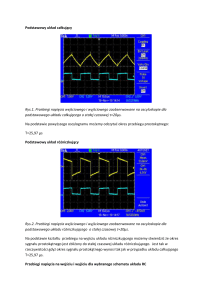
2,07 Å
Rys. 1
Powstawanie kryształków żółtego AgF jest doskonałym
próbnikiem reakcji redukcji brązowego AgF2 (obserwacje pod
wbudowanym w glovebox mikroskopem, powiększenie do 320x)
(Rys. 4)
AgF
AgF2
Fluorki AgII są izoelektronowe z tlenkami CuII [1];
dyskutowano możliwość wysokotemperaturowego
nadprzewodnictwa w tych związkach
Binarny AgF2 jest zbudowany z pofałdowanych
warstw [AgF2] (rys. 1); koordynacja atomu AgII
otoczonego przez 6 atomów F to wydłużony oktaedr[2]
AgF2 – pod ciśnieniem 15 GPa
następuje wypłaszczenie warstw [AgF2]
(obliczenia teoretyczne[3]), co powinno
promować nadprzewodnictwo
Rys. 4.
Większość użytych związków jest cieczami lub niskotopliwymi ciałami stałymi. W celu
umożliwienia reakcji mieszanina stałych reagentów była ogrzewana powyżej temperatury
topnienia związków organicznych.
F
F
F
F
F
F
Rys. 3
F 3C
F
N
O
F
F
F
F
F
F
F
F
F
F
F
O
F
F
F
O
F
F O
O
F
F
F
O
O
F
F
F
F
F F F F
S
F
F
F
F
F
F
F
P
F
F
F
F
F
F
F
F
F
F
F
III. Alifatyczne i aromatyczne
chlorowcopochodne
Cl
F
Cl
I
F F F
I
F F F
F
F
F
Br
Br
F
F
F F F
F F F
F
F
F
I
Ciemnobrązowy AgF2 rozkłada się błyskawicznie pod wpływem H2O do
czarnego Ag2O, dlatego wszystkie operacje (w tym ogrzewanie) prowadzone były
wewnątrz gloveboxu (atmosfera czystego Ar, zawartość H2O i O2 < 0,1 ppm)
F
F
F
OH
Br
F
F
F
F
O
F
F
OH
F
F
F O
F
S OH
F O
F
F
OH
F
F
O
O
S
N
S
O
H
O
N
F
H
F
F
F
Br
ANALIZA WYBRANYCH STAŁYCH PRODUKTÓW
WIZUALNA
(MIKROSKOP LEICA)
MASOWA
(ICHO)
ELEMENTARNA
(ICHO)
90 o C
C6F5 n PF5n
(3)
Rys. 5.
WNIOSKI
O
F
F
(1)
AgF2 gwałtownie reaguje ze związkami, które są źródłem protonu, takimi jak kwasy
słabe (CF3CONH2), średniej mocy (CF3COOH), a nawet bardzo mocne (CF3SO3H).
Zaskakujące jest, że alkohol 3orzędowy C4F9OH nie poddaje się działaniu AgF2.
F
F
?
AgF2 nie reaguje ze związkami posiadającymi kowalencyjne wiązania z Cl czy Br
(CCl4, C6F4Br2, C4F8Br2), natomiast łatwo rozrywa wiązanie C-I w C6F4I2 i C4F8I2
F
V. Kwasy – związki
zawierające grupy –OH i –NH
F
Cl
AgF2 (C6F5 )3 P
F O
F
AgF2 C6F5CN C6F6CN C6F5N2 ? (2)
N
F
AgF2 C6F5NCS Ag2S
Ag2S
115 0 C
C
O
F
Ze względu na silne właściwości utleniające AgII do pracy z AgF2 używano
jedynie narzędzi pokrytych ochronną warstwą teflonu; rurki teflonowe służyły jako
naczynka reakcyjne.
F
F
F F F F F F F F O
F
F
I
Świeżo zsyntetyzowany, bardzo reaktywny AgF2 pochodził
z laboratorium prof. B. Žemvy w Ljubljanie (Słowenia)
F
F
C
F FF F
Cl
F
S
C4F 9
F F
F
N
CF 2
F
O
F
CF 2
N
AgF2 jest bardzo silnym utleniaczem i jego reaktywność wobec organicznych
grup funkcyjnych[5] nie została dostatecznie zbadana, dlatego konieczne było
przeprowadzenie szeregu reakcji dla różnych związków organicznych.
METODOLOGIA BADAŃ
F
F
F 2C
F
AgF2 ulega redukcji do Ag2S (Rys. 5) pod wpływem działania C6F5NCS (równ. 1),
inicjuje złożoną polimeryzację C6F5CN (równ. 2) oraz gwałtownie fluoryzuje P(C6F5)3
dając mieszaninę różnych związków PV (równ. 3).
250 o C
F
F
O
F F
F
CF 3
F
N
II. Związki zawierające N, S, O lub P
w łańcuchu lub pierścieniu
ZAKRES I CELE PRACY
Głównym elementem jest wytypowanie grupy związków, które nie poddają się
utlenianiu przez AgF2 (potencjalnych kandydatów na utworzenie organicznej
warstwy w WHON)
N
F
F
F
F
CF 3
PŁASKA
WARSTWA AgF2
F
N
N
Hipoteza:
mogłyby
istnieć
analogiczne WHON, zbudowane z
płaskich warstw [AgF2] oddzielonych
nieutlenialnymi
związkami
organicznymi obdarzonymi wolną
parą elektronową (rys. 3)
Pomysł: za pomocą przemian
chemicznych uzyskać podobny efekt
(wypłaszczenie warstw AgF2), jaki daje
zastosowanie wysokiego ciśnienia
F
AgF2 nie tworzy w warunkach reakcji adduktów z tlenowymi i azotowymi zasadami
Lewisa (wolne pary elektronowe azotu i tlenu w N(C2F5)3, C10F20O5, C8F16O).
IV. Związki posiadające różne
grupy funkcyjne
F
F
W
1998
zsyntetyzowano
UFO
(Uranium Fluorides from Oxford)[4] –
pierwsze Warstwowe Hybrydy Organiczno
- Nieorganiczne (WHON) (rys. 2)
NIEUTLENIALNA
ZASADA LEWISA
AgF2 nie utlenia także fluoronitrobenzenu (C6F5NO2), ani fluorku sulfonylu
(C8F17SO2F), mimo prowadzenia reakcji w podwyższonej temperaturze.
BADANE ZWIĄZKI
KONCEPT
PŁASKA
WARSTWA AgF2
Zastosowana metodologia pozwala jednoznacznie stwierdzić, czy wybrana grupa
funkcyjną reaguje z AgF2 (związki organiczne pozbawione są protonów C-H, które z
łatwościa uległyby utlenieniu przez AgF2).
AgF2 nie reaguje z C6F6 ani jego pochodnymi nawet w ich temperaturze wrzenia
(C5F5N, C3N3F3, C6F4O2), mimo że jest silniejszym utleniaczem niż Ni2F5 . Ni2F5 utlenia
C6F6 do C6F12[6].
Wszystkie związki organiczne charakteryzują się wysokim
stopniem sfluoryzowania, ponieważ AgF2 fluoryzuje wiązanie C-H.
I. Fluorobenzen i jego analogi
Rys. 2
WYNIKI
RAMANOWSKA
(W. CHEMII UW)
H
Do skonstruowania WHON nie nadają się substancje zawierające jakikolwiek proton
(w tym kwasy -OH, -NH)
Odporność chloro- i bromopochodnych jest prawdopodobnie spowodowana bardzo
wolną kinetyką reakcji
Związki posiadające wolne pary elektronowe na tlenie i azocie są dobrymi
kandydatami do utworzenia organicznej warstwy w WHON, jednak konieczne jest
opracowanie metody interkalacji zasad Lewisa pomiędzy warstwy AgF2. Warto
przeprowadzić próby syntezy w środowisku ciekłego, bezwodnego HF (do reakcji z
użyciem HF konieczna jest specyficzna aparatura, pokryta perfluoropolimerami)
WYBRANA LITERATURA
[1] W. Grochala, R. Hoffmann, Angew. Chem. Int. Ed. Engl. (2001) 40, 2743.
[2] A. Jesih, K. Lutar, B. Žemva, B.G. Müller et al. Anorg. Allg. Chem (1990) 588, 77.
[3] J. Romiszewski, W. Grochala, L. Z. Stolarczyk, J. Phys.: Cond. Matter. (2006) 19, 116206.
[4] R. J. Francis, P. S. Halasyamani, D. O’Hare, Chem. Mater. (1998) 10, 3131.
[5] A. D. Rausch, R. A. Davis, D. W. Osborne, J. Org. Chem. (1963) 28, 494.
[6] M. Tramšek, B. Žemva, Acta Chim. Sloven. (2002) 49, 209.
Przedstawione tu rezultaty zostaną zaprezentowane na
XV Europejskim Sympozjum Chemii Fluoru w Pradze
w dniach 15 - 20 lipca 2007
Chemia UW