cw 133_teoria.doc
(142 KB) Pobierz
1.
PRZEWODNICTWO ELEKTRYCZNE CIAŁ STAŁYCH
Przewodnictwo elektryczne w ciałach stałych. polega na ruchu nośników ładunków elektr., np.
elektronów; wartość przewodnictwa zależy więc od liczby tych nośników w c. stałych Pod tym
względem c. stałe. dzielą się na 3 grupy:
- przewodniki (metale),
- półprzewodniki
- dielektryki (izolatory).
Wraz ze wzrostem temp. przewodnictwo elektryczne przewodników (metali) maleje, natomiast
w tempera turach bliskich 0°K staje się ono bardzo duże (nadprzewodnictwo). Przewodnictwo
półprzewodników i dielektryków rośnie ze wzrostem temp.; w temp. niskich pół-przewodniki,
praktycznie biorąc, nie przewodzą prądu elektr.
Możliwa jest również klasyfikacja ciał stałych ze względu na ich zdolność przewodzenia prądu
elektrycznego pod wpływem przyłożonego z zewnątrz pola elektrycznego. Zdolność
przewodzenia prądu elektrycznego określa się przez podanie przewodności właściwej lub jej
odwrotności - oporu właściwego. Ciała stałe z tego punktu widzenia dzielimy na trzy grupy:
o dobre przewodniki (głównie metale) o δ od 10-8 do 10-6 Ω · m
o złe przewodniki (izolatory) o δ > 109 Ω · m
o ciała o pośrednich wartościach δ leżących w szerokich granicach około 14 rzędów wielkości.
Do tej grupy ciał zaliczamy również półprzewodniki.
W półprzewodnikach mamy zawsze do czynienia z przewodnictwem elektronowym. Również
przewodnictwo dziurowe polega, podobnie jak elektronowe, na przemieszczaniu się elektronów.
Natomiast, np. w kryształach jonowych nośnikami prądu są jony, a nie elektrony. (Czasami
przewodniki jonowe zaliczane są do półprzewodników, w szerszym sensie tego pojęcia).
Zależność oporu właściwego od temperatury T przebiega w sposób charakterystyczny, inny dla
metali i inny dla półprzewodników:
o dla metali δ = δ0 (l +ΔT), gdzie T - temperatura, α - współczynnik temperaturowy oporu
przyjmujący wartości dodatnie rzędu 10-6 na kelwin,
o dla półprzewodników δ = δ0eΔE/kT, gdzie k - stała Boltzmanna, ΔE - miara tzw. energii
aktywacji. Jest to energia, jaką muszą mieć elektrony, aby mogły uczestniczyć w przewodzeniu
prądu.
2.
Prawa Kirchhoffa- dwa podstawowe prawa dotyczące przepływu prądu stałego w obwodach:
I prawo Kirchhoffa: wektorowa suma wszystkich natężeń prądu dopływających do punktu
rozgałęzienia w obwodzie elektrycznym równa jest zeru (inaczej: suma natężeń prądów wpływających
do punktu rozgałęzienia równa jest sumie natężeń prądów wypływających).
II prawo Kirchhoffa: suma spadków napięcia w każdym zamkniętym obwodzie elektrycznym równa
jest zewnętrznej sile elektromotorycznej SEM działającej na ten obwód.
Prawa Kirchhoffa pozwalają ułożyć i rozwiązać układ równań opisujący przepływ prądu stałego w
dowolnie skomplikowanym obwodzie elektrycznym.
Prawo Ampčre'a - prawo określające siłę, z jaką pole magnetyczne o indukcji B działa na przewodnik,
przez który płynie prąd o danym natężeniu I: dF = I (dL * B), gdzie dL - element przewodnika, dF przyczynek siły działającej na element dL.
Prawo Ohma - prawo fizyki głoszące, że stały prąd I płynący w przewodniku jest wprost
proporcjonalny do przyłożonego napięcia U (napięcie elektryczne). U=RI, gdzie współczynnik
proporcjonalności R jest oporem elektrycznym (oporność elektryczna). Uogólnione prawo Ohma dla
prądów zmiennych ma postać: ZI=e gdzie Z - zespolona oporność (impedancja), e - siła
elektromotoryczna. Prawo odkrył G.S. Ohm.
3
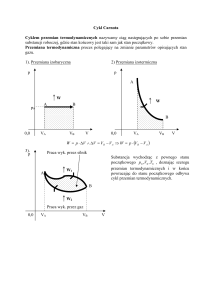
Cykl Carnota - przemiana termodynamiczna, złożona z dwóch przemian izotermicznych i
dwóch przemian adiabatycznych. Cykl Carnota jest procesem kołowym i odwracalnym. Do
realizacji cyklu potrzebny jest czynnik termodynamiczny, który może wykonywać pracę np. gaz
w naczyniu z tłokiem a także dwa nieograniczone źródła ciepła jedno jako źródło ciepła (o
temperaturze T1) a drugie jako chłodnica (o temperaturze T2).
Przemiana izotermiczna - przemiana gazowa, zachodząca przy określonej, stałej temperaturze.
W przemianach tych, zgodnie z prawem Boyla'a-Mariotte'a, ciśnienie gazu doskonałego
wywierane na ścianki naczynia jest odwrotnie proporcjonalne do zajmowanej przez niego
objętości, co zapisuje się jako:
pV = const
gdzie:
p - ciśnienie
V - objętość
Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego
wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość energii dostarczana lub odbierana
jest z niego jako praca.
Przemiana adiabatyczna jest przemianą, w której zmieniają się trzy parametry stanu gazu:
ciśnienie, objętość i temperatura. Przemiana ta nie wymaga ciepła z otoczenia, dlatego podczas
sprężania rośnie jego temperatura, a podczas rozprężania temperatura maleje. Podobnie jak w
przypadku sprężania izotermicznego - maleje objętość a rośnie ciśnienie, w sprężaniu
adiabatycznym trzeba dodatkowo uwzględnić wzrost ciśnienia gazu (spowodowany wzrostem
temperatury).
Przebieg przemiany adiabatycznej określa się prawem Poissona:
gdzie:
p - ciśnienie
V - objętość
- wykładnik adiabaty, równy stosunkowi pojemności cieplnej przy stałej objętości i
przy stałym ciśnieniu.
Krzywe obrazujące procesy adiabatyczne zwiemy adiabatami. Proces adiabatyczny jest
szczególnym przypadkiem procesu politropowego.
Przebieg cyklu
Cykl składa się z następujących procesów:
1. Sprężanie izotermiczne – czynnik roboczy styka się z chłodnicą, ma temperaturę
chłodnicy i zostaje poddane procesowi sprężania w tej temperaturze (T2). Czynnik
roboczy oddaje ciepło do chłodnicy.
2. Sprężanie adiabatyczne – czynnik roboczy nie wymienia ciepła z otoczeniem, jest
poddawany sprężaniu aż uzyska temperaturę źródła ciepła (T1).
3. Rozprężanie izotermiczne – czynnik roboczy styka się ze źródłem ciepła, ma jego
temperaturę i poddawany jest rozprężaniu izotermicznemu w temperaturze T1, podczas
tego cyklu ciepło jest pobierane ze źródła ciepła.
4. Rozprężanie adiabatyczne – czynnik roboczy nie wymienia ciepła z otoczeniem i jest
rozprężany aż czynnik roboczy uzyska temperaturę chłodnicy (T2).
Sprawność cyklu
Dla układu tego definiuje się sprawność jako stosunek pracy wykonanej do ilości ciepła
pobranego ze źródła ciepła.
Parser nie umiał rozpoznać (Can't write to or create math output directory): \eta = \frac{Q
_1 - Q _2}{Q_1} = \frac{T_1-T_2}{T_1} = 1- \frac{T_2}{T_1}
Wzór powyższy wyprowadzony przez Carnota określa, że sprawność cyklu nie zależy od
czynnika roboczego, ani sposobu realizacji, a zależy tylko od temperatur źródła ciepła i
chłodnicy.
Warto zwrócić uwagę na to, że sprawność silnika pracującego w temperaturach T1=373K
(temperatura wrzenia wody) i T2=300K (temp. pokojowa) wynosi około 24%.
Carnot udowodnił też, że dowolny odwracalny cykl zamknięty w którym podczas pobierania
ciepła układ ma temperaturę mniejszą od Tmax a podczas oddawania ciepła większą od Tmin ma
sprawność mniejszą od cyklu Carnota opartego o temperatury Tmax i Tmin. Dlatego często
sprawność silników termodynamicznych określa się w odniesieniu do cyklu Carnota zwanego
silnikiem idealnym.
Cykl Carnota jest odwracalny i może przebiegać w odwrotnym kierunku (zamienione sprężanie z
rozprężaniem) wówczas układ przekazuje energię cieplną od ciała o niższej temperaturze do
ciała o wyższej temperaturze. Układ taki nazywany jest pompą ciepła (lub cieplną) i pracuje on
kosztem wykonywania pracy nad nim. Sprawność cyklu Carnota określa też parametry idealnej
pompy cieplnej działającej przy zadanych temperaturach. Rzeczywiste pompy cieplne mają
sprawność mniejszą od cyklu Carnota.
[Edytuj]
Przykładowy diagram cyklu na wykresie ciśnienie vs.
objętość
Źródło: "http://pl.wikipedia.org/wiki/Cykl_Carnota"
Cykl Carnota
Francuski inżynier i fizyk Leonarda Sadi Carnota na początku XIX-go wieku rozpatrywał tzw.
cykl Carnota. Jest on cyklem odwracalnym składającym się z dwóch przemian izotermicznych
oraz dwóch adiabatycznych. Przebieg tych przemian ilustruje
wykres:
Rys 1
Na schemacie tym kolorem różowym zaznaczone są izotermy, kolorem zielonym - adiabaty. Ich
odcinki, które wchodzą w skład cyklu, są oznaczone na niebiesko. Przebieg
cyklu rozpoczyna się w punkcie 1 przemianą izotermiczną zachodzącą przy temperaturze T1, w
wyniku której następuje rozprężanie gazu od objętości V1 do V2 przy czym ciśnienie zmienia się
od p1 do p2. Równocześnie ciepło pobierane jest ze zbiornika o nieograniczonej pojemności
cieplnej, dzięki czemu jego temperatura nie ulega zmianie, pomimo przekazania układowi ciepła.
Proces zachodzący pomiędzy punktami 2 i 3 jest procesem adiabatycznym, natomiast proces w
przedziale 3-4 jest znów procesem izotermicznym, ale zachodzącym przy niższej temperaturze
T2; proces 4-1 jest drugim procesem adiabatycznym.
Przemiana
Izotermiczna,
rozprężanie
Adiabatyczna,
rozprężanie
Izotermiczna,
sprężanie
Parametry
p1
V1
T1
p2
V2
T1
p3
V3
T2
p2
V2
T1
p3
V3
T2
p4
V4
T2
Położenie Ciepło Ciepło
cylindra pobrane oddane
Z1
Q1
p
W2
...
Plik z chomika:
JareckiKrk
Inne pliki z tego folderu:
Praca
gazu
W1
239a.jpg (489 KB)
240.jpg (756 KB)
Praca sił
zew.
241.jpg (461 KB)
242.jpg (617 KB)
243.jpg (861 KB)
Inne foldery tego chomika:
10 - Wyznaczenie temperatury punktu obojętnego i temperatury inwersji dla termopary
żelazo-miedź
101 - Pomiar przekroju czynnego na zderzenia
103 - Promieniowanie kosmiczne
113 - Tranzystor. Kriogenika
121 - Termometr oporowy i termopara
Zgłoś jeśli naruszono regulamin
Strona główna
Aktualności
Kontakt
Dla Mediów
Dział Pomocy
Opinie
Program partnerski
Regulamin serwisu
Polityka prywatności
Ochrona praw autorskich
Platforma wydawców
Copyright © 2012 Chomikuj.pl