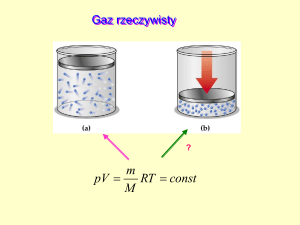
Cykl Carnota
Cyklem przemian termodynamicznych nazywamy ciąg następujących po sobie przemian
substancji roboczej, gdzie stan końcowy jest taki sam jak stan początkowy.
Przemiana termodynamiczna proces polegający na zmianie parametrów opisujących stan
gazu.
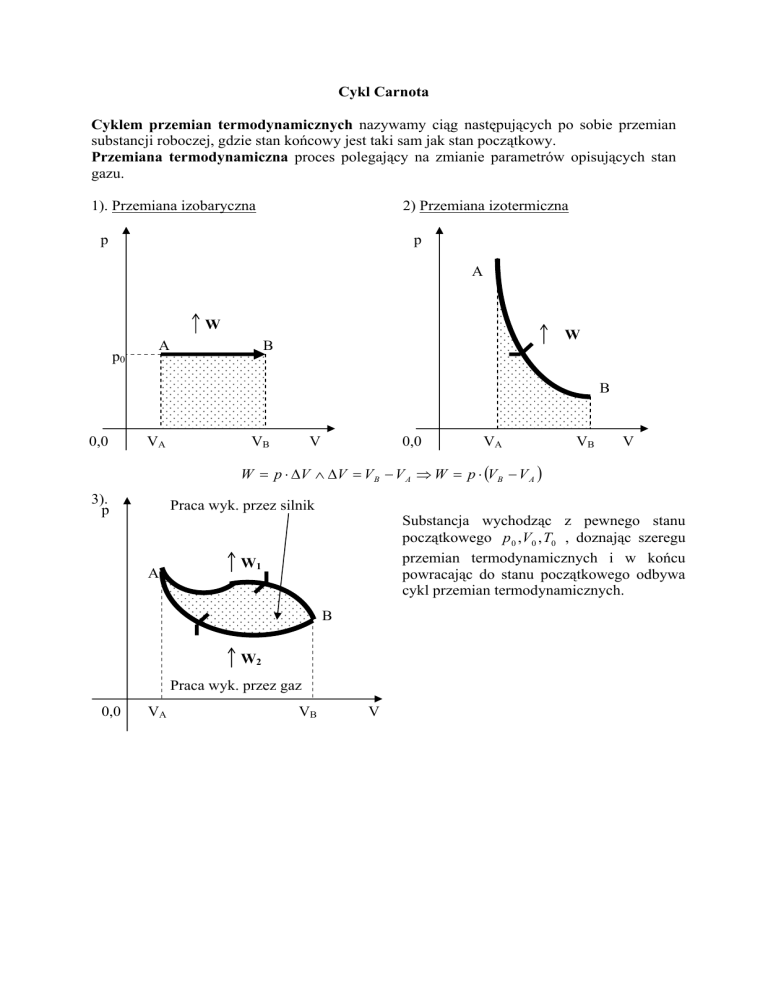
1). Przemiana izobaryczna
2) Przemiana izotermiczna
p
p
A
W
p0
A
W
B
B
0,0
VA
VB
V
0,0
VA
VB
V
W = p ⋅ ΔV ∧ ΔV = V B − V A ⇒ W = p ⋅ (V B − V A )
3).
p
Praca wyk. przez silnik
A
Substancja wychodząc z pewnego stanu
początkowego p 0 ,V0 , T0 , doznając szeregu
przemian termodynamicznych i w końcu
powracając do stanu początkowego odbywa
cykl przemian termodynamicznych.
W1
B
W2
Praca wyk. przez gaz
0,0
VA
VB
V
4). Cykl Carnota
Ogólna zasada pracy silników cieplnych:
1. Silnik pobiera ciepło ze źródła.
2. Część ciepła zamienia na pracę.
3. Pozostałe ciepło oddaje chłodnicy
Źródło
ciepła
Z1
T1
T1 > T2
Chłodnica
Z2
T2
Silnik
p
pA
Źródło
B
IV
0
II
D
C
III
VA
VD
Q2
Chłodnica
I – rozprężenie izotermiczne, gaz wykonuje
pracę przeciwko siłom ciśnienia zew.
ΔU=0 to gaz pochłania ze zbiornika Z1
równoważną pracy ilość ciepła. (+W, -Q)
II – rozprężanie adiabatyczne, temperatura
spada do T2 – gaz wykonuje pracę kosztem
energii wewnętrznej gazu
(+W)
pB
pD
pC
Silnik
W
A
I
Q1
VB
VC
V
III – sprężanie izotermiczne, pobiera
pracę W, a oddaje chłodnicy
równoważoną tej pracy ilość ciepła
Q2 gdzie (+W,-Q) Q2 < Q1
IV – Sprężanie adiabatyczne. Pobrana
praca W a temperatura podnosi się do
temperatury początkowej (+W).
Wielkością charakteryzującą silniki cieplne jest ich sprawność:
Sprawnością silnika nazywamy stosunek pracy wykonanej przez silnik W do ciepła przez
silnik pobranego Q1 .
W Q1 − Q2
n=
=
Q1
Q1
Ciepłem spalania danej substancji nazywamy ilość ciepła wydzielanego przy spalaniu 1kg
substancji
Q
[C s ] = 1 J
Cs =
m
kg
C s - wielkość stabelaryzowana, zależna od rodzaju substancji.