Nr wniosku: 150808, nr raportu: 2533. Kierownik (z rap.): mgr Elżbieta Świętek
O wykorzystaniu danego półprzewodnika jako fotokatalizatora decydują głównie trzy parametry. Pierwszy z nich,
stosunkowo łatwo mierzalny, to energia potrzebna do wzbudzenia danego fotomateriału i wygenerowania pary
elektron-dziura, odpowiedzialnej za przebieg reakcji fotokatalitycznej. Energia ta związana jest ze składem,
strukturą krystaliczną i morfologią półprzewodników. Zachowanie elektronów w sieci krystalicznej z dobrym
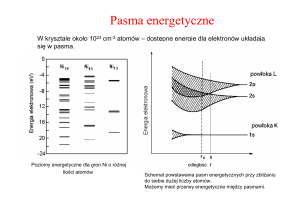
przybliżeniem, opisuje model pasmowy ciała stałego. W stanie podstawowym, czyli w przypadku, kiedy
półprzewodnik nie absorbuje światła, elektrony znajdują się na poziomach energetycznych, które tworzą pasmo
zwane walencyjnym (rozważamy tutaj jedynie elektrony walencyjne, znajdujące się na ostatniej, najbardziej
zewnętrznej powłoce atomów). Elektrony te posiadają pewną energię, która może przyjmować tylko konkretne
wartości (jest skwantowana). W półprzewodniku istnieją również inne poziomy, o wyższych energiach. Nie są one
obsadzone przez elektrony i tworzą tzw. pasmo przewodnictwa (jeżeli elektrony się tam znajdą, półprzewodnik
zaczyna przewodzić prąd, w przeciwnym wypadku zachowuje się jak izolator). Między tymi pasmami istnieje jednak
przerwa energetyczna, czyli pasmo wzbronione. Szerokość tego pasma decyduje o tym, jaką energię musi
posiadać foton, aby został zaabsorbowany. Im szersze pasmo, tym większej energii potrzeba, aby przenieść
elektron z pasma walencyjnego do pasma przewodnictwa. Aby odpowiedzieć na pytanie, jakim światłem wzbudzimy
dany materiał, wystarczy zmierzyć szerokość tego pasma. Metod, pozwalających na wyznaczenie tej wielkości jest
wiele. W wyniku absorpcji kwantu promieniowania o energii wystarczającej na przeniesienie elektronu z pasma
walencyjnego do pasma przewodnictwa, generowane zostają ładunki – elektron w paśmie przewodnictwa oraz
dziura w paśmie walencyjnym. To one odpowiedzialne są za właściwości redukujące (elektrony) i utleniające
(dziury) fotokatalizatora. Aby określić, w jakich reakcjach fotokatalitycznych można wykorzystać dany
półprzewodnik, musimy znać energię (lub potencjał) fotogenerowanych elektronów i dziur. Pomimo wielokrotnych
prób opracowania uniwersalnej i prostej metody, pozwalającej na wyznaczenie tych wielkości, brak jest obecne
takiej, która miałaby zastosowanie do różnego typu materiałów, zwłaszcza modyfikowanych. Celem projektu było
opracowanie procedury, która pozwalałaby charakteryzować właściwości redoksowe różnych półprzewodników
w warunkach najbardziej zbliżonych do warunków przeprowadzania reakcji fotokatalicznych z ich udziałem.
Opracowana w ramach projektu metoda opiera się na wykorzystaniu zależności zmiany w widmie
absorpcyjnym/odbiciowym materiału półprzewodnikowego przy zadanej długości fali, związanej ze zmianą gęstości
elektronowej (ilości elektronów) w paśmie przewodnictwa. W przypadku najpopularniejszego z fotokatalizatorów,
tlenku tytanu(IV), elektrony spułapkowane w paśmie przewodnictwa jako centra TiIIImożna obserwować przy
długości fali równiej 780 nm. Niewzbudzony materiał (brak elektronów w paśmie przewodnictwa) nie absorbuje
promieniowania o tej długości fali, jednak już częściowa redukcja elektrochemiczna pasma przewodnictwa zmienia
gęstość elektronową w materiale, który zmienia właściwości spektroskopowe. W ten sposób wyznaczyć można
potencjał redukcji elektrody wykonanej z badanego półprzewodnika, w którym elektrony spułapkowane w paśmie
przewodnictwa zmieniają właściwości absorpcyjne.
Pomiary takie można przeprowadzić dla różnego typu materiałów. Metoda umożliwia również scharakteryzowanie
zmian po wprowadzeniu modyfikacji, scharakteryzowanie stanów pułapkowych (z naciskiem na te występujące na
powierzchni materiału) – innymi słowy, jest przeznaczona dla nieidealnych kryształów i z powodzeniem jest
wykorzystywana do charakteryzowania różnych, rzeczywistych układów.
A)
Ag/AgCl
Pt
źródło światła
(spektrofotometr UV-vis)
detektor
(spektrofotometr UV-vis)
przeźroczysta elektroda pracująca
(półprzewodnik w postaci półprzeźroczystej powłoki
na powierzchni ITO)
kuweta kwarcowa
z elektrolitem
Ag/AgCl
B)
kuweta
kwarcowa
z elektrolitem
źródło światła
(spektrofotometr UV-vis)
sfera całkująca
Pt
elektroda pracująca
detektor
(spektrofotometr UV-vis)
(półprzewodnik w postaci
nieprzeźroczystej powłoki na
powierzchni folii Pt)
Rys.1
Schemat
przedstawiający
układ
pomiarowy
pozwalający
na
wykonanie
pomiarów
spektroelektrochemicznych: A) dla pomiarów zmian w widmie absorpcyjnym, B) dla pomiarów zmian w widmie
odbiciowym.