01.06.2009r. - 1
Dane epidemiologiczne – świat
Liczba osób zakażonych
Liczba ogólna
Dorośli
Kobity
Dzieci <15lat
Liczba ogólna
Dorośli
Kobiety
Dzieci <15lat
Liczba ogólna
Dorośli
Dzieci <15lat
Nowe zakażenia 2001
Zgony w wyniku AIDS 2001
40mln
37mln
18,5mln
3mln
5mln
4,2mln
2mln
800tys
3mln
2,42mln
580tys
Subsaharyjska Afryka
28,5mln zakażonych
nowe zakażenia rocznie ok. 3,5mln
ok. 1,5mln leczonych (30% wymagających leczenia)
osieroconych dzieci 11mln
w całym regionie 23% zakażonych kobiet w wieku 15-19lat
Europa Wschodnia i Centralna Azja
region najszybciej rozwijającej się epidemii
w 2001r – 250tys nowozakażonych co daje ogólną liczbę 1mln
Ukraina – najbardziej dotknięte państwo tego regionu (1% ludności dorosłej jest zakażona HIV, z
tego ¾ to narkomani)
rozciąganie się epidemii na szerszą populację (coraz więcej zakażeń heteroseksualnych oraz u
kobiet w ciąży)
Dane epidemiologiczne – Polska
(od 1985 – 31.12.2008)
HIV (+) 12 068 z tego narkomani 5476
AIDS – 2189 z tego nie żyje 962
U 40% nie podano drogi zakażenia
Diagnostyka
wykrycie przeciwciał
antygenów wirusa
wirusowego RNA/DNA
hodowla
Diagnostyka zakażeń HIV
Wykrycie antry-HIV1 i anty-HIV2
testem ELISA (w przypadku wyniku pozytywnego badanie powtarzamy z kolejnej próbki surowicy)
wykrycie anty-HIV przeciwko glikoproteinom wirusa testem Western-Blott (test potwierdzenia
wykonywany w przypadku dwukrotnie dodatniego testu ELISA)
1
Szybkie testy
czas wykonania około 10 minut
dodatni wynik musi być potwierdzony tradycyjnymi metodami serologicznymi
wskazania:
o gdy zawodowe narażenie
o kobieta w ciąży w trakcie porodu
Wykrywanie materiału genetycznego – PCR, bDNA
nie mogą zastępować badań serologicznych
zastosowanie:
o gdy rutynowa serologia może zawodzić
o u osób z agammaglobulinemią
o ostrą chorobą retrowirusową
o u noworodków
o w okresie okienka serologicznego
o do kwalifikacji do leczenia i monitorowania jego wyników
Drogi przenoszenia HIV
droga krwi
droga kontaktów seksualnych
droga wertykalna matka – dziecko
Droga krwi
- przetoczenie
- narzędzia naruszające ciągłość skóry
- kontakt uszkodzonej skóry lub śluzówki z materiałem zakaźnym
Okienko serologiczne
HIV 22dni
HBV 59dni
HCV 82dni (66dni)
Zakaźność nosicieli HIV i HBV
HBV
ok. 100 000 000
0,00004ml
100
stężenie we krwi
kom/ml
ilość krwi potrzebna do
zakażenia
wskaźnik zakaźności
HIV
ok. 1000 000
<50
0,1ml
1
Ryzyko transmisji HIV przy jednorazowej ekspozycji na krew
przezskórna
o zakłucie igłą – zawodowe
0,32%
o wspólne użycie igły do inj. IV
0,67%
błony śluzowe
0,09%
skóra uszkodzona – ryzyko mniejsze niż w przypadku błony śluzowej (opisano kilka przypadków)
ekspozycja na inne płyny zawierające HIV – ryzyko jeszcze niższe
2
Płyny ustrojowe uważane za materiał zakaźny
krew
płyny ustrojowe z widoczną domieszką krwi
płyn mózgowo – rdzeniowy
nasienie, wydzieliny pochwowe, płyn maziówkowy, opłucnowy, otrzewnowy, osierdziowy,
owodniowy, tkanki
mleko kobiece
koncentrat wirusa używany w badaniach laboratoryjnych
mocz
kał
slina
łzy
pot
plwocina
wymiociny
Płyny ustrojowe uważane za materiał niezakaźny
Droga kontaktów seksualnych
Ryzyko około 0,5%
Ryzyko transmisji HIV przy jednorazowej ekspozycji
Kontakt seksualny:
- bierny
analny
0,5 – 3,2 %
waginalny
0,05 – 0,15 %
- czynny
0,03 – 0,09 %
Ryzyko przenoszenia infekcji po jednorazowym kontakcie seksualnym z osobą zakażoną
HIV
0,5%
Rzeżączka
22 – 25%
Ryzyko przeniesienia infekcji na stałego partnera seksualnego (para monogamiczna, jedna osoba
zakażona)
HIV
15%
HBV
20 – 25%
Kiła
30%
Droga wertykalna matka – dziecko
Częstość 30% - 1%
Afryka 40%
Transmisja wertykalna zakażenia HIV
zależy od etapu zakażenia matki (liczba CD4, wiremia HIV)
ryzyko w naturalnym przebiegu:
o ok. 25% w Europie i USA
o ok. 40% w Afryce
drogi przenoszenia wirusa HIV:
o w czasie porodu (70 – 80%)
o przez łożysko (zwykle w II połowie ciąży)
o prze karmienie piersią (do 30%)
Nie ma embriopatii, dzieci rodzą się klinicznie zdrowe
3
Nie można zakazić się wirusem HIV przez:
podanie reki
przyjacielski pocałunek
picie z jednej szklanki
używanie tych samych sztućców i talerzy
założenia ubrania osoby zakażonej
korzystanie ze wspólnej wanny i toalety
kąpiel w basenie
spanie w tym samym łóżku
ukłucia owadów
Zakażenie HIV
W warunkach naturalnych przeniesienie jednej jednostki zakaźnej (TCID) wymagałoby wchłonięcia ok.
0,5l zakażonej śliny
1990r.
Obserwacja 757 kontaktów domowych osób HIV (+) nie wykazała żadnego przypadku przeniesienia
zakażenia wirusem HIV (wykluczono możliwość transmisji drogą typową)
Drogi przenoszenia HIV
Grupy ryzyka => zachowania ryzykowne
Patogeneza zakażenia HIV
Flora powierzchowna
Skóra:
gronkowce, paciorkowce
Śluzówki:
gronkowce, paciorkowce
beztlenowce (Fusobacterium)
Escherichia coli
pal. Doederleina
candida spp.
Pęch. płucne: kryptokoki (90% osób)
Pneumocystis jiroveci
Saprofity chronią przed kolonizacją innych, bardziej wirulentnych patogenów
(konkurencja o substancje odżywcze, produkowanie substancji hamujących)
Zakażenia latentne – wczesne zasiedlenie wnętrza organizmu
Patogen
Miejsce bytowania
HSV
Zwój czuciowy neuronu zawiadującego
VZV
odpowiednim odcinkiem skóry
EBV
Nabłonki j. ustnej i gardła – limfocyty B
CMV
Makrofagi
Toxoplasma gonidii
Otorbione cysty w różnych tkankach
4
Mechanizm niedoboru limfocytów T
niszczenie limfocytów, w których namnaża się wirus HIV – tworzenie syncycjów, liza komórek
włączanie programu apoptozy
Następstwa niedoboru limfocytów T4
uaktywnienie się patogenów powierzchniowych (Candida albicans, Cryptococcus neoformans,
Pneumocystis jiroveci)
reaktywacja zakażeń latentnych (VZV, toxo, CMV)
rozwój nowotworów (mięsak Kaposi’ego, chłoniaki nieziarnicze (EBV), rak szyjki macicy)
niemiarodajność badań serologicznych
zła odpowiedź na szczepionki
Historia naturalna rozwoju AIDS
Zakażenie HIV →ostra infekcja retrowirusowa (objawy paragrypowe) →okres utajenia (PGL)
(bezobjawowy, powiększone węzły chłonne) →zakażenie objawowe (gorączka, chudnięcie, zmęczenie,
poty nocne, biegunka, wysypki) →AIDS (PCP, CMVr, Tbc, MAC, KS
Przebieg zakażenia HIV/AIDS
Zakażenie wirusem HIV → niszczenie limfocytów CD4 → spadek odporności → zakażenia
oportunistyczne rozwój - nowotworów
Kryteria
immunologiczne
CD4/ul
1. >500
2. 200-499
3. <200
Klasyfikacja zakażenia HIV wg CDC (1992)
Kryteria kliniczne
zakażenia
zakażenia objawowe
bezobjawowe
A
B
A1
B1
A2
B2
A3
B3
AIDS
C
C1
C2
C3
Klasyfikacja zakażeń HIV
Kategoria kliniczna A
pierwotne zakażenie HIV
o bezobjawowe
o ostra choroba retrowirusowa
przetrwała limfadenopatia
bezobjawowe zakażenie HIV
Ostra choroba retrowirusowi
gorączka
powiększenie węzłów chłonnych
zapalenie gardła
wysypka
bóle stawowo – mięśniowe
biegunka
bóle głowy
nudności, wymioty
powiększenie wątroby i śledziony
>95%
74%
70%
70%
54%
32%
32%
29%
14%
5
Kategoria kliniczna B
kandydoza j. ustnej
leukoplakia włochata
półpasiec
neuropatia obwodowa
rak przedinwazyjny szyjki macicy
małopłytkowość samoistna
objawy ogólne utrzymujące się ponad miesiąc
choroby zapalne miednicy małej
Kategoria kliniczna C
(choroby wskaźnikowe)
I
o
o
o
o
o
gruźlica płuc i pozapłucna
MAC
zapalenia płuc > 2x w roku
PCP
toksoplazmoza mózgu
o
o
o
o
o
kandydoza przełyku, tchawicy, oskrzeli
kryptokokowe zapalenie opon mózgowo – rdzeniowych
chłoniaki nieziarnicze
mięsak Kaposi’ego
rak szyjki macicy – inwazyjny
o
o
o
o
CMV retinitis
owrzodzenia HSV > 1 miesiąca
HIV encefalopatia
zespół wyniszczenia wywołany wirusem HIV
II
III
Leczenie osoby HIV (+)
usuwanie ognisk infekcji
leczenie infekcji oportunistycznych
profilaktyka infekcji oportunistycznych
leczenie antyretrowirusowe
Cel leczenia antyretrowirusowego
zahamowanie replikacji HIV
wzrost liczby limfocytów CD4
odbudowa układu immunologicznego
zmniejszenie ryzyka infekcji oportunistycznych i progresji do AIDS
przedłużenie życia w dobrym stanie ogólnym
Czego nie można osiągnąć leczenie antyretrowirusowym
wyleczenie
zniesienie zakaźności osoby zakażonej
Rezerwuary wirusa:
- OUN
- węzły chłonne
- układ moczowo – płciowy
6
Grupy leków antyretrowirusowych
inhibitory odwrotnej trankryptazy
o nukleotydowe
o nukleozydowe
o nienukleozydowe
inhibitory proteazy
inhibitory fuzji
inhibitory wejścia (koreceptorów)
Dowody skuteczności leczenia ARV
spadek poziomu wiremi HIV <50 kopii/ml
wzrost liczby komórek CD4
poprawa ogólnego stanu chorego
7
01.06.2009r. - 2
Choroby Tropikalne W Polsce
Zimnica
Cholera
Pełzakowica
Gorączka u osób powracających z podróży
Pierwszy tydzień po powrocie z podróży
biegunka podróżnych
czerwonka bakteryjna
choroby przenoszone drogą płciową
grypa
wirusowe gorączki krwotoczne:
o arbowirusy – denga, żółta gorączka
o arenawirusy – g. Lassa, g. Argentyńska
o filowirusy – choroba marburska, g. k. Ebola
o
1-2 tyg. po powrocie z podróży
Zimnica – malaria
wirusowe zapalenie wątroby A
dur brzuszny
paradury
riketsjozy
2-4 tygodnie po powrocie z podróży
dur brzuszny
czerwonka pełzakowata
wirusowe zapalenie wątroby C
schistosomoza
1-6 miesięcy po powrocie z podrózy
wirusowe zapalenie wątroby B
serokonwersja zakażenia HIV
wirusowe zapalenie wątroby E
czerwonka pełzakowata
wścieklizna
leiszmanioza skórna
leiszmanioza układowa
Powyżej 6 miesięcy po powrocie z podróży
nawroty zimnicy (P. falciparum)
uaktywnienie zakażenia P. malariae
strongyloidoza
wscieklizna
leiszmanioza układowa
AIDS
Żółta gorączka jest chorobą podlegającą międzynarodowemu obowiązkowi zgłaszania. Kraje, w których
występuje są wymienione w cotygodniowym raporcie WHO
Międzynarodowe świadectwo szczepienia jest jedynym, obowiązkowo wymaganym w podróżach
międzynarodowych, wydawanym prze punkty szczepień zatwierdzone przez WHO.
8
Żółta gorączka – Febris flava
szczepionka – STAMARIL, żywe, atenuowane wirusy
1 x 0,5ml s. c. powyżej 1-go roku życia skuteczność prawie 100%, dobra tolerancja
okres ważności międzynarodowego świadectwa szczepienia wynosi 10 lat, zaczynając od 10
dnia po podaniu szczepionki
zalecana jest w strefie endemicznej
Zimnica
Malaria
Plasmodiosis
Zimnica powinna zostać bezwzględnie wykluczona u każdej gorączkującej osoby powracającej z
tropików.
Epidemiologia
40% ludności kuli ziemskiej żyje na terenach endemicznych
w ponad 100 krajach świata
300-500mln nowych zachorowań rocznie
1,5-2,7mln zgonów rocznie
0,8-1,0mln dzieci do 5 roku życia
w Polsce zgłaszanych do PZH ok. 30 przypadków rocznie w tym 2-3 zgony
w Europie ok. 10 000
Etiologia
1. Zarodziec sierpowy (Plasmodium falciparum) – wywołuje zimnicę tropikalną, złośliwą, jest to
choroba zawsze groźna, która może przebiegać z nagle pojawiającymi się i szybko narastającymi
objawami bezpośredniego zagrożenia zycia.
2. Zarodziec ruchliwy (Plasmodium vivax) – łagodna zimnica trzydniowa, trzeciaczka typowe napady
gorączki występujące co 48 godzin.
3. Zarodziec owalny (Plasmodium ovale) – łagodna zimnica trzydniowa, trzeciaczka
4. Zarodziec pasmowy (Plasmodium malariae) – łagodna zimnica czterodniowa, czwartaczka napady
gorączki co 72 godziny
5. Nowy gatunek (Plasmodium knowlesi) – podobny do P. malariae, przebieg ciężki jak P. falciparum;
Malezja, Birma, Indonezja, Filipiny
Drogi zakażenia
ukłucie samicy komara widliszka (Anopheles )
krew zarażonej osoby – transfuzje krwi, zanieczyszczenia igły, strzykawki (gł. wśród
narkomanów)
przeszczepione zarażone narządy
inwazje wrodzone
Obraz kliniczny
okres wylęgania 8-37dni
objawy prodromalne grypopodobne
typowe napady
o cold phase – uczucie zimna, dreszcze przez 15-20 min
o hot phase – gwałtowny wzrost temp. ciała do 40-41C0, uczucie gorąca, rozgrzania,
płonienia, skóra sucha, czerwona, zaburzenia świadomości, bóle w lewym podżebrzu
o defervescence phase – ustępowanie objawów, gorączki, zlewne poty przez 1-2 godziny,
sen
9
objawy nieswoiste – silne bóle głowy, bóle mięśniowe, ok. lędźwiowej, nudności, wymioty,
wzdęcie i bóle brzucha, biegunka, nieżyt gardła, kaszel, duszność, postępujące osłabienie,
dyzunia, żółtaczka
„MASKI” – BRZUSZNA, WSZTRZĄSOWA, MOCZNICOWA
Diagnostyka
Gruba kropla krwi – parazytemia (10-40/1μl)
Cienki rozmaz krwi – gatunek (500-1000/μl)
Antygeny t. immunochromatograficznym:
o OptiMAL Rapid Malaria Test wykrywa dehydrogenazę mleczanową P. vivax i
falciporum;
o Test Para-Sight-F – swoisty antygen P. f;
o Indywidualne testy – ICT Malaria P.f
PCR – gatunki, lekooporność (1/20-50μl)
P/ciała met. immunofluorescencji
Badania dodatkowe
Morfologia krwi – niedokrwistość, wzrost liczby retikulocytów, leukopenia, rzadziej eozynofilia,
trombocytopenia
Hemoglobinuria
Żółtaczka hemolityczno – miąższowa
Hipoglikemia, hiperkaliemia
Kwasica metaboliczna
Zimnica tropikalna
Encefalopatia (zimnica mózgowa)
Obrzęk płuc
Ostra niewydolność nerek
Ciężka hemoliza wewnątrznaczyniowa
Hemoglobinuria, czarnomocz
Żółtaczka hemolityczno – miąższowa
Głęboka niedokrwistość
Hyperparazytemia > 10% krwinek zarażonych
Krwotoki z nosa i przewodu pokarmowego
Niewydolność krążenia z niedociśnieniem, wstrząsem hypowolemicznym
Hyperpyreksja
Rozsiane wykrzepianie wewnątrznaczyniowe
Kwasica metaboliczna
Hipoglikemia, hyperkaliemia
OIT
Strefa lekooporności A
Ryzyko zachorowania niskie, występuje sezonowo, na wielu obszarach nie ma go wcale, np. w
miastach
Dominuje P. vivax, występują chlorochinowrażliwe szczepy P. falciporum
Karaiby, Meksyk, Am. środkowa, niektóre regiony Bliskiego Wschodu
Strefa B
Ryzyko zachorowania umiarkowane
Bez dominacji konkretnego gatunku, coraz liczniejsze występowanie chlorochinoopornych
szczepów P. falciparum, pojawienie się chlorochinoopornych szczepów P. vivax
Subkontynent indyjski
10
Strefa C
Ryzyko zachorowania
Dominuje P. f. szczepy chlorochinooporne
Afryka subsacharyjska, Oceania, dorzecze Amazonki i Orinoko, Azja Południowo-Wschodnia
Strefa C1
Występują meflochinooporne szczepy P. f. oraz szczepy wielolekowej oporności
Wietnam, pogranicze między Kambodżą a Tajlandią, Myanmarem/ Birmą a Tajlandią
Leczenie
Chloroquine
o Arechin tabl. 250mg (150mg zasady)
o I doba 4 tabl. (600mg), po 6 godz. 2 tabl. II i III doba 1 x 2 tabl. (po 24 i 48 godz.)
Malarone
o 100mg proguanil + 250mg atovaquone
o p. wątrobowe i czerwonokrwinkowe
o 4 tabl. w jednej dawce przez 3 dni
Mefloquine – Larami a 250mg, 3 tabl. po 12 godz. 2 tabl. lub 1 x 4 tabl.
Fansidar 1 x 3 tabl., 500mg sulfadoksyny + 25mg pirymetaminy
Riamet, Coartem – 20mg asrtemeter + 120mg lumefantryny 2 x 4 tabl. przez 3 kolejne dni
Primaquina 1 x 15mg przez 10 – 14 dni, p. wątrobowe – hipnozoity P. vivax i P. ovale
Chinina dozylnie 10mg/kg w 2 – 3 dawkach (I dawka 20mg/kg m. c. ), tabl. 300mg, 3 x 2 tabl.
przez 7 – 10 dni
równolegle z doksycykliną dożylnie 2 x 100mg lub klindamycyną
Artesunate 2 mg/kg m.c./dawkę dozylnie, po 4 godz. 1mg/kg m.c./dawkę, w 24 godz. terapii i
przez 7 dni 1 x na dobę
Artemether domięśniowo przez 5 – 7 dni, I dawka uderzeniowa 3,2mg/kg m.c. , następne
1,6mg/kg m.c. co 24 godz.
Związki artemizyny, halofantryny
Zapobieganie
Likwidacja miejsc lęgowych komarów przez osuszanie zbiorników wodnych, stosowanie
środków larwobójczych
Opylanie domostw insektycydami
Programy zwalczania malarii
Indywidualna profilaktyka
Właściwa chemioprofilaktyka
Indywidualna profilaktyka
Unikanie kontaktu z komarem
Noszenie odzieży z długimi rękawami, długie spodnie, grube skarpety – jasne barwy
Repelenty
Siatki w oknach i drzwiach
Moskitiery impregnowane permetryną
Środki owadobójcze w pomieszczeniach – rozpylacze, trociczki, spirale
11
Właściwa chemioprofilaktyka
Chlorochina (Arechin) 2 tabl. (300mg) raz w tygodniu, po posiłku 1 tydzień przed, podczas, 4
tygodnie po
Chlorochina + Proguanil 2 tabl. (200mg) codziennie, po posiłku, 1 tydzień przed, podczas, 4
tygodnie po
Malarone 1 tabl. codziennie, po posiłku, 1-2 dni przed, podczas, 7 dni po
Meflochina (Lariam) 1 tabl. (250mg) raz w tygodniu, 2 tygodnie przed, podczas, 4 tygodnie po
Doxycyclina (Vibramycin) 1 kaps. (100mg) w czasie posiłku, 1 tyg. przed, podczas, 4 tyg. po,
nie dłużej niż przez 8 tyg.
Typ I
Typ II
Typ III
Typ IV
Zalecenia WHO
Ryzyko malarii
bardzo ograniczone
ryzyko P. vivax i chlorochinowrażliwych P.
falciparum
ryzyko malarii chlorochinoopornej
wysokie ryzyko P. falciparum + lekooporność lub
niskie ryzyko, ale wysoka lekooporność
Typ prewencji
ochrona przed komarami
j.w. + chlorochina
j.w. + chlorochina z proguanilem
meflochina, doxycyclina,
malarone
Cholera
Ostra choroba bakteryjna przewodu pokarmowego szerząca się epidemicznie
Epidemiologia
Źródłem zakażenia jest chory lub nosiciel
Droga zakażenia pokarmowa
o woda zanieczyszczona fekaliami
o potrawy z mięczaków, skorupiaków i ryb (owoce morza, kraby, krewetki, małże), owoce,
warzywa
o bezpośredni kontakt z chorym i przedmiotami używanymi przez chorego
Etiologia
Przecinkowiec cholery – Vibrio cholerae, pałeczka Gram-ujemna, serotyp O1, poruszająca się
świdrowatymi ruchami
Biotyp klasyczny i El-Tor
Serotyp Ogawa i Inaba
Nowy biotyp klasyczny – O139 (Indie i Bangladesz = ósma pandemia?)
Przebieg kliniczny
Okres wylęgania od kilku godzin do 5 dni
Wydalanie przecinkowców z wymiocinami i kałem przez okres choroby i kilka dni po
Zakażenia bezobjawowe, postać poronna z biegunką, łagodny nieżyt ż-jelitowy, cholera gravis
(1:10, 1:100)
Przewlekłe zakażenie dróg żółciowych trwające lata
Nagły początek bez gorączki
Stolce wodnisto-ryżowe, b. częste i w dużych ilościach, bez domieszki krwi, wydalanie bez
parcia i bólów brzucha
Obfite wymioty
Objawy odwodnienia i dyselektrolitemii
Niewydolność krążenia, nerek
cholera gravis
12
Rozpoznanie
Mikroskopowe w ciemnym polu widzenia – świderkowaty ruch
Izolacja V. cholerae O1 z kału, wymiocin, wymazu z odbytu
Testy serologiczne – miano przeciwciał vibrio-bójczych, aglutynacyjnych i anatoksycznych
Leukocytoza obojętnochłonna
Leczenie
Leżenie
Płyny wieloelektrolitowe i.v. + potas początkowo 4 – 6l. (krótko!), następnie nawadnianie
doustne (WHO oral rehydration solution, gastrolit), soki
Tetracyklina 2g jednorazowo lub przez 2 dni (dz: 50mg/kg/dobę przez 2 – 3dni)
Doksycyklina 300mg jednorazowo (dz: 6mg/kg 1 x)
Ciprofloksacyna 0,5g co 12 godz. p.o. lub 200mg co 12 godz. i.v. przez 3 – 5 dni
Dzieci:
o Erytromycyna 30mg/kg/dobę przez 3 dni
o Furazolidon 5mg/kg/dobę przez 3 dni
o Kotrimoksazol 8mg/kg/dobę przez 3 dni
o Chloramfenikol 50mg/kg/dobę co 6 godz. przez 2-3 dni
Nosicielstwo leczy się antybiotyki przez 4 – 5 dni.
Zapobieganie
Przestrzeganie zasad higieny zaopatrzenia w wodę, żywność i usuwanie nieczystości
Rygorystyczne przestrzeganie mycia rąk
Używanie do picia (kostki lodu!), mycia zębów, mycia owoców i naczyń wyłącznie wody
świeżo przegotowanej
Potrawy szczególnie z ryb i mięczaków dobrze ugotowane
Szczepionka inaktywowana – 2 dawki w odstępie 7 – 10 dni i dawka przypominająca po 6m. s.c.
(powyżej 1-go r.ż.) chroni przez 2 – 6 m-cy; skuteczność 60%, WHO nie zaleca szczepień w
rejonie epidemii
Wykrywanie i leczenie bezobjawowych nosicieli
Obowiązkowa hospitalizacja do czasu 3 ujemnych b. kału
Izolacja osób z bezpośredniej styczności 5 dni
Pełzakowica
Ameboza
Epidemiologia
500mln nosicieli
Rocznie choruje 35 – 50mln ludzi
Umiera 50mln, głównie niemowlęta, dzieci, kobiety ciężarne, niedożywieni, przewlekle ch.
Meksyk, Republika Południowej Afryki, Indie, Indonezja
Polska 2 – 5% n. rocznie 5 – 17 p. zawleczonych
W Europie np. GB 1000 przypadków rocznie gł. importowanych
Etiologia
Entamoeba histolytica – Pełzak czerwonki
Kosmopolityczny pierwotniak
Zakażenie następuje na skutek połknięcia dojrzałej cysty – postać zakaźna
W dolnym odcinku j. cienkiego z cysty uwalnia się tryfozolit, dzieli na 8 trofazoitów – postać
inwazyjna
Do jelita grubego – pogrubienia bł. śluzowej, płytkie ubytki, flaszkowate owrzodzenia
Przekształcenie w cystę, wydalane z kałem
13
Pełzakowica jelitowa
Bezobjawowa kolonizacja (90% zarażeń)
Czerwonka pełzakowa
Nieczerwonkowe pełzakowe zapalenie jelita grubego
Amoeboma – pełzakowy guz okrężnicy
Pełzakowe zwężenia
Pełzakowe zap. wyrostka robaczkowego
Przewlekłe objawy jelitowe
Czerwonka pełzakowa
Okres inkubacji powyżej 7 dni, śr. 21; Przebieg podostry, b. rzadko gwałtowny
Początek powolny, podstępny, stopniowo narasta biegunka i dyskomfort w j. brzusznej
Wodnista biegunka, krwisto-śluzowa (kał cuchnący, brak lub mało leukocytów, krew w kale
zmieniona)
Kolkowy ból brzucha, bolesna kątnica i okrężnica, bez bolesnego parcia na stolec
Z reguły bez gorączki
Ostre rozszerzenie j. grubego, perforacja, posocznica – colitis amoebica fulminans
Rozpoznawanie
Bad. mikroskopowe – na podstawie cech morfologicznych nie można odróżnić patogennych E.
histolytica od niepatogennych E. dispar
3 x badanie kału co 2 – 3 dni
w kale płynnym trofozoity zawierające krwinki czerwone, w kale uformowanym cysty
Decydują badania izoenzymatyczne i molekularne (PCR)
p/ciała sowiste klasy M i G – odczyn immunoenzymatyczny ELISA, hemaglutynacji pośredniej,
immunofluorescencji pośredniej
Badania endoskopowe – kolonoskopia ma największą wartość diagnostyczną
Badanie bioptatu – flaszkowate owrzodzenia
Badania obrazowe
Leczenie
P. jelitowe
o Nawadnianie, leki łagodzące ból
o I etap – leki pełzakobójcze
o II etap – leki kontaktowe w celu
eradykacji cyst, po zakończeniu I
etapu lub równolegle
P. pozajelitowe
o dożylne leki pełzakobójcze
o Metronidazol – 800mg co 8 godz.
Leki pełzakobójcze
Metronidazol 4 x 500mg p.o. przez 10 dni
Ornidazol 3 x 500mg p.o. przez 7 dni
Tynidazol 2 x 1000mg p.o. przez 3-5 dni
Secnidazol 4 x 500mg p.o. przez 5 dni
Leki kontaktowe
Tilbroquinol 4 x 400mg przez 10 dni
Diloksanid 3 x 500mg przez 10 dni
Paramomycyna 4 x 500mg przez 10 dni
Nosicieli powracających z tropików leczy się lekami kontaktowymi
Zapobieganie
Przestrzeganie zasad higieny osobistej i żywienia
Sprawna sieć wodno-kanalizacyjna
14
02.06.2009r. - 2
Choroby Zakaźne Pochodzenia Zawodowego
Proces Epidemiczny
proces szerzenia się choroby w populacji uwarunkowany oddziaływaniem na siebie trzech
czynników:
o czynnika chorobotwórczego
o wrażliwej populacji
o warunków środowiskowych
Źródło zakażenia: człowiek lub zwierzę, chory lub nosiciel
Drogi zakażenia: kontakt bezpośredni, przewód pokarmowy, układ oddechowy, zabiegi
inwazyjne, wektory
Ofiara zakażenia: człowiek bez odporności naturalnej lub nabytej (czynnej, biernej)
Choroba zawodowa (morbus professionalis)
jest spowodowana wyłącznie lub głównie przez szkodliwe warunki środowiska pracy. Występuje
znacznie częściej lub wyłącznie przy zawodowym narażeniu na dany czynnik niż w innych
warunkach
w znaczeniu prawnym do chorób zawodowych zalicza się choroby zamieszczone w ustawowo
przyjętym wykazie chorób zawodowych
Choroba Zawodowa
„za choroby zawodowe uważa się choroby określone w wykazie chorób zawodowych, jeżeli zostały
spowodowane działaniem czynników szkodliwych dla zdrowia występujących w środowisku pracy”
Rok
2000
2001
2002
2003
2004
2005
2006
2007
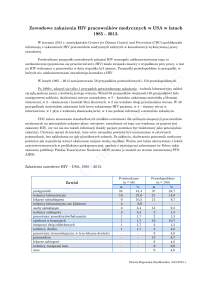
Choroby zakaźne pochodzenia zawodowego
Liczba ogółem
Choroby zakaźne pochodzenia Odsetek wszystkich chorób
zawodowego
zawodowych
7339
690
12,9
6007
715
16,2
4915
684
16,3
4365
550
16,7
3790
541
17,5
3241
615
23,8
3129
603
19,3
3295
671
20,4
Choroby zakaźne w wykazie chorób zawodowych (1)
Pozycja 26. „Choroby zakaźne lub pasożytnicze lub ich następstwa”
1) wirusowe zapalenie wątroby
2) borelioza
3) gruźlica
4) bruceloza
5) pełzakowica
6) zimnica
7) inne choroby zakaźne lub pasożytnicze
Choroby zakaźne w wykazie chorób zawodowych (2)
Pozycja 18. „Choroby skóry”
1) Drożdżakowate zapalenie skóry u osób pracujących w warunkach sprzyjających rozwojowi
drożdżaków chorobotwórczych
2) grzybice skóry u osób stykających się z materiałem biologicznym pochodzącym od zwierząt
15
Wirusowe zapalenie wątroby (WZW)
Jest ostrą chorobą zakaźną wywołaną przez następujące wirusy pierwotnie hepatotropowe:
HAV =
WZW A
B. 15
HBV =
WZW B
B. 16
HCV =
WZW C
B. 17
HDV =
WZW D
(występuje wyłącznie z HBV)
HEV =
WZW E
HGV =
WZW G
TTV =
Transfusion Transmitted Virus
Możliwe i spotykane jest zakażenie 2-3tymi wirusami równocześnie (nadkażenie lub
współzakażenie), co pogarsza rokowanie
Wirusowe zapalenie wątroby typu A
Źródło zakażenia: człowiek chorujący jawnie lub skąpoobjawowo
Droga zakażenia: feralno-oralna (dominująca), krwiopochodna, ślina
Zawodowe grupy ryzyka:
o personel medyczny
o personel zakładów zamkniętych (internaty, domu opieki, koszary. więzienia, żłobki)
o pracownicy kanalizacji i hydraulicy
o personel cywilny i wojskowy pracujący w Azji, Afryce, Ameryce Płd.
Klinicznie: żółtaczka, mdłości, wymioty, bóle brzucha, brak łaknienia – lub przebieg
bezżółtaczkowy
Rozpoznanie:
o bilirubina w surowicy ↑↑
o ALT i AST ↑↑↑
o anty-HAV IgM+ w surowicy
Hospitalizacja nie jest przymusowa
Obowiązek zgłoszenia do PPIS !
Rokowanie: nadostre zapalenie wątroby 0,1 – 0,5%; samowyleczenie bez pozostawienia
trwałego uszczerbku na zdrowiu
Zapobieganie WZW A
przestrzeganie wysokiego standardu higieny osobistej (choroba brudnych rąk!)
przestrzeganie wysokiego standardu higieniczno – sanitarnego w miejscu pracy
BEZWZGLĘDNE PRZESTRZEGANIE uniwersalnych zasad profilaktyki zakażeń
krwiopochodnych
szczepienia ochronne wg schematu: 0 – 6 m-cy
o HAVRIX 1440
o AVAXIM
UODPORNIENIE BIERNE!
o VAQTA Adult
o TWINRIX Adult (wzw A + B)
Seroprotekcja występuje u 100% szczepionych i trwa co najmniej 20 lat
SEROPROTEKCJA = anty HAV IgG+
Wirusowe zapalnie wątroby typu B
źródło zakażenia: nosiciel HBV (HBsAg), bezobjawowo lub chory z tego powodu
drogi zakażenia: krwiopochodna (zawodowa!), płciowa, odmatczyna, horyzontalna
zawodowe grupy ryzyka:
o pielęgniarki
o lekarze wszystkich specjalności
o pracownicy laboratoriów medycznych
o personel salonów kosmetycznych i tatuażu
o służby mundurowe narażone na brutalne kontakty z ludźmi
Ok. 5% personelu medycznego w Polsce jest HBV+, a 40-50% przebyło zakażenie HBV
(anty HBcIgG+)
16
Konkretne ryzyko po ekspozycji zawodowej
HBV jest obecny we krwi, nasieniu, wydzielinie pochwowej, ślinie, pocie, łzach, mleku, PMR,
płynie stawowym i puchlinowym!!!
0,00004ml
ryzyko zakażenia po zakłuciu się igłą:
o pacjent HBsAg+ HBeAg+/HBV-DNA+: 10-40%
o pacjent HBsAg+ HBeAg(-)/HBV-DNA(-): 2-10%
ryzyko zakażenia po kontakcie krwi pacjenta HBV+ z błonami śluzowymi lub skórą
nieuszkodzoną trudne do oceny liczbowej, ale prawdopodobnie wysokie
MOZLIWOŚĆ PROFILAKTYKI PRZED- I POEKSPOZYCYJNEJ
klinicznie osłabienie, brak łaknienia, objawy „grypowe”, bóle brzucha, żółtaczka
rozpoznanie:
o bilirubina w surowicy ↑
o ALT i AST ↑↑↑
o anty-HBcIgM+, HBsAg+, HBeAg+
hospitalizacja nie jest przymusowa
obowiązek zgłoszenia do PPIS!
rokowanie: nadostre wzw B 0,5 – 1%; samowyleczenie 80 – 90%; przetrwanie zakażenia HBV
ponad 6 m-cy i rozwój następstw 10 – 20%
HBsAg
+
HBeAg
HBV-DNA
HBsAg nb
anty HBcIgG+
HBsAg nb
anty HBs +>10j/l
Markery serologiczne WZW B
zakażenie HBV (ostre lub przewlekłe)
znaczna replikacja HBV
znaczna zaraźliwość chorego
aktywna choroba wątroby
znaczna replikacja HBV
znaczna zaraźliwość chorego
aktywna choroba wątroby wymagająca leczenia
zakres: 2000-100x106 kopii/ml
NAJWAZNIEJSZY MARKER HBV!!!
stan po przebyciu zakażenia HBV
- nie trzeba szczepić
seroprotekcja po szczepieniu
przeciwko wzw B
Zapobieganie WZW B
STAŁE BEZWZGLĘDNE STOSOWANIE uniwersalnych zasad profilaktyki zakażeń
krwiopochodnych
Szczepienia ochronne wg schematu: 0-1-6m-cy przed podjęciem pracy zawodowej
o ENGERIX B 10μg, 20μg
o HB VAX II 5Μg, 10μg
seroprotekcja
o H-B-Vax PRO 40μg
u 40-95%
o Hepavex-Gene
szczepionych
o Euvax B
Immunoglobulina swoista HBIG; po ekspozycji zawodowej: Hepatest
Wysoki standard higieny indywidualnej i wysoki standard higieniczno – sanitarny miejsca oraz
stanowiska pracy
17
Wirusowe zapalenie wątroby typu C
Źródło zakażenia: nosiciel HVC, bezobjawowo lub chory z tego powodu (~1,5%)
Drogi zakażenia: krwiopochodna (zawodowa!), płciowa, odmatczyna, horyzontalna
Zawodowe grupy ryzyka:
o pielęgniarki i lekarze wszystkich specjalności
o pracownicy laboratoriów medycznych
o personel salonów kosmetycznych i tatuaży
o służby mundurowe narażone na brutalne kontakty z ludźmi
SZACUNKOWO 5% personelu medycznego ma anty-HCV
HVC jest obecny we krwi, ślinie, spermie, wydzielinie pochwowej i w każdym materiale
biologicznym zawierającym krew
ryzyko zakażenia po zakłuciu się igłą:
o pacjent HCV-RNA+
~10%
ryzyko zakażenia po kontakcie krwi pacjenta HCV+ z błonami śluzowymi lub skórą
nieuszkodzoną: trudne do oceny liczbowej, ale prawdopodobnie niskie – lecz MOŻLIWE
NIE MA SWOISTEJ PROFILAKTYKI !
Klinicznie: 95% przypadków przebiega bezżółtaczkowo i skąpoobjawowo
Rozpoznanie: często przypadkowo, przy próbie oddania krwi lub w badaniach okresowych
o ALT i AST ↑/↑↑
o anty-HCV+ (pojawiają się późno!)
Hospitalizacja nie jest przymusowa
Obowiązek zgłoszenia do PPIS !
Rokowanie: nadostre wzw C jest rzadkie; samowyleczenie 20%; przetrwanie zakażenia HCV
ponad 6m-cy i rozwój następstw 80%
HCV-RNA OBECNY WE KRWI POTWIERDZA ROZPOZNANIE
Markery serologiczne WZW C
Anty HCV prawdopodobne zakażenie HCV lub stan po przebyciu WZW C ale:
anty HCV mogą być fałszywie dodatnie u osób z chorobami autoimmunologicznymi
anty HCV pojawiają się niekiedy wiele tygodni (nawet 26) po wzw C
u 7-10% zakażonych anty-HCV są trudne do wykrycia lub ich nie ma
HCV-RNA met. RT PCR z całkowitą pewnością potwierdza trwające zakażenie HCV i jego replikację,
umożliwia oznaczenie genotypu i wiremii
HCV-RNA może być oznaczany
Zapobieganie WZW C
STAŁE BEZWGLĘDNE STOSOWANIE uniwersalnych zasad profilaktyki zakażeń
krwiopochodnych
wysoki standard higieny osobistej i wysoki standard higieniczno – sanitarny miejsca oraz
stanowiska pracy
NIE ISTNIEJE I NIE BĘDZIE SKONSTRUOWANA W NAJBLIŻSZYM CZASIE ANI
SZCZEPIONKA ANI IMMUNOGLOBULINA ANTY-HCV !
Wirusowe zapalenie wątroby typu D
Źródło zakażenia: nosiciel HBV i HDV, bezobjawowy lub choru z tego powodu
Drogi zakażenia: identyczne jak dla HBV
Zawodowe grupy ryzyka: identyczne jak dla HBV
Klinicznie:
o nadważenie HDV osoby HBV+ = zaostrzenie choroby
o współzakażenie HBV i HDV – cięższy przebieg wzw, 50% procentowe ryzyko
przewlekłego zakażenia HBV+HDV
Profilaktyka: zapobieganie HBV chroni przed HDV
W POLSCE ZAKAŻENIE HDV JEST BARDZO RZADKIE
18
Inne typy wirusowych zapaleń wątroby
Kolejność odkryć wirusów pierwotnie hepatotrpowych
HBV
1968r (nagroda Nobla!)
HDV
1977r
HAV
1978r
HCV
1988r
HEV
1990r daleki Wschód, Afryka
HGV
1995r brak rutynowej diagnostyki
TTV
1997r wykryty w Japonii, brak diagnostyki
……
????
Zakażenie HEV, HCV, TTV wymaga NIESTANDARDOWEJ diagnostyki w specjalnych przypadkach
Wirusy CMV, EBV, HSV, VZV, Adenowirusy TAKŻE mogą powodować zawodowe zapalenia
wątroby
Przewlekłe wirusowe choroby wątroby
Przewlekłe wirusowe zapalenie wątroby typu B lub C
co najmniej 6 miesięczne udokumentowane trwanie zakażenia HBV/HCV i choroby wątroby
badania molekularne HBV z wiremią; HCV z genotypem i wiremią
ocena histopatologiczna biopunktatu wątroby met. Scheura (G… S…)
Marskość wątroby pozapalna B lub C
aktywna marskość wątroby: diagnostyka j. w.
dokonana marskość wątroby z objawami niewydolności: endoskopia, USG dopplerowskie
HEPATOMA:
USG co 6 miesięcy, TK, MR
AFP co 6 miesięcy
Zespoły pozawątrobowe u zakażonych przewlekle HBV/HCV
choroby krwi: trombocytopenia, leukopenia, aplazja szpiku
choroby skóry: porfiria skórna późna, liszaj płaski, bielactwo, rumień guzowaty
choroby reumatoidalne: zapalenia stawów, myalgia rheumatica
Guzkowe zapalenie tętnic
Krioglobulinemia typu mieszanego
Zespół Guillaina-Barrego
WSZYSCY CI CHORZY MOGĄ STANOWIĆ ŹRÓDŁO ZAKAŻENIA HBV/HCV DLA
PERSONELU MEDYCZNEGO
Borelioza
Klinika: jedynym typowym objawem jest rumień wędrujący w kilka- kilkanaście dni po ukąszeniu przez
kleszcza (I faza)
II faza:
limfocytowe zapalenie opon
porażenie nn. twarzowych i innych
zapalenie korzeni rdzeniowych
zapalenie stawów
zapalenie mięśnia sercowego
III faza:
późne zmiany skórne i neurologiczne
Rozpoznanie:
stwierdzenie swoistych przeciwciał met. ELISA w klasie IgM (I faza)
stwierdzenie swoistych przeciwciał w klasie IgG+IgM (II faza)
TEST POTWIERDZENIA (Western-blot) JEST OBOWIĄZKOWY
19
Rozpoznanie rumienia wędrującego nie wymaga badań serologicznych (50% wyników fałszywie
ujemnych)
Podejrzenie neuroinfekcji boreliozowej wymaga hospitalizacji (przymus prawny)
Obowiązek hospitalizacji innych przypadków nie istnieje, ale rozpoznanie wymaga warunków
szpitalnych (koszty, test potwierdzenia)
Borelioza wymaga zgłoszenia do PPIS
WCZESNA PRAWIDŁOWA ANTYBIOTYKOTERAPIA GWARANTUJE WYLECZENIE
Zapobieganie
noszenie szczelnego obuwia i ubrania w czasie pracy w lesie
dokładna kontrola ciała po powrocie z lasu w celu wykrycia kleszczy
wczesne usuwanie kleszcza ze skóry, odkażenie i opatrznie miejsca ukłucia
używanie środków odstraszających kleszcze (repelentów)
antybiotykoterapia poekspozycyjna nie jest zalecana w Europie, ale dopuszczalna w USA
NIE ISTNIEJE ANI SZCZEPIONKA ANI IMMUNOGLOBULINA SWOISTA
OBSERWUJE SIĘ U LEKARZY ZBYTNIĄ ŁATWOŚĆ ROZPOZNANIA BORELIOZY
20
03.06.2009r. - 1
Choroby wysypkowe
Odra – mobilli
Czynnik etiologiczny – Morbillivirus – Rodzina – Paramyksoviridae
Droga zakażenia – kropelkowa
Okres wylęgania – 9 – 11 dni
Zakaźność – okres nieżytowy i 3 dni po wystąpieniu wysypki
Obraz kliniczny
Okres nieżytowy (2-4dni): ostry metaliczny kaszel, nieżyt nosa, zapalenie spojówek,
światłowstręt, gorączka, złe samopoczucie, plamki Koplika (2 dni przed wysypką, znikają w
ciągu 3 dni okresu wysypkowego)
Okres wysypkowy (3-5 dni): wysypka grubo-plamisto-grudkowa; nie swędząca; ma charakter
zstępujący; pozostawia po sobie skórę lamparcią i drobnootrębiaste łuszczenie naskórka;
Inne objawy: zapalenie gardła, zapalenie węzłów chłonnych szyjnych, wymioty, biegunka
Następstwa odry – wczesne
zapalenie płuc – pierwotne, wtórne
zapalenie ucha srodkowego
podgłośniowe zapalenie krtani z suchym, szczekającym kaszlem
zapalenie mózgu, zapalenie opon m-rdz, poprzeczne zapalenie rdzenia
Następstwa odry – późne
powolne stwardniające zapalenie istoty białej mózgu – SSPE
stwardnienie rozsiane
Powikłania odry w krajach uprzemysłowionych
Rodzaj powikłania
U kogo występuje
Częstość występowania
Zapalenie ucha środkowego
7 – 9%
Zapalenie płuc
Częściej u dzieci poniżej 1 roku
1–6%
życia
Zapalenie mózgu
Częściej u dorosłych
1 na 1000 przypadków odry
Podostre stwardniejace zapalenie Średnio 7 lat po przechorowaniu 1 na 100 000 przypadków odry
istoty białej mózgu (SSPE)
odry
Zgon
1 – 3 na 1000 przypadków
Profilaktyka
Czynna: dwukrotne szczepienie
- w 2 roku życia MMR
- w 10 roku życia MMR
Bierna:
- Hyperimmunizowana, poliwalentna immunoglobulina podana do 72 godz. od kontaktu z osobą
chorującą
Różyczka – Rubeolla
Czynnik etiologiczny – Togavirus – Rodzina – Tovaviridae
Droga zakażenia – kropelkowa
Okres wylęgania – 14 – 21 dni
Zakaźność – 3 dni przed wysypką i 4 dni okresu wysypkowego
21
Obraz kliniczny
Przebieg często bezobjawowy (25-50%0
Łagodny przebieg: okres nieżytowy nie zawsze występuje, wysypka plamisto grudkowa nie
swędząca, pojawiająca się na całym ciele
Wysypka utrzymuje się 12 godz. – 5 dni
Ustępuje bez pozostawienia śladów
Charakterystyczne powiększenie węzłów chłonnych potylicznych, karkowych, zausznych
Powikłania
Przemijające zapalenie stawów (0,5-15% przypadków różyczki)
Małopłytkowa skaza krwotoczna (1/3000 przypadków)
Zapalenie mózgu (1/6000 przypadków)
Zakażenie wewnątrzmaciczne
Zespół różyczki wrodzonej (ZRW):
Zespół różyczki wrodzonej występuje w 1/1000 urodzeń i stanowi 5 – 10% wszystkich wad
wrodzonych
Wady wrodzone to: zaćma, mikrooftalmia, jaskra, niedorozwój tęczówki, zmętnienie rogówki,
wady serca, zahamowanie rozwoju umysłowego, głuchota, heptaosplenomegalia, zmiany
radiologiczne w kościach długich, plamica małopłytkowa
Śmiertelność w ZRW – ponad 15%
Ryzyko wystąpienia różyczki wrodzonej
Zakażenie wewnątrzmaciczne
Tydzień ciąży
Ryzyko embriopatii
1-6
56%
7-9
25%
10 - 12
15%
13 - 21
10 - 15%
powyżej 22
spadek do 0
Przebycie różyczki na kilka tygodni przed zapłodnieniem może mieć wpływ na powstanie wad u płodu,
a nawet utratę ciąży
Profilaktyka
Czynna:
- Szczepienia w 2 roku życia MMR
- Szczepienia w 10 roku życia MMR
Bierna:
- Dotyczy kobiet ciężarnych i osób z zaburzeniami immunologicznymi – podawanie
hyperimmunizowanej poliwalentnej immunoglobuliny do 72 godz. po kontakcie z osobą chorą
Varicella-zoster:
jeden wirus – dwie choroby
Wirus varicella-zoster – Rodzina Herpesviridae
- Ospa wietrzna
- Półpasiec
22
Ospa wietrzna (varicella)
Roczna liczba zachorowań – Ogółem na Świecie: 90mln
o USA – 4mln
o Polska – 130tys
Drogi zakażenia
o Inhalacja zakażonej wydzieliny na drodze kropelkowej
o Bezpośredni kontakt z osobą chorą
o Zakażenie przezłożyskowe
Okres wylęgania – 14 – 21 dni
Zakaźność – 1 – 2 dni przed wysypką do przyschnięcia pęcherzyków w strupki
Objawy kliniczne
Wzrost temperatury ciała bez uchwytnej przyczyny
Wysypka skórna – swędząca, umiejscowiona dośrodkowo, zajmująca skórę owłosioną i błony
śluzowe, dośrodkowe części ciała, polimorfizm zmian (grudka, pęcherzyk, krostka, strupek,
blizenka)
Po odpadnięciu strupków i wyrównaniu blizenki nie pozostają trwałe ślady
Powikłania
Powikłania ogólnoustrojowe
o Powikłania neurologiczne
zapalenie mózgu pod postacią zapalenia móżdżku
porażenie nn. Czaszkowych, zapalenie opon m-rdz
zespół Guillain-Barre
poprzeczne zapalenie rdzenia
o Inne powikłania ogólnoustrojowe
posocznica
Zapalenie płuc (pierwotne i wtórne)
zapalenie ucha środkowego i zatok obocznych nosa
Zapalenie tkanki łącznej podskórnej
małopłytkowość
Powikłania miejscowe
zapalenie spojówek i rogówki z nastepową ślepotą
ropniem, czyraki, szpecące, trwałe blizny na skórze
Zgon w następstwie choroby
Ospa wrodzona – pierwotne zakażenie VZV w I i II trymestrze ciąży
zakażenie płodu
o ryzyko urodzenia martwego dziecka
o poronienie
o poród przedwczesny
o urodzenie dziecka o niskiej masie ciała
o urodzenie dziecka z zespołem wrodzonej ospy płodu
Zespół ospy wrodzonej
Trwałe blizny skórne
Zaburzenia wykształcenia kończyn
Zaburzenia w obrębie oczu
Zaburzenia w OUN
Ospa noworodkowa
Zakażenie matki wcześniej niż 6 dni przed porodem
o wytworzenie ochronnych przeciwciał w klasie IgG chroniących płód
Zakażenie matki od 5 dni przed porodem do 2 dni po porodzie – ospa noworodkowa
23
Profilaktyka
Czynna:
- Szczepionka przeciwko ospie wietrznej (w Polsce zarejestrowana – Varilrix)
Bierna:
- Hyperimmunizowana immunoglobulina monowalentna – Varitect podana do 72 godz. po
kontakcie z osobą chorującą
Zakażenie HSV
HSV – 1 (HHV – 1) – Hermes labialis – opryszczka wargowa
HSV – 2 (HHV – 2) – Hermes genitalia – opryszczka narządów płciowych HSV – 1
Postacie kliniczne zakażenia pierwotnego
opryszczkowe zapalenie jamy ustnej i dziąseł
wyprysk opryszczkowy
opryszczkowe zakażenie błon śluzowych i skóry zewnętrznych narządów płciowych
opryszczka noworodków
opryszczkowe zapalenie mózgu i opon mózgowo-rdzeniowych
opryszczkowe zapalenie spojówek i rogówki
Płonica – scarlatina
Czynnik etiologiczny – paciorkowiec β – hemolizujący grupy A
Droga zakażenia – kropelkowa
Okres wylęgania – 1 – 5 dni
Zakaźność – 3 dni po wystąpieniu wysypki do 24 godz. po rozpoczęciu antybiotykoterapii
Obraz kliniczny:
Nagły początek z bólami brzucha, wymiotami
Wzrost temperatury ciała
Na skórze wysypka drobno-plamisto-grudkowa, nie swędząca, zajmuje całe ciało pacjenta z
wyjątkiem trójkąta nosowo-brudkowego, zlewająca się, pozostawia po sobie grubopłatowe
łuszczenie naskórka
Dodatni objaw Pastii i inne objawy naczyniowe
W jamie ustnej – język malinowy
Następstwa
Wczesne
o ropień około migdałkowy
o śródmiąższowe zapalenie nerek
Późne
o kłębkowe zapalenie nerek
o Zapalenie mięśnia sercowego
o Zapalenie stawów
Leczenie
antybiotykoterapia – penicyliny, makrolidy
leki przeciwgorączkowe
leki przeciwhistaminowe
24
03.06.2009r. - 2
Ropne zapalenie opon mózgowo – rdzeniowych
Ropne zapalenie opon mózgowo – rdzeniowych i mózgu jest ostrą chorobą zakaźną:
o etiologii bakteryjnej
objawiającą się stanem zapalnym opony miękkiej i pajęczynówkowej mózgu i rdzenia, oraz
wypełnionej płynem m-rdz przestrzeni międzyoponowej
występującą endemicznie za skłonnością do zaostrzeń epidemicznych
objętą obowiązkiem diagnostyki i leczenia w warunkach szpitalnych
Podział:
Pierwotne – ograniczone wyłącznie do OUN
Wtórne – ogniska pierwotne poza OUN (zatoki oboczne nosa, migdałki podniebienne, zastawki
serca, skóra)
Drogi zakażenia:
kropelkowa
naczyń krwionośnych
naczyń chłonnych
bezpośredni kontakt przez blaszkę sitową do jamy czaszki
Etiologia:
Anaerobem
o Peptostreptococcus species
o Bacteroides fragilis
o Bacteroides thetaiotaomicron
Gram-Positives
o Methicillinsusceptible Staphylococcus aureus (MSSA)
Gram-Negatives
o Escherichia coli
o Haemophilus influenzae
o Proteusz mirabillis
Etiologia RZOM w zależności od wieku
Noworodki < 2m-ca życia
Dzieci starsze > 2m-ca
Osoby dorosłe
Bakterie Gram (-)
Streptococcus Pneumoniae
Neisseria meningitidis
50 – 60%
35 – 45%
30 – 45%
Paciorkowiec grupy B
Neisseria meningitidis
Streptococcus pneumoniae
10 – 25%
30 – 40%
10 – 30%
L. Monocytogenes
Haemophilus influenzae
S. aureus, S. epidermidis
2 – 10%
10 – 20%
5 – 15%
S. aureus, S. epidermidis
S. aureus, S. epidermidis
L. Monocytogenes
5%
5%
5%
RZOM – zależność pomiędzy etiologią, a czynnikami predysponującymi
ostre zapalenie ucha środkowego, zapalenie zatok, zapalenie płuc – S. pneumoniae, HIB
uraz czaszki z płynotokiem nosowym – S. pneumoniae, HIB, (skłonność do nawrotów)
uraz czaszki penetrujący do mózgu – S. aureus, S. epidermidis, pałeczki G(-)
zaburzenia odporności komórkowej – L. monocytogenes
zabieg neurochirurgiczny – P. aeruginisa, S. aureus (często metycylinooporny) MRSA
alkoholizm i wiek > 60lat – S. pneumoniae
25
Diagnostyka
podstawowym badaniem w diagnostyce zapaleń opon m-rdz jest badanie płynu m-rdz
uzyskanego drogą punkcji lędźwiowej
punkcja lędźwiowa wykonywana jest w warunkach szpitalnych
punkcja lędźwiowa poprzedzona powinna być badaniem okulistycznym dna oka i badaniem
neurologicznym,
Przeciwwskazania do wykonania nakłucia lędźwiowego
kliniczne objawy znacznego wzrostu ciśnienia śródczaszkowego
objawy ogniskowego uszkodzenia OUN (niedowłady, porażenia)
udar, guz mózgu
ciężka niewydolność krążeniowo – oddechowa
zmiany ropne w okolicy wkłucia
zaburzenia krzepnięcia
Powikłania nakłucia lędźwiowego
wgłobienie pnia mózgu i migdałków móżdżku do otworu wielkiego – zejście śmiertelne pacjenta
Zespół popunkcyjny
o objawy: bóle głowy, wymioty, sztywność karku
o przyczyna: podciśnienie PMR w następstwie jego wycieku do przestrzeni nad- lub
podtwardówkowej przez nieobkurczający się otwór po nakłuciu opony
o leczenie: podanie dużej ilości płynów (często drogą dożylną), leki przeciw bólowe,
leżenie w łóżku
Badanie płynu m-rdz
Rodzaj komórek
Białko (mg%)
limfocyty
< 45
granulocyty
↑
Płyn m-rdz
Prawidłowy
Ropny
L. kom w 1 mm3
<4
kilkakilkadziesiąt tys.
Wirusowy
kilkaset
limfocyty
N/↑
(0)
N
Gruźliczy
do 1000
limfocyty
↑
↓
(> 200)
Glukoza (MG%)
> 40
↓
Diagnostyka bakteriologiczna
badanie płynu m-rdz
o bakterioskopia bezpośrednia po wybarwieniu metodą Grama
o szybkie testy lateksowe określające antygeny bakteryjne
o posiew płynu m-rdz i uzyskanie antybiogramu
posiew krwi i uzyskanie antybiogramu
wymaz z gardła i ewentualnych ognisk ropnych poza OUN
Morfologia krwi – leukocytoza
białka ostrej fazy zapalnej (CRP, Prokalcytonina)
Stężenie kwasu mlekowego w PMR
Obrzęk mózgu w RZOM
Toksyczny – zaburzenia metabolizmu komórkowego spowodowane hipoksemią,
niedociśnieniem, niedokrwieniem, prowadzące do zaburzeń elektrolitowych i uwolnienia
substancji neuroprzekaźnikowych
Naczyniowy – wzrost przepuszczalności bariery krew/płyn m-rdz i przenikanie surowiczych
makromolekuł do PMR
Śródmiąższowe – wzrost oporu odpływu PMR z powodu upośledzenia jego resorpcji przez
ziarnistości pajęczynówki powoduje zaburzenia w przepływie krwi przez naczynia mózgowe co
doprowadza do niedotlenienia tkanki mózgowej i kwasicy
26
Symptomatologia:
gorączka do 39-40OC z dreszczami
silne, rozlane bóle głowy nieustępujące po lekach przeciwbólowych, u małych dzieci niepokój i
długotrwały płacz
nudności i wymioty niezależnie od przyjmowania posiłków
zaburzenia świadomości
o zamroczenia, całkowita utrata przytomności
pobudzenie psychoruchowe z przeczulicą
szybko narastające cechy wstrząsu septycznego
o sinica, duszność, zlanie zimnym potem, spadek RR
drgawki kloniczno toniczne (głównie u dzieci), stan padaczkowy
afazja – motoryczna lub mieszana
badaniem przedmiotowym
o dodatni zespół objawów oponowych
ułożenie odgięciowe
u niemowląt uwypuklone, tętniące, napięte ciemię przednie
Efekt leczenia RZOM zależy od:
wieku pacjenta
czasu jaki upływa od początku choroby do włączenia leczenia
czynnika etiologicznego
Schemat leczenia RZOM
leki przeciwzapalne
o preparaty sterydowe np. dexamethazon
o niesterydowe leki przeciwzapalne
antybiotykoterapia – antybiotyki bakteriobójcze, szerokowidmowe, przenikające przez barierę
krew/płyn m-rdz
o Cefalosporyny III generacji
Ceftriakson (Rocephin)
Ceftazidim (Fortum)
o Penicyliny półsyntetyczne o szerokim spektrum działania
Carbenicylina, Azlocylina, Piperacylina
o Penicylina krystaliczna
o Przy braku skuteczności leczenia dodatkowo Aminoglikozydy
Netromycyna
Amikacyna
Leki przeciwobrzękowe: 20% Mannitol, Dexaven, Furosemid
Leki przeciwdrgawkowe: Relanium, lub Luminal, lub Rivotril
Cechy „dobrego” antybiotyku:
Aktywność przeciwbakteryjna – 85% ropnych zapaleń opon m-rdz w naszej szerokości
geograficznej jest wywołanych przez S. pneumoniae i N. meningitidis, aktywność
przeciwbakteryjna stosowanych leków musi być skierowana przeciw tym patogenom
Bakteriobójczość, terapia szerokowidmowa (monoterapia wyjątkowo, nigdy jako leczenie
pierwszego rzutu)
Przenikanie antybiotyku przez barierę krew-mózg i jego stężenie w PMR. Penetracja
antybiotyków przez tę barierę jest uwarunkowana wielkością cząsteczki leku oraz obecnością
stanu zapalnego. W wyniku skutecznego leczenia stopniowo łagodnieje stan zapalny, ale
jednocześnie przenikanie leków przez barierę krew-mózg ulega zmniejszeniu
Dawkowanie i droga podania (maksymalne i pozajelitowe) – antybiotyki uważane za dobrze
przenikające do PMR osiągają w nim ok. 50% stężenia w surowicy. Uzyskanie stężeń
terapeutycznych w OUN wymaga więc zastosowania najwyższych możliwych dawek
27
Antybiotykoterapia w RZOM
Narastanie oporności na klasyczne antybiotyki oraz wysoka śmiertelność w RZOM, są
przyczyną poszukiwania nowych leków.
Należą do nich, niedostępne w Polsce:
o telavancin (TD-6424) – nowy lipoglikopeptyd o znacznej aktywności wobec wysoce
opornych pneumokoków (33) oraz
o daptomycin – nowy antybiotyk lipopeptydowy
Inne niż antybiotykoterapia metody terapeutyczne. Niesteroidowe leki przeciwzapalne
ograniczają aktywność mediatorów zapalenia i skutki ich działań w zakresie OUN. W fazie
badań klinicznych pozostają antyoksydanty, czy inhibitory metaloproteinaz
Schemat leczenia RZOM c. d.
leki przeciwbólowe i przeciwgorączkowe
immunoterapia: hyperimmunizowane immunoglobuliny dożylne np. Sandoglobulina
w przypadku współistnienia zespołu DIC – heparyna, osocze antyhemofilowe
nakłucie lędźwiowe w 1, 3, 5, 7 … dniu hospitalizacji połączone z doskonałym podaniem leków:
glikokortykoidy (przeciwobrzękowo, przeciwzapalnie, przeciwzlepnie), antybiotyki??
Następstwa RZOM
Zaburzenia neuroradiologiczne
o wodogłowie wewnętrzne
o zarostowe zapalenie pajęczynówki
o poszerzenie przestrzeni płynowych zewnątrzmózgowych
wodniaki podoponowe
wodogłowie zewnętrzne
o ogniskowe uszkodzenie tkanki mózgowej
ropnie mózgu
ogniska krwotoczne i niedokrwienne
blizny oponowo-mózgowe
o zaniki korowe i/lub korowo-podkorowe
Zaburzenia neurologiczne
o uszkodzenie nerwów czaszkowych
o zaburzenia słuchu
o padaczka
Zmiany psychopatologiczne
Zgon
28