PRACE POGL¥DOWE
Aleksandra WYCZA£KOWSKA-TOMASIK
Jolanta ¯EGARSKA
£añcuchowa reakcja polimerazy w czasie
rzeczywistym zastosowanie w badaniach
naukowych i diagnostyce medycznej
Real-time polymerase chain reaction applications
in research and clinical molecular diagnostics
Klinika Immunologii, Transplantologii i Chorób
Wewnêtrznych, Instytut Transplantologii,
Warszawski Uniwersytet Medyczny
Warszawa, Polska
Kierownik: Prof. dr hab. n. med. Leszek P¹czek
Dodatkowe s³owa kluczowe:
PCR w czasie rzeczywistym
badania naukowe
diagnostyka medyczna
ekspresja genu
³adunek wirusów
³adunek bakterii
Additional key words:
real time PCR
research
clinical molecular diagnostics
gene expression
viral load
bacterial load
Adres do korespondencji:
Dr n. med.
Aleksandra Wycza³kowska-Tomasik
Klinika Immunologii, Transplantologii i Chorób
Wewnêtrznych
Instytut Transplantologii
02-006 Warszawa, ul. Nowogrodzka 59
Tel.: 0225021190; Fax.: 0225022127
e-mail: [email protected]
Przegl¹d Lekarski 2009 / 66 / 4
Ostatnie lata przynios³y szybki rozwój jednej z technik biologii molekularnej, ³añcuchowej reakcji polimerazy w czasie rzeczywistym (ang. real
time polymerase chain reaction, real
time PCR). Zosta³a ona wprowadzona
do powszechnego u¿ytku. Za pomoc¹
PCR w czasie rzeczywistym mo¿na
wykryæ i okreliæ ilociowo bardzo
ma³e iloci specyficznych sekwencji
kwasów nukleinowych. W badaniach
naukowych g³ównym zastosowaniem
tej metody jest szybka i dok³adna detekcja zmian w ekspresji genów, bêd¹cej wyrazem mechanizmów fizjologicznych lub patofizjologicznych. Dla
celów klinicznych metodê tê wykorzystuje siê do pomiaru ³adunku wirusów
lub bakterii, b¹d oceny statusu nowotworowego.
Resent years have brought fast
development of one of the molecular
biology methodology, real time
polymerase chain reaction. It has been
introduced in common use. Real time
PCR allows to detect and qualify very
small amounts of specific nucleic acid
sequences. As a research tool, a major application of this method is the
rapid and accurate detection of genes
expression changes as a result of
physiological and pathophysiological
mechanisms. In clinical diagnostics,
this method is used to measure viral
or bacterial load or to assess cancer
status.
W ostatnich latach nast¹pi³ gwa³towny
rozwój jednej z technik biologii molekularnej, ³añcuchowej reakcji polimerazy w czasie rzeczywistym (ang. real time polymerase chain reaction, real time PCR) i zosta³a
ona wprowadzona do powszechnego u¿ytku. Za pomoc¹ PCR w czasie rzeczywistym
mo¿na wykryæ i okreliæ ilociowo bardzo
ma³e iloci specyficznych sekwencji kwasów
nukleinowych. W badaniach naukowych
g³ównym zastosowaniem tej metody jest
szybka i dok³adna detekcja zmian w ekspresji genów, bêd¹cej wyrazem mechanizmów fizjologicznych lub patofizjologicznych. Dla celów klinicznych metodê tê wykorzystuje siê do pomiaru ³adunku wirusów
lub bakterii, b¹d oceny statusu nowotworowego.
PCR w czasie rzeczywistym jest oparta
na rewolucyjnej metodzie PCR, pozwalaj¹cej na amplifikacjê fragmentu DNA ponad
bilion razy, opracowanej przez Kary'ego
Mullisa w po³owie lat osiemdziesi¹tych XX
wieku [13,23,25]. Za to odkrycie w 1993 roku
otrzyma³ on Nagrodê Nobla w dziedzinie
chemii [13,23].
PCR, tak¿e PCR w czasie rzeczywistym,
wykorzystuje polimerazê DNA w celu amplifikacji specyficznego fragmentu DNA oraz
primery, czyli krótkie, specyficzne dla danej
sekwencji oligonukleotydy. Reakcja PCR
sk³ada siê z powtarzaj¹cych siê cykli, a ka¿dy z nich z³o¿ony jest z trzech faz. Pocz¹tkowo, w temperaturze 95oC dochodzi do
rozpadu podwójnej nici DNA na dwie pojedyncze nici (denaturacja). Nastêpnie temperatura jest obni¿ana do oko³o 50-75oC i
do pojedynczej nici DNA, tzw. matrycy, przy³¹czaj¹ siê primery (przy³¹czanie, ang. annealing). W kolejnym etapie polimeraza
DNA w temperaturze 72-78oC rozpoczyna
ich wyd³u¿anie, poprzez dobudowanie pojedynczych komplementarnych nukleotydów
(wyd³u¿anie) i w ten sposób powstaje nowa
niæ DNA [17]. Przed nastêpnym cyklem PCR
nowe dwuniciowe DNA musi ulec ponownie
degradacji. Takich cykli PCR jest kilkadziesi¹t, a reakcja zachodzi w termocyklerze.
Zak³adaj¹c, ¿e skutecznoæ reakcji jest idealna, iloæ specyficznego dwuniciowego
DNA by³aby podwojona po ka¿dym cyklu
PCR. Poniewa¿ polimeraza DNA nie mo¿e
u¿yæ RNA jako matrycy, potrzebny jest wówczas inny enzym odwrotna transkryptaza,
który podczas reakcji odwrotnej transkrypcji na matrycy RNA syntetyzuje pojedyncz¹
komplementarn¹ niæ DNA.
PCR w czasie rzeczywistym, w odró¿nieniu od klasycznego PCR, posiada system monitoruj¹cy zaawansowanie amplifikacji przy pomocy technologii fluorescencyjnej. Prekursorami badania kinetyki reakcji
PCR byli Higuchi i wsp. [13,25]. W 1992 roku
stworzyli oni system zdolny do detekcji produktów PCR podczas ich akumulacji. System ten zawiera³ w mieszaninie reakcyjnej
interkaluj¹c¹ cz¹steczkê bromku etydyny.
Termocykler zaadaptowano do nawietlania
209
próbek wiat³em UV. Detekcja powsta³ej fluorescencji natomiast odbywa³a siê przy u¿yciu po³¹czonej z komputerem kamery
[10,11,25]. Podczas amplifikacji wzrasta³a
iloæ dwuniciowego DNA (dsDNA), z którym interkalowa³ bromek etydyny. Wi¹za³o
siê to ze wzrostem fluorescencji. Wynikiem
by³ wykres zale¿noci miêdzy fluorescencj¹ a numerem cyklu.
Bromek etydyny szybko zast¹piono
mniej toksycznym, bardziej specyficznym i
bardziej czu³ym barwnikiem fluorescencyjnym SYBR Green I. Barwnik ten ³¹czy siê z
dsDNA, nie wi¹¿e siê natomiast z jednoniciowym DNA (ssDNA). W wyniku po³¹czenia barwnika z DNA nastêpuje wzrost fluorescencji. Ograniczeniem tej metody jest
fakt, ¿e SYBR Green I rozpoznaje równie¿
sekwencje niespecyficzne, wynikiem tego
jest przy³¹czanie siê barwnika do ka¿dej
dwuniciowej cz¹steczki DNA. W celu wyeliminowania wszelkich nieprawid³owoci
procesu stosuje siê analizê krzywej topnienia, która pozwala odrzuciæ produkty niespecyficzne [16,25].
Problem specyficznoci fluorescencyjnej amplifikowanego fragmentu zosta³ rozwi¹zany poprzez zastosowanie specyficznych sond znakowanych fluorescencyjnie.
Obecnie w metodzie real-time PCR oprócz
barwników interkaluj¹cych DNA bromku
etydyny i SYBR Green I wykorzystuje siê
sondy hybrydyzuj¹ce, np. Fluorescence
Resonance Energy Transfer (FRET),
TaqMan, Molecular Beacons, Scorpions,
TaqMan Minor Groove Binder (TaqMan
MGB; pol. wi¹¿¹ca mniejsz¹ bruzdê)
[16,17,25]. W zale¿noci od zastosowanej
sondy mamy do czynienia z ró¿nym przebiegiem reakcji. Zostanie ona omówiona na
przyk³adzie sondy TaqMan.
Metoda ta oparta jest na zastosowaniu
sondy podwójnie znakowanej barwnikami
fluorescencyjnymi. Sondê stanowi zazwyczaj oligonukleotyd o d³ugoci 20-30 zasad.
Na jej koñcu 5' znajduje siê barwnik zwany
reporterem, a na koñcu 3' tzw. quencher
(wygaszasz). Wród najczêciej stosowanych barwników wystêpuj¹, jako reporter:
6-karboksyfluoresceina (FAM), VIC, 2,7-dimetoksy-4,5-dichloro-6-karboksyfluoresceina (JOE) i jako quencher 6-karboksytetrametylrodamina (TAMRA). Dodatkowo
wystêpuje tzw. barwnik pasywny 6-karboksy-N,N,N',N'-tetrametylorodamina (ROX).
Jest on wewnêtrznym odnonikiem w reakcji, stosowany do normalizacji i porównania z barwnikiem reporterowym w celu korekty b³êdów, wynikaj¹cych z pipetowania
lub zmiennych stê¿eñ próbek [16,17,25].
Podczas reakcji PCR sonda wi¹¿e siê
z matryc¹ pomiêdzy miejscami wi¹zania
primerów (rycina 1A). W momencie, gdy
oba barwniki s¹ po³¹czone z nienaruszon¹
sond¹, emisja fluorescencji reportera jest
zahamowana przez quencher (rycina 1B).
Podczas fazy wyd³u¿ania dochodzi do degradacji sondy przez polimerazê DNA (rycina 1C). Sonda ulega przeciêciu w miejscu miêdzy reporterem a quencherem. W
wyniku tego nastêpuje uwolnienie reportera i emisja fluorescencji.
PCR w czasie rzeczywistym jest bardzo
czu³a i precyzyjna oraz pozwala na monitorowanie reakcji w czasie, w którym ona rze210
A
Q
R
R
B
Q
Taq
R
C
Q
Taq
Rycina 1
Zasada dzia³ania real-time PCR z zastosowaniem sondy TaqMan (R: reporter, Q: quencher, Taq: polimeraza
Taq).
The rule of effect of real-time PCR with the use of TaqMan probe (R: reporter, Q: quencher, Taq: polimerase Taq).
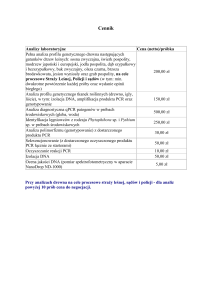
Ct
Rycina 2
Kinetyka przyrostu iloci produktów w reakcji PCR prowadzonej w aparacie ABI PRISM 7700 Sequence
Detection System (Applied Biosystems).
Kinetic of products' quantity increase in PCR reaction in the ABI PRISM 7700 Sequence Detection System (Applied
Biosystems).
czywicie zachodzi. W tej metodzie powielana jest specyficzna badana sekwencja w
próbce, a nastêpnie monitorowane zaawansowanie amplifikacji przy pomocy technologii fluorescencyjnej. Reakcja PCR zwi¹zana jest z emisj¹ sygna³u fluorescencyjnego
proporcjonalnego do iloci produktu powstaj¹cego w ka¿dym cyklu reakcji, a tym samym do iloci matrycy. Iloæ kopii badanego fragmentu kwasu nukleinowego jest monitorowana w ka¿dym cyklu reakcji amplifikacji. Numer cyklu reakcji PCR, przy którym poziom fluorescencji wzronie powy¿ej
sygna³u podstawowego i przekroczy zdefiniowany próg, (Ct; ang. threshold cycle) jest
stosowany do obliczenia iloci DNA obecnego w mieszaninie reakcyjnej na jej pocz¹tku. Ct najczêciej jest to moment wejcia
kinetyki reakcji w fazê logarytmicznego przyPrzegl¹d Lekarski 2009 / 66 / 4
rostu iloci produktu (rycina 2) [4,9].
W sk³ad mieszaniny reakcyjnej real-time
PCR wchodz¹: sonda znakowana barwnikami fluorescencyjnymi, odpowiednio dobrane primery, enzym polimeraza DNA oraz
matryca DNA. Poza tym mieszaninê tê stanowi bufor reakcyjny, zawieraj¹cy niezbêdne do pracy enzymu jony metali, jak równie¿ dwufosforany dezoksyrybonukleotydów
(dNTPs).
Reakcja zachodzi w aparacie, na który
sk³adaj¹ siê: termocykler, posiadaj¹cy mo¿liwoæ szybkich zmian temperatury, urz¹dzenie do wzbudzania energii fluorochromów
diodê, lampê emituj¹c¹ wiat³o (LED) lub
laser, a tak¿e fotodetektor. Obecny jest tak¿e komputer z odpowiednim oprogramowaniem, s³u¿¹cym do analizy danych. Obecnie dostêpnych jest wiele aparatów tego
A. Wycza³kowska-Tomasik i wsp.
typu: ABI Prism 7000 (Applied Biosystems),
ABI Prism 7900HT (Applied Biosystems),
Mx4000 (Stratagene), Mx3000P (Stratagene), iCycler iQ (Bio-Rad), LightCycler (Roche), SmartCycler (Cepheid), Rotor-Gene
(Corbett) i DNA Engine Opticon 2 (MJ Research) [25].
Sposób prowadzenia reakcji real-time
PCR mo¿liwy jest na dwa sposoby. Pierwszy z nich to wzglêdne oznaczenie ilociowe. Polega ono na wyznaczeniu ró¿nicy Ct
genu badanego i genu referencyjnego (kontrola wewnêtrzna, tzw. housekeeping gene),
o konstytutywnej, sta³ej ekspresji, w danej
grupie badanej (DCt). Najczêciej stosowanymi genami referencyjnymi s¹: dehydrogenaza gliceraldehydo-3-fosforanowa
(GAPDH), ß-aktyna, cyklofilina, 18S rRNA i
receptor dla transferyny. Nastêpnie otrzymana wartoæ dla grupy badanej porównywana jest z grup¹ kontroln¹ (DDCt) [15,16].
Drugi sposób przeprowadzenia powy¿szego oznaczenia polega na wykorzystaniu
krzywej standardowej. Obok prób badanych,
reakcji poddaje siê równie¿ próbki standardu o znanym stê¿eniu. Nastêpnie aparat na
podstawie krzywej standardowej wylicza
stê¿enia matrycy DNA w ka¿dej próbie badanej [9,14].
Istnieje wiele metod biologii molekularnej, s³u¿¹cych do oceny ilociowej kwasów
nukleinowych, min.: hybrydyzacje Northern
i Southern, HPLC, PCR-ELISA, RNase protection assay, hybrydyzacja in situ oraz ró¿ne systemy PCR z elektroforez¹ na ¿elu.
Wiêkszoæ z nich posiada pewne wady: s¹
czasoch³onne, pracoch³onne, nie wystarczaj¹co czu³e, nieilociowe, wymagaj¹ u¿ycia materia³ów radioaktywnych lub obarczone s¹ du¿ym ryzykiem zanieczyszczeñ.
PCR w czasie rzeczywistym posiada wiele
zalet w porównaniu z innymi metodami. Jedn¹ z wa¿niejszych jest mo¿liwoæ analizy
ilociowej kwasów nukleinowych w bardzo
szerokim zakresie, co najmniej 5 jednostek
logarytmicznych. Poza tym charakteryzuje
siê wyj¹tkow¹ czu³oci¹, pozwalaj¹c¹ na
wykrycie mniej ni¿ 5 kopii badanej sekwencji [25]. Cechuje siê ponadto powtarzalnoci¹, jest szybka i zautomatyzowana. W
koñcu, reakcja przeprowadzana jest w systemie zamkniêtym i nie wymaga dodatkowych manipulacji po zakoñczeniu PCR.
Dziêki temu zminimalizowaniu ulega ryzyko kontaminacji próbek.
Oczywicie, PCR w czasie rzeczywistym posiada te¿ ograniczenia. Etapami krytycznymi, warunkuj¹cymi prawid³owy przebieg dowiadczenia s¹: zaprojektowanie
eksperymentu, standaryzacja protoko³ów
ilociowego RT-PCR, wybór odczynników,
przygotowanie matrycy oraz analiza danych.
Jeli którykolwiek z tych etapów zostanie
przeprowadzony w sposób nieprawid³owy,
otrzymane dane mog¹ byæ niemiarodajne i
prowadziæ do b³êdnych wniosków.
ród³em b³êdów przy ocenie ekspresji
genów bywa niewystarczaj¹ca jakoæ RNA.
Pobranie materia³u biologicznego, jego zabezpieczenie, transport i przechowywanie,
a tak¿e izolacja RNA maj¹ wp³yw na jakoæ
RNA. Stanowi to jeden z najwa¿niejszych
czynników, warunkuj¹cych powtarzalnoæ i
wiarygodnoæ wyników. RNA, które mo¿na
wykorzystaæ do PCR w czasie rzeczywistym
Przegl¹d Lekarski 2009 / 66 / 4
powinno spe³niaæ nastêpuj¹ce kryteria: byæ
najlepszej jakoci, wolne od DNA, wolne od
inhibitorów odwrotnej transkrypcji oraz wolne od nukleaz (wa¿ne przy d³ugim przechowywaniu) [5]. Jakoæ RNA powinna byæ oceniona poprzez elektroforezê na ¿elu agarozowym lub, najlepiej, w systemie takim jak
Agilent Bioanalyzer, który stanowi nowy
standard kontroli jakoci.
W zwi¹zku z tym, ¿e materia³em biologicznym, z którego izoluje siê RNA jest czêsto niejednorodna tkanka, z³o¿ona z wielu
ró¿nych subpopulacji komórek, ró¿nych linii, w ró¿nym stopniu zró¿nicowanych, wyniki PCR w czasie rzeczywistym s¹ urednione. Za szczególnie heterogenne próbki
uwa¿a siê te pochodz¹ce z biopsji tkanki litej, w tym guzów [4]. Ekspresja mRNA jest
zmienna nie tylko w ró¿nych komórkach, ale
i u ró¿nych osobników tej samej grupy.
Istotny dla wyników jest równie¿ etap
odwrotnej transkrypcji, min. wybór primerów.
Zarówno primery typu random, jak i oligodT, czy specyficzne dla danej sekwencji,
maj¹ swoje zalety i wady, a ich wybór powinien zale¿eæ od konkretnej sytuacji [4]. Niska skutecznoæ reakcji przeprowadzenia
RNA w cDNA mo¿e byæ znacz¹cym ograniczeniem reakcji RT-PCR.
Reakcjê PCR mog¹ tak¿e zak³ócaæ inhibitory obecne w materiale biologicznym
(hemoglobina, wapñ, acyklowir, mocznik).
Problemem mo¿e byæ nieodpowiednie
wykorzystanie kontroli wewnêtrznej. Prawdopodobnie nie istnieje pojedynczy gen, który spe³nia³by kryteria wymagane dla uniwersalnego genu referencyjnego. Wszystkie w
pewnym stopniu podlegaj¹ regulacji oraz
¿aden z nich nie ulega ekspresji w sposób
konstytutywny we wszystkich typach komórek i we wszystkich warunkach, niezale¿nie
od zaprojektowanego dowiadczenia. Coraz
wiêcej badañ wskazuje na to, ¿e b³êdem
mo¿e byæ u¿ycie tylko jednego genu referencyjnego [26]. Tak¿e wybrany gen mo¿e
wykazywaæ zmienn¹ ekspresjê w danych
warunkach eksperymentalnych. Wykazano
np., ¿e ekspresja mRNA dla GAPDH ró¿ni
siê istotnie pomiêdzy osobnikami oraz pomiêdzy tkank¹ zdrow¹ i tkank¹ guza w raku
jelita grubego u ludzi [6]. Tak wiêc jeli geny
referencyjne maj¹ byæ wykorzystane, powinny byæ poddane walidacji w specyficznych
warunkach danego dowiadczenia oraz najprawdopodobniej nale¿y wybraæ wiêcej ni¿
jeden z nich [5]. Nieprawid³owa normalizacja prowadzi do subiektywnych wyników,
które nie odzwierciedlaj¹ biologicznej istotnoci. Mimo, ¿e w³aciwa normalizacja jest
niezwykle istotna dla uzyskania wiarygodnych wyników, nie istnieje jedna, uniwersalna strategia, któr¹ mo¿na by zastosowaæ w
ka¿dym dowiadczeniu. Pozostaje wiêc w
gestii badacza znaleæ i sprawdziæ metodê
najw³aciwsz¹ dla warunków jego dowiadczenia.
Nie bez znaczenia pozostaje równie¿
odpowiednia analiza danych. Po przeprowadzeniu reakcji PCR mo¿e zajæ potrzeba
korekcji linii bazowej lub threshold, co zmienia wartoæ Ct. W przeciwnym razie, wyniki
zostan¹ zafa³szowane. Threshold powinien
przecinaæ krzyw¹ amplifikacji w fazie ekspotencjalnej. Czasami jest wskazane ustalenie kilku wartoci threshold dla jednej p³ytki
poddanej reakcji PCR [5].
PCR w czasie rzeczywistym posiada
ogromn¹ moc, daje wiarygodne i powtarzalne wyniki, ale sukces w zastosowaniu tej
metody mo¿e zapewniæ tylko niezwyk³a dba³oæ w zaprojektowaniu, zastosowaniu oraz
walidacji dowiadczenia. Wydaje siê, ¿e istnieje pal¹ca potrzeba stworzenia ujednoliconych zaleceñ dotycz¹cych izolacji RNA,
odwrotnej transkrypcji, analizy danych, oceny wyników oraz protoko³ów standaryzacji.
W publikacji pracy, w której zastosowano tê
metodê powinny byæ podane dok³adne informacje dotycz¹ce zastosowanych procedur dowiadczalnych. W przeciwnym razie,
PCR w czasie rzeczywistym zamiast staæ
siê metod¹ o ogromnym potencjale, pozostaje jedynie narzêdziem badañ naukowych.
W badaniach naukowych PCR w czasie rzeczywistym wykorzystywany jest do
oceny ekspresji genów. Oczekuje siê, ¿e
ocena ekspresji genów pozwoli na zrozumienie z³o¿onej sieci regulacyjnej, identyfikacjê genów zwi¹zanych z nowymi procesami biologicznymi lub prowadz¹cych do
rozwoju choroby. PCR w czasie rzeczywistym i mikromacierze s¹ to dwie niedawno
rozwiniête metody, które zyska³y du¿¹ popularnoæ i które siê w tym celu czêsto stosuje. Mikromacierze pozwalaj¹ na jednoczesn¹ analizê tysiêcy genów w dwóch odmiennie znakowanych populacjach RNA, natomiast PCR w czasie rzeczywistym zapewnia równoczesny pomiar ekspresji genów w
wielu ró¿nych próbkach dla ograniczonej
liczby genów i jest metod¹ z wyboru, gdy
dostêpna jest jedynie ma³a liczba komórek.
Obie techniki w porównaniu do konwencjonalnych metod ilociowych, takich jak: hybrydyzacja Northern, czy kompetycyjny RTPCR, posiadaj¹ wiele korzyci szybkoæ,
wydajnoæ, mo¿liwoæ automatyzacji. Niemniej jednak, PCR w czasie rzeczywistym
jako metoda s³u¿¹ca do oceny ekspresji
mRNA posiada pewne ograniczenia, o których wspomniano powy¿ej.
Najm³odsz¹ dziedzin¹ diagnostyki medycznej jest diagnostyka molekularna, bêd¹ca najczulsz¹ i najszybsz¹ metod¹ odkrywaj¹c¹ pierwotne przyczyny choroby.
Czo³owe miejsce w diagnostyce molekularnej zajmuje PCR w czasie rzeczywistym.
Zalet¹ tej metody jest jej szybkoæ i prostota badania oraz mo¿liwoæ odczytu wyników
bezporednio na ekranie monitora, bez koniecznoci wykonywania elektroforezy na
¿elu. Pozwala to na przeprowadzenie pomiarów ilociowych wirusów, bakterii i innych mikroorganizmów.
PCR w czasie rzeczywistym wykorzystywany jest do okrelenia zmian ³adunku
wirusa. Poniewa¿ ³adunek wirusa i ciê¿koæ
choroby s¹ ze sob¹ powi¹zane, metoda ta
pozwala oceniæ progresjê choroby i skutecznoæ leczenia przeciwwirusowego. Okrelenie liczby kopii wirusa (oznaczenie poziomu wiremii) jest jednym z najwa¿niejszych
wskaników efektywnoci leczenia. Metody
biologii molekularnej s¹ najlepszym sposobem potwierdzenia lub wykluczenia zaka¿enia zw³aszcza wówczas, gdy przeciwcia³a nie s¹ wykrywalne, mimo, ¿e zaka¿enie
nast¹pi³o. Ma to miejsce we wczesnym okresie infekcji oraz u chorych z niedoborami
odpornoci. Technika ta przy u¿yciu abso211
lutnej oceny ilociowej mo¿e równie¿ s³u¿yæ do ró¿nicowania pomiêdzy aktywn¹ a
przetrwa³¹ infekcj¹. Pozwala tak¿e na wykazanie zwi¹zku pomiêdzy unikaln¹ sekwencj¹ wirusa a objawami klinicznymi pacjenta.
Przyk³adem wirusów oznaczanych z
wykorzystaniem PCR w czasie rzeczywistym s¹ Hepatitis B Virus (HBV), Hepatitis
C Virus (HCV), Cytomegalovirus (CMV),
Human Immunodeficiency Virus (HIV), Epstein-Barr Virus (EBV) [3,7,8,16,18-22,24].
Ilociowa diagnostyka zaka¿enia niektórymi wirusami, takimi jak Enterovirus czy
Parvovirus B19 umo¿liwia wykluczenie powa¿nych zagro¿eñ dla pacjentów z obni¿on¹ odpornoci¹, np. leczonych immunosupresyjnie po przeszczepieniu narz¹dów.
Powy¿sz¹ metod¹ oznaczane s¹ równie¿:
Dengue Virus, HPA-Coronavirus (SARS),
HSV 1/2, Orthopox, Varicella-Zoster Virus i
West Nile Virus [2].
Wykorzystanie real-time PCR w parazytologii pozwala na precyzyjn¹ ocenê poziomu inwazji paso¿yta. Mo¿liwe jest to w
przypadku Toxoplasma gondii. Z du¿¹ dok³adnoci¹ mo¿na oceniæ iloæ komórek
paso¿yta zarówno we krwi jak i p³ynie mózgowo-rdzeniowym czy owodniowym [3,
12]. Przyk³adem stosowania powy¿szej
metody s¹ równie¿ inne pierwotniaki Entamoeba histolityca, Plasmodium sp. [2].
Zastosowanie technik biologii molekularnej pozwala na ³atwe potwierdzenie lub
wykluczenie infekcji bakteryjnej bez koniecznoci zak³adania hodowli. Szybkie i wczesne wykrycie patogenu pozwala na natychmiastowe w³¹czenie celowanego leczenia
antybiotykiem, ogranicza stosowanie antybiotyków o szerokim spektrum, a tym samym przyczynia siê do ograniczenia wystêpowania szczepów antybiotykoopornych.
Metoda ta jest szczególnie przydatna w
przypadkach tych drobnoustrojów, które rosn¹ bardzo wolno lub nie namna¿aj¹ siê w
hodowli, np. Mycobacterium tuberculosis [8].
PCR w czasie rzeczywistym jest wykorzystywana do wykrywania bakterii takich jak:
Legionella pneumophila, Neisseria gonorrhoeae, Bacillus anthracis, Campylobacter
sp., Chlamydia trachomatis, Listeria monocytogenes, Mycobacterium paratuberculosis, Salmonella sp. [2]. Analiza mutacji pozwala monitorowaæ opornoæ na antybiotyki wród: Staphylococcus aureus, Staphylococcus epidermidis, Helicobacter pylori,
Enterococcus faecalis, i Enterococcus faecium [25]. ród³em b³êdów mo¿e byæ jednak fakt, ¿e metoda ta wykrywa DNA zarówno ¿ywych, jak i martwych patogenów.
Z metod biologii molekularnej czêsto
korzystaj¹ równie¿ onkolodzy. PCR w czasie rzeczywistym pozwala na wykrycie i ocenê ilociow¹ translokacji chromosomalnych
lub transkryptów genów fuzyjnych w celu
stwierdzenia minimalnej choroby resztkowej
(minimum residual disease, MRD) lub progresji choroby. Technikê tê stosuje siê w celu
wykrycia minimalnej choroby resztkowej u
212
pacjentów poprzez pomiar AML-1/MTG8 produktu genu fuzyjnego w ostrej bia³aczce
szpikowej, wiele rearan¿acji produktów genu
w ostrej bia³aczce limfoblastycznej, a tak¿e
oceny odpowiedzi pacjenta na leczenie interferonem- alfa przez pomiar produktu genu
fuzyjnego BCR-ABL w przewlek³ej bia³aczce szpikowej [25]. Metoda ta s³u¿y tak¿e do
oceny liczby kopii DNA w nowotworach z³oliwych oraz analizy ekspresji genów w guzach litych przy u¿yciu tkanki pobranej za
pomoc¹ biopsji ig³owej. Mo¿e to byæ istotne
dla okrelenia skuteczniejszych metod leczniczych oraz lepszej stratyfikacji ryzyka nawrotu choroby. PCR w czasie rzeczywistym
pomaga tak¿e w wyborze schematu leczenia przeciwnowotworowego w zale¿noci od
typu stwierdzonych zaburzeñ genetycznych
w komórkach nowotworowych. Przyk³adem
jest rodzina genów koduj¹cych bia³ka opornoci na leki, MRP (ang. multidrug resistance-associated protein). Komórki nowotworowe, które wykazuj¹ ekspresjê tych genów
potrafi¹ usuwaæ leki przeciwnowotworowe
ze swojego wnêtrza. Ma to niekorzystny
wp³yw na przebieg leczenia [8].
Omawiana metoda biologii molekularnej
wykorzystywana jest równie¿ w testach wykrywaj¹cych mutacje, jak równie¿ polimorfizm, zw³aszcza polimorfizm zmian pojedynczego nukleotydu w okrelonym miejscu
sekwencji DNA, SNP (ang. single -nucleotide polymorphism). Przyk³adem zastosowania PCR w czasie rzeczywistym jest wykrywanie mutacji genu CLN2, które wystêpuj¹
w zwyrodnieniowej chorobie uk³adu nerwowego, pónoniemowlêcej postaci ceroidolipofuscynozy [1,8].
PCR w czasie rzeczywistym z powodzeniem wykorzystywany jest równie¿ w badaniach nad lekami. Okrelana jest kinetyka
ekspresji badanego genu w odpowiedzi na
lek oraz odpowied transporterów lub enzymów metabolicznych zwi¹zanych z dystrybucj¹ lub wydalaniem. Za pomoc¹ tej
metody oznaczeniom ilociowym poddawane s¹ np. dehydrogenaza dihydropyrimidynowa (DPD), reduktaza metylenotetrahydrofolanu (MTHFR), N-acetylotransferaza 2
(NAT2) i S-metylotransferaza tiopurynowa
(TPMT) [2].
W chwili obecnej badania naukowe i diagnostyka laboratoryjna dysponuj¹ bardzo
dok³adn¹ i czu³¹ metod¹, jak¹ jest PCR w
czasie rzeczywistym. Niestety istniej¹ pewne problemy zwi¹zane z jej stosowaniem.
Jednym z nich jest wysoki koszt aparatu i
odczynników, co sprawia, ¿e w Polsce jej
dostêpnoæ jest ograniczona. Wobec braku
ujednoliconych zaleceñ, powa¿ny problem
mo¿e stanowiæ niedostateczna dba³oæ i
precyzja na którymkolwiek z etapów dowiadczenia: izolacji RNA, odwrotnej transkrypcji, walidacji, analizy danych oraz oceny wyników, co prowadzi do subiektywnych
wyników, które nie odzwierciedlaj¹ biologicznej istotnoci.
Przegl¹d Lekarski 2009 / 66 / 4
Pimiennictwo
1. Bal J. (red.): Biologia molekularna w medycynie.
Elementy genetyki klinicznej. Wyd. Nauk. PWN Wwa 2001.
2. Biuletyn informacyjny firmy Artus.
3. Bretagne S.: Molecular diagnostics in clinical parasitology and mycology: limits of the current polymerase chain reaction (PCR) assays interest of the realtime PCR assays. Clin Microbiol Infect 2003, 9, 505.
4. Bustin S.A., Benes V., Nolan T. et al.: Quantitative
real-time RT-PCR - a perspective. J. Mol. Endocrinol.
2005, 34, 597.
5. Bustin S.A., Nolan T.: Pitfalls of Quantitative RealTime Reverse-Transcription Polymerase Chain Reaction. J. Biomol. Tech. 2004, 15, 155.
6. Bustin S.A.: Absolute quantification of mRNA using
real-time reverse transcription polymerase chain reaction assays. J. Mol. Endocrinol. 2000, 25, 169.
7. Chen F.H., Samson K.T., Chen H. et al.: Clinical
applications of real-time PCR for diagnostic and treatment of human cytomegalovirus infection in children.
Pediatr Allergy Immunol, 2004, 15, 210.
8. Dembiñska-Kieæ A., Naskalski J.W. (red.): Diagnostyka laboratoryjna z elementami biochemii klinicznej.
Urban & Partner Wroc³aw 2002.
9. Giulietti A., Overbergh L., Valckx D. et al.: An overview of real-time PCR: Applications to cytokine gene
expression. Methods, 2001, 25, 386.
10. Higuchi R., Dollinger G., Walsh P.S. et al.: Simultaneous amplification and detection of specific DNA
sequences. Biotechnology, 1992, 10, 413.
11. Higuchi R., Fockler C., Dollinger G. et al.: Kinetic
PCR: Real-time monitoring of DNA amplification reactions. Biotechnology, 1993, 11, 1026.
12. Kozak-Ciêszczyk M.: Diagnostyka molekularna w
parazytologii. Kosmos. Problemy Nauk Biologicznych, 2005, 54(1/266), 49.
13. Kubista M., Andrade J.M., Bengtsson M. et al.:
The real-time polymerase chain reaction. Mol Aspects Med, 2006, 27(2-3), 95.
14. Larinov A., Krause A., Miller W.: A standard curve
based method for relative real time PCR data
processing. BMC Bioinformatics 2005, 6, 62.
15. Livak K.J., Schmittgen T.D.: Analysis of relative
gene expression data using real-time PCR and the
2 (-Delta Delta C(T)) Method. Methods 2001, 25, 402.
16. Mackay I.M., Arden K.E., Nitsche A.: Real-Time
PCR in virology, Nucleic Acids Res. 2002, 30, 1292.
17. Mackay I.M.: Real-time PCR in the microbiology laboratory. Clin Microbiol Infect, 2004, 10, 190.
18. Moghaddam A., Reinton N., Dalgard O.: A rapid
real - time PCR assay for determination of hepatitis
C virus genotypes 1, 2 and 3a. J. Viral. Hepat. 2006,
13, 222.
19. Najioullah F., Thouvenot D., Lina B.: Development
of real-time PCR procedure including an internal
control for the measurement of HCMV viral load. J.
Virol. Methods 2001, 92, 55.
20. Niesters H.G.M., van Esser J., Fries E. et al.: Development of real-time quantitative assay for detection of Epstein-Barr Virus. J. Clin. Microbiol. 2000,
38, 712.
21. Nitsche A., Steuer N., Schmidt C.A. et al.: Detection of Human Cytomegalovirus DNA by real-time
quantitative PCR. J. Clin. Microbiol. 2000, 38, 2734.
22. Ryan J.L., Fan H., Glaser S.L. et al.: Epstein-Barr
Virus Quantitation by Real-Time PCR Targeting Multiple Gene Segments. J. Mol. Diagn. 2004, 6, 378.
23. Saiki R.K., Scharf S., Faloona F. et al.: Enzymatic
amplification of ß-globin genomic sequences and
restriction site analysis for diagnosis of sickle cell
anemia. Science 1985, 230, 1350.
24. Tanaka N., Kimura H., Saito Y. et al.: Quantitative
analysis of cytomegalovirus load using real-time PCR
assay. J. Med. Virol. 2000, 60, 455.
25. Valasek M.A., Repa J.J.: The power of real-time
PCR. Advan. Physiol. Edu. 2005, 29, 151.
26. Vandesompele J., De Preter K., Pattyn F. et al.:
Accurate normalization of real-time quantitative RTPCR data by geometric averaging of multiple internal control genes. Genome Biology 2002, 3, 0034.1.
A. Wycza³kowska-Tomasik i wsp.