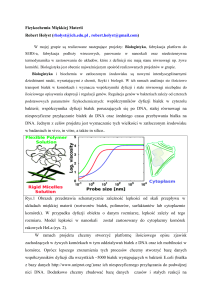
Wybrane techniki badania białek
-proteomika funkcjonalna
Proteomika:
• umożliwia badanie zestawu wszystkich (lub prawie wszystkich)
białek komórkowych
Zalety analizy proteomu w porównaniu z analizą
trankryptomu:
•analiza transkryptomu komórki – identyfikacja mRNA nie
oznacza jeszcze że będziemy wiedzieć jakie białko pojawi się
w komórce
•badając proteom analizujemy ostateczne elementy
strukturalne i funkcjonalne komórki
Etapy „klasycznej” analizy proteomu komórki
•dwukierunkowa elektroforeza białek w żelu poliakrylamidowym
•identyfikacja poszczególnych białek poprzez spektrometrię mas
np. typu MALDI-TOF
Zadania proteomiki funkcjonalnej:
•Identyfikacja i charakterystyka białek uczestniczących w złożonych
procesach biochemicznych
•Analiza oddziaływań białek z innymi białkami, kwasami
nukleinowymi, ligandami niskocząsteczkowymi
•Określanie składu i funkcji kompleksów makromolekularnych
•Badanie powiązań pomiędzy kaskadami przemian biochemicznych
•Poznanie mechanizmów ich regulacji
Interakcje DNA-białko
•Technika opóźnienia (reterdacji) migracji fragmentów DNA w
żelu poliakrylamidowym – EMSA (electrophoretic mobility shift
assay) lub Gel shif assay
•Technika badania odcisku stopy – ang. footprinting
Przykładowe zastosowania:
•Badanie oddziaływań czynników transkrypcyjnych wiążących
się z operatorami, enhacerami, silencerami
EMSA- Gel Shift Assay
Footprinting to metoda pozwalająca nie tylko stwierdzić
wiązanie białka do DNA, ale także precyzyjne określić pozycję
wiązania
•Wyznakować jeden koniec odcinka DNA np.
izotopowo
•Poddać trawieniu DNA za pomocą DNazy I,
która trawi DNA przypadkowo (UWAGA!!! Należy
zastosować łagodne warunki trawienia, tak aby
każda cząsteczka została przecięta tylko raz)
•Reakcję trawienia fragmentów DNA robi się w
dwu powtórzeniach: do jednego dodaje się
białko, które ma oddziaływać z fragmentem DNA
•Powstanie mieszanka wyznakowanych
fragmentów DNA, różnej długości (różniących
się o jeden nt), które rozdziela się na żelu
poliakrylamidowym
•Związanie białka zapobiega trawieniu DNA
przez DNazę I
•Uzyskujemy przerwę w prążkach tzw. „odcisk
stopy” – footprint powstały w miejscu
związania z białkiem.
•Jeśli równocześnie fragment użyty do doświadczenia podda się
sekwencjowaniu to możemy także podać sekwencję nukleotydów w miejscu
wiązania białka
• Przez porównanie z wzorem prążków próbki bez białka możemy dokładnie
zlokalizować miejsce wiązania
+
A
T
G
C
G
C
T
G
A
T
G
G
C
C
System dwuhybrydowy
•służy do badania interakcji białko-białko (zwykle są to dwa znane
białka) (tzw. przynęta i zdobycz)
•pozwala precyzyjnie zmapować takie interakcje
•podobnie jak -komplementacja opiera się na łączeniu dwóch
cząsteczek białek
•w tym systemie wykorzystujemy geny reporterowe
•tworzymy tzw. fuzje genowe, czyli łączymy sekwencje kodujące (geny)
w taki sposób, żeby ich fazy odczytów były zgodne
•Bezpośrednie oddziaływanie dwóch białek możemy
pokazać przez pośrednie połączenie dwóch domen
czynnika transkrypcyjnego
•Funkcjonalny czynnik transkrypcyjny złożony z domeny
wiążącej się z DNA i aktywującej transkrypcję) powstanie
nawet wtedy, kiedy obie te domeny znajdą się w komórce w
postaci osobnych polipetydów, które mogą one ze sobą
asocjować (podobnie jak w -komplementacji)
gen reporterowy
białko fuzyjne – zgodne
połączenie ramek odczytu genu X i
genu domeny wiążącej się z DNA
czynnika transkrypcyjnego w
zgodnych fazach odczytu kodonów
(fuzja genowa)
przynęta
zdobycz
zgodne miejsca startu
replikacji oriV
Macierze peptydowe (ang. peptide arrays)
•Bezkomórkowe układy peptydów przeznaczone do równoczesnych analiz
stanowiące reprezentację wszystkich lub prawie wszystkich białek danego
organizmu
•Zawierają szereg peptydów o różnych sekwencjach, połączonych
kowalencyjnie z powierzchnią stałego nośnika, pokrytego warstwą
odpowiedniego polimeru.
•Pomiędzy peptydem a podłożem znajduje się tzw. grupa dystansowa
(ang. spacer), który zapewnia większą swobodę konformacyjną i ułatwia
dostęp składników badanej próbki do immobilizowanych peptydów.
•W przeciwieństwie do kwasów nukleinowych, białka stanowią populację
bardzo heterogennych cząsteczek pod względem stabilności i własności
fizykochemicznych. Utrzymanie poprawnie zwiniętych i funkcjonalnych
peptydów na macierzy jest trudne, ale dzięki bezkomórkowym systemom
ich otrzymywania powielanie macierzy peptydowych jest dość łatwe i nie
ma potrzeby długiego przechowywania gotowych macierzy
Przykładowe
zastosowania:
•Badanie specyficzności
substratowej enzymów
proteolitycznych
•Mapowanie epitopów
•Badanie
oddziaływań
fragmentów białek z
innymi białkami i
DNA