PRACE POGLĄDOWE
Robert Krysiak1
Witold Szkróbka1
Beata Kowalska1,2
Bogusław Okopień1
Przedwczesne dojrzewanie płciowe u chłopców
Klinika Chorób Wewnętrznych i Farmakologii
Klinicznej Katedry Farmakologii Śląskiego
Uniwersytetu Medycznego w Katowicach
Kierownik:
Prof. zw. dr hab. n. med. Bolesław Okopień
Przedwczesne dojrzewanie płciowe u chłopców jest definiowane jako
początek pokwitania poniżej 9 roku
życia. Jest dzielone na dwa główne typy: ośrodkowe przedwczesne
dojrzewanie płciowe, które charakteryzuje przedwczesna aktywacja osi
podwzgórzowo-przysadkowo-gonadalnej, oraz obwodowe przedwczesne dojrzewanie płciowe, określane
jako wcześniejszy rozwój płciowy w
następstwie zwiększonej produkcji
hormonów płciowych, niezależnej od
wytwarzania gonadotropin. Chociaż
przedwczesne dojrzewanie płciowe
występuje częściej u dziewcząt, w
przypadku chłopców jego obecność
częściej kojarzy się z identyfikowalną
chorobą organiczną ośrodkowego
układu nerwowego, nadnerczy lub
gonad. Postępowanie diagnostyczne
powinno obejmować: szczegółowy
wywiad, dokładne badanie fizykalne,
ocenę stężenia hormonów przysadkowych i płciowych, określenie wieku
kostnego oraz diagnostykę obrazową
podwzgórza, przysadki, nadnerczy i
jąder. Wskazania do leczenia zależą
od typu przedwczesnego dojrzewania
płciowego i szybkości jego progresji,
wieku kostnego, przewidywanego
wzrostu ostatecznego oraz oceny
psychologicznej. Celem artykułu jest
omówienie etiopatogenezy przedwczesnego dojrzewania płciowego u
chłopców oraz przedstawienie zaleceń
dotyczących jego rozpoznawania, różnicowania i leczenia.
Precocious puberty in boys is defined as the onset of puberty before
the age of 9 years. It is divided into
two categories: central precocious
puberty, characterized by the premature activation of the hypothalamicpituitary-gonadal axis, and peripheral
precocious puberty presents when
premature sexual development is
dependent on steroid production regardless of gonadotropin secretion.
Although precocious puberty occurs
more frequently in girls, in the case
of boys it is more often associated
with identifiable organic disorders
of the central nervous system, adrenal glands or testes. The diagnosis
should include detailed anamnesis and
clinical examination, measurement of
pituitary and sex hormones, assessment of bone age, and imaging of the
hypothalamus, pituitary gland, adrenal
glands and testes. Indications for treatment are based on the type of precocious puberty and its progression rate,
advancement of bone age, predicted
adult height and psychological evaluation. The purpose of this article was
to discuss the etiopathogenesis of
precocious puberty in boys and to
provide the approach to its diagnosis,
differentiation and treatment.
Pojęcie przedwczesnego dojrzewania
płciowego
Choć przedwczesne dojrzewanie płciowe stanowi częstą, gdyż rozwijającą się u
jednego dziecka na 5000-10000, jednostkę
endokrynologiczną, jest ono problemem
zdrowotnym 10-krotnie częściej dotykającym dziewcząt niż chłopców [1,2]. Fakt ten
może tłumaczyć mniejsze zainteresowanie
wielu autorów problematyką przedwczesnego dojrzewania płciowego u chłopców.
Trzeba jednak pamiętać, iż pomimo swojej
rzadkości, wystąpienie przedwczesnego
dojrzewania u chłopców jest związane ze
znacznie większym niż u dziewcząt ryzykiem współistniejącej patologii [1].
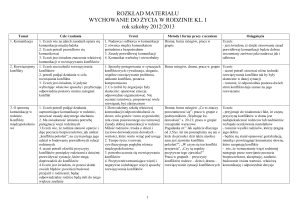
Zgodnie z obecnie przyjmowanymi kryteriami warunkiem rozpoznania przedwczesnego dojrzewania płciowego u chłopców jest wykazanie zwiększenia objętości jąder powyżej
4 ml (stadium G2 według Tannera) poniżej 9
roku życia, czemu zwykle towarzyszy długość
jądra powyżej 2,5 cm [3,4]. Powszechnie
wyróżnia się podział przedwczesnego dojrzewania płciowego na postać ośrodkową,
określaną niekiedy nazwą gonadoliberynozależnej lub gonadotropinozależnej, oraz
postać obwodową, określaną nazwą gonadoliberynoniezależnej, gonadotropinoniezależnej lub rzekomej. W przypadku pierwszej
z nich dochodzi do przedwczesnej aktywacji
osi podwzgórze-przysadka-nadnercza, natomiast w drugiej wzrost androgenemii nie tylko
nie jest związany z aktywacją powyższej osi,
ale nawet wtórnie hamuje jej aktywność [5,6].
W niewyselekcjonowanej pod względem płci
populacji postać ośrodkowa stanowi 80%,
zaś obwodowa 20% przypadków przedwczesnego dojrzewania płciowego [6,7].
Wiek wystąpienia oraz szybkość progresji
przedwczesnego dojrzewania płciowego są
zmienne i mają istotne znaczenie w określeniu podłoża przedwczesnego dojrzewania
płciowego.
1
Oddział Chorób Wewnętrznych – Pododdział
Endokrynologii Szpitala Wojewódzkiego w
Opolu
Kierownik:
Lek. Elżbieta Łomna-Bogdanov
2
Dodatkowe słowa kluczowe:
przedwczesne dojrzewanie płciowe
podział
etiopatogeneza
obraz kliniczny
diagnostyka
leczenie
Additional key words:
precocious puberty
classification
etiopathogenesis
clinical picture
diagnosis
treatment
Adres do korespondencji:
Robert Krysiak
Klinika Chorób Wewnętrznych i Farmakologii
Klinicznej Katedry Farmakologii Śląskiego
Uniwersytetu Medycznego w Katowicach,
ul. Medyków 18, 40-752 Katowice,
tel./fax 322523902,
e-mail: [email protected]
Przegląd Lekarski 2014 / 71 / 10
Precocious puberty in boys
549
Postać ośrodkowa przedwczesnego
dojrzewania płciowego
Hamartoma podwzgórza
Hamartoma jest zmianą nienowotworową,
którą w badaniu histopatologicznym charakteryzuje występowanie heterotopowej masy
tkankowej. Pod względem budowy przypomina istotę szarą, zaś w jej skład wchodzą
duże i małe neurony, częściowo wykazujące
tendencję do skupiania się, ale częściowo
rozproszone, zawierającą ponadto komórki
glejowe (astrocyty, ependymocyty), przy
czym elementy komórkowe hamartoma nie
wykazują cech dysplazji [8,9]. Zmiana lokalizuje się w obrębie podwzgórza w obszarze
pomiędzy szypułą przysadki a ciałami
suteczkowatymi [10]. Ma najczęściej kształt
owalny, zaś jej wielkość mieści się w przedziale 5-50 mm (najczęściej 10-30 mm) [11].
W większości przypadków hamartoma nie
wykazuje tendencji do powiększania swoich
wymiarów i dlatego wzrost wielkości zmiany
przemawia zwykle za innym jej charakterem
[9,11]. Z anatomicznego punktu widzenia
hamartoma może przylegać do dna trzeciej
komory na wąskiej lub szerokiej podstawie,
być połączona z podwzgórzem przez konary
lub też wpuklać się do podwzgórza [9,11].
Częstość występowania hamartoma podwzgórza jest szacowana na 1-2 przypadki na
100 000 osób, przy czym przyjmuje się, iż
wyżej podana wartość może być zaniżona
[10]. Istnieją nawet przypuszczenia, iż
bardzo małe zmiany hamartomatyczne
(o średnicy 0,5-1 mm), niepowodujące
objawów klinicznych, są stwierdzane
powszechnie (nawet u co 5 osoby) w badaniach autopsyjnych [11]. Choć przypadki
hamartoma były opisywane u osób obu
płci, częściej rozwijają się one u chłopców
niż dziewcząt [12]. U większości pacjentów
hamartoma jest zmianą izolowaną, jednak w
nielicznych przypadkach współistnieje ona
z innymi wykładnikami zespołu PallisteraHalla, schorzenia o podłożu genetycznym, dziedziczącego się autosomalnie
dominująco [10].
Przedwczesne dojrzewanie płciowe
dotyczy połowy przypadków udokumentowanego hamartoma oraz jeszcze większego odsetka (powyżej 80%) tego guza,
w przypadku wystąpienia jego manifestacji
klinicznej [11,13]. Hamartoma jest odpowiedzialna za 14-36% wszystkich organicznych
przyczyn przedwczesnego dojrzewania
płciowego o charakterze ośrodkowym, co
czyni ją najczęstszą przyczyną tej formy
przedwczesnego pokwitania u chłopców
[11]. Zwraca uwagę wczesny początek
dojrzewania, który w 80% ma miejsce do
końca 2 roku życia, a prawie zawsze poniżej
4 roku życia [14]. Pokwitanie jest więc w
tych przypadkach znacznie wcześniejsze
niż w postaciach idiopatycznych [15,16].
Dochodzi do równoległego powiększenia
jąder i prącia oraz obniżenia tembru głosu,
którym towarzyszy nadmierny szybki rozwój
szkieletu, mięśni oraz pojawienie się owłosienia łonowego [11]. Postęp pokwitania jest
znacznie szybszy niż w postaci idiopatycznej i większa jest różnica pomiędzy wiekiem
metrykalnym a wiekiem kostnym [17]. Do
rzadszych manifestacji endokrynologicznych obserwowanych w przypadku hamartoma podwzgórza należą: współistnienie
550
hipogonadyzmu hipogonadotropowego
z niedoborem hormonu wzrostu (growth
hormone - GH), akromegalia, uwarunkowana nadmierną sekrecją somatoliberyny,
oraz objawy podwzgórzycy [11]. Mogą one
powodować rzadkie przypadki opóźnienia
rozwoju płciowego lub osiągnięcie wyższego wzrostu ostatecznego [18]. Czynnikami
zwiększającymi ryzyko przedwczesnego
dojrzewania płciowe w przypadku hamartoma są: duże wymiary zmiany oraz kontakt
z guza popielatym lub lejkiem, a także połączenie guza z podwzgórzem za pomocą
konarów [16,19]. Przedwczesne dojrzewanie płciowe w przypadku hamartoma ma
charakter ośrodkowy za czym przemawia
obecność pulsacyjnego wzorca wydzielania
LH, charakterystycznego dla okresu pokwitania, jak również pokwitaniowy wzorzec
odpowiedzi LH na podanie gonadoliberyny,
bądź jej analogu [18].
Przyczyna przedwczesnego dojrzewania płciowego u chłopców z hamartoma
jest najprawdopodobniej złożona. U części
chorych może ono wynikać z obecności w
obrębie guza komórek, będących ektopowym źródłem gonadoliberyny [18]. U innych
stanowić ono może konsekwencję wytwarzania przez komórki glejowe (a być może
również nerwowe) substancji aktywujących
neurony produkujące gonadoliberynę w podwzgórzu, takich jak transformujący czynnik
wzrostu-α [16,19]. Bierze się również pod
uwagę aktywację komórek podwzgórza
przez zmielinizowane włókna nerwowe,
których ciała komórkowe zlokalizowane są
w obrębie hamartoma lub też mechaniczny
ucisk guza na podwzgórze [9].
Drugą charakterystyczną manifestacją
kliniczną hamartoma jest obecność nietypowych objawów padaczkowych, o charakterze kilku- lub kilkunastosekundowych
napadów śmiechu z niepamięcią wsteczną,
które niejednokrotnie kojarzą się z rozszerzeniem źrenicy, zaczerwienienie twarzy,
różnymi objawami motorycznymi i napadami
przymusowego patrzenia się w stały punkt
[10]. Zmiany elektroencefalograficzne są
słabiej wyrażone niż w przypadku innych
typów padaczki i często niecharakterystyczne [10]. Rzadziej hamartoma kojarzy
się z obecnością innych postaci padaczki,
takich jak napady krzyku, padaczka wtórnie
uogólniona o charakterze zbliżonym do zespołu Lennox-Gastaut, napady atoniczne,
napady toniczne, napady toniczno-kloniczne, atypowe napady nieświadomości,
napady częściowe ruchowe proste oraz
napady częściowe złożone [10,20]. Ryzyko
napadów padaczkowych jest proporcjonalne
do wielkości zmiany, występując głównie w
zmianach o średnicy przekraczającej 10 mm
[19]. Jak przemawiają za tym zestawienia
zbiorcze prawdopodobieństwo napadów
śmiechu u chłopców jest dwukrotne większe
niż dziewcząt (u chłopców, u których wystąpiło przedwczesne dojrzewanie płciowe
ocenia się je na 2/3) [16].
W przypadku obecności zespołu Pallistera-Halla, w którym to zespole hamartoma jest
stwierdzana zawsze, obserwuje się ponadto
obecność: wielopalczastości, hipoplazji
przysadki i opuszek węchowych, przodomózgowia jednokomorowego, dysplazji
paznokci, niewykształcenia odbytu oraz wad
rozwojowych nagłośni i nerek [9,20].
W przypadku podejrzenia hamartoma
kluczowe znaczenie przypada diagnostyce
obrazowej (biopsja ze względu na lokalizację jest trudna do przeprowadzenia). Tym
bardziej, iż w świetle dostępnych danych w
takich przypadkach uzasadnione jest leczenie farmakologiczne analogami gonadoliberyny, co oznacza możliwość zrezygnowania
z leczenia zabiegowego [10]. W badaniu
rezonansu magnetycznego hamartoma jest
zmianą zlokalizowaną w dnie komory trzeciej, pomiędzy guzem popielatym a ciałami
suteczkowatymi. Intensywność sygnału w
obrazach T1-zależnych jest zbliżona do
intensywności sygnału istoty szarej, zaś w
obrazach T2-zależnych jest ona zbliżona
do intensywności sygnału istoty szarej lub
nieco od niej większa [21]. Zmiana nie ulega
wzmocnieniu po podaniu kontrastu [11]. Powiększanie się zmiany, jak również występowanie zwapnień, przestrzeni wypełnionych
płynem, wzmocnienia kontrastowego oraz
niejednorodnego obrazu zmiany sugeruje
inne rozpoznanie [21].
Poza powyższymi objawami hamartoma
znamiennie częściej kojarzy się z otyłością,
zaburzeniami rozwoju intelektualnego, zaburzeniami behawioralnymi oraz zmianami
pola widzenia [11].
Przedwczesne dojrzewanie płciowe
pochodzenia ośrodkowego na tle innych
zmian organicznych ośrodkowego układu nerwowego
U chłopców schorzenia ośrodkowego
układu nerwowego odpowiadają za 2/3
przypadków przedwczesnego dojrzewania
pochodzenia ośrodkowego, w tym same
zmiany ogniskowe za prawie 50% [13].
Dlatego w każdym przypadku przedwczesnego dojrzewania płciowego u chłopców
należy bezwzględnie wykluczyć obecność
zmiany ekspansywnej w obrębie ośrodkowego układu nerwowego. Przypadki
przedwczesnego dojrzewania opisywano na
tle różnych nowotworów: czaszkogardlaka,
glejaków (gwiaździak, wyściółczak, glejak
nerwu wzrokowego), jak również guzów
przysadki wydzielających gonadotropiny
(gonadotropinoma) [17]. Ryzyko takiej
zmiany jest szczególnie duże w przypadku
początku dojrzewania poniżej 4 roku życia,
przy dużej szybkości postępu dojrzewania
oraz w przypadku obecności jakichkolwiek
objawów klinicznych sugerujących istnienie procesu ekspansywnego w obrębie
ośrodkowego układu nerwowego [22]. Poza
zmianami nowotworowymi przedwczesne
dojrzewanie płciowe może być konsekwencją zmian zapalnych ośrodkowego układu
nerwowego (w tym ropni), wodogłowia,
zespołu pustego siodła, torbieli nadsiodłowych, torbieli pajęczynówki, innych przyczyn
nadciśnienia śródczaszkowego, urazu,
niedotlenienia (w tym okołoporodowego),
przepukliny oponowo-rdzeniowej, dysplazji
przegrodowo-ocznej, czy też krwawienie
śródczaszkowego w okresie noworodkowym
[9, 23, 24]. Z bliżej nieokreślonych względów
ryzyko wystąpienia przedwczesnego dojrzewania płciowego pochodzenia ośrodkowego
jest również zwiększone w nerwiakowłókniakowatości typu I oraz zespole WilliamsBeurena [25,26].
R. Krysiak i wsp.
W przypadku guzów wydzielających
gonadotropiny przedwczesne dojrzewanie
płciowe stanowi konsekwencję sekrecji tych
hormonów lub ich fragmentów wykazujących
aktywność hormonalną [6]. W pozostałych
przypadkach zmian ekspansywnych przedwczesne pokwitanie najprawdopodobniej
wynika z ucisku lub
��������������������������
nacieczenia przez proces nowotworowy komórek wydzielających
gonadoliberynę, bądź też wytwarzania
przez komórki��������������������������
guza substancji aktywujących neurony wydzielające gonadoliberynę
[5,27]. Natomiast w przypadkach nienowotworowych jest ono najprawdopodobniej
uwarunkowane niespecyficzną aktywacją
otaczającej tkanki podwzgórza [17].
Przedwczesne dojrzewanie płciowe
po radioterapii
W przeciwieństwie do hamującego wpływu wysokich (powyżej 40 Gy) dawek radiacji
na aktywność osi podwzgórze-przysadkagonady, w przypadku zastosowania mniejszych dawek może dochodzić, zwłaszcza w
najmłodszych przedziałach wiekowych, do
przedwczesnego dojrzewania płciowego o
podłożu ośrodkowym [28]. Rozwija się ono
najczęściej w wyniku prewencyjnego napromieniowania mózgowia z powodu ostrej
białaczki limfoblastycznej oraz rzadziej w
przypadku guzów litych. Przy dawkach
poniżej 24 Gy przedwczesne dojrzewanie
dotyczy głównie dziewcząt, jednak po zastosowaniu wyższych dawek nie stwierdza
się różnic pomiędzy osobami obu płci [29].
Należy pamiętać, że przedpokwitaniowy
wzrost szybkości wzrastania może u chłopców maskować objawy niedostatecznej
sekrecji GH [30]. Patomechanizm tej postaci
przedwczesnego pokwitania nie jest znany.
Najprawdopodobniej jest on podobny do
postulowanego w postaci idiopatycznej zaburzenia równowagi pomiędzy czynnikami
pobudzającymi oraz hamującymi funkcję
generatora pulsów endogennej gonadoliberyny [17].
Inne postacie przedwczesnego dojrzewania płciowego o charakterze ośrodkowym
Wystąpienie przedwczesnego dojrzewania opisano w nielicznych przypadkach
chłopców (znacznie częściej u dziewcząt) z
krajów trzeciego świata, którzy zostali adoptowani przez rodziny z krajów rozwiniętych.
Przypisuje się, iż w jego powstawaniu istotne
znacznie odgrywać mogą: poprawa stanu
odżywienia i normalizacja masy ciała, jak
również uwarunkowania środowiskowe lub
psychologiczne [15,31].
W pojedynczych przypadkach do przedwczesnego dojrzewania płciowego u
chłopców dochodziło również w wyniku
chemioterapii lub leczenia chirurgicznego
nowotworów ośrodkowego układu nerwowego [23].
Idiopatyczne przedwczesne dojrzewanie płciowe pochodzenia ośrodkowego
Przypadki przedwczesnego dojrzewania
płciowego pochodzenia ośrodkowego u
chłopców, w których nie można ustalić
czynnika etiologicznego, określane niekiedy
nazwą idiopatycznego przedwczesnego
Przegląd Lekarski 2014 / 71 / 10
dojrzewania płciowego, są znacznie rzadsze niż u dziewcząt i stwierdza się je u
10-50% chłopców z ośrodkową postacią
przedwczesnego dojrzewania [1,27]. W
etiologii idiopatycznej postaci przedwczesnego dojrzewania płciowego o podłożu
ośrodkowym postuluje się udział zwiększonej produkcji substancji endogennych
pobudzających komórki wytwarzające
gonadoliberynę, bądź też zmniejszenia
sekrecji związków hamujących aktywność
neuronów zawierających gonadoliberynę.
Rolę takich związków spełniać mogą
neuroprzekaźniki, czynniki wzrostowe, bądź
też peptydy sygnałowe [5,6]. Do pierwszej
grupy należą przede wszystkim: kisspeptyna, neuropeptyd Y, α-melanotropina,
aminokwasy pobudzające (zwłaszcza
glutaminian) oraz niektóre czynniki wzrostowe, szczególnie transformujący czynnik
wzrostu-α, czynnik wzrostu fibroblastów,
czy insulinopodobny czynnik wzrostu-1
[32]. Natomiast najważniejszymi czynnikami
hamującymi sekrecję gonadoliberyny są:
kwas γ-aminomasłowy, β-endorfiny oraz
prolaktyna [32]. W ostatnich latach opisano
ponadto pojedyncze przypadki ośrodkowego dojrzewania płciowego na tle aktywującej
mutacji (R386P) receptora dla kisspeptyny GPR54 [10]. W przypadku przedwczesnego
dojrzewania płciowego o podłożu idiopatycznym rozwój jego dotyczy zwykle chłopców
w wieku starszym niż w większości zmian
organicznych, zaś postęp dojrzewania jest
tylko nieznacznie przyspieszony [1].
Postać obwodowa przedwczesnego
dojrzewania płciowego
Rodzinne męskie przedwczesne
dojrzewanie płciowe (testotoksykoza)
Rzadką, ale bardzo charakterystyczną
do chłopców, jednostką chorobową, której
obecność doprowadza do wystąpienia
przedwczesnego dojrzewania płciowego o
charakterze obwodowym jest tzw. rodzinne
męskie przedwczesne dojrzewanie płciowe
(familial male precocious puberty), inaczej
nazywane testotoksykozą. U jego podłoża
leży mutacja punktowa receptora genu
receptora dla LH/β-gonadotropiny kosmówkowej, który jest obecny w rejonie p21 chromosomu 2. W wyniku mutacji dochodzi do
konstytutywnej aktywacji białka Gsα i zwiększonej produkcji cAMP nawet w warunkach
znikomych stężeń LH [33,34]. W skrajnych
przypadkach aktywacja tego receptora nie
wymaga obecności nawet śladowych stężeń
tego hormonu [35]. Do występowania objawów klinicznych dochodzi u zdecydowanej
większości, gdyż ponad 90%, chłopców z
obecnością omówionej mutacji [34]. Pewnym paradoksem rodzinnego męskiego
przedwczesnego dojrzewania płciowego
jest obecność jego manifestacji fenotypowej
wyłącznie u chłopców pomimo autosomalnie
dominującego charakteru dziedziczenia
[36]. Przyczyna nieobecności manifestacji
klinicznej u dziewcząt jest złożona i składa
się na nią: śladowa ekspresję receptora dla
LH/β-gonadotropiny kosmówkowej u dziewcząt przed pokwitaniem, zmniejszona aktywność 17-20-liazy w komórkach ziarnistych,
jak również degradujący wpływ temperatury
jamy brzusznej na aktywność białek Gsα,
pośredniczących w efektach pobudzenia
tego receptora (temperatura w jamie brzusznej wynosi 370C i jest o około 40C wyższa
niż w worku mosznowym) [36].
Rodzinne męskie przedwczesne dojrzewanie płciowe charakteryzuje się wczesnym
początkiem występowania, najczęściej pomiędzy 2 a 4 rokiem życia [13]. Klinicznie u
dotkniętych procesem chorobowym pacjentów dochodzi do wystąpienia przedwczesnego owłosienia płciowego oraz zwiększenia
wymiarów prącia [35]. Choć również jądra
ulegają zwykle niewielkiemu lub umiarkowanemu symetrycznemu powiększeniu,
jednak jest ono stosunkowo niewielkie w
stosunku do powiększenia prącia [2,36].
Powyższe objawy mogą być stwierdzane
nawet w chwili urodzenia [37]. Konsekwencją konstytutywnej aktywacji receptora dla
LH/β-gonadotropiny kosmówkowej jest
obecność wykazywanego w badaniu biopsyjnym jąder rozrostu komórek Leydiga
[37]. Niejednokrotnie stwierdza się ponadto
cechy przedwczesnej spermatogenezy [35].
Chociaż u części osób dochodzi z czasem
do rozwoju oligospermii, w większości
przypadków płodność jest zachowana, co
sprzyja przekazywaniu genów [36]. Choć
we wczesnym dzieciństwie wzrost kostny
jest przyspieszony, jednak wskutek przedwczesnego zarastania chrząstek stawowych
wzrost końcowy jest mniejszy niż u osób
zdrowych [2,34]. Za możliwą obecnością
rodzinnego męskiego przedwczesnego
dojrzewania płciowego przemawia dodatni
wywiad, choć jego nieobecność nie wyklucza istnienia powyższej choroby z uwagi
na możliwość występowania mutacji de
novo [13,34].
Zespół McCune-Albrighta
Zespół McCune-Albrighta cechuje
obecność trzech objawów klinicznych: przebarwień skóry w postaci plam o zabarwieniu
kawy z mlekiem (cafe au lait), włóknistej
dysplazji kości oraz przedwczesnego dojrzewania płciowego o charakterze izoseksualnym [38]. Ocenia się, że schorzenie
dotyka 1 osobę na 100 000 - 1 000 000 [39].
W zdecydowanej większości przypadków u
podłoża schorzenia leży substytucja argininy
przez histydynę lub cysteinę w pozycji 201
genu GNAS-1 [40], obecnego na długim
ramieniu chromosomu 20 i kodującego powstawanie heterotrimerycznego białka Gsα
[5,41]. W konsekwencji mutacji dochodzi do
przewlekłego utrzymywania się aktywnej
konformacji niektórych receptorów oraz
konstytutywnej aktywacji cyklazy adenylowej [38], akumulacji cAMP w komórkach,
proliferacji komórkowej oraz zwiększenia
aktywności różnych typów komórek [42].
Ponieważ mutacja dotyczy postzygotycznych komórek somatycznych i występuje po
kilku-kilkunastu podziałach komórkowych,
dlatego tylko pewna część komórek organizmu wykazuje zmiany genetyczne [43].
Tłumaczy to, dlaczego w poszczególnych
narządach stwierdza się współistnienie (w
różnych proporcjach) komórek niezmienionych i zmutowanych [41]. Powyższa
mozaikowatość zmian wyjaśnia ponadto
dużą różnorodność w występowaniu oraz
nasileniu poszczególnych objawów klinicznych tego zespołu [44].
Chociaż przedwczesne dojrzewanie
551
płciowe jest uważane za najczęstszą
manifestację endokrynologiczną zespołu
McCune-Albrighta, jednak zaledwie 10%
osób, u których postawiono rozpoznanie
tego zespołu to chłopcy [12,41]. U podłoża
przedwczesnego dojrzewania leży aktywacja sygnalizacji receptora gonadotropinowego, pomimo bardzo niskich stężeń gonadotropin [45]. Większość opisanych danych
przypadków przedwczesnego dojrzewania
płciowego u chłopców ma charakter doniesień kazuistycznych lub opisów niewielkiej
serii pacjentów [40]. Wyniki tych badań
wydają się jednak przemawiać za tym, iż
w stosunku do dziewcząt przedwczesne
dojrzewanie płciowe u chłopców pojawia się
w późniejszym wieku, zaś jego przebieg jest
wolniejszy [46]. W badaniu fizykalnym zwraca uwagę powiększenie jąder, które najczęściej dotyczy obu jąder, a znacznie rzadziej
jednego jądra, a także ich mikrokamica
[46,47]. Natomiast w badaniu biopsyjnym
zwraca uwagę hiperplazja komórek Sertoliego [46], spowodowana mutacją aktywującą
allelu GNAS1 w tych komórkach [44]. Wbrew
starszym opisom, obecnie coraz częściej
stwierdza się również obecność hiperplazji
komórek Leydiga, jednak pojawia się ona
później niż rozrost komórek Sertoliego, gdyż
w okresie pokwitania [38]. Jednostronnemu
lub obustronnemu powiększeniu towarzyszy
równolegle powiększenie prącia, pofałdowanie moszny, pojawienie się zapachu potu
apokrynowego, owłosienia pachowego i
łonowego oraz typowych reakcji seksualnych [39]. Spermatogeneza, choć ilościowo
zaburzona, jest przeważnie zachowana [44].
Należy pamiętać, iż do przedwczesnego
dojrzewania płciowego może nie dochodzić
w przypadku współistniejącego nadmiaru
prolaktyny [43]. U niektórych chorych szybkość wzrastania jest większa niż w innych
postaciach przedwczesnego dojrzewania
płciowego, zaś wzrost ostateczny może być
prawidłowy. Dotyczy to chorych z współistniejącą nadmierną sekrecja GH [41]. Na
drugim biegunie znajdują się pacjenci z
obecnością rozległej dysplazji włóknistej
kości lub wykładników zespołu Cushinga, u
których wzrost ostateczny jest niski [48].
Zmiany skórne, stanowiące konsekwencję powiększenia melanosomów w skórze
właściwej są zwykle obecne już w chwili
urodzenia się lub wkrótce potem, zaś w
analizach retrospektywnych są one uważane za najbardziej typową manifestację tego
schorzenia [2,44]. Najczęstszymi miejscami
występowania tych zmian są: czoło, szyja,
górna część grzbietu, barki, górna część
ramion, okolica lędźwiowo-krzyżowa oraz
pośladki [7,13]. Mają one często charakter
asymetryczny, kończąc się nagle w środkowej linii ciała [2]. Hiperpigmentacja wynika
z powiększenia melanosomów w skórze
właściwej, podczas gdy liczba i wielkość
samych melanocytów jest prawidłowa [40].
Granice przebarwień skórnych są nieregularne (obraz “wybrzeża Maine”) czy zmiany
te różnią się od stwierdzanych w innym
stanie sprzyjającym przedwczesnemu dojrzewaniu płciowemu - nerwiakowłókniakowatości (obraz “wybrzeża Kalifornii”) [39].
Zmiany kostne ujawniają się najczęściej
do 15 roku życia i lokalizują się zwykle w
obrębie czaszki (najczęściej w podstawie
552
czaszki) lub kończyn (głównie proksymalna część kości udowej) [39], rzadziej w
miednicy [44]. Przyjmują charakter zmian
ekspansywnych wyścielonych śródkostną,
współistniejących ze ścieńczeniem warstwy
korowej i radiologicznym obrazem „matowego szkła” [40]. Do najbardziej typowych objawów dysplazji włóknistej należą: obecność
zmiany guzowatej, ból oraz - choć rzadziej
- obecność złamania patologicznego, które
najczęściej rozwija się pomiędzy 6 a 10 r.ż.
[39]. U niewielkiego odsetka chorych (poniżej 4%) dochodzić może do rozwoju zmian
złośliwych w kościach [43,44].
Poza powyższymi objawami do manifestacji klinicznych zespołu McCune-Albrighta
należą: nadczynność tarczycy, akromegalia,
hiperprolaktynemia, nerkowa utrata fosforanów w następstwie produkcji czynnika
wzrostu fibroblastów-23, krzywica lub osteomalacja, zespół Cushinga w następstwie
hiperplazji guzkowej oraz rzadko zmiany
w innych narządach: kamica pęcherzyka
żółciowego czy przerost serca [39,43].
Wrodzony przerost nadnerczy
We wrodzonym przeroście nadnerczy,
stanowiącym grupę schorzeń o dziedziczeniu autosomalnie recesywnym i uwarunkowanych zmniejszoną aktywnością jednego
z enzymów uczestniczących w procesie
biosyntezy kortyzolu, u podłoża przedwczesnego dojrzewania płciowego leży podwyższone stężenie androgenów nadnerczowych
jako wynik stymulującego wpływu wysokich
stężeń ACTH na czynność hormonalną
warstwy siatkowatej kory nadnerczy [49].
Przyczyną przedwczesnego dojrzewania
płciowego u chłopców są dwa defekty
enzymatyczne: niedobór 21-hydroksylazy
oraz niedobór 11β-hydroksylazy, stanowiące
odpowiednio ponad 90% oraz 5-8% wszystkich przypadków wrodzonego przerostu
nadnerczy i uwarunkowane istnieniem mutacji odpowiednio w obrębie genu P450c21
oraz genu P450c11 [50]. Stopień niedoboru
enzymatycznego determinuje ciężkość objawów klinicznych tego schorzenia oraz jego
podział na postać klasyczną oraz postać
nieklasyczną [51,52]. W przypadku niedoboru 21-hydroksylazy postać klasyczna
jest dodatkowo dzielona na typ z utratą soli
(„salt-wasting”) (75%) oraz typ związany z
izolowaną wirylizacją („simple virilization”)
(25%) [50,51]. Warto pamiętać, iż wrodzony przerost nadnerczy na tle niedoboru
21-hydroksylazy jest uznawany za jedno z
najczęstszych schorzeń uwarunkowanych
genetycznie, gdyż postać klasyczna jest
rozpoznawana u jednej osoby na 15 000,
zaś w postać nieklasyczna nawet u 1%
całkowitej populacji (choć te ostatnie dane
te dotyczą głównie kobiet) [49].
W chwili urodzenia u chłopców (w przeciwieństwie do dziewczynek) z klasyczną
postacią niedoboru 21-hydroksylazy nie obserwuje się widocznych objawów nadmiaru
androgenów [50]. W przypadku niedoboru
21-hydroksylazy we wczesnym dzieciństwie mogą jednakże występować objawy
niedoboru mineralokortykoidów, które nierozpoznane doprowadzić mogą do zgonu
[16]. W późniejszym okresie dzieciństwa w
wyniku utrzymującego się przewlekle nadmiaru androgenów dochodzi u chłopców do
przyspieszenia dojrzewania kostnego i wystąpienia przedwczesnego izoseksualnego
dojrzewania płciowego [50]. W badaniu fizykalnym zwracają uwagę cechy pokwitania,
takie jak powiększenie prącia, dyskretna hiperpigmentacja narządów płciowych, rozwój
gruczołów apokrynowych oraz pojawienie
się owłosienia płciowego, podczas gdy objętość jąder nie ulega zwykle zwiększeniu [50].
W przypadku niedoboru 21-hydroksylazy
ujawniać się mogą cechy niewydolności
mineralokortykoidowej nadnerczy, natomiast
w niedoborze 11β-hydroksylazy występować
może nadciśnienie tętnicze, współistniejące
z zasadowicą nieoddechową i hipokaliemią,
sugerujące istnienie pierwotnego hiperaldosteronizmu, od którego różnią go obniżone
stężenia aldosteronu [52].
Objawy nieklasycznej postaci wrodzonego przerostu nadnerczy na tle niedoboru
21-hydroksylazy lub 11β-hydroksylazy są u
chłopców mniej zaznaczone niż u dziewcząt
i najczęściej manifestują się pod postacią
przedwczesnego rozwoju owłosienie łonowego oraz przyspieszonego, lecz przedwcześnie zakończonego wzrostu [53].
Nowotwory nadnerczy
W przeciwieństwie do rzadkiego występowania łagodnych gruczolaków, rak
nadnerczy charakteryzuje się bimodalnym
rozkładem, przy czym pierwszy szczyt jego
występowania dotyczy wieku rozwojowego
(poniżej 15 r.ż.) [54]. U podłoża przedwczesnego dojrzewania płciowego u chorych z
gruczolakiem lub rakiem nadnerczy leży
zwiększona sekrecja dehydroepiandrosteronu i androstendionu, które w tkankach
obwodowych ulegają albo konwersji do
testosteronu i dihydrotestosteronu, albo też
dalszej aromatyzacji do estronu i estradiolu
[55]. W pierwszym przypadku, mającym
miejsce znacznie częściej, dojrzewanie
płciowe u chłopców ma charakter izoseksualny, natomiast w drugim (rzadszym) jest
ono heteroseksualne. Do tego ostatniego
dochodzi również w stanach zwiększonej
aktywności aromatazy w nadnerczach. O ile
zwiększone powstawanie androgenów jest
stwierdzane zarówno w gruczolakach, jak i
rakach nadnerczy, wystąpienie u chłopców
heteroseksualnej postaci przedwczesnego
dojrzewania płciowego, a zwłaszcza cech
feminizacji jest niepokojące, gdyż sekrecja
estrogenów przez nadnercza prawie zawsze przemawia za złośliwym charakterem
zmiany [56].
Za rozpoznaniem guza nadnercza przemawia szybki postęp pokwitania, wyraźnie
zaznaczone cechy androgenizacji oraz
obecne u wieku pacjentów objawy współistniejącego zespołu Cushinga [54]. Rzadziej
występuje feminizacja, bądź współistnienie
androgenizacji i feminizacji [55].
W badaniach dodatkowych zwraca
uwagę bardzo wyraźny wzrost stężenia
siarczanu dehydroepiandrosteronu, podczas gdy stężenie testosteronu jest najczęściej umiarkowanie (rzadziej znacznie)
podwyższone [57]. Podwyższone stężenia
dehydroepiandrosteronu nie ulegają najczęściej normalizacji po podaniu deksametazonu, co przemawia za autonomicznym
wydzielaniem androgenów nadnerczowych
[54]. Zwraca ponadto uwagę zwiększone
R. Krysiak i wsp.
wydalanie 17-ketosteroidów z moczem [23],
zaś w przypadku guzów feminizujących zwiększone stężenie estrogenów [56]. W
tomografii komputerowej i rezonansie magnetycznym stwierdza się obecność zmiany
w nadnerczy, przy czym duże jej rozmiary
i nieregularne kształty wskazują na możliwość występowania raka nadnerczy [54].
Należy wyraźnie podkreślić, iż w diagnostyce hormonalnie czynnych zmian
rozrostowych nadnerczy (podobnie jak i
jąder) przydatność oznaczeń hormonalnych
jest ograniczona, z powodu dużej rzadkości występowania tych guzów (względem
innych schorzeń doprowadzających do
podobnych odchyleń hormonalnych) oraz
ze względu na stosunkowo niewielką czułość i specyficzność obecnie stosowanych
oznaczeń (wykrywają one zwykle zmiany
zaawansowane) [56].
Nowotwory jąder
Objawy przedwczesnego dojrzewania
płciowego u chłopców w rzadkich przypadkach stanowią konsekwencję guzów jądra.
Możemy je podzielić na guzy wywodzące
się ze sznurów płciowych i podścieliska
(sex cord-stromal tumors), do których należą guzy z komórek Leydiga (leydigioma),
guzy z komórek Sertoliego (sertolioma),
oraz omówione w osobnym podrozdziale
guzy zarodkowe.
Guzy z komórek Leydiga stanowią zaledwie 1-3% wszystkich guzów jąder [13].
Około 10% z nich wykazuje cechy złośliwości [13]. Tylko u co 10 osoby z guzem z
komórek Leydiga dochodzi do wystąpienia
objawów klinicznych, przy czym średni wieku
ujawnienia się przedwczesnego dojrzewania
płciowego u chłopców o tym podłożu to 7 lat
[58]. Dojrzewanie to stanowi konsekwencję
zwiększonego wydzielania androgenów,
zwłaszcza testosteronu przez komórki
guza [59]. U chorych z obecnością guzów
z komórek Leydiga opisywano ponadto
kazuistyczne przypadki heteroseksualnego
dojrzewania płciowego, uwarunkowanego
zwiększoną produkcją estrogenów przez
nowotwór, bądź też zwiększoną aromatyzacją androgenów w tkankach obwodowych
[60]. U niektórych chorych z guzami Leydiga
stwierdza się obecność aktywującej mutacji
receptora dla LH (Asp578His) [13]. Cechą
charakterystyczną przedwczesnego dojrzewania płciowego o takiej etiologii jest jednostronne powiększenie jąder, współistniejące
niejednokrotnie z obrzękiem dotkniętego
procesem chorobowym jądra. Natomiast w
następstwie spadku stężenia LH przeciwstronne jądro często ulega zanikowi [59]. Z
racji niewielkich wymiarów tych nowotworów
dużą wartość w ich rozpoznawaniu przypisuje się badaniu ultrasonograficznemu [60].
U młodych dorosłych dochodzić może do
rozwoju ginekomastii [58].
Opisywano ponadto przypadki przedwczesnego dojrzewania płciowego pochodzenia obwodowego o charakterze
heteroseksualnym w przypadku guzów z
komórek Sertoliego współistniejących z
zespołem Peutza-Jeghersa (bardzo rzadko
izolowanych), najprawdopodobniej wskutek
lokalnie zwiększonej aktywności aromatazy
w obrębie samego guza [61].
Za rozpoznaniem guza jądra jako
Przegląd Lekarski 2014 / 71 / 10
przyczyny przedwczesnego pokwitania
przemawia wykazanie wysokiego stężenia
testosteronu całkowitego i wolnego oraz
bardzo niskiego stężenia gonadotropin
[45]. W przypadku zwiększenia aktywności
aromatazy zwraca uwagę podwyższone
stężenie estrogenów [23].
Guzy zarodkowe
Guzy zarodkowe (germ cell tumors)
stanowią grupę nowotworów rozwijających
się z komórek germinalnych. Wyróżniamy
dwie podgrupy tych nowotworów. Pierwszą
z nich stanowią rozrodczaki (germinoma),
które dodatkowo dzieli się na „czyste”
rozrodczaki oraz rozrodczaki z obecnością
komórek olbrzymich syncytiotrofoblastu [62].
Rozrodczaki zlokalizowane w jądrze określa
się często nazwą nasieniaków [63]. Drugą
grupę nowotworów zarodkowych stanowią
tzw. „guzy nienasieniakowe”, do których
należą: rak zarodkowy, guz pęcherzyka
żółtkowego, rak kosmówki, potworniak; jak
również gorzej zdefiniowane wielozarodkowiak i rozrodczak zarodkowy (gonadoblastoma) [62]. Poza jądrami guzy zarodkowe mogą lokalizować się w śródpiersiu
przednim (zwłaszcza grasicy), przestrzeni
zaotrzewnowej, jak również w ośrodkowym
układzie nerwowym (szyszynka, okolica
nadsiodłowa) [63].
U podłoża postaci obwodowej leży
zwiększone wytwarzanie przez guza
β-gonadotropiny kosmówkowej, która wykazuje zdolność pobudzanie receptora dla
LH/β-gonadotropiny kosmówkowej [64]. Ta
postać dojrzewania płciowego występuje
praktycznie wyłącznie u chłopców, zaś jej
patogeneza jest zbliżona do patogenezy
rodzinnego męskiego dojrzewania płciowego [63]. Relatywnie słaby rozwój jąder,
typowy dla tych chorych, wynika z faktu,
iż izolowana sekrecja β-gonadotropiny
kosmówkowej doprowadza do hiperplazji
komórek Leydiga, nie powodując równocześnie stymulacji komórek Sertoliego [63].
Ponieważ warunkiem wystąpienia postaci
obwodowej przedwczesnego dojrzewania
płciowego jest obecność podwyższonych
stężeń β-gonadotropiny kosmówkowej, ta
postać przedwczesnego dojrzewania płciowego nie występuje w przypadku czystych
rozrodczaków, może być jednak obecna w
przypadku współwystępowania komórek
olbrzymich syncytiotrofoblastu lub też w
przebiegu guzów nienasieniakowych, takich
jak rak kosmówki i niektóre potworniaki
niedojrzałe, raki zarodkowe oraz rozrodczaki zarodkowe [64]. Podobny mechanizm
odpowiada za przedwczesne dojrzewanie
płciowe w przypadku obecności zmiany o
morfologii hepatoblastoma [45].
Poza postacią obwodową guzy germinalne ośrodkowego układu nerwowego
mogą powodować postać ośrodkową
przedwczesnego dojrzewania płciowego.
Dochodzi do niej niezależnie ich budowy
histopatologicznej, przy czym mechanizm
jest taki sam jak w innych zmianach rozrostowych ośrodkowego układu nerwowego
[63].
Wrodzona hipoplazja nadnerczy
Przedwczesne izoseksualne dojrzewanie płciowe u chłopców było w pojedynczych
przypadkach wynikiem wrodzonej hipoplazji nadnerczy, uwarunkowanej mutacją
genu DAX-1 [10]. Przyjmuje się, iż bardzo
wysokie u tych chorych stężenia ACTH
wykazują zdolność pobudzania komórek
Leydiga do produkcji testosteronu [13]. W
takich przypadkach korzystny efekt wykazuje podawanie glukokortykoidów [65].
Należy podkreślić, iż znacznie częściej we
wrodzonej hipoplazji nadnerczy dochodzi
do opóźnionego dojrzewania płciowego
w następstwie często obserwowanego u
takich osób hipogonadyzmu hipogonadotropowego [65].
Zespół oporności na glukokortykosteroidy
Opisano kazuistyczne przypadku izoseksualnego przedwczesnego dojrzewania
płciowego u chłopców z zespołem oporności
na glukokortykoidy, u podłoża którego leżała
częściowa niezdolność glukokortykoidów do
wykazywania swojego działania w tkankach
[66]. Konsekwencją upośledzonego działania glukokortykoidów jest wzrost sekrecji
mineralokortykoidów oraz androgenów nadnerczowych, warunkujący objawy kliniczne
[67]. Za takim podłożem przedwczesnego
dojrzewania płciowego przemawia obecność u chorych nadciśnienia tętniczego i
hipokaliemii (jako wynik nadmiaru mineralokortykoidów) oraz przewlekłego osłabienia
(w następstwie upośledzonego działania
glukokortykoidów) [45]. W przypadkach
nieleczonych u mężczyzn rozwijać się mogą
zaburzenia spermatogenezy, a nawet niepłodność, jako wynik hamującego wpływu
wysokich stężeń androgenów nadnerczowych na sekrecję FSH oraz stymulowanie
wzrostu reszt nadnerczowych pod wpływem
wysokich stężeń ACTH [67].
Charakterystyczną cechą schorzenia
jest bardzo duża zmienność nasilenia dolegliwości, tłumaczona z jednej strony różnego
stopnia opornością tkanek na glukokortykoidy oraz różnego stopnia wrażliwością
tkanek na mineralokortykoidy i androgeny
nadnerczowe [45].
Mutacje genu aromatazy
W bardzo rzadkich przypadkach u podłoża przedwczesnego dojrzewania płciowego pochodzenia obwodowego może leżeć
obecność zmniejszonej lub zwiększonej
aktywności aromatazy, enzymu odpowiedzialnego za konwersję androgenów do
odpowiadających im estrogenów, wskutek
mutacji aktywującej lub hamującej genu
CYP19 [68].
Przedwczesne dojrzewanie płciowe na
tle niedoboru aromatazy jest spowodowane
nadmierną kumulację dehydroepiandrosteronu i - w mniejszym stopniu - androstendionu i testosteronu, charakteryzując się zwykle
wystąpieniem przedwczesnego owłosienia
w okolicy narządów płciowych [69]. W
przeciwieństwie do większości przypadków
przedwczesnego dojrzewania płciowego
zwraca uwagę wysoki wzrost, stanowiący
konsekwencję opóźnionego zarastania
chrząstek nasadowych, które wymaga
odpowiednio wysokich stężeń estrogenów,
niemożliwych do osiągnięcia w stanach
niedoboru powyższego enzymu [45]. Innymi objawami mogącymi przemawiać za
553
niedoborem aromatazy są: eunochoidalna
budowa ciała, osteopenia lub osteoporoza,
koślawość kolan, otyłość trzewna, cechy
insulinooporności, dyslipidemia aterogenna
oraz zwiększone ryzyko wystąpienia cukrzycy [68]. W badaniach dodatkowych zwraca
uwagę bardzo niskie stężenie estradiolu i
estronu, współistniejące z podwyższonym
poziomem gonadotropin i podwyższonym
lub mieszczącym się w granicach normy stężeniem androgenów [68]. Stąd w leczeniu
próbuje się stosować estrogeny [68].
Mutacja aktywująca genu aromatazy powoduje rozwój bardzo rzadkiego schorzenia
określanego nazwami zespołu nadmiaru
aromatazy lub rodzinnego hiperestrogenizmu [69]. Jak dotąd opisano je u kilkunastu
osób należących do jednej z czterech rodzin
[70]. Obserwowane w tych przypadkach dojrzewanie płciowe ma u chłopców charakter
heteroseksualny i współistnieje z innymi objawami klinicznymi, takimi jak: ginekomastia
przedpokwitaniowa lub okołopokwitaniowa
(zwykle o dużym nasileniu), przyspieszenie
wieku kostnego, niski wzrost ostateczny,
rozwój małego prącia oraz niekiedy również
inne objawy hipogonadyzmu [71]. Obecności powyższego schorzenia dowodzi zwiększone stężenie estrogenów (wyraźniejsze
dla estronu niż estradiolu), prawidłowe lub
obniżone stężenie gonadotropin, niskie
stężenia androstendionu i testosteronu
oraz zwiększenie wartości stosunku stężeń
estradiolu do testosteronu, zwłaszcza po
podaniu testosteronu (stosunek ten może
nawet 100-krotnie przewyższać wartość
u osób zdrowych) [70]. Zwraca ponadto
uwagę obniżenie, a niekiedy nawet normalizacja, estrogenemii po podaniu inhibitorów
aromatazy [70].
Niedoczynność tarczycy
Chociaż niedoczynność tarczycy opóźniać może wystąpienie pokwitania, jednak
w rzadkich przypadkach dzieci z niedoczynnością tarczycy opisywano występowanie
przedwczesnego obwodowego dojrzewania
płciowego [45]. W przypadku dziewcząt,
stanowiących większość takich pacjentów,
współistniało ono często z występowaniem
torbieli w jajnikach, co określane jest nazwą zespołu van Wyk-Grumbacha [72].
Kazuistyczne przypadki dotyczyły jednak
również chłopców [12]. Duża rzadkość
przedwczesnego dojrzewania o takim podłożu wynika bowiem z faktu, iż do ujawnienia
się go wymagana jest obecność ciężkiej
i utrzymującej się przewlekle pierwotnej
niedoczynności tarczycy, za czym przemawia obserwowany niekiedy w badaniach
obrazowych przerost przysadki (jako wynik
powiększenia się komórek tyreotropowych)
[45]. Typowe dla ciężkiej niedoczynności
tarczycy wysokie stężenia TSH wykazują,
wskutek niewielkiego powinowactwa do
receptorów dla FSH, zdolność pobudzenia
tych receptorów i w sprzyjających warunkach
wystąpienie przedwczesnego dojrzewania
płciowego, które ma charakter izoseksualny
i towarzyszy mu - w przeciwieństwie do innych postaci przedwczesnego dojrzewania
-opóźnienie (a nie przyspieszenie wieku
kostnego) [13]. Stężenie LH jest niskie [13].
W badaniu fizykalnym zwraca uwagę powiększenie jąder (jako wynik zwiększonej
554
proliferacji komórek Sertoliego), przy braku
cech wirylizacji i owłosienia okolic płciowych
[45]. Zastosowanie terapii suplementacyjnej
L-tyroksyną doprowadzać może do powrotu
stanu chorych do stanu prepubertalnego
[27].
Inne postacie przedwczesnego dojrzewania płciowego o charakterze obwodowym
Opisano nieliczne przypadki obwodowej postaci przedwczesnego dojrzewania
płciowego o charakterze izoseksualnym u
chłopców w wyniku stosowania egzogennych androgenów, głównie maści, mazideł i
kremów zawierających testosteron lub dihydrotestosteron [2] oraz pojedyncze przypadki na tle nadaktywności 5-α reduktazy, która
warunkuje przekształcania testosteronu do
dihydrotestosteronu [72].
Przedwczesne adrenarche
W rzadkich przypadkach u chłopców
poniżej 9 r.ż. dochodzić może do pojawienia się owłosienia łonowego i pachowego,
współistniejącego niekiedy z niewielkim
przyspieszeniem wzrastania i nieznacznie
przyspieszonym wiekiem kostnym, jednak
bez innych wykładników przedwczesnego
dojrzewania płciowego [4]. Czynnikami predysponującymi do wystąpienia powyższych
objawów, określanych nazwą przedwczesnego adrenarche (adrenarche praecox),
są: niski wzrost i masa urodzeniowa,
współistniejąca nadwaga lub otyłość [73].
Nie stwierdza się jednak powiększenia jąder
[73]. Choć traktowane jako wariant normy,
zwiększają ryzyko rozwoju w późniejszym
wieku insulinooporności i dyslipidemii [74].
Przypadki takie wymagają różnicowania z
przedwczesnym dojrzewaniem płciowym
na tle chorób nadnerczy (zwłaszcza ich
wrodzonego przerostu) i nowotworów
wytwarzających androgeny [74]. W przypadku przedwczesnego adrenarche stężenia siarczanu dehydroepiandrosteronu
(i dehydroepiandrosteronu) oraz - choć
rzadziej - androstendionu i testosteronu
są niewiele podwyższone względem wieku
metrykalnego dziecka, odpowiadając wartościom spotykanym we wczesnym okresie
pokwitania [4].
Wtórne przedwczesne dojrzewanie
płciowe pochodzenia ośrodkowego
Szczególną (i trudną do leczenia)
postacią przedwczesnego dojrzewania
płciowego jest tzw. wtórne przedwczesne dojrzewanie płciowe pochodzenia
ośrodkowego, rozwijające się pod wpływem
terapii chłopców (i dziewcząt) z obwodową
postacią przedwczesnego dojrzewania
płciowego, u których wysokie stężenia
hormonów płciowych utrzymywały się
przez dłuższy okres czasu [72]. Dotyczy to
zwłaszcza przypadków ma tle wrodzonego
przerostu nadnerczy, rodzinnego męskiego
przedwczesnego dojrzewania płciowego,
zespołu McCune-Albrighta oraz zmian nowotworowych i wymaga leczenia [25].
W przebiegu tych schorzeń może
bowiem dochodzić do pewnej stymulacji
komórek wydzielających gonadoliberynę,
jednak charakterystyczny dla tej choroby
nadmiar androgenów blokuje aktywność osi
podwzgórzowo-przysadkowo-gonadalnej na
poziomie przysadki [12,15]. W warunkach
rozpoczętego leczenia i wynikającego z tego
spadku stężenia androgenów dochodzi po
różnym okresie czasu (niekiedy po zaledwie
paru tygodniach) do zwiększonego wyrzutu
gonadotropin połączonego z aktywacją neuronów wydzielających gonadoliberynę i - w
konsekwencji - rozwoju ośrodkowej postaci
przedwczesnego dojrzewania [14,72].
Diagnostyka przedwczesnego dojrzewania płciowego
W przypadku chłopca z wykładnikami
przedwczesnego dojrzewania płciowego
należy ustalić wiek, w którym rozpoczęło
się pokwitanie, określić szybkość progresji
pokwitania, zbadać przebieg krzywej wzrastania, przeprowadzić dokładne badanie
fizykalne z oceną wtórnych cech płciowych
i określeniem stadium rozwoju płciowego w
skali Tannera, jak również przeprowadzić
diagnostykę różnicową [12,26]. Jest ona
szczególnie ważna w przypadku objawów
sugerujących obecność zmiany organicznej
w obrębie ośrodkowego układu nerwowego,
nadnerczy lub jąder, takich jak: początek
pokwitania przed 4 r.ż., szybki postęp pokwitania oraz objawy mogące sugerować
zmianę ogniskową (drgawki, bóle głowy
oraz neurologiczne objawy uciskowe, cechy
nadmiaru glukokortykoidów, jednostronne
powiększenie jąder) [5,27].
W każdym przypadku kluczowe znaczenie przypada określeniu czy przedwczesne
dojrzewanie płciowe ma charakter ośrodkowy czy też obwodowy. Za ośrodkowym podłożem przemawia zachowanie fizjologicznej
sekwencji pokwitania, której pierwszym
objawem jest powiększenie jąder poprzedzające pojawienie się owłosienia łonowego, jak również wystąpienie szczytu skoku
wzrostowego w środkowej fazie pokwitania
[4]. Ponadto, o ile w przypadku postaci
ośrodkowej powiększenie jąder współistnieje z wykształceniem owłosienia pachowego
i łonowego oraz zwiększeniem wymiarów
prącia, w wielu przypadkach postaci obwodowej dwóm ostatnim objawom towarzyszą
przedpokwitaniowe wymiary jądra lub tylko
niewielkie ich powiększenie [7]. Obustronne
powiększenie jąder dotyczy osób z postacią
ośrodkową przedwczesnego pokwitania
oraz - co jest znacznie słabiej wyrażone
(nigdy nie przekracza stadium 3 w skali Tannera) w rodzinnym męskim przedwczesnym
dojrzewaniem płciowym, guzach zarodkowych, przeroście reszt nadnerczowych we
wrodzonym przeroście nadnerczy i bardzo
rzadko we wrodzonej hipoplazji nadnerczy,
natomiast asymetryczne ich powiększenie
jest obserwowane u pacjentów z zespołem
McCune-Albrighta lub guzem z komórek
Leydiga 72].
Pomimo różnic w obrazie klinicznym,
rozpoznawanie postaci przedwczesnego
dojrzewania płciowego wymaga wykonania
badań hormonalnych. Pewną ograniczoną
wartość przesiewową odgrywać może ocena
stężenia LH lub jego wydalania z moczem
[75]. Nieco większa wartość przypada ocenie rytmu dobowego LH, które w przypadku
ośrodkowej postaci przedwczes������������
nego dojrzewania płciowego charakteryzuje się większą
amplitudą i pojawieniem się wyrzutów w
R. Krysiak i wsp.
godzinach nocnych [6]. Za rozpoznaniem
postaci obwodowej przedwczesnego dojrzewania płciowego przemawia stwierdzenie
niskiego stężenia gonadotropin, jak również
braku nocnych wyrzutów LH [37]. Z uwagi
na pokrywanie się wartości oznaczeń ze
stwierdzanymi w okresie przedpokwitaniowym znaczenie oceny stężenia FSH
w osoczu lub jego wydalania z moczem
jest mniejsze niż LH [75]. Nie oznacza się
stężeń gonadoliberyny, gdyż podobnie jak
w przypadku większości innych hormonów
podwzgórza ma ona bardzo krótki okres
półtrwania (2-4 minuty), zaś jest stężenie we
krwi obwodowej nie odzwierciedla stężenia
w krążeniu przysadkowym [6,13].
Kluczowe znaczenie w określeniu postaci przedwczesnego dojrzewania przypada
testowi z egzogenną gonadoliberyną lub jej
analogami. Gonadoliberyna jest podawana
dożylnie lub podskórnie w dawce 100 µg
(po całonocnym powstrzymywaniu się od
posiłków), zaś ocena stężeń gonadotropin
(przynajmniej LH) powinna być dokonywana
na czczo oraz w odstępach 15 minutowych
przez godzinę od jej podania [6,7]. W przypadku wyboru analogu gonadoliberyny, krew
jest pobierana od 30 do 120 minuty [13].
Przy interpretacji wyniku należy pamiętać
o tym, że wzrost stężenia gonadotropin
jest uwarunkowany etapem dojrzewania
płciowego. W przypadku ośrodkowej postaci przedwczesnego dojrzewania płciowego dochodzi do co najmniej 2-3-krotnego
wzrostu stężenia LH, które osiąga wartości
przekraczające 10 IU/l [6,27]. Wzrost stężenia LH jest zwykle nie tylko większy niż u
rówieśników, ale również niż u dzieci z tym
samym stadium pokwitania [25]. Dochodzi
również do zmian proporcji stężeń LH/FSH,
mającego znaczenie w określeniu okresu
pokwitania [75]. W przeciwieństwie do
postaci ośrodkowej w postaci obwodowej
nie dochodzi do wzrostu stężeń gonadotropin lub jest on minimalny i odpowiada
przedpokwitaniowemu wzorcowi odpowiedzi
gonadotropin (szczególnie LH) na podanie
gonadoliberyny [14].
W przypadku przedwczesnego dojrzewania płciowego wskazane jest oznaczenie stężeń testosteronu, siarczanu dehydroepiandrosteronu (lub dehydroepiandrosteronu),
17-hydroksyprogesteronu, β-gonadotropiny
kosmówkowej, α-fetoproteiny, ACTH oraz
kortyzolu [75]. Zbadanie dwóch pierwszych
hormonów ma wartość w różnicowaniu
jądrowego i nadnerczowego źródła nadmiarów androgenów. Ocena kolejnych trzech
markerów umożliwia wykluczenie wrodzonego przerostu nadnerczy (nadmiar ������
17-hydroksyprogesteronu) oraz niektórych guzów
zarodkowych (nadmiar β-gonadotropiny
kosmówkowej oraz/lub α-fetoproteiny) [45].
Natomiast zbadanie stężeń TSH i wolnej tyroksyny pozwala na wykluczenie niedoczynności tarczycy. O ile w postaci klasycznej
wrodzonego przerostu nadnerczy stężenie
17-hydroksyprogesteronu jest podwyższone
już w warunkach wyjściowych, w postaciach
nieklasycznych wymagane jest wykonanie
testu z tetrakozaktydem, będącym fragmentem cząsteczki ACTH, który w przypadku
niedoboru 21-hydroksylazy powoduje wzrost
stężenia 17-hydroksyprogesteronu do powyżej 15 ng/ml. Natomiast w niedoborze
Przegląd Lekarski 2014 / 71 / 10
11β-hydroksylazy po podaniu tetrakozaktydu obserwuje się co najmniej trzykrotny
wzrost stężenia 11-dezoksykortykosteronu
i/lub 11-dezoksykortyzolu, jak również
zwiększone wydalanie w dobowej zbiórce
moczu tetrahydrodezoksykortyzolu oraz
tetrahydrodezoksykortykosteronu [14,52]. W
przypadku zespołu oporności na glukokortykoidy zwraca uwagę wzrost stężeń ACTH
i kortyzolu z zachowanym rytmem dobowym, jak również wzrost stężeń siarczanu
dehydroepiandrosteronu, androstendionu,
kortykosteronu i dezoksykortykosteronu w
osoczu [76]. Po podaniu 1 mg deksametazonu nie obserwuje się spadku stężenia
kortyzolu poniżej 1,8 µg/dl, natomiast po
podaniu insuliny obserwuje się prawidłowy
wzrost stężeń ACTH i kortyzolu [66,76].
W większości przypadków zwraca wówczas uwagę przyspieszenie wieku kostnego
względem wieku metrykalnego, przy czym
w przypadku, gdy różnica ta przekracza
dwa odchylenia standardowe istnieje duże
prawdopodobieństwo organicznej przyczyny
przedwczesnego dojrzewania [26]. W sugerowanej przez niektórych autorów ocenie
stosunku ∆ wieku kostnego do ∆ wieku
metrykalnego - typowa dla przedwczesnego
dojrzewania płciowego jest wartość tego
ilorazu powyżej 1,2 [25]. Przyspieszenie
wieku kostnego może nie być stwierdzane,
a nawet wiek kostny może być opóźniony
względem metrykalnego w przypadku
współistniejącego niedoboru GH oraz niedoczynności tarczycy [14].
W każdym przypadku ośrodkowej postaci przedwczesnego dojrzewania płciowego
wskazane jest wykonanie badania obrazowego ośrodkowego układu nerwowego
(najlepiej rezonansu magnetycznego) [17].
Natomiast w postaci obwodowej, w przypadku podejrzenia patologii w obrębie jąder
lub nadnerczy wymagane jest wykonanie
odpowiednio USG jąder lub tomografii komputerowej albo rezonansu magnetycznego
nadnerczy [1]. Niektórzy autorzy zalecają
ocenę jąder nawet w postaci ośrodkowej,
w której to postaci stwierdza się ich symetryczne powiększenie [17].
Leczenie
Różnicowanie pomiędzy ośrodkową i
obwodową postacią przedwczesnego dojrzewania płciowego ma istotne znaczenie,
nie tylko ze względów diagnostycznych i rokowniczych, ale również z uwagi na zupełnie
odmienne podejście terapeutyczne.
Postać ośrodkowa przedwczesnego
dojrzewania płciowego
Podstawową formą leczenia przedwczesnego dojrzewania płciowego o podłożu
ośrodkowym jest stosowanie analogów gonadoliberyny. W przypadkach nieleczonych
bowiem wzrost chłopców jest średnio trzy
odchylenia standardowe mniejszy niż ich
zdrowych rówieśników [77]. Znajdują one
wykorzystanie w leczeniu postaci idiopatycznej, postaci wtórnej do nienowotworowych
schorzeń ośrodkowego układu nerwowego,
a także w przypadkach, w których leczenie
przyczynowe nie jest znane lub jest nieefektywne [18]. Postępowanie zabiegowe
jest natomiast wymagane w przypadku
obecności zmiany ekspansywnej w obrębie
ośrodkowego układu nerwowego [22]. Za
zasadnością farmakoterapii w przypadku
hamartoma przemawia jej nienowotworowy charakter, rzadkie przypadki wzrostu
zmiany oraz ryzyko powikłań w przypadku
postępowania operacyjnego, które obecnie
rezerwuje się dla dużych zmian, których
obecność jest związana z wystąpieniem
objawów neurologicznych [17,18].
Jedyną rekomendowaną obecnie metodą farmakoterapii przedwczesnego dojrzewania płciowego pochodzenia ośrodkowego
jest stosowanie analogów gonadoliberyny.
Sam hormon z uwagi na bardzo krótki
okres półtrwania nie znajduje zastosowania w terapii. W przypadku stosowania
agonistów gonadoliberyny wykorzystuje
się zjawisko „chemicznej kastracji”, czyli
zmniejszenie aktywności osi podwzgórzeprzysadka-jądro w warunkach przewlekłego
podawania analogów gonadoliberyny [32].
O ile bowiem zastosowanie gonadoliberyny
w dawkach fizjologicznych z zachowaniem
pulsacyjnego wzorca podawania pobudza
swoiste receptory i zwiększa sekrecję gonadotropin, utrzymywanie się przewlekle
podwyższonych stężeń tego hormonu powoduje desensytyzację receptora i hamuje
sekrecję FSH i LH [78]. Do obecnie stosowanych należą: tryptorelina, leuprorelina,
goserelina, histrelina i rzadziej stosowane:
buserelina i deslorelina [77]. Leczenie to
powinno być podjęte u wszystkich chłopców
z ośrodkową postacią przedwczesnego
dojrzewania płciowego, u których stężenie
testosteronu oraz maksymalny wzrost LH
w teście z gonadoliberyną odpowiadają
wartościom pokwitaniowym, przewidywany
wzrost końcowy mieści się poniżej 3 centyla
lub poniżej zakładanego przedziału wzrostu,
zakładany wzrost ostateczny zmniejsza
się w czasie kolejnych wizyt kontrolnych,
występuje progresja dojrzewania oraz pojawiają się problemy natury psychologicznej
lub behawioralnej pacjentów związane z
przyspieszonym dojrzewaniem [77]. Pod
wpływem podawania analogów gonadoliberyny dochodzi u chłopców do zmniejszenia
objętości jąder, spadku częstości erekcji, jak
również rzadziej występują i mają mniejsze
nasilenia zachowania agresywne [26].
Ponadto zwraca uwagę zwolnienie tempa
wzrastania i wskaźnika dojrzałości kośćca
[14]. Ponieważ owłosienie łonowe jest kontrolowane przez androgeny nadnerczowe,
pod wpływem analogów gonadoliberyny
nie dochodzi natomiast do zmniejszenia lub obserwuje się jedynie niewielkie
zmniejszenie tego owłosienia [7]. Poprawie
klinicznej towarzyszy normalizacja stężeń
gonadotropin (w tym stężeń oznaczanych
po podawaniu gonadoliberyny lub jej analogów) oraz testosteronu, obserwowana
już w ciągu pierwszego miesiąca terapii i
utrzymująca się przez cały okres terapii [4].
Ponadto w wyniku zaburzenia transkrypcji
genów podjednostek LH, po zastosowaniu
agonistów gonadoliberyny powstały LH jest
pozbawiony pełnej aktywności biologicznej
[25]. Działanie agonistów gonadoliberyny
jest jednak odwracalne i ustępuje po przerwaniu leczenia i tym samym nie wpływa na
aktywność seksualną i płodność w późniejszym okresie życia [78].
W leczeniu ośrodkowej postaci przed555
wczesnego dojrzewania płciowego stosuje się najczęściej preparaty agonistów
gonadoliberyny o przedłużonym działaniu,
zapewniające lepszy stopień współpracy z
pacjentem i jego rodzicami, a zdaniem niektórych autorów umożliwiające osiągniecie
wyższego wzrostu końcowego, niż w przypadku preparatów podawanych codziennie
[12,78]. Najczęściej zastosowanie znajdują
tryptorelina (3,75 mg), leuprorelina (3,75 mg
w Europie, 7,5-15 mg w Stanach Zjednoczonych) oraz goserelina (3,6 mg) podawane
zwykle co 28 dni [77]. Niektórzy agoniści gonadoliberyny mogą być podawani raz na trzy
miesiące: tryptorelina i leuprorelina w dawce
11,25 mg, natomiast goserelina w dawce
10,8 mg [13]. Najdłuższe działanie wykazują
podskórne implanty histreliny, uwalniające
średnio 65 µg dziennie tego związku przez
12 miesięcy [79]. Czas trwania leczenia
jest osobniczo zmienny i zależy od wieku
kostnego, uwarunkowań psychosocjalnych
oraz opinii rodziny [78]. Zwykle leczenie u
chłopców przerywa się pomiędzy 13 a 13,5
[13] lub 13,5-14 [77] rokiem życia.
Leczenie analogami gonadoliberyny
wymaga okresowych badań kontrolnych,
które w pierwszym roku leczenia powinny
odbywać się raz na trzy miesiące, a w kolejnych - w zależności od efektywności terapii
[13]. Obejmują one - poza oceną kliniczną (w
tym określeniem wzrostu i masy ciała, zbadaniem przebiegu krzywej wzrastania oraz
stopnia zaawansowania rozwoju płciowego
w skali Tannera z uwzględnieniem stopnia
regresji drugorzędowych cech płciowych)
wykonanie oznaczeń hormonalnych. Dowodem efektywności stosowanej terapii jest
obniżenie stężeń hormonów do wartości
stwierdzanych przed pokwitaniem [79]. Stężenie testosteronu powinno wynosić poniżej
0,3 ng/ml, LH poniżej 0,6 U/L, natomiast
stężenie LH po podaniu gonadoliberyny lub
jej analogu poniżej 2,3 U/L [17]. Ponieważ
niskie stężenie testosteronu u chłopców
przemawia za wystarczającym zahamowaniem funkcji hormonalnej jądra, niektórzy
autorzy nie zalecają jednak rutynowego
wykonywania testu z gonadoliberyną lub
jej analogiem [3].
Lepsze efekty leczenia obserwuje się u
chłopców ze zmianami czynnościowymi niż
organicznymi [77]. Do czynników mających
korzystne znaczenie prognostyczne należą:
relatywnie młody wiek kostny, młodszy wiek
metrykalny, wczesne wdrożenie leczenia w
stosunku do ujawnienia się objawów klinicznych, wyjściowo szybki postęp pokwitania,
dłuższy okres leczenia, wyższy wzrost rodziców [80,81]. Celem osiągnięcia wyższego
wzrostu ostatecznego niektórzy autorzy
kojarzą podawanie analogów gonadoliberyny z hormonem wzrostu lub - rzadziej - z
oksandrolonem, który jest androgenem niepodlegającym aromatyzacji [3,80].
Terapia agonistami gonadoliberyny jest
dobrze tolerowana. Działania niepożądane
obserwowane są rzadko (jeszcze rzadziej
niż u dziewcząt) i najczęściej mają charakter
objawów uczuleniowych [72, 77]. Brakuje
danych, by terapia taka, zastosowana w
okresie dojrzewania, powodowała niekorzystny wpływ na gęstość mineralną tkanki
kostnej [82].
Pewną alternatywą do podawania
556
agonistów gonadoliberyny jest stosowanie
antagonistów gonadoliberyny, do których
należą: ganirelix, cetrorelix oraz abarelix,
wykazujących zdolność blokowania receptora dla gonadoliberyny i których początek
działania ujawnia się wkrótce po ich zastosowaniu. Brakuje jednak wystarczającej
liczby danych uzasadniających tę formę
terapii ośrodkowej postaci przedwczesnego
dojrzewania płciowego u chłopców [78].
Postać obwodowa przedwczesnego
dojrzewania płciowego
Z uwagi na zahamowanie aktywności
osi podwzgórze-przysadka-jądro stosowanie analogów gonadoliberyny jest nieuzasadnione za wyjątkiem wtórnej postaci
ośrodkowej przedwczesnego dojrzewania
płciowego [12].
Leczenie rodzinnego męskiego przedwczesnego dojrzewania płciowego opiera
się głównie na stosowaniu leków antyandrogenowych, inhibitorów aromatazy
oraz leków hamujących steroidogenezę
naderczową. Działanie antyandrogenowe
charakteryzuje zwłaszcza spironolakton,
którego stosowanie jest jednak związane
z ryzykiem wystąpienia ginekomastii [37].
Do innych leków antyandrogenowych używanych w terapii tego schorzenia należą:
bikalutamid, octanu cyproteronu oraz octan
medroksyprogesteronu [42]. Natomiast
spośród leków hamujących syntezę androgenów zastosowanie znajduje najczęściej
ketokonazol, blokujący steroidogenezę
gonadalną i nadnerczową na poziomie kilku
enzymów [12,34]. Lek ten wykazuje jednak
działanie hepatotoksyczne, jak również
może sprzyjać rozwojowi niedoczynności
nadnerczy [47]. Ponadto z uwagi na ryzyko rozwoju wtórnej ośrodkowej postaci
przedwczesnego dojrzewania płciowego
stosowanie tego leku jest zwykle ograniczone do chłopców, u których wiek kostny
osiągnął już przedział pubertalny [34,37].
Wyniki badań z zastosowaniem inhibitora
aromatazy starszej generacji - testolaktonu
dostarczyły sprzecznych wyników. Wbrew
niezbyt zachęcającym wynikom początkowych badań w kolejnych wykazano, iż
zastosowanie testolaktonu, z następczym
(w momencie ujawnienia się wykładników
wtórnej postaci przedwczesnego dojrzewania płciowego) podawaniem desloreliny spowodowało zwolnienie szybkości wzrastania i
normalizację wieku kostnego [71]. Wyraźny
i korzystny wpływ na szybkość wzrastania
i normalizację wieku kostnego dostarczyły
ponadto kolejne badania z zastosowaniem
łącznego podawania anastrozolu z octanem cyproteronu, jak również kombinacji
anastrozolu i bikalutamidu [71]. Ta ostatnia
wiąże się jednak z bólami sutków i ginekomastią [13].
Terapia przedwczesnego dojrzewania
płciowego u chłopców z zespołem McCune-Albrighta opiera się na tych samych
zasadach co terapia rodzinnego męskiego
przedwczesnego dojrzewania płciowego
[45]. W ostatnich latach wykazano w tej
grupie pacjentów korzyści z terapii skojarzonej anastrozolem z bikalutamidem
[83]. Próbuje się również stosować octan
medroksyprogesteronu [83]. Obok leczenia
przedwczesnego dojrzewania płciowego u
chorych na ten zespół obowiązuje ponadto
leczenie innych endokrynopatii: hiperprolaktynemii (bromokryptyna, kwinagolid oraz
kabergolina), nadmiernego wydzielania
GH (analogi somatostatyny, kabergolina,
pegwisomant) oraz dysplazji włóknistej kości
(bisfosfoniany) [41,43].
Postępowaniem z wyboru w przedwczesnym dojrzewaniu płciowym na tle
wrodzonego przerostu nadnerczy jest
stosowanie glukokortykoidów [51]. Jest
ono konieczne we wszystkich przypadkach
klasycznej postaci tego zespołu, jak również
u tych pacjentów z postacią nieklasyczną,
u których występują objawy kliniczne [52].
W przypadku postaci choroby skojarzonej
z utratą soli, rozwijającej się w przebiegu
niedoboru 21-hydroksylazy, konieczne jest
ponadto podawanie fludrokortyzonu [50].
Natomiast w niedoborze 11β-hydroksylazy,
w którym często rozwija się nadciśnienie
tętnicze, wskazane jest podawanie antagonistów aldosteronu [52]. Preferowanym
glukokortykoidem dla dzieci w wieku rozwojowym jest hydrokortyzon, z uwagi na
mniej wyrażone objawy niepożądane (w tym
zaburzenie wzrostu) niż w przypadku prednizonu, prednizolonu czy deksametazonu,
wynikające z krótkiego okresu biologicznego
półtrwania tego hormonu [51]. Stosunkowo
niewielu autorów uważa ponadto za celowe
stosowanie w tym schorzeniu inhibitorów
aromatazy [42].
U chorych z nadmiarem aromatazy
logicznym postępowaniem z wyboru jest
stosowanie inhibitorów tego enzymu, z którym najlepiej przebadany jest anastrozol lub
androgenów niepodlegających konwersji do
estrogenów. Postępowanie takie poza zahamowaniem pokwitanie może u niektórych
chorych pozwalać na osiągnięcie wyższego
wzrostu końcowego [69,70]. Natomiast w
zespole oporności na glukokortykoidy stosuje się deksametazon w dawkach 1,5-3 mg
na dobę, podawanych zwykle jednorazowo
w godzinach wieczornych, w których wykazuje on zdolność pobudzenia receptora
glukokortykoidowego i hamowania sekrecji
ACTH [45]. Po uzyskaniu wymiernego efektu klinicznego u wielu chorych było możliwe
obniżenie dawki glukokortykoidów, nawet do
dawki 0,25-0,5 mg na dobę [76]. W przypadku współistniejącego nadciśnienia stosuje
się spironolakton [76].
W przypadku obecności zmian ogniskowych w nadnerczach lub gonadach zastosowanie znajduje leczenie zabiegowe [7]. W
przypadku guzów zarodkowych istotne znaczenie przypadać może radioterapii [62].
Podsumowanie
Przedwczesne dojrzewanie płciowe u
chłopców jest stosunkowo rzadko spotykanym problemem zdrowotnym. Jego obecność każdorazowo jednak powinna budzić
podejrzenie istnienia choroby wyjściowej,
gdyż prawdopodobieństwo wcześniejszej
aktywacji osi podwzgórzowo-przysadkowo-gonadalnej na tle idiopatycznym jest
u nich znacznie mniejsze niż u dziewcząt.
U podłoża przedwczesnego dojrzewania
u chłopców leżeć nadto mogą schorzenia,
które w istotny sposób wpływają na długość
życia, takie jak: nowotwory ośrodkowego
układu nerwowego, nadnerczy czy jąder, czy
R. Krysiak i wsp.
też wrodzony przerost nadnerczy. Dlatego
u każdego chłopca, u którego dochodzi
do rozwoju przedwczesnego dojrzewania
płciowego niezbędne jest przeprowadzenie dokładnej diagnostyki, uwzględniającej
oznaczenia hormonalne i badania obrazowe, która (poza potwierdzeniem istnienia
przedwczesnego pokwitania) powinna:
wykluczyć istnienie wariantu normy, jakim
jest przedwczesne adrenarche, ustalić postać pokwitania oraz - w miarę możliwości
- określić chorobę wyjściową. Zróżnicowanie
na postać obwodową i postać ośrodkową
jest niezmiernie istotne z uwagi na zupełnie odmienne podejście terapeutyczne w
obu tych przypadkach, natomiast ustalenie
podłoża umożliwia zastosowanie leczenia
objawowego, co powinno skutkować poprawą skuteczności terapii, której wyniki jak
dotąd są ciągle niezadowalające.
Piśmiennictwo
1. Nathan BM, Palmert MR: Regulation and disorders
of pubertal timing. Endocrinol Metab Clin North Am.
2005; 34: 617-641.
2. Wit JM , Hero M, Nunez SB: Aromatase inhibitors in
pediatrics. Nat Rev Endocrinol. 2011; 8: 135-147.
3. Carel JC, Lahlou N, Roger M, Chaussain JL: Precocious puberty and statural growth. Hum Reprod
Update. 2004; 10: 135-147.
4. Iughetti L, Predieri B, Ferrari M, Gallo C, Livio L. et
al: Diagnosis of central precocious puberty: endocrine
assessment. J Pediatr Endocrinol Metab. 2000; 13
(Suppl. 1): 709-715.
5. Tessaris D, Matarazzo P, Mussa A, Tuli G, Verna
F. et al: Combined treatment with bicalutamide and
anastrozole in a young boy with peripheral precocious
puberty due to McCune-Albright syndrome. Endocr
J. 2012; 59: 111-117.
6. Völkl TM, Dörr HG: McCune-Albright syndrome:
clinical picture and natural history in children and
adolescents. J Pediatr Endocrinol Metab. 2006; 19
(Suppl. 2): 551-559.
7. Jorsal T, Rørth M: Intracranial germ cell tumours. A
review with special reference to endocrine manifestations. Acta Oncol. 2012; 51: 3-9.
8. Krysiak R, Marek B, Okopień B: Przedwczesne
dojrzewanie płciowe pochodzenia ośrodkowego.
Endokrynol Pol. 2008; 5: 530-540.
9. Al-Agha OM, Axiotis CA: An in-depth look at Leydig
cell tumor of the testis. Arch Pathol Lab Med. 2007;
131: 311-317.
10. Cesario SK, Hughes LA: Precocious puberty: a
comprehensive review of literature. J Obstet Gynecol
Neonatal Nurs. 2007; 36: 263-274.
11. Arita K, Kurisu K, Kiura Y, Lida K, Otsubo H:
Hypothalamic hamartoma. Neurol Med Chir. 2005;
45: 221-231.
12. Charmandari E: Primary generalized glucocorticoid
resistance and hypersensitivity. Horm Res. Paediatr.
2011; 76: 145-155.
13. Antoniazzi F, Zamboni G, Bertoldo F, Lauriola S,
Tato L: Bone development during GH and GnRH
analog treatment. Eur J Endocrinol. 2004; (151
Suppl, 1): S47-S54.
14. Czajka-Oraniec I, Simpson ER: Aromatase research
and its clinical significance. Endokrynol Pol. 2010;
61: 126-134.
15. Rajput R, Bhansali A, Bhat R, Sialy R: Precocious
pseudopuberty with testicular enlargement. Indian J
Pediatr. 2006; 73: 356-358.
16. Jung H, Parent AS, Ojeda SR: Hypothalamic hamartoma: a paradism/model for studying the onset
of puberty. Endocr Dev. 2005; 8: 81-93.
17. Reiter EO, Norjavaara E: Testotoxicosis: current
viewpoint. Pediatr Endocrinol Rev. 2005; 3: 77-86.
18. Müller J: Impact of cancer therapy on the reproductive
axis. Horm Res. 2003; 59 (Suppl. 1): 12-20.
19. Soriano-Guillén L, Corripio R, Labarta JI, Cañete
R, Castro-Feijóo L. et al: Central precocious puberty
in children living in Spain: incidence, prevalence,
and influence of adoption and immigration. J Clin
Endocrinol Metab. 2010; 95: 4305-4313.
20. Jung H, Ojeda SR: Pathogenesis of precocious
Przegląd Lekarski 2014 / 71 / 10
puberty in hypothalamic hamartoma. Horm Res.
2002; 57 (Suppl. 2): 31-34
21. Jung H, Neumaier-Probst E, Hauffa BP, Partsch
CJ, Dammann Q: Association of morphological
characteristics with precocious puberty and/or gelastic seizures in hypothalamic hamartoma. J Clin
Endocrinol Metab. 2003; 88: 4590-4595.
22. Kakarla N, Bradshaw K.D: Disorders of pubertal
development: precocious puberty. Semin Reprod
Med. 2003; 21: 339-351.
23. Dumitrescu CE, Collins MT: McCune-Albright syndrome. Orphanet J Rare Dis. 2008; 3: 12.
24. Marshall GA, McMahon SK, Nicholls W, Pretorius CJ, Ungerer JP: Gonadotrophin-independent
precocious puberty in an eight-year-old boy due to
ectopic human chorionic gonadotrophin from the
central nervous system. Ann Clin Biochem. 2010;
47: 271-274.
25. Krysiak R, Okopień B, Herman ZS: Wrodzony
przerost nadnerczy na tle niedoboru 21-hydroksylazy
steroidowej. Pol Merkur Lek. 2006; 20: 236-241.
26. Masiakos PT, Flynn CE, Donahoe PK: Masculinizing
and feminizing syndromes caused by functioning
tumors. Semin Pediatr Surg. 1997; 6: 147-155.
27. Mieszczak J, Eugster EA: Treatment of precocious
puberty in McCune-Albright syndrome. Pediatr Endocrinol Rev. 2007; 4 (Suppl. 4): 419-422.
28. New MI: Inborn errors of adrenal steroidogenesis.
Mol Cell Endocrinol. 2003; 211: 75-83.
29. Gleeson HK, Shalet SM: The impact of cancer
therapy on the endocrine system in survivors of
childhood brain tumours. Endocr Relat Cancer.
2004; 11: 589-602.
30. Haddad N, Eugster E: An update on the treatment
of precocious puberty in McCune-Albright syndrome
and testotoxicosis. J Pediatr Endocrinol Metab. 2007;
20: 653-661.
31. Speiser PW: Nonclassic adrenal hyperplasia. Rev
Endocr Metab Disord. 2009; 10: 77- 82.
32. Krysiak R, Okopień B, Herman ZS: Analogi gonadoliberyny. Pol Merk Lek. 2005; 18: 585-589.
33. Diaz A, Danon M, Crawford J: McCune-Albright
syndrome and disorders due to activating mutations
of GNAS1. J Pediatr Endocrinol Metab. 2007; 20:
853-880.
34. Forest MG: Recent advances in the diagnosis and
management of congenital adrenal hyperplasia due
to 21-hydroxylase deficiency. Hum Reprod Update.
2004; 10: 469-485.
35. Harvey AS, Freeman JL: Epilepsy in hypothalamic
hamartoma: clinical and EEG features. Semin Pediatr
Neurol. 2007; 14: 60-64.
36. Traggiai C, Stanhope R: Disorders of pubertal
development. Best Pract Res Clin Obstet Gynaecol.
2003; 17: 41-56.
37. Tuvemo T: Treatment of central precocious puberty.
Expert Opin Investig Drugs. 2006; 15: 495-505.
38. Papathanasiou A, Hadjiathanasiou C: Precocious
puberty. Pediatr Endocrinol Rev. 2006, 3 (Suppl.
1): 182-187.
39. Christoforidis A, Maniadaki I, Stanhope R: McCune-Albright syndrome: growth hormone and prolactin
hypersecretion. J Pediatr Endocrinol Metab. 2006; 19
(Suppl. 2): 623-625.
40. Boyce AM, Chong WH, Shawker TH, Pinto PA, Linehan WN. et al: Characterization and management
of testicular pathology in McCune-Albright syndrome.
J Clin Endocrinol Metab. 2012; 97: E1782-E1790.
41. Brämswig J, Dübbers A: Disorders of pubertal development. Dtsch Arztebl Int. 2009; 106: 295-303.
42. Cassio A, Cacciari E, Zucchini S: Central precocious puberty: clinical and imaging aspects. J Pediatr
Endocrinol Metab. 2000; 13 (Suppl. 1): 703-708.
43. Ghizzoni L, Mastorakos G, Vottero A: Adrenal
hyperandrogenism in children. J Clin Endocrinol
Metab. 1999; 84: 4431-4435.
44. White PC, Bachega TA: Congenital adrenal hyperplasia due to 21 hydroxylase deficiency: from birth to
adulthood. Semin Reprod Med. 2012; 30: 400-409.
45. Oberfield SE, Garvin JH Jr: Thalamic and hypothalamic tumors of childhood: endocrine late effects.
Pediatr Neurosurg. 2000; 32: 264-271.
46. Chrousos GP, Detera-Wadleigh SD, Karl M: Syndromes of glucocorticoid resistance. Ann Intern Med.
1993; 119: 1113-1124.
47. Krege S, Beyer J, Souchon R, Albers P, Albrecht
W. et al: European consensus conference on diagnosis and treatment of germ cell cancer: a report
of the second meeting of the European Germ Cell
Cancer Consensus group (EGCCCG). Eur Urol.
2008; 53: 478-496.
48. Volta C, Regazzi C, Ndaka J, Vitale R, Bernasconi
S: Combined therapy with luteinizing hormone
releasing hormone agonist (LHRHa) and growth
hormone (GH) in central precocious puberty. Acta
Biomed. 2005; 76: 73-78.
49. Lin L, Ferraz-de-Souza B, Achermann JC: Genetic
disorders involving adrenal development. Endocr
Dev. 2007; 11: 36-46.
50. Ibáñez L, Dimartino-Nardi J, Potau N, Saenger P:
Premature adrenarche - normal variant or forerunner
of adult disease? Endocr Rev. 2000; 21: 671-696.
51. Partsch CJ, Sippell WG: Treatment of central
precocious puberty. Best Pract Res Clin Endocrinol.
Metab. 2002; 16: 165-189.
52. Muir A: Precocious puberty. Pediatr Rev. 2006; 27:
373-381.
53. Colecchia M, Nistal M, Gonzalez-Peramato P,
Carmiqnani L, Salvioni R. et al: Leydig cell tumor
and hyperplasia: a review. Anal Quant Cytol Histol.
2007; 29: 139-147.
54. Partsch CJ, Heger S, Sippell WG: Management
and outcome of central precocious puberty. Clin
Endocrinol. 2002; 56: 129-148.
55. Stanhope R, Traggiai C: Precocious puberty (complete, partial). Endocr Dev. 2004; 7: 57- 65.
56. Martin RM, Lin CJ, Nishi MY, Billerbeck AE,
Latronico AC. et al: Familial hyperestrogenism in
both sexes: clinical, hormonal, and molecular studies
of two siblings. J Clin Endocrinol Metab. 2003; 88:
3027-3034.
57. Zacharin M: The spectrum of McCune Albright
syndrome. Pediatr Endocrinol Rev. 2007; 4 (Suppl.
4): 412-418.
58. Berberoğlu M: Precocious puberty and normal
variant puberty: definition, etiology, diagnosis and
current management. J Clin Res Pediatr Endocrinol.
2009; 1: 164-174.
59. Grumbach MM: The neuroendocrinology of human
puberty revisited. Horm Res. 2002; 57 (Suppl. 2):
2-14.
60. Fahmy JL, Kaminsky CK, Kaufman F, Nelson MD
Jr, Parisi MT: The radiological approach to precocious puberty. Br J Radiol. 2000; 73: 560-567.
61. López PJ, Cadena Y, Paulos A, Angel L, Zubieta
R: Unusual presentation of a Leydig cell tumor. Arch
Esp Urol. 2010; 63: 303 305.
62. Eugster EA: Aromatase inhibitors in precocious
puberty. Rationale and experience to data. Treat
Endocrinol. 2004; 3: 141-151.
63. Bertelloni S, Mul D: Treatment of central precocious
puberty by GnRH analogs: long-term outcome in
men. Asian J Androl. 2008; 10: 525-534.
64. Fulmer BR: Diagnosis and management of adrenal
cortical carcinoma. Curr Urol Rep. 2007; 8: 77-82.
65. Chan YM, Fenoglio-Simeone KA, Paraschos S,
Muhammad L, Troester MM. et al: Central precocious puberty due to hypothalamic hamartomas correlates with anatomic features but not with expression
of GnRH, TGFalpha, or KISS1. Horm Res Paediatr.
2010; 73: 312-319.
66. Heger S, Sippell WG, Partsch CJ: Gonadotropinreleasing hormone analogue treatment for precocious
puberty. Endocr Dev. 2005; 8: 94-125.
67. Huhtaniemi IT: Mutations affecting gonadotropin
secretion and action. Horm Res. 2003; 60 (Suppl.
3): 21-30.
68. Grumbach MM: Mutations in the synthesis and action
of estrogen: the critical role in the male of estrogen on
pubertal growth, skeletal maturation, and bone mass.
Ann N Y Acad Sci. 2004; 1038: 7-30.
69. Maixner W: Hypothalamic hamartomas-clinical,
neuropathological and surgical aspects. Childs Nerv
Syst. 2006; 22: 867-873.
70. Bolger WE, Ross AT: McCune-Albright syndrome: a
case report and review of the literature. Int J Pediatr
Otorhinolaryngol. 2002; 65: 69-74.
71. Brito VN, Latronico AC, Arnhold IJ, Mendonça BB:
Update on the etiology, diagnosis and therapeutic
management of sexual precocity. Arq Bras Endocrinol
Metabol. 2008; 52: 18-31.
72. Kaplowitz PB: Precocious puberty: update on secular
trends, definitions, diagnosis, and treatment. Adv
Pediatr. 2004; 51: 37-62.
73. Giglio M, Medica M, De Rose AF, Germinale F,
Ravetti JL. et al: Testicular sertoli cell tumours and
557
relative sub-types. Analysis of clinical and prognostic
features. Urol Int. 2003; 70: 205-210.
74. Aziz AA, Jafri SM, Haque NU: Testotoxicosis:
gonadotrophin-independent male sexual precocity.
Postgrad Med J. 1992; 68: 225-228.
75. Fassnacht M, Libé R, Kroiss M, Allolio B: Adrenocortical carcinoma: a clinician’s update. Nat Rev
Endocrinol. 2011; 7: 323-335.
76. van Rossum E.F, Lamberts SW: Glucocorticoid
resistance syndrome: a diagnostic and therapeutic
approach. Best Pract Res Clin Endocrinol Metab.
558
2006; 20: 611-626.
77. Kaplowitz PB: Precocious puberty: update on secular
trends, definitions, diagnosis, and treatment. Adv
Pediatr. 2004; 51: 37-62.
78. Williams RM, Ward CE, Hughes IA: Premature
adrenarche. Arch Dis Child. 2012; 97: 250-254.
79. Lenz AM, Shulman D, Eugster EA, Rahhal S,
Fugua JS. et al: Bicalutamide and third-generation
aromatase inhibitors in testotoxicosis. Pediatrics.
2010; 126: e728-e733.
80. Toogood AA: Endocrine consequences of brain
irradiation. Growth Horm IGF Res. 2004; 14 (Suppl.
A): S118-S124.
81. Wit JM, Balen HV, Kamp GA, Oostdijk W: Benefit of
postponing normal puberty for improving final height.
Eur J Endocrinol. 2004; 151 (Suppl. 1): S41-S45.
82. Striano S, Santulli L, Ianniciello M, Ferretti M, Romanelli P. et al: The gelastic seizures-hypothalamic
hamartoma syndrome: facts, hypotheses, and perspectives. Epilepsy Behav. 2012; 24: 7-13.
83. Kaplowitz PB: Treatment of central precocious
puberty. Curr Opin Endocrinol Diabetes Obes. 2009;
16: 31-36.
R. Krysiak i wsp.