1. CYKL KWASU CYTRYNOWEGO DOSTARCZA SUBSTRATU DLA
ŁAŃCUCHA ODDECHOWEGO.
Istotą cyklu jest połączenie cząsteczki acetylo-CoA z 4-węglowym
dikarboksylowym kwasem szczawiooctowym, czego wynikiem jest powstanie 6węglowego kwasu trikarboksylowego - cytrynianu.
Enzymy cyklu kwasu cytrynowego znajdują się w macierzy mitochondrialnej albo
w formie wolnej, albo przyłączone do wewnętrznej powierzchni wewnętrznej
błony mitochondrialnej, co ułatwia przenoszenie równoważników redukujących na
odpowiednie enzymy łańcucha oddechowego, umiejscowionego również w
wewnętrznej błonie mitochondrialnej.
2. REAKCJE CYKLU KWASU CYTRYNOWEGO UWALNIAJĄ
RÓWNOWAŻNIKI REDUKUJĄCE I CO2.
Enzym kondensujący - syntaza cytynianowa - katalizuje inicjującą cykl
kondensację acetylo-CoA ze szczawiooctanem i powstanie cytrynianu. Po reakcji
kondensacji, następuje hydroliza wiązania trioestrowego CoA połączona ze
znaczną utratą energii swobodnej w postaci ciepła, co zapewnia przebieg reakcji
do końca.
Acetylo-CoA + Szczawiooctan + H2O ® Cytrynian + Co-A
Cytrynian « Cis-akonitan « Izocytrynian
H2O (związany z enzymem) H2O
Izocytrynian przy udziale dehydrogenazy izocytrynianowej ulega odwodornieniu i
powstaje szczawiobursztynian. Znane są 3 różne dehydrogenazy izocytrynianowe.
Jedna, swoista względem NAD+, znajduje się tylko w mitochondriach. Pozostałe
2 enzymy są swoiste względem NADP+, jeden z nich znajduje się w
mitochondriach, a drugi w cytozolu. Utlenianie izocytrynianu związane z
łańcuchem oddechowym odbywa się niemal wyłącznie przy udziale enzymu
zależnego od NAD+.
Izocytrynian + NAD+ « Szczawiobursztynian « a-Ketoglutaran + CO2 + NADH + H+
(związany z enzymem)
a-Ketoglutaran + NAD+ + Co-A ® Sukcynylo-CoA + CO2 + NADH + H+
Sukcynylo-CoA + Pi + GDP « Bursztynian + GTP + CoA
Reakcja ta wymaga GDP lub IDP, które w obecności fosforanów nieorganicznych
zostają przekształcone odpowiednio w GTP lub ITP. W cyklu kwasu cytrynowego
jest to jedyny przypadek powstawania bogatoenergetycznego wiązania
fosforanowego na poziomie substratu. Występuje on dlatego, że uwolnienie
energii swobodnej w reakcji dekarboksylacji oksydacyjnej a-ketoglutaranu jest
wystarczające do dodatkowego utworzenia wiązania bogatoenergetycznego,
oprócz wytwarzania NADH. Przy udziale kinazy difosfonukleozydowej z GTP lub
ITP. Może powstawać ATP, np.:
GTP + ADP « GDP + ATP
Bursztynian + FAD « Fumaran + FADH2
Pierwszą reakcję odwodornienia katalizuje dehydrogenaza bursztynianowa, która
jest związana z wewnętrzną powierzchnią wewnętrznej błony mitochondrialnej, w
odróżnieniu od pozostałych enzymów cyklu, które znajdują się w matriks. Jest to
jedyna reakcja odwodornienia w cyklu kwasu cytrynowego, w której następuje
bezpośrednie przeniesienie wodoru z substratu na flawoproteinę bez udziału
NAD+. Enzym zawiera FAD i białko żelazosiarkowe (Fe:S). Wynikiem
odwodornienia jest powstanie fumaranu. Dodanie malonianu lub szczawiooctanu
hamuje kompetycyjnie dehydrogenazę bursztynianową, powodując nagromadzenie
się bursztynianu.
Fumaraza (hydrataza fumaranowa) katalizuje reakcję przyłączenia cząsteczki
wody do fumaranu, dając jabłczan.
Fumaran + H2O « L-Jabłczan
Oprócz swoistości dla L-izomeru jabłczanu, fumaraza katalizuje przyłączenie
elementów wody do podwójnego wiązania fumaranu w konfiguracji trans. Jabłczan
ulega przekształceniu przez dehydrogenazę jabłczanową w szczawiooctan reakcji
wymagającej obecności NAD+.
L-Jabłczan + NAD+ « Szczawiooctan + NADH + H+
Enzymy cyklu kwasu cytrynowego, z wyjątkiem dehydrogenaz a-ketoglutaranowej
i bursztynianowej oraz syntazy cytrynianowej, występują również poza
mitochondriami. Chociaż katalizują one podobne reakcje, niektóre z enzymów, np.
dehydrogenaza jabłczanowa, nie muszą być w rzeczywistości tymi samymi
białkami, co enzymy mitochondrialne o tej samej nazwie.
3. KAŻDY OBRÓT CYKLU KWASU CYTRYNOWEGO UMOŻLIWIA
SYNTEZĘ 12 CZĄSTECZEK ATP.
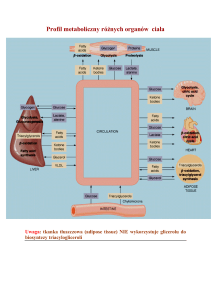
4. CYKL KWASU CYTRYNOWEGO ODGRYWA WĘZŁOWĄ ROLĘ
METABOLICZNĄ.
Niektóre szlaki metaboliczne kończą się na związku pośrednim cyklu kwasu
cytrynowego, a inne szlaki wywodzą się z tego cyklu. Dotyczy to takich procesów,
jak: glukoneogeneza, transaminacja, deaminacja i synteza kwasów tłuszczowych.
Cykl kwasu cytrynowego odgrywa rolę zarówno w procesach oksydacyjnych, jak i
w procesach syntez, a zatem jest amfiboliczny.
Wszystkie ważniejsze metabolity cyklu, od cytrynianu do szczawiooctanu, są
potencjalnie glukogenne, gdyż mogą zwiększyć wytwarzanie glukozy w wątrobie
lub nerce, narządach zawierających pełny zestaw enzymów niezbędnych do
przeprowadzenia glukoneogenezy. Kluczowym enzymem, umożliwiającym przejście
z cyklu do głównego szlaku glukoneogenezy, jest karboksykinaza
fosfoenolopirogronianowa, katalizująca reakcję dekarboksylacji szczawiooctanu
do fosfoenolopirogronianu z GTP jako źródłem fosforanu bogatoenergetycznego
Szczawiooctan + GTP ® Fosfoenolopirogronian + CO2 + GDP
Wprowadzenie do cyklu następuje jako wynik kilku różnych reakcji. Jedną z
najważniejszych jest tworzenie szczawiooctanu w reakcji karboksylacji
pirogronianu katalizowanej przez karboksylazę pirogronianową.
ATP + CO2 + H2O + Pirogronian ® Szczawiooctan + ADP + Pi
W reakcjach katalizowanych przez transaminazy (aminotransferazy) wytwarza
się: pirogronian z alaniny, szczawiooctan z asparaginianu oraz a-ketoglutaran z
glutaminianu. Ponieważ reakcje te są odwracalne, cykl służy również jako źródło
szkieletów węglowych do syntezy aminokwasów endogennych, np.
Asparaginian + Pirogronian « Szczawiooctan + Alanina
Glutaminian + Pirogronian « a-ketoglutaran + Alanina
5. GLIKOLIZA I UTLENIANIE PIROGRONIANU.
Znaczenie biomedyczne - glikoliza jest nie tylko podstawową drogą metabolizmu
glukozy prowadzącą do wytwarzania acetylo-CoA i utleniania w cyklu kwasu
cytrynowego, lecz także stanowi główny szlak metabolizmu fruktozy i galaktozy
pochodzenia pokarmowego.
6. GLIKOLIZA MOŻE PRZEBIEGAĆ W WARUNKACH BEZTLENOWYCH.
Jeżeli tlen jest dostępny tylko przez krótki okres, to jest ograniczona
reoksydacja NADH powstałego w czasie glikolizy. W tych warunkach NADH jest
utleniany w reakcji redukcji pirogronianu do mleczanu, a tak utworzony NAD
umożliwia dalszy przebieg glikolizy. W ten sposób glikoliza może zachodzić w
warunkach beztlenowych, lecz dochodzi do ograniczenia ilości energii uwalnianej
na mol utlenianej glukozy. W konsekwencji, aby wytworzyć tę samą ilość energii,
więcej glukozy musi ulec glikolizie w warunkach beztlenowych niż w warunkach
tlenowych.
7. CIĄG REAKCJI W GLIKOLIZIE TO GŁÓWNY SZLAK ZUŻYCIA
GLUKOZY.
Ogóle równanie glikolizy do mleczanu jest następujące:
Glukoza + 2ADP + 2Pi ® 2L(+)-Mleczan + 2ATP + 2H2O
Wszystkie enzymy szlaku glikolitycznego znajdują się w pozamitochondrialnej
rozpuszczalnej frakcji komórkowej, w cytozolu. Katalizują one reakcje
zachodzące podczas przemiany glukozy do pirogronianu i mleczanu następująco:
Glukoza wchodzi do szlaku glikolitycznego przez fosforylację do glukozo-6fosforanu. Zachodzi to przy udziale enzymu heksokinazy, a w hepatocytach przy
udziale glukokinazy, której aktywność jest indukowana i modyfikowana w wyniku
zmian odżywiania.
Glukoza + ATP ® Glukozo-6-fosforan + ADP
Glukozo-6-fosforan przekształcany w fruktozo-6-fosforan przez izomeryzację
aldozowo-ketozową przy udziale izomerazy fosfoheksozowej
Glukozo-6-fosforan « Fruktozo-6-fosforan
Po tej reakcji następuje druga fosforylacja z udziałem ATP, katalizowana przez
enzym fosfofruktokinazę.
Nieodwracalna w warunkach fizjologicznych
Fruktozo-6-fosforan + ATP ® Fruktozo-1,6-bisfosforan
Fruktozo-1,6-bisfosforan jest rozczepiany przez aldolazę na 2 fosfotriozy,
gliceraldehydo-3-fosforan i dihydroksyacetonofosforan.
Fruktozo-1,6-bisfosforan « Gliceraldehydo-3-fosforan +
Dihydroksyacetonofosforan
Gliceraldehydo-3-fosforan oraz dihydroksyacetonofosforan przekształcają się
jeden w drugi pod wpływem enzymu izomerazy fosfotriozowej.
D-Gliceraldehydo-3-fosforan « Dihydroksyacetonofosforan
Następny etap glikolizy to utlenienie gliceraldehydo-3-fosforanu do 1,3bisfosfoglicerynianu. Dzięki aktywności izomerazy fosfotriozowej również
dihydroksyacetono-fosforan, przechodząc uprzednio w gliceraldehydo-3fosforan, jest utleniany do 1,3-bisfosfoglicerynianu.
D-Gliceraldehydo-3-fosforan + NAD+ + Pi « 1,3-bisfosfoglicerynian + NADH + H+
Enzym warunkujący utlenianie - dehydrogenaza gliceraldehydo-3-fosforanowa jest zależny od NAD. Bogatoenergetyczny fosforan znajduje się następnie w
ATP w wyniku katalizowanej przez kinazę fosfoglicerynianową reakcji
zachodzącej w obecności ADP i tworzącej 3-fosfoglicerynian.
1,3-bisfosfoglicerynian + ADP « 3-fosfoglicerynian + ATP
Ponieważ z cząsteczki glukozy podlegającej glikolizie powstają dwie cząsteczki
fosfotrioz, na tym etapie wytwarzają się również dwie cząsteczki ATP na
cząsteczkę glukozy; jest to przykład fosforylacji „na poziomie substratu”
(fosforylacja substratowa).
Powstający w powyższych reakcjach 3-fosfoglicerynian jest przekształcany w 2fosfoglicerynian przez enzym mutazę fosfoglicerynianową. Prawdopodobnie 2,3bisfosfoglicerynian jest związkiem pośrednim w tej reakcji.
3-Fosfoglicerynian « 2-Fosfoglicerynian
Następny etap glikolizy jest katalizowany przez enolazę, która powoduje
odłączenie wody.
2-Fosfoglicerynian « Fosfoenolopirogronian + H2O
Następnie fosforan bogatoenergetyczny jest przenoszony z
fosfoenolopirogronianu na ADP przez enzym kinazę pirogronianową, tworzący w
tym etapie 2 cząsteczki ATP na cząsteczkę utlenianej glukozy. Utworzony w tej
reakcji enolopirogronian przekształca się spontanicznie w formę ketonową
pirogronianu. Jest to kolejna reakcja, której towarzyszy znaczna utrata energii
swobodnej w postaci ciepła i musi być ona traktowana jako fizjologicznie
nieodwracalna.
Fosfoenolopirogronian + ADP ® Pirogronian + ATP
Teraz stan red.-oks. tkanki jest czynnikiem decydującym, który z 2 możliwych
szlaków metabolicznych zajdzie.
Jeżeli przeważają warunki beztlenowe, to uniemożliwiona jest reoksydacja
NADH w łańcuchu oddechowym przez przeniesienie równoważników redukujących
na tlen. Pirogronian ulega redukcji przez NADH do mleczanu w reakcji
katalizowanej przez dehydrogenazę mleczanową.
Pirogronian + NADH + H+ « Mleczan + NAD+
Reoksydacja NADH w reakcji powstawania mleczanu, przez odtworzenie NAD+
potrzebnego w następnym cyklu reakcji katalizowanej przez dehydrogenazę
gliceraldehydo-3-fosforanową, umożliwia przebieg glikolizy w nieobecności tlenu.
Tkanki funkcjonujące w warunkach niedotlenienia wytwarzają więc mleczan.
Jedynie w erytrocytach ssaków około 90% całkowitego zapotrzebowania
energetycznego pokrywa glikoliza. Poza mięśniem szkieletowym i erytrocytami,
tkankami, które również czerpią energię głównie z glikolizy i wytwarzają mleczan,
są: mózg, jelito, rdzeń nerki, siatkówka i skóra. Wątroba, nerki i serce zwykle
pobierają mleczan i utleniają go, ale w warunkach niedotlenienia narządy te mogą
wytwarzać mleczan.
Glikoliza jest regulowana na 3 etapach obejmujących reakcje „nieodwracalne”.
Chociaż większość reakcji glikolitycznych jest odwracalna, to jednak 3 z nich są
wyraźnie egzoergiczne i z tego powodu muszą być uważane za reakcje
fizjologicznie nieodwracalne. Są to reakcje katalizowane przez heksokinazę (i
glukokinazę), fosfofruktokinazę i kinazę pirogronianową. Reakcje te stanowią
zasadnicze miejsca regulacji glikolizy. Komórki, mające różne systemy
enzymatyczne, pozwalające na alternatywny przebieg nieodwracalnych reakcji
katalizowanych przez wyżej wymienione enzymy, mają możliwość dokonywania w
szlaku glikolitycznym przesunięcia metabolitów w kierunku syntezy
(glukoneogenezy).
8. UTLENIANIE PIROGRONIANU DO ACETYLO-CoA JEST
NIEODWRACALNYM PROCESEM ŁĄCZĄCYM GLIKOLIŻE Z CYKLEM
KWASU CYTRYNOWEGO.
Aby pirogronian mógł wejść do cyklu kwasu cytrynowego, musi najpierw zostać
przetransportowany do wnętrza mitochondrium przez przenośnik pirogronianowy,
który umożliwia przejście pirogronianu przez wewnętrzną błonę mitochondrialną.
Wewnątrz mitochondrium pirogronian ulega dekarboksylacji oksydacyjnej do
acetylo-CoA. Reakcja ta jest katalizowana przez kilka różnych enzymów,
działających kolejno w kompleksie wieloenzymatycznym. Enzymy te określa się
zbiorowo mianem kompleksu dehydrogenazy pirogronianowej, który jest
analogiczny do kompleksu dehydrogenazy a-ketoglutaranowej w cyklu kwasu
cytrynowego.
Pirogronian + NAD+ + CoA ® Acetylo-CoA + NADH + H+ + CO2
9. METABOLIZM GLIKOGENU.
Glikogen jest główną formą magazynowania węglowodanów u zwierząt i jest
odpowiednikiem skrobi u roślin. Występuje głównie w wątrobie (do 6%) i w
mięśniach, gdzie rzadko przekracza 1%.
W szlaku biosyntezy glikogenu bierze udział specjalny aktywny nukleotyd glukozy
Glukoza jest fosforylowana do glukozo-6-fosforanu w reakcji, która jest również
pierwszą reakcją szlaku glikolizy z glukozy. Ta reakcja jest katalizowana przez
heksokinazę w mięśniu i przez glukokinazę w wątrobie. Glukozo-6-fosforan jest w
glukozo-1-fosforan w reakcji katalizowanej przez fosfoglukomutazę. Sam enzym
jest fosforylowany w przebiegu reakcji, a grupa fosforanowa bierze udział w
reakcji odwracalnej, w której związkiem pośrednim jest glukozo-1,6-bisfosforan.
Enz-P. + Glukozo-6-fosforan « Enz + Glukozo-1,6-bisfosforan « Enz-P. + Glukozo1-fosforan
Następnie glukozo-1-fosforan reaguje z urydynotrifosforanem (UTP), aby
utworzyć urydynodifosfoglukozę (UDPGlc).
Reakcja między glukozo-1-fosforanem i urydynotrifosforanem jest katalizowana
przez enzym pirofosforylazę UDPGlc.
UTP + Glukozo-1-fosforan « UDPGlc + PPi
Następująca potem hydroliza nieorganicznego pirofosforanu pod wpływem
nieograniczonej pirofosfatazy przesuwa reakcję na prawą stronę równania.
Działaniem enzymu syntazy glikogenowej, C1 aktywnej glukozy UDPGlc tworzy
wiązanie glikozydowe z C4 końcowej reszty glukozowej glikogenu, uwalniając
urydynodifosforan (UDP). Aby zainicjować tę reakcję, musi być obecna istniejąca
już wcześniej cząsteczka glikogenu, czyli primer. Sam primer (wym. prajmer)
glikogenu może być utworzony na szkielecie białkowym, co może być procesem
podobnym do syntezy innych glikoprotein.
W wątrobie i w nerce (ale nie w mięśniach) występuje swoisty enzym glukozo-6fosfataza, który usuwa fosforan z glukozo-6-fosforanu, umożliwiając
powstającej glukozie dyfundowanie z komórkami do krwi. Jest to końcowy etap
glikogenolizy wątrobowej, która odzwierciedla się zwiększeniem stężenia glukozy
we krwi.
GLUKONEOGENEZA I KONTROLA STĘŻENIA GLUKOZY WE KRWI.
W procesie glukoneogenezy uczestniczą wszystkie mechanizmy i szlaki
odpowiedzialne za przekształcenie związków niewęglowodanowych w glukozę lub
glikogen. Głównymi substratami dla glukoneogenezy są glikogenne aminokwasy,
mleczan oraz glicerol. Głównymi tkankami, w których odbywa się ten proces, są
wątroba i nerki, gdyż one właśnie zawierają pełen zestaw niezbędnych do tego
enzymów.
Glukogeneza zaspokaja zapotrzebowanie organizmu na glukozę wówczas, gdy
węglowodany nie są dostępne w wystarczającej ilości z dostarczanych pokarmów.
Ciągłe dostarczanie glukozy jest niezbędne jako źródło energii, zwłaszcza dla
układu nerwowego i dla erytrocytów.
10. GLUKONEOGENEZA OBEJMUJE REAKCJE GLIKOLIZY, CYKLU
CYTRYNIANOWEGO ORAZ NIEKTÓRE REAKCJE SPECJALNE
Bariery termodynamiczne zapobiegają prostemu odwróceniu glikolizy.
Krebs zwracał uwagę na to, że bariery energetyczne nie pozwalają na proste
odwrócenie glikolizy pomiędzy 1)pirogronianem a fosfoenolopirogronianem,
2)pomiędzy fruktozo-1,6-bisfosforanem a fruktozo-6-fosforanem, 3)pomiędzy
glukozo-6-fosforanem a glukozą, 4) pomiędzy glukozo-1-fosforanem a
glikogenem. Wszystkie te reakcje nie są w stanie równowagi, uwalniają dużą ilość
energii w postaci ciepła i wobec tego są fizjologicznie nieodwracalne.
Pirogronian i fosfoenolopirogronian.
W mitochondriach znajduje się enzym karboksylaza pirogronianowa, który w
obecności ATP oraz CO2 przekształca pirogronian w szczawiooctan. Funkcją
biotyny jest związanie CO2 na enzymie przed przyłączeniem go do pirogronianu.
Drugi enzym, karboksykinaza fosfoenolopirogronianowa, katalizuje
przekształcenie szczawiooctanu do fosfoenolopirogronianu. W tej reakcji jest
niezbędny bogatoenergetyczny fosforan w postaci GTP lub ITP., a uwalnia się
CO2. Za pomocą tych 2 enzymów i dehydrogenazy mleczanowej, mleczan może
być przekształcony w fosfoenolopirogronian.
Fruktozo-6-fosforan i fruktozo-1,6-bisfosforan
Przekształcenie fruktozo-1,6-bisfosforanu do fruktozo-6-fosforanu konieczne
do osiągnięcia odwrócenia glikolizy, jest katalizowane przez swoisty enzym
fruktozo-1,6-bisfosfatazę. Obecność tego enzymu warunkuje, czy dana tkanka
jest zdolna do biosyntezy glikogenu nie tylko z pirogronianu, lecz także z
fosfotrioz.
Glukozo-6-fosforan i glukoza.
Przekształcenie glukozo-6-fosforanu w glukozę jest katalizowane przez inną
swoistą fosfatazę - glukozo-6-fosfatazę.
Glukozo-1-fosforan i glikogen.
Rozpad glikogenu do glukozo-1-fosforanu jest katalizowany przez fosforylazę.
Biosynteza glikogenu odbywa się całkiem odmiennym szlakiem, przez utworzenie
urydynodifosfoglukozy i z udziałem syntazy glikogenowej.
Te kluczowe enzymy pozwalają na to, że odwrócenie glikolizy odgrywa zasadniczą
rolę w glukoneogenezie. Aminokwasy glikogenne po transaminacji lub deaminacji
tworzą albo pirogronian albo stają się członami cyklu kwasu cytrynowego. Wobec
tego powyżej opisane reakcje są odpowiedzialne za przekształcenie w glukozę lub
glikogen zarówno aminokwasów glikogennych, jak i mleczanu. Wiadomo, że
mleczan przekształca się w pirogronian i wnika do mitochondriów przed
przekształceniem do szczawiooctanu i ewentualnym przekształceniem w glukozę.