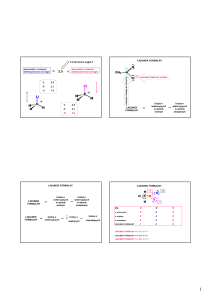
Liczby kwantowe
1
Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można
scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m.
Liczby kwantowe nie mogą być dowolne, muszą przyjmować jedynie pewne wartości.
Liczba n jest nazywana główną liczbą kwantową może przyjmować wartości kolejnych
liczb naturalnych (całkowitych, dodatnich): 1, 2, 3...... opisuje energię elektronu, tj. określa
numer powłoki elektronowej,do której należy elektron;
Poboczna liczba kwantowa l może przybierać wartości 0, 1, 2... (n – 1) (gdzie n to główna
liczba kwantowa); opisuje gęstość prawdopodobieństwa znalezienia się elektronu w
określonej odległości od jądra, tj. określa kształt orbitalu: dla l=0 orbital jest chmurą kulistą
(sferyczną), której gęstość maleje, gdy wzrasta odległość od jądra - kształt takiego orbitalu
oznacza się literą s; dla l=1 orbital jest obrotową ósemką, a w jej płaszczyźnie węzłowej
znajduje się jądro atomu - kształt takiego orbitalu oznacza się literą p.
Liczb m nazywana jest magnetyczną liczba kwantową. Liczba m osiąga wartości z
przedziału <-l,+l> (gdzie l to poboczna liczba kwantowa); określa sposób rozszczepienia
orbitalu w polu magnetycznym. W polu magnetycznym orbital typu s ma charakter
bezkierunkowy, natomiast orbital typu p ma wyróżnione trzy prostopadłe kierunki.Istnieją
trzy orbitale p o danej energii: px, py i pz.
Zestaw tych trzech liczb kwantowych nosi nazwę orbitalu.
Poszczególne orbitale określa się skrótami podanymi w tabeli, które zawierają głowną liczbę
kwantową oraz poboczną liczbę kwantową, przy czym ta ostatnia podana jest w postaci
litery. Przyjęto nazywać wartość l = 0 literą s, l =1 literą p, l = 2 literą d oraz l = 3 literą f.
Litery te pochodzą od angielskich słów sharp, principle, diffuse, fundamental i zostały
wzięte z określeń stosowanych dla określenia widm w analizie spektralnej.
Obrazem graficznym orbitalu jest fragment przestrzeni, w której prawdopodobieństwo
znalezienia elektronu jest duże. Każdy orbital ma inny kształt i orientację przestrzenną, a
zajmujący go elektron charakteryzuje się inną energia. Orbitale typu s mają kształt kuli.
Pozostałe orbitale wykazują orientację przestrzenną, co znaczy, że niektóre kierunki w
przestrzeni charakteryzują się wyższym prawdopodobieństwem spotkania elektronu. Np.:
kształt orbitali p przypomina sferyczne ósemki nabite na poszczególne osie współrzędnych
2
Istnieje znacznie większe prawdopodobieństwo spotkania elektronu wewnątrz tego orbitalu,
niż na zewnątrz. Ale prawdopodobieństwo zajęcia orbitalu px, py lub pz jest takie samo.
Każda „ósemka” ma tę samą charakterystykę energetyczną; żadna z nich nie jest
uprzywilejowana, prawdopodobieństwo obsadzenia każdej nich przez elektron jest
dokładnie takie samo. Takie orbitale nazywa się zdegenerowanymi. Orbital p jest trójkrotnie
zdegenerowany, ze względu na równocenność energetyczną orbitali px, py i pz. Analogicznie
orbital d jest pięciokrotnie zdegenerowany
Każdy orbital może pomieścić dwa elektrony. Muszą się one różnić liczbą spinową. Liczba
spinowa s jest czwartą liczbą kwantową. Może przyjąć tylko dwie wartości: -1/2 lub +1/2.
Na jednym orbitalu nie mogą się znajdować dwa elektrony o jednakowej liczbie
spinowej. Zasada ta jest znana jako zakaz Pauliego: W atomie nie mogą znajdować się
dwa elektrony charakteryzowane jednakowym zestawem liczb kwantowych.
3
Przedstawiając zakaz Pauliego stosuje się niekiedy „klatkowy” zapis orbitali. Zajęte orbitale
są przedstawiane w postaci kwadratów zawierających strzałki o zwrotach zgodnych lub
przeciwnie skierowanych. Jest to umowny sposób przedstawiania elektronów o tych samych
lub przeciwnych liczbach spinowych. Zakaz Pauliego zabrania obecności dwu elektronów o
tych samych spinach na jednym i tym samym orbitalu:
źle
dobrze
Wraz ze wzrostem liczby atomowej pierwiastka wzrasta liczba elektronów. Zajmują one
kolejne orbitale zaczynając od najniższych poziomów energetycznych. Kolejność
zajmowania poszczególnych poziomów jest następująca: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s,
4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, co przedstawiono na rysunku:
Zasadniczo energia elektronów zależy od głównej liczby kwantowej n. Im większa główna
liczba kwantowa, tym elektron osiąga wyższą energię. Co prawda orbitale s, p i d różnią się
energią, ale decydujące znaczenie ma numer powłoki. Zasada ta jest zachowana na
pierwszych trzech poziomach energetycznych atomu. Na wyższych poziomach
energetycznych energia elektronów zależy nie tylko od głównej liczby kwantowej, lecz
także - i to w istotniejszy sposób niż poprzednio - od pobocznej liczby kwantowej. Wpływ
pobocznej liczby kwantowej może być tak duży, że niektóre poziomy energetyczne d lub f o
mniejszej głównej liczbie kwantowej będą charakteryzowały się wyższą energią od
poziomów o większej głównej liczbie kwantowej. Ma to miejsce np.: w przypadku orbitali
4s - 3d lub 6s – 4f - 5d. Wcześniej zapełnia się orbital 4s niż 3d, 6s niż 4f, mimo iż inaczej
to nakazywałaby wartość głównej liczby kwantowej.
W tabeli 3 można zauważyć inne wyjątki od „regularnego” zapełniania orbitali np. w
przypadku pierwiastków chromu lub miedzi. Przy rozbudowie powłoki wanadu o
konfiguracji1s2 2s2p6 3s2p6d3 4s2 o jeden elektron w miejsce spodziewanej konfiguracji 1s2
2s2p6 3s2p6d4 4s2 pojawia się 1s2 2s2p6 3s2p6d5 4s1 co wynika z korzystniejszej sytuacji
energetycznej.
4
Kolejność zapełniania orbitali zdegenerowanych jest zgodna z regułą Hundta, która mówi,
że pary elektronowe na tych orbitalach pojawiają się dopiero po zapełnieniu
wszystkich orbitali zdegenerowanych przez pojedyncze elektrony. Spiny tych
niesparowanych elektronów są jednakowe. Np. w przypadku orbitalu d, na którym może
zmieścić się 10 elektronów, pierwsze pięć elektronów będzie zajmowało kolejno wolne
orbitale pozostając niesparowanymi
Dopiero dalsze elektrony zajmują wolne miejsca tworząc pary np. szósty elektron:
Przykładowe zapisy konfiguracji elektronowych za pomocą wzorów klatkowych:
5