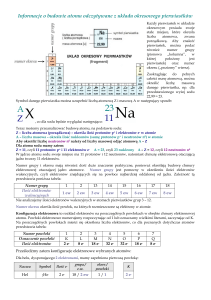
Dział: Budowa atomu– konfiguracja elektronowa
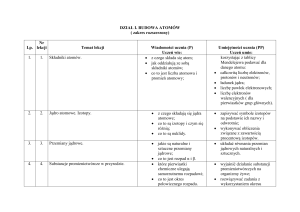
1. Ile powłok elektronowych oraz ile elektronów na ostatniej powłoce mają atomy następujących pierwiastków:
a) Mg, b) C, c) As, d) Ne.
2. Który z pierwiastków 15 grupy tablicy Mendelejewa ma 3, a który 6 powłok elektronowych?
3. Który z pierwiastków piątego okresu ma 4, a który 7 elektronów na ostatniej powłoce?
4. Który pierwiastek tworzy wodorek EH3, a jego atom ma na powłoce L pięć elektronów?
5. Który pierwiastek spełnia równocześnie następujące warunki: 1) atom ma trzy powłoki elektronowe, 2) tworzy
tlenek typu E2O?
6. Na podstawie podanej powłokowej konfiguracji elektronowej ustalić: 1) liczbę atomową pierwiastka, 2) liczbę
elektronów walencyjnych:
a) K2 L8 M 5
b) K2 L8 M 18 N 6
c) K2 L8 M 18 N 8 O 2
7. Odszukaj w układzie okresowym pierwiastki o następujących liczbach elektronów w poszczególnych powłokach:
a) K2 L8 M 18 N 7
b) K2 L5
c) K2 L8 M18 N 18 O8P1
8. Które pierwiastki mają następującą powłokową konfigurację walencyjną: a) M 3, b) N 4 ,c) L 6 ,d) O 7 ?
9. Wymień pierwiastki, w których liczba elektronów na ostatniej powłoce jest równa maksymalnej liczbie
elektronów, jaka może znajdować się na tej powłoce?
10. Ile elektronów zawiera rdzeń następujących pierwiastków: a) Sr, b) Na, c) Ar, d) Al. ?
11. Ile elektronów walencyjnych zawierają atomy:
Na, N, Al., Br, Mg, Cr, Fe, Ag, Ce?
12. Zapisać powłokową konfigurację walencyjną: a) węgla, b) magnezu, c) tytanu, d) miedzi.
13. Ile powłok zajmują elektrony w atomie o konfiguracji:
1s2 2s2 2p6 3s2 3p6 4s1 ?
14. Dla pierwiastków o konfiguracjach powłokowych: a) K2 L4 b) K2 L8 M 8 N 2zapisać konfiguracje
podpowłokowe.
15. Które pierwiastki mają następującą podpowłokową konfigurację walencyjną:
a)
b)
c)
d)
3s2 3p1
5s2 5p6
3d7 4s2
4f 25d 0 6s2
e) 4s2
f) 6s2 6p2
g) 3d10 4s1
h) 5f 3 6d1 7s2
16. Odszukaj w układzie okresowym pierwiastki o następującej konfiguracji elektronowej:
a) 1s2 2s2 2p6 3s2 3p4
b) 1s2 2s2 2p6 3s2 3p6 4s2 3d1.
17. Zidentyfikować pierwiastki o następujących konfiguracjach:
a) [Ne] 3s2 3p3 b) [Kr] 4d10 5s2 5p2
c) [He] 2s2
d) [Xe] 6s1.
18. Stosując notację opisaną w poprzednim zadaniu, podać konfigurację elektronową pierwiastków o liczbach
atomowych: 4, 13, 34, 38, 82.
19. Na podstawie podanej niżej liczby elektronów w powłokach, posługując się notacją z zadania 17 podaj
konfigurację podpowłokową:
a)
b)
c)
b)
Cr: K2 L8 M 13 N 1
Cu: K2 L8 M 18 N 1
Nb; K2 L8 M 18 N 12 O 1
Pt: K2 L8 M18 N 32 O17 P1
20. Zapisać podpowłokową konfigurację elektronową rdzeni atomów: Li, F, S, Cl.
21. Zapisać podpowłokową konfigurację walencyjną a) węgla, b) magnezu, c) tytanu, d) miedzi.
22. Ile elektronów niesparowanych zawierają w stanie podstawowym atomy o następujących liczbach atomowych:
11, 15,20, 32, 36.
23. Przedstawić graficznie opis walencyjnych stanów orbitalnych w atomach: a) magnezu, b) galu, c) krzemu, d)
telluru, e) bromu, f) neonu.
24. Które z niżej podanych konfiguracji dotyczą stanu wzbudzonego:
a)
b)
c)
1s2 2s1 2p1
2
2
6
2
12Mg: 1s 2s 2p 3s
2
1
2
5B: 1s 2s 2p .
4Be:
Ile elektronów niesparowanych zawierają atomy o podanej konfiguracji?