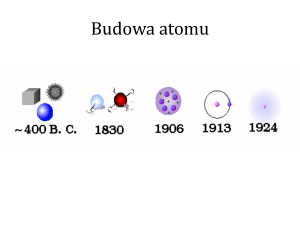
Budowa Atomu
Rozwój poglądów na budowę materii
ARYSTOTELES
• - materia jest ciągła i jednolita
Demokryt
• - materia składa się z bardzo małych i
niepodzielnych „cząsteczek” – atomów
(atomos z greckiego oznacza niepodzielny),
• - pogląd praktycznie był odrzucany do
początku XIX wieku.
John Dalton - XIXw
• - cała materia zbudowana jest z trwałych,
niepodzielnych i niezmiennych jednostek
wchodzących w reakcje chemiczne atomów,
• - teoria o niepodzielności atomów została
obalona na przełomie XIX/XX wieku.
Michael Faraday i Joseph John
Thomson
• - wykrywają istnienie ujemnie
naładowanych cząstek wchodzących w
skład atomu – elektronów,
• - Robert Millikan w 1912r. wyznaczył
ładunek i masę elektronu
Wilhelm Roentgen
• - odkrycie promieni „X” (promienie
Roentgena),
• - w 1896r. przedstawił zdjęcie z
prześwietlenia ręki żony,
Antoine Henri Becquerel
• - kilka miesięcy po odkryciu Roentgena
stwierdził, że istnieją substancje, które
wysyłają promieniowanie powodujące
zaczernienie kliszy fotograficznej
Maria Curie - Skłodowska
i Piere Curie
• - kontynuują badania A. H. Becquerel`a,
zjawisko to nazywają promieniotwórczością
(radioaktywnością)
Ernest Rutherford
• - w 1902r. stwierdził, że atomy
pierwiastków promieniotwórczych ulegają
samorzutnemu rozpadowi, emitują
różnorodne promieniwanie (alfa, beta,
gama),
• - odkrycie to umożliwiło potwierdzenie, że
atom ma złożoną budowę.
Joseph John Thomson – budowa
atomu
• - elektrony rozmieszczone są wewnątrz
materialnej kulki o ładunku dodatnim
(ciasta z rodzynkami)
Ernest Rutherford – budowa
atomu
• - ogłosił koncepcję planetarnej budowy
atomu: atom składa się z dodatniego małego
jądra skupiającego prawie całą jego masę, a
wokół jądra po orbitach porusza się
określona liczba elektronów (planety wokół
Słońca).
Niels Bohr
• - udoskonalił model budowy atomu
Rutherford`a
Max Planck
• - stwierdził, że światło jest wysyłane i
pochłanianie nie w sposób ciągły, lecz
porcjami – kwantami (quantum - ilość)
Louis Victor de Broglie
• - udowodnił, że elektrony mają podwójną
(daualistyczną) naturę, zachowują się zarówno jak
fala, i jak cząstka,
• - powyższe odkrycie umożliwiło sformułować
kwantowo-mechaniczny model budowy atomu:
atom zbudowany jest z dodatniego jądra, w skład
którego wchodzą protony i neutrony, jądra
każdego atomu otacza chmura elektronów,
których liczba jest równa liczbie protonów w
jądrze atomu, elektrony poruszają się w
określonych miejscach przestrzeni zgodnie z
prawami mechaniki kwantowej.
Cząsteczki elementarne atomu
Masa cząsteczki
proton
Symbol
cząsteczki
p
1,6725·10-27 kg
Ładunek
cząsteczki
+
neutron
n
1,6748·10-27 kg
0
elektron
e
Nazwa cz.
elementarnej
9,1093·10-31 kg
-