Spis treści
1 Atom i pierwiastek — podstawowe definicje
2 Modele atomu
2.1 Model planetarny Rutherforda (1911)
2.2 Model Bohra (1913)
3 Przełomowe doświadczenia w badaniach nad strukturą atomów
3.1 Widmo atomu wodoru
4 Falowa natura elektronu
5 Równanie Schrödingera
6 Co wynika z postulatów mechaniki kwantowej?
7 Cechy mikroświata
8 Energia atomu wodoru
9 Kwantowanie momentu pędu i spinu
10 Orbitale atomowe wodoru
11 Orbitale w atomach wieloelektronowych
12 Zapełnianie powłok elektronowych
13 Konfiguracje elektronowe pierwiastków
Atom i pierwiastek — podstawowe definicje
Atom jest najmniejszą częścią pierwiastka zachowującą jego właściwości. Zbudowany jest z jądra
atomowego oraz elektronów. W skład jądra wchodzą protony i neutrony (nukleony). Podstawowe
właściwości tych cząstek elementarnych zebrano w tabeli.
Cząstka Symbol Zapis
proton
Masa [kg]
Ładunek [e] Ładunek [C]
p
1
neutron n
0
elektron e
-1
0
Atom przedstawia się za pomocą symbolu odpowiedniego pierwiastka oraz liczby masowej i
atomowej:
A — liczba masowa (liczba nukleonów)
— symbol pierwiastka
Z — liczba atomowa (liczba protonów)
Pierwiastek chemiczny jest zbiorem atomów o takiej samej liczbie protonów, a nuklid zbiorem
atomów o tej samej liczbie atomowej i masowej.
Izotopy — atomy tego samego pierwiastka różniące się liczbą masową
Izobary — zbiory atomów o takiej samej liczbie masowej
Izotony — zbiory atomów o takiej samej liczbie neutronów
Odmiany alotropowe — odmiany tego samego pierwiastka różniące się liczbą atomów w cząsteczce
(tlen i ozon) lub postacią krystaliczną (diament i grafit).
Modele atomu
Model atomu Rutherforda
Model atomu Bohra
Model atomu Schrödingera
Modele zaproponowane przez Rutherforda i Bohra były oparte na prawach fizyki klasycznej
Newtona. Mechanika klasyczna pozwala dokładnie określić położenie i pęd obiektów materialnych w
każdym punkcie czasowym oraz przewiduje możliwość wzbudzenia ruchów translacyjnych,
rotacyjnych i oscylacyjnych do dowolnych wartości energii pod wpływem przyłożenia siły.
Model planetarny Rutherforda (1911)
W centralnej części atomu znajduje się dodatnio naładowane jądro, dookoła którego krążą elektrony
po torach kołowych lub eliptycznych.
Model Bohra (1913)
Elektron w atomie może przebywać w ściśle określonych stanach o określonej energii. Podczas
przejścia elektronu ze stanu o wyższej energii (E2) do stanu o niższej energii (E1) następuje emisja
energii, natomiast przejście ze stanu (E1) do stanu (E2) wymaga absorpcji energii
E2 - E1 = hν
Teoria Bohra wyjaśniała emisje fal świetlnych pozwalającą wytłumaczyć widmo emisyjne atomu
wodoru oraz atomów wodoropodobnych (brak możliwości opisu pozostałych atomów).
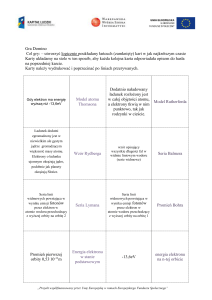
Przełomowe doświadczenia w badaniach nad strukturą
atomów
Elektryczne wyładowania w gazach
Spektroskopia atomowa
Efekt fotoelektryczny
Widmo atomu wodoru
Linie spektralne tworz grupy o zbliżonych długościach fal, zwane seriami
(Lymana, Balmera, Paschena).
Spektrum widzialne atomu wodoru (seria Balmera).Występowanie
dyskretnych linii spektralnych wskazuje, że elektron w atomie może
przyjmowad pewne określone energie.
Efekt fotoelektryczny
Wyładowania elektryczne w gazowym
wodorze. Strumień elektronów rozszczepia
cząsteczki wodoru i wzbudza powstające
atomy do wyższych stanów energetycznych.
Oddając nadmiar energii atomy emitują
promieniowanie, które przechodząc przez
pryzmat ulega załamaniu i na ekranie
powstaje widmo liniowe gazu.
Model prostego spektroskopu złożonego z
kartonu ze szczeliną i pryzmatu.
Falowa natura elektronu
Louis de Broglie (1924) przypisał elektronom właściwości korpuskularne oraz falowe (dualizm
korpuskularno-falowy) wyrażone wzorem
gdzie m oznacza masę cząstki, v — prędkość , h — stałą Plancka.
Doświadczalne potwierdzenie dualizmu elektronu nastąpiło w roku 1927, kiedy odkryto
zjawisko dyfrakcji elektronów (C.J. Davisson, L.H. Germer).
W przypadku cząstek elementarnych niemożliwe jest równoczesne dokładne określenie
położenia i pędu (zasada nieoznaczoności Heisenberga).
Zasada nieoznaczoności wyrażana jest w postaci
gdzie
jest miarą niedokładności oznaczenia współrzędnej określającej położenie cząstki, a
miarą niedokładności oznaczenia pędu cząstki.
Równanie Schrödingera
Równanie Schrödingera opisuje ruch cząstek. Funkcja będąca jego rozwiązaniem, nazywana funkcją
falową ( ), opisuje stan pojedynczej cząstki lub wielu cząstek.
Kwadrat bezwzględnej wartości funkcji
wokół jądra
jest miarą gęstości elektronowej w różnych obszarach
Dla atomu wodoru funkcje falowe można dokładnie wyznaczyć, jednak tylko niektóre z nich, tzw.
funkcje porządne (ciągłe, jednoznaczne i przyjmujące wartości skończone), nadają się do wyrażenia
prawdopodobieństwa napotkania elektronu.
Co wynika z postulatów mechaniki kwantowej?
Nie da się określić toru elektronu, lecz jedynie prawdopodobieństwo jego znalezienia w
wybranym rejonie przestrzeni wokół jądrowej. Przyjmuje się, że elektron wytwarza chmurę
ładunku ujemnego wokół jądra a kształt chmury zależy od stanu kwantowego.
Ruch elektronu jest opisywany za pomocą równania Schrödingera, którego rozwiązaniem są
funkcje falowe. Znajomość tych funkcji pozwala na obliczanie różnych wielkości związanych z
ruchem elektronu.
W zależności od wartości parametrów charakteryzujących stan elektronu wprowadzono
umowną, trójstopniową klasyfikację stanów kwantowych: powłoki, podpowłoki, poziomy
orbitalne.
Cechy mikroświata
Wielkości fizyczne związane z ruchem cząstki nie mogą przyjmować wartości dowolnych — są to
wielkości skwantowane.
W przypadku elektronu kwantowaniu podlega 5 parametrów ruchu:
energia,
orbitalny moment pędu,
orientacja przestrzenna orbitalnego momentu pędu,
spin,
orientacja przestrzenna spinu.
Stan elektronu określony za pomocą wartości poszczególnych parametrów jest nazywany stanem
kwantowym.
Energia atomu wodoru
Rozwiązaniem równania Schrödingera mogą być funkcje porządne tylko wtedy, gdy energia
elektronu w atomie o liczbie atomowej Z wyraża się równaniem
gdzie n - główna liczba kwantowa, która może przybierać wartości kolejnych liczb naturalnych, e ładunek elementarny,
— masa elektronu,
— przenikalność elektryczna próżni, h — stała
Plancka.
Energia elektronu w atomie wodoru może przyjmować następujące wartości:
E1 =-13,59 eV dla n = 1
E2 =-3,44 eV dla n = 2
E3 =-1,56 eV dla n = 3
Ujemne wartości energii wynikają z założenia, że energia potencjalna elektronu znajdującego się w
nieskończenie dużej odległości od jądra ma wartość zerową, zatem w miarę zbliżania się elektronu
do jądra przyjmuje wartości coraz bardziej ujemne.
Stany kwantowe o takiej samej energii nazywa się stanami zdegenerowanymi. W atomie wodoru
liczba stanów zdegenerowanych wynosi
.
Wartość energii (-13,6 eV) wynikającą z warunku kwantowego
posiadają dwa stany kwantowe.
Kolejna wartość energii (-3,4 eV) uzyskana dla
, odpowiada 8 stanom kwantowym.
Zbiór stanów kwantowych o tej samej wartości n (głównej liczby kwantowej) jest nazywany powłoką
elektronową (zarówno w atomie wodoru, jak i w atomach wieloelektronowych).
Główna liczba kwantowa n spełnia następujące funkcje:
określa liczbę stanów kwantowych w powłoce jako równą
kwantuje energię.
,
Powłoki elektronowe w atomie (wartości energii dotyczą atomu wodoru):
powłoka K zawierająca 2 stany o energii -13,6 eV
powłoka L zawierająca 8 stanów o energii -3,4 eV
powłoka M zawierająca 18 stanów o energii -1,5 eV
powłoka N zawierająca 32 stany o energii -0,85 eV
powłoka Q zawierająca 50 stanów o energii -0,54 eV
Kwantowanie momentu pędu i spinu
Ruch elektronu opisywany jest wielkością wektorową zwaną orbitalnym momentem pędu, co
powoduje konieczność oddzielnego kwantowania jego wartości i orientacji przestrzennej .
Wartość momentu pędu kwantuje poboczna (orbitalna) liczba kwantowa , która może
przybierać wartości od 0 do
.
Zbiór stanów kwantowych o tej samej energii i tej samej wartości momentu pędu (czyli zbiór
stanów opisywanych tym samym zestawem liczb i ), jest nazywany podpowłoką
elektronową.
Każda powłoka elektronowa zawiera inną liczbę podpowłok, równą , które oznacza się
symbolami: (dla
), (dla
), (dla
), (dla
), a dalej alfabetycznie.
Wektor momentu pędu może przyjmować
ustawień względem zewnętrznego pola
magnetycznego.
Kwantowanie orientacji przestrzennej wektora momentu pędu polega na znalezieniu rzutów
tego wektora na kierunek zewnętrznego pola magnetycznego. Określa je magnetyczna liczba
kwantowa
przybierająca wartości liczb całkowitych od –l do +l. Zbiór stanów kwantowych
o jednakowych wartościach liczb
nazywa się poziomem orbitalnym.
Wielkość zwaną spinem przypisano ruchowi wewnętrznemu elektronu, odpowiedzialnemu za
wytworzenie pola magnetycznego wokół elektronu. Wartość spinu określa spinowa liczba
kwantowa
, która przyjmuje tylko jedną wartość (½), natomiast wektor spinu może ustawić
się względem zewnętrznego pola magnetycznego na dwa sposoby: „spin równoległy” i „spin
antyrównoległy”.
Kwantowanie orientacji przestrzennej spinu wprowadza magnetyczną spinową liczbę
kwantową ( ), która może przyjmować dwie wartości (+ ½) i (- ½).
Poziom orbitalny to 2 stany kwantowe opisane tymi samymi liczbami kwantowymi
, a różniące się orientacją przestrzenną wektora spinu w zewnętrznym polu
magnetycznym.
Orbitale atomowe wodoru
Każdej kombinacji 3 liczb kwantowych
równanie Schrödingera.
odpowiada jedna funkcja falowa spełniająca
Funkcja taka nazywa się orbitalem atomowym
. Liczbę możliwych orbitali
odpowiadających poszczególnym wartościom głównej liczby kwantowej (poszczególnym
dozwolonym stanom energetycznym atomu wodoru) określa się na podstawie różnych
możliwych kombinacji liczb kwantowych.
Znajomość postaci funkcji stanowiących orbitale atomowe pozwala obliczyć
prawdopodobieństwo napotkania elektronu w określonych odległościach od jądra i w
określonych kierunkach.
Kształty orbitali s, p, d
Orbitale w atomach wieloelektronowych
Dla atomów wieloelektronowych równanie falowe ma tak skomplikowaną postać, że nie można
go rozwiązać w sposób ścisły (problemem jest konieczność uwzględnienia współrzędnych
wszystkich elektronów oraz oddziaływań pomiędzy nimi).
Możliwe jest uzyskanie rozwiązań przybliżonych za pomocą metody pola samouzgodnionego
(Hartree-Focka), w której rozpatruje się ruch poszczególnych elektronów w uśrednionym polu
elektrycznym innych elektronów. Pozwala to na opisanie każdego elektronu oddzielną funkcją
falową, uwzględniającą tylko współrzędne opisywanego elektronu. Działanie takie nazywa się
przybliżeniem jednoelektronowym, a funkcja falowa opisująca zachowanie się wszystkich
elektronów jest iloczynem orbitali jednoelektronowych
Istotna różnica pomiędzy atomem wodoru a atomami wieloelektronowymi polega na tym, że o
energii elektronu w atomie wodoru decyduje wyłącznie główna liczba kwantowa, podczas gdy
w pozostałych atomach na energie elektronów wpływa również orbitalna liczba kwantowa.
Zapełnianie powłok elektronowych
W atomie wieloelektronowym nie może być dwóch elektronów, których stan jest opisywany za
pomocą zestawów identycznych liczb kwantowych, muszą się różnić przynajmniej jedną liczbą
kwantową.
Zgodnie z zakazem Pauliego, jeden orbital o liczbach kwantowych n,l,m może opisywać
zachowanie się co najwyżej dwóch elektronów różniących się spinową liczbą kwantową.
Z punktu widzenia właściwości chemicznych znaczenie mają elektrony tworzące najbardziej
zewnętrzną powłokę elektronową, tzw. elektrony walencyjne.
Przyporządkowując elektrony orbitalom zdegenerowanym (o jednakowych energiach), należy
je rozmieszczać pojedynczo ze zgodnie skierowanymi spinami, ponieważ zgodnie z regułą
Hunda najniższą energię dla danej konfiguracji ma stan o najwyższym możliwym całkowitym
spinie.
Stan, w którym pojawiają się niesparowane elektrony (ze zgodnie skierowanymi spinami)
nazywa się stanem trypletowym. Stan, w którym atom nie zawiera żadnego elektronu
niesparowanego, nazywa się stanem singletowym.
W miarę przechodzenia do atomów o coraz większej liczbie atomowej poziomy energetyczne są
zajmowane w kolejności, według której wzrasta ich energia.
Konfiguracje elektronowe pierwiastków
Konfiguracją elektronową pierwiastka określa się rozmieszczenie elektronów w podpowłokach
i powłokach
Kolejność zapełniania podpowłok elektronami określa reguła
:
elektrony zajmują w pierwszej kolejności tę podpowłokę, dla której suma
najmniejsza; gdy dwie podpowłoki mają jednakową sumę
zapełniania decyduje mniejsza wartość :
Przykładowe konfiguracje:
12
Mg
25
Mn
lub w formie skróconej [Ne]
lub w formie skróconej [Ar]
to o kolejności
jest