BIOCHEMIA 4.doc
(633 KB) Pobierz
WYKŁAD 4
WYTWARZANIE ENERGII W KOMÓRCE:
Istotą życia w ujęciu biologicznym jest nieustanne przetwarzanie materii i energii, zwane metabolizmem
(katabolizm i anabolizm).
Z pewnym uproszczeniem można przyjąć, iż źródłem energii dla organizmu ludzkiego jest utlenianie
(spalanie) wodoru w tlenie. Wodory pochodzą z wysoko zredukowanych substratów energetycznych:
głównie glukozy i kwasów tłuszczowych, a także z glicerolu, ciał ketonowych oraz szkieletów
węglowodorowych aminokwasów. Poprzez szereg reakcji utleniania substraty te rozpadają się do CO i H O.
Utlenianie wodoru w komórkach zachodzi powoli, wieloetapowo, a znacząca część uwalnianej energii
(ponad 40%) jest magazynowana w postaci przetworzonej energii chemicznej – której głównym nośnikiem
jest ATP.
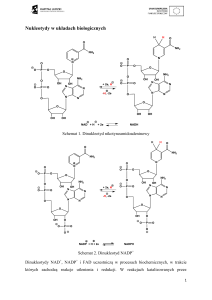
Substraty energetyczne są dawcami par atomów wodoru dla specjalnych koenzymów: dinukleotydu
nikotynoamido-adeninowego (NAD) lub dinukleotydu flawinoadeninowego (FAD) tworząc ich
zredukowane formy, które przekazują dalej protony i elektrony na kolejne akceptory, a w końcowym etapie
na atom tlenu.
System przenośników protonów i elektronów z substratu energetycznego na tlen, prowadzący do
wytworzenia H O, pod nazwą łańcucha oddechowego.
Elektrony, które przechodzą przez łańcuch oddechowy, tracą znaczną część ich wolnej energii. Część tej
energii jest przetwarzana w energię chemiczną i magazynowana w postaci ATP.
Proces powstawania ATP, sprzężony z mitochondrialnym systemem transportu elektronów przez
łańcuch oddechowy pod nazwą fosforylacji oksydacyjnej.
2
2
Energia zmagazynowana w postaci ATP jest zużytkowana przede wszystkim do:
skurczu mięśni szkieletowych
skurczu mięśnia sercowego
utrzymania gradientu stężeń jonów i metabolitów po obydwu stronach błon biologicznych
prawidłowego funkcjonowania OUN
na pokrycie potrzeb energetycznych związanych z przebiegiem różnych syntez
PRZEKAZYWANIE ENERGII CHEMICZNEJ PRZEZ ATP
2
ZWIĄZKI FOSFORANOWE O WYSOKIEJ ENERGII
Do związków fosforanowych o wysokiej energii należą: 1,2-bisfosfoglicerynian, fosfoenolopirogronian,
fosfokreatyna. Ta ostatnia jest rezerwuarem energii potrzebnej do skurczu mięśnia. Bezpośrednim dawcą
energii dla tego procesu jest ATP, lecz jego zasoby w komórkach mięśniowych wystarczyłyby zaledwie na
kilka sekund. Doraźny mechanizm szybkiego odtwarzania ATP polega na przenoszeniu reszty fosforanowej
z fosfokreatyny na ADP.
Uwalnianie energii ze związków wysokoenergetycznych nosi nazwę fosforylacji substratowej
(powstawanie energii z pominięciem łańcucha oddechowego).
ZWIĄZKI FOSFORANOWE O BARDZO WYSOKIEJ ENERGII
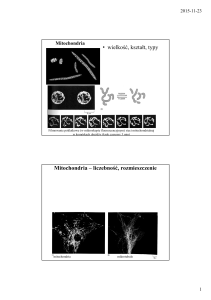
MITOCHONDRIUM
Mitochondrium pełni rolę generatora energii (siłowni energetycznej). Niektóre komórki (komórki czerwone) w ogóle
nie posiadają mitochondriów – nie mają zdolności utleniania substratów energetycznych ani produkcji ATP drogą
fosforylacji oksydacyjnej. Mięsień sercowy, komórki wątrobowe potrzebują dużo energii, zawierają dużo
mitochondriów.
ORGANIZACJA ŁAŃCUCHA TRANSPORTU
PROTONÓW I ELEKTRONÓW
Łańcuch zlokalizowany jest w wewnętrznej błonie mitochondrialnej.
Pierwszym akceptorem atomów wodoru odłączanych od substratu jest najczęściej NAD (niekiedy FAD ),
kolejnym FMN, następnym koenzym Q (ubichinon), a dalszy transport elektronów zachodzi niezależnie od
transportu protonów. Elektrony poprzez cytochrom b, cytochrom c1, cytochrom c oraz cytochrom a+a
przechodzą na tlen. Powstaje anion tlenkowy O , który wiąże się z dwoma protonami tworząc cząsteczkę
wody.
+
+
3
2-
ŁAŃCUCH ODDECHOWY SPRZĘŻONY
Z OKSYDACYJNĄ FOSFORYLACJĄ
Łańcuch transportu elektronów jest sprzężony w trzech miejscach z reakcjami fosforylacji, w których ADP
wiąże Pi tworząc ATP. Transport jednej pary atomów wodoru z substratu na tlen przy udziale NAD dostarcza
3 cząsteczek ATP, a transport przy udziale FAD – 2 cząsteczek ATP. Wodory z FADH są przekazywane
bezpośrednio na koenzym Q, z pominięciem NAD i FMN, a także miejsca pierwszej fosforylacji.
+
2
+
KOMPLEKSY ODDECHOWE
Elementy składowe łańcucha oddechowego można podzielić na:
Kompleks I. Oksydoreduktaza NADH-ubichinon (dehydrogenaza NADH), zawiera trwale związaną cząsteczkę
FMN. Jest sprzężony z reakcją fosforylacji.
Kompleks II. Oksydoreduktaza bursztynian-ubichinon. Jest kompleksem dehydrogenazy bursztynianowej z FAD
oraz białek Fe:S.
Kompleks III. Oksydoreduktaza ubichinon-utleniony cytochrom c, zawiera cytochrom b, białka Fe:S oraz
cytochrom c1. Jest sprzężony z reakcją fosforylacji.
Kompleks IV. Oksydoreduktaza zredukowany cytochrom c-tlen, zwany oksydazą cytochromową. Zawiera
cytochromy a i a3. Jest sprzężony z reakcją fosforylacji.
Kompleks V. Syntaza ATP złożona z dwóch domen, zawierających liczne podjednostki.
TEORIA CHEMIOSMOTYCZNA
Mechanizm sprzężenia transportu elektronów przez łańcuch oddechowy z syntezą ATP jest przedmiotem
kilku hipotez. Najbardziej przekonywującą wydaje się być teoria chemiosmotyczna, która zakłada, iż
kompleksy I, III i IV pełnią funkcję pompy protonowej. Transport elektronów przez łańcuch oddechowy jest
sprzężony z przemieszczaniem protonów (H ) w poprzek wewnętrznej błony mitochondrialnej. Wytwarza
się gradient elektryczny i gradient pH po obydwu stronach. Strona zewnętrzna błony staje się bardziej
dodatnio naładowana niż strona wewnętrzna. Po stronie zewnętrznej wytwarza się niższe pH niż po stronie
wewnętrznej. Energia generowana przez gradient protonów napędza syntezę ATP. Proces ten jest
katalizowany przez kompleks enzymatyczny, zwany syntezą ATP.
INHIBITORY TRANSPRTU ELEKTRONÓW
Niektóre substancje hamują w sposób wybiórczy transport elektronów przez określone ogniwa łańcucha
oddechowego, hamując równocześnie syntezę ATP. Amytal i rotenon hamują przepływ elektronów z FMN
na koenzym Q, antymycyna hamuje przekazywanie elektronów z cytochromu b na cytochrom c, a cyjanek
i tlenek węgla hamują funkcję oksydazy cytochromowej.
Możliwe jest zahamowanie fosforylacji przy zachowaniu transportu elektronów przez łańcuch oddechowy.
Taka sytuacja nosi nazwę rozprzężenia fosforylacji oksydacyjnej. Transport elektronów i fosforylacja
mogą być rozprzężone przez: 2,4-dinitrofenol, dikumarol, wysokie stężenia tyroksyny lub duże dawki
leków z grupy salicylanów (np. aspiryny). Rozprzężenie fosforylacji oksydacyjnej sprawia, iż substraty
energetyczne podlegają utlenianiu, lecz nie towarzyszy temu powstawanie ATP.
+
UTLENIANIE SUBSTRATÓW NIEZALEŻNE
OD ŁAŃCUCHA ODDECHOWEGO
Procesy te nie mają udziału w tworzeniu ATP.
Oksydazy przenoszą pary atomów wodoru z substratu bezpośrednio na tlen. Uczestniczą w oksydacyjnej
deaminacji L-aminokwasów. Zwykle zawierają FMN lub FAD jako grupy prostetyczne. FMNH jak i
2
FADH powstające w wyżej wymienionych reakcjach, są utleniane bezpośrednio przez tlen – powstaje
nadtlenek wodoru (H O ):
FMNH + O FMN + H O
FADH + O FAD + H O
Oksygenazy utleniają substraty poprzez bezpośrednie wbudowywanie do nich tlenu. Dzielą się na: mono i
dioksygenazy.
REAKTYWNE FORMY TLENU – RTF
2
2
2
2
2
2
2
2
2
2
2
Funkcjonowanie łańcucha oddechowego i procesów utleniania od niego niezależnych wiąże się z
powstawaniem reaktywnych form tlenu (RTF). Niektóre z nich noszą nazwę wolnych rodników tlenowych
(aktywnych form tlenu). Wolnymi rodnikami nazywamy atomy lub cząsteczki mające niesparowany
elektron.
Do reaktywnych form tlenu należy zaliczyć przede wszystkim:
anionorodnik ponadtlenkowy
rodnik wodoronadtlenkowi
rodnik wodorotlenowy
oraz tlenek azotu, dwutlenek azotu, tlen singletowy.
Reaktywne formy tlenu wywierają szereg efektów toksycznych. Powodują uszkodzenia błon
plazmatycznych (np. erytrocytów). Utleniają różne związki biologiczne – tym samym inaktywują wiele
enzymów i białek transportowych. Degradują białka macierzy pozakomórkowej. W różny sposób naruszają
strukturę kwasów nukleinowych – co może powodować mutacje i transformacje nowotworowe. RFT
powodują degradację nienasyconych kwasów tłuszczowych.
RFT powodują miażdżycę, pełnią istotną rolę w procesach zapalnych, są bezpośrednią przyczyną wielu
schorzeń, a także powodują starzenie się organizmu.
Wolne rodniki są bardzo nietrwałe i mogą być unieczynnione w komórce przez odpowiednie enzymy
oksydoredukcyjne i dostateczną ilość substratów redukujących. Enzymy: katalaza i peroksydaza rozkładają
nadtlenek wodoru, uniemożliwiając powstawanie rodników wodorotlenowych. Wolne rodniki przekształca
dysmutaza ponadtlenkowa. Liczne antyoksydanty jak: glutation (związki tiolowe) oraz witaminy E, C, A
zdolne są do detoksykacji wolnych rodników tlenowych.
Plik z chomika:
mixstar
Inne pliki z tego folderu:
BIOCHEMIA 2.doc (3068 KB)
BIOCHEMIA 20.doc (1623 KB)
BIOCHEMIA 1.doc (899 KB)
BIOCHEMIA 5.pdf (817 KB)
BIOCHEMIA 15.doc (60 KB)
Inne foldery tego chomika:
Egzamin
Giełdy
Obliczenia biochemiczne
Podręczniki
Szlak pentozofosforanowy
Zgłoś jeśli naruszono regulamin
Strona główna
Aktualności
Kontakt
Dział Pomocy
Opinie
Regulamin serwisu
Polityka prywatności
Copyright © 2012 Chomikuj.pl