Uniwersytet Przyrodniczy we Wrocławiu
Wydział Przyrodniczo-Technologiczny
Kierunek: Ochrona Środowiska
Wpływ dodatków organicznych na wzrost i rozwój
siewek Dactylorhiza sambucina (L.) Soó
Natalia Lipińska
Praca magisterska
wykonana
pod kierunkiem dr inż. Joanny Pokorny
Wrocław, 2009
Na terenie Polski występuje około 50 gatunków storczyków reprezentujących 22 rodzaje i
są to głównie przedstawiciele rodzajów Dactylorhiza i Orchis (Michalik 1975, Szlachetko,
Skakuj 1996, Szlachetko 2001). Wśród gatunku storczyków występujących na terenie
Dolnego Śląska należy wymienić Dactylorhiza sambucina. Jest to gatunek narażony na
wyginięcie i znajduje się w Polskiej Czerwonej Księdze Roślin (kategoria VU)
(Kaźmierczakowa Zarzycki 2001) oraz na Liście Roślin Rzadkich i Zagrożonych (Kategoria
V) (Szeląg ,Zarzycki 1992). Podlega on więc ścisłej ochronie gatunkowej (Piękoś-Mirkowa
2003).
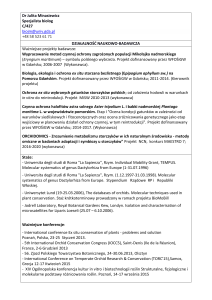
Dactylorhiza sambucina (kukułka bzowa) (ryc.1) to geofit należący do rodzaju Dactylorhiza
Necker ex Nevski, o krótkich bulwach, płytko podzielonych osiągający wysokość 10-25 cm.
Łodyga jest mocna, sztywna i pusta w środku. Liście zazwyczaj występują w ilości 4-6 i
osiągając długość do 10 cm i szerokość 2,5 cm. Kwiatostan jest krótki, złożony z kilku do
kilkunastu kwiatów. Kwiaty występują w dwóch odmianach barwnych: żółtej i czerwono
purpurowej (Mróz 1993, Van der Cingel 1995,Piękoś-Mirkowa 2003).
Ryc.1. Kukułka bzowa Dactylorhiza sambucina forma czerwono kwiatowa i żółto kwiatowa.
Dactylorhiza sambucina to gatunek europejski, reprezentujący typ zasięgowy alpijskopółnocnoeuropejski. Rozmieszczony jest w strefie umiarkowanej i śródziemnomorskiej
(Kaźmierczakowa 2001, Zarzycki 2001, Zając, Zając 2001). Występowanie Dactylorhiza
sambucina obejmuje południową Skandynawię, środkową i południową Europę, Kaukaz,
Azję Mniejszą, środkową Francję i południowe Niemcy (Zając, Zając 2001). W Polsce została
ona odnotowana na około 160 stanowiskach, gdzie w ostatnich latach została potwierdzona na
40. Występuje ona głównie w Sudetach (do 1000 m n.p.m) i Karpatach (do 1115 m n.p.m).
Jego najbardziej wysunięte stanowiska znajdują się na Pogórzu Kaczawskim. W przypadku
Karpat największe skupienia znajdują się w Pieninach (ryc.2).
Ryc.2. Mapa występowania Dactylorhiza sambucina na terenie Polski (Zając, Zając 2001).
Występuje ona więc w miejscach o południowej ekspozycji światła. Rośnie głównie na
łąkach, trawiastych zboczach i świetlistych zaroślach. Preferuje gleby świeże brunatne, które
są mniej lub bardziej wyługowane o odczynie kwaśnym do obojętnego. Najczęściej jednak
występuje na łąkach należących do rzędu Arrhenatheretalia i ubogich murawach
kserotermicznych rzędu Nardetalia oraz Festuco-Brometea. Największym zagrożeniem dla
Dactylorhiza sambucina jest intensywna gospodarka łąkowa i zarastanie naturalnych
stanowisk. Roślinie zagraża także bezpośrednie niebezpieczeństwo ze strony człowieka, co
szczególnie jest widoczne na szlakach turystycznych.
W celu ochrony tego gatunku można wykorzystać hodowlę roślin w kulturach in vitro
do jego wegetatywnego rozmnażania. Z jednego wierzchołka wzrostu można bowiem uzyskać
nieograniczoną liczbę roślin charakteryzująca się odpornością np. na warunki stresowe
(Arczewska 1993, Kopcewicz, Lewak 2002). Kultury in vitro są jedną z metod ex situ, które
przyniosły ogromne korzyści w rozmnażaniu storczyków. Metoda ta, znalazła zastosowanie
przede wszystkim w ogrodnictwie a także w rolnictwie i produkcji roślin, które trudno
rozmnażać wegetatywnie za pomocą tradycyjnych metod (Grabowski et al.1986). Obecnie
liczba gatunków roślin, które rozmnaża się za pomocą technik in vitro wynosi około 300,
natomiast na świecie produkuje się około 800 milionów sztuk roślin, z czego 90% stanowią
rośliny ozdobne. Wynikiem hodowli jest wzrost danego eksplantu, który objawia się
wydłużeniem komórek i podziałami.
Dzięki tej metodzie można szybciej otrzymać nowe rośliny, ale także uwolnić je od
patogenów. Mogą być one wykorzystywane do zachowania zasobów genowych zagrożonych
i bardzo rzadkich gatunków roślin (Znaniecka, Wojkowska 2008).
Celem pracy było poznanie wpływu dodatków organicznych na wzrost i rozwój
zagrożonego gatunku Dactylorhiza sambucina i wskazanie na możliwość wykorzystania ich
do wegetatywnego rozmnażania. Badania nad wpływem dodatków organicznych na wzrost i
rozwój Dactylorhiza sambucina w kulturach in vitro przeprowadzono w miesiącach: marzeclistopad 2008 w Pracowni Kultur Tkankowych Ogrodu Botanicznego Uniwersytetu
Wrocławskiego. Materiał liczył 454 sztuk siewek Dactylorhiza sambucina. Zastosowane w
doświadczeniu dodatki organiczne zostały podzielone na trzy grupy:
•
I dodatki scalające pożywkę: kasza gryczana i jęczmienna, mąka kukurydziana i
ziemniaczana, płatki owsiane, ryż, soja i len
•
II ekstrakty takie jak : herbata
•
III kwasy organiczne: kwas nonanowy 1µM oraz 2 µM; kwas nonanowy 1µM i 2 µM
+ perlit; kwas kaprynowy 1 µM i 2 µM; kwas kaprynowy 1 µM i 2 µM + perlit
(ryc.3,4)
Ryc.3. Pożywki z dodatkami organicznymi.
Ryc.4. Kwasy organiczne dodane do pożywki Fa.
W celu określenia wpływu dodatków organicznych na siewki Dactylorhiza sambucina
zmierzono następujące cechy: liczbę liści (szt.), liczbę korzeni (szt.), długość liści (cm),
długość korzeni (cm), masę siewek (mg), żywotność siewek. Kolby w których znajdowała się
pożywka zostały poddane autoklawowaniu w temp. 1200C i ciśnieniu 1 atm czyli 0,1 MPa.
Czas przetrzymywania kolb w autoklawie wynosił 20 min. Etap pasażowania został
wykonany w komorze laminarnej, w której odbywa się ciągły przepływ jałowego powietrza,
co uniemożliwia wtargnięcie do jej wnętrza drobnych zanieczyszczeń, które unoszą się w
powietrzu (Górska et al. 2008). W czasie pracy założono rękawiczki chirurgiczne oraz
maseczkę, tak aby zapewnić w marę najbardziej sterylne warunki pracy a narzędzia poddano
odkażaniu 70% alkoholem etylowym.
Do każdej z kolb przenoszono po 5 siewek Dactylorhiza sambucina zamykając je folią z
aluminium. Wszystkie kolby zostały następnie przeniesione do fitotronów (ryc.5), które
mieszczą się w piwnicy Pracowni Kultur Tkankowych Ogrodu Botanicznego Uniwersytetu
Wrocławskiego.
Ryc.5. Fitotrony w pracowni kultur in vitro Ogrodu Botanicznego we Wrocławiu.
W fitotronach siewki Dactylorhiza sambucina przechowywane były w temperaturze 100C o
natężeniu światła około 6000 lx. W doświadczeniu posłużono się następującymi parametrami
statystycznymi: średnią arytmetyczną (x), błędem standardowym (s), wartością minimum
(min), wartością maksimum (max), wariancją ( S2).
Wyznaczenie wartości średnich w poszczególnych pożywkach pozwoliło na wyodrębnienie
dodatku organicznego, który najlepiej wpłynął na określoną cechę siewek Dactylorhiza
sambucina. Na liczbę liści najlepiej wpłynęły pożywki Fa + ryż oraz Fa + mąka
ziemniaczana, na których stwierdzono największy średni przyrost lisci : 2,4 sztuki oraz na
pożywce Fa gdzie odnotowano pojawienie się średnio 2 sztuk nowych liści (ryc.6,7). Na
pożywkach: Fa + kwas kaprynowy 2µM, Fa + kwas nonanowy 1 µM + perlit wartości były
zbliżone i odnotowano pojawienie się jednego liścia w siewkach. W przypadku długości liści
najwyższe wartości średnie odnotowano na pożywce Fa + kwas kaprynowy 2µM i na
pożywce Fa+ mąka ziemniaczana. Z kolei na pożywkach Fa + soja (ryc.8,9), Fa + herbata, Fa
+ kwas kaprynowy 2 µM, Fa + kwas kaprynowy 1 µM + perlit nie odnotowano przyrostów.
Na zwiększenie się liczby korzeni najlepiej wpłynęły z kolei pożywki: Fa, Fa + ryż, Fa +
mąka kukurydziana , Fa + mąka ziemniaczana oraz Fa + kwas kaprynowy 2µM (wyk.2).
W przypadku długości korzeni dodatni wpływ odnotowano na pożywkach: Fa + kwas
kaprynowy 2µM ( średnia równa 3,27 cm), Fa + kwas kaprynowy 2 µM + perlit ( średnia
równa 2,68 cm) oraz pożywce Fa (średnia 2,54 cm).
Przyrostów nie odnotowano natomiast na pożywkach: Fa + kasza gryczana, Fa + kasza
jęczmienna, Fa + ryż, Fa + soja co świadczy o negatywnym ich wpływie tych na długość
8
koniec doświadczenia
6
początek doświadczenia
4
2
Fa+ kw.nonanowy Fa+perlit
2uM
Fa+ kw.nonanowy Fa+perlit
1uM
Fa+ kw.kapronowy 2uM
Fa+ kw.kaprynowy 2uM
Fa+ kw.kaprynowy Fa+perlit
1uM
Fa+ kw.kaprynowy Fa + perlit
2uM
Fa+ soja
Fa+ płatki owsiane
Fa+ herbata
Fa+ ryż
Fa+ len
Fa+ mąka ziemniaczana
Fa+ mąka kukurydziana
Fa+ kasza jęczmienna
rodzaj pożywki
Fa+ kasza gryczana
0
Fa
długość [cm]
korzeni (wyk.1).
35
30
25
20
15
10
5
0
koniec doświadczenia
początek doświadczenia
Fa+ kw.nonanowy Fa+perlit 2uM
Fa+ kw.nonanowy Fa+perlit 1uM
Fa+ kw.kapronowy 2uM
Fa+ kw.kaprynowy 2uM
Fa+ kw.kaprynowy Fa+perlit 1uM
Fa+ kw.kaprynowy Fa + perlit 2uM
Fa+ soja
Fa+ płatki owsiane
Fa+ ryż
Fa+ herbata
Fa+ len
Fa+ mąka ziemniaczana
Fa+ mąka kukurydziana
Fa+ kasza gryczana
Fa+ kasza jęczmienna
rodzaj pożywki
Fa
liczba sztuk [szt.]
Wykres.1. Długość korzeni Dactylorhiza sambucina w zależności od dodatku organicznego.
Wykres.2. Liczba korzeni Dactylorhiza sambucina w zależności od dodatku.
9000
koniec doświadczenia
8000
początek doświadczenia
masa [mg]
7000
6000
5000
4000
3000
2000
Fa+ kw.nonanowy 2um+perlit
Fa+ kw.nonanowy 1um+perlit
Fa+ kw.kapronowy 2um
Fa+ kw.kaprynowy 2um
Fa+ kw.kaprynowy 2um +perlit
Fa+ kw.kaprynowy 1um +perlit
r odzaj pożyw k i
Fa+ soja
Fa+ płatki owsiane
Fa+ herbata
Fa+ ryż
Fa+ len
Fa+ mąka ziemniaczana
Fa+ mąka kukurydziana
Fa+ kasza jęczmienna
Fa+ kasza gryczana
0
Fa
1000
Wykres.3.Zróżnicowanie masy siewek Dactylorhiza sambucina w zależności od dodatku organicznego na
początku i na końcu doświadczenia.
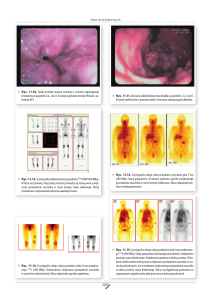
Ryc.6. Pożywka Fa na początku doświadczenia.
Ryc.7. Pożywka Fa na końcu doświadczenia.
Ryc.8. Pożywka Fa+ soja na początku doświadczenia.
Ryc.9. Pozywka Fa+soja na końcu doświadczenia.
Ryc.10. Pożywka Fa+len na początku doświadczenia.
Ryc.11. Pożywka Fa+len na końcu doświadczenia.
Największa liczba żywych siewek Dactylorhiza sambucina została stwierdzona na
pożywkach z dodatkiem: ryżu 89%, lnu 80%, mąki kukurydzianej 100%,herbaty 81% oraz
kwasu kaprynowego Fa 2 µm 100%. W przypadku kontroli (Fa) oraz kaszy gryczanej liczba
żywych siewek wyniosła 55 %, z kolei na płatkach owsianych, mące ziemniaczanej, soi oraz
kaszy jęczmiennej liczba ta wyniosła 60%. Największą liczbą zamarłych siewek
charakteryzowały się: Fa + kwas kaprynowy 1µM, Fa + kwas nonanowy 1 µM, Fa + kwas
nonanowy 2 µM, Fa + kwas nonanowy 1 µM oraz w kwas nonanowy 2 µM (wyk.4).
120
liczebność [%]
100
80
siewki żywe
siewki martwe
60
40
Fa+ kw. nonanowy 2um
Fa+ kw. nonanowy 1um
Fa+ kw. nonanowy Fa 2um
Fa+ kw. nonanowy Fa 1um
Fa+ kw. nonanowy 2um + perlit
Fa+ kw.kaprynowy 2um
Fa+ kw. nonanowy 1um + perlit
Fa+ kw. kapronowy 2um
Fa+ kw. kaprynowy 1um
Fa+ kw.kaprynowy 2um + perlit
Fa+ kw. kaprynowy 1um + perlit
Fa+ soja
Fa+ herbata
Fa+ mąka ziemniaczana
Fa+ kasza gryczana
Fa+ mąka kukurydziana
Fa+ len
Fa+ płatki owsiane
Fa+ kasza jęczmienna
Fa
0
Fa+ ryż
20
rodzaj pożywki
Wykres. 4. Żywotność siewek Dactylorhiza sambucina.
Tabela 1. Porównanie wartości
średnich w poszczególnych cechach przy zastosowaniu
pożywek z różnymi dodatkami organicznymi.
Rodzaj
pożywki
Cecha
Liczba liści
Długość liści
Liczba korzeni
Długość korzeni
[szt.]
[cm]
[szt.]
[cm]
Fa
2
0,72
5,6
2,54
Fa + płatki
owsiane
Fa + kasza
gryczana
Fa + kasza
jęczmienna
Fa + ryż
0,4
0,73
3,4
0,23
-1
0,48
1,6
-0,26
-1
0,51
0,34
-0,07
2,4
0,36
2,2
-0,06
Fa + mąka
kukurydziana
0,6
0,42
2,4
0,07
Fa + mąka
ziemniaczana
Fa + soja
2,4
1
3,4
1,3
-3,67
-0,23
-0,3
-0,38
Fa + len
-3
0,59
0,75
0,07
Fa + herbata
-4
-0,4
1,2
0,03
Fa + kwas
kaprynowy
2µm
Fa + kwas
kaprynowy Fa
2 µm
Fa + kwas
nonanowy 1
µm + perlit
Fa + kwas
kaprynowy 1
µm + perlit
Fa + kwas
kaprynowy 2
µm + perlit
Fa + kwas
nonanowy 2
µm + perlit
1
6,38
3
3,27
1
1,02
-3
0,39
1
-0,03
1
2,3
-1
-0,13
0
1,52
-4
-0,25
2
2,68
-1
0,93
0
0,1
Storczyki jako rośliny o wyspecjalizowanych wymaganiach pokarmowych potrzebują
do swojego prawidłowego rozwoju w kulturach in vitro pożywek odpowiednich pod
względem
konsystencji,
odczynu,
ilości
oraz
jakości
składników
mineralnych
i witamin. Analiza badanych cech wykazała, że skład chemiczny zastosowanych dodatków
organicznych w doświadczeniu wyraźnie wpłynął na liczbę liści, liczbę korzeni, długość liści
oraz długość korzeni Dactylorhiza sambucina. Wszystkie dodatki organiczne w swoim
składzie chemicznym zawierały: wodę, białko, tłuszcze, cukrowce, błonnik. Jedynie w
przypadku soi i lnu w składzie chemicznym pojawiły się substancje bezazotowe, natomiast w
herbacie znalazły się także garbniki i kofeina. W doświadczeniu wykazano iż kasza gryczana,
kasza jęczmienna oraz płatki owsiane negatywnie wpłynęły na liczbę liści oraz długość
korzeni. Na zahamowanie wzrostu długości liści i korzeni wpływ miały pożywki z dodatkiem
mąki kukurydzianej, mąki ziemniaczanej i ryżu. Do badań nad storczykiem Dactylorhiza
sambucina wybrano pożywkę Fa, która charakteryzuje się niską zawartością soli mineralnych,
obecnością peptonu, ekstraktu drożdżowego a także zawartością sacharozy i fruktozy.
Pożywka Fa wpływa najlepiej na wzrost i rozwój siewek storczyków w doświadczeniu o
czym świadczy zwiększona liczba liści oraz korzeni pod koniec doświadczenia.
Europejskie gatunki storczyków w naturze rosną głównie na siedliskach ubogich w
składniki pokarmowe, zatem pożywka Fa w skład, której wchodzą m.in. mikro i
makroskładniki, wpłynęła korzystnie na ich wzrost i rozwój. W miarę trwania doświadczenia
można było także zaobserwować iż kolor pożywki stał się ciemniejszy co świadczy o
wydzielaniu fenoli przez siewki Dactylorhiza sambucina. Wydzielany fenol mógł być zatem
przyczyną zamierania większości siewek np. na pożywkach Fa+ mąka kukurydziana, Fa+
mąka ziemniaczana, Fa+ soja.
Dodatkowo wzrost i rozwój siewek Dactylorhiza sambucina zależy w dużym stopniu
od
składu
chemicznego
zastosowanej
pożywki.
Istotna
jest
bowiem
zawartość
poszczególnych mikro i makroskładników. Niedobór składników pokarmowych prowadzi do
słabego przyrostu, liście stają się najczęściej jasnozielone, pseudobulwy natomiast są słabo
rozwinięte. Ich nadmiar natomiast może spowodować deformację liści, oraz obumieranie
korzeni. Na wzrost i rozwój Dactylorhiza sambucina wpływ ma także dostępność eksplantów
do wody, która dodawana jest do pożywki. W przypadku Fa + kasza gryczana
prawdopodobnie przyczyną zamierania większości siewek był utrudniony dostęp do wody.
Woda w przypadku tej pożywki związana była z ziarnami kaszy gryczanej uniemożliwiając
pobieranie jej przez siewki. W przypadku siewek Dactylorhiza sambucina stężenie soli
wynosiło 1 ml zaś zawartość sacharozy w pożywce była równa 14 g/l, jednak na siewkach nie
pojawiły się nekrozy a przyrost masy był dość wysoki, w szczególności w przypadku
dodatków organicznych takich jak: mąka ziemniaczana, mąka kukurydziana, ryż czy płatki
owsiane. W tych pożywkach zaobserwowano także szybki wzrost liści i rozwój korzeni w
porównaniu z pozostałymi dodatkami. W doświadczenia z Dactylorhiza sambucina do
pożywki Fa dodany został pepton w ilości 2 g/l ,mimo to nie wpłynął on na tworzenie się
dodatkowych protokormów. Agar natomiast dodawany do pożywki umożliwia dyfuzję
składników pokarmowych znajdujących się w pożywce. Zbyt duże stężenie agaru w pożywce
może utrudniać dyfuzję co wpływa na zmniejszenie się dostępności substancji odżywczych
dla komórek i być może jest to przyczyną nieformowania się dodatkowych protokormów.
Spis literatury:
1. Arczewska A., 1993. Wstępne stadia rozwojowe storczyków europejskich w kulturze in
vitro. Acta Universitatis Wratislaviensis 1515, Prace Botaniczne LVII: 215-221
2. Grabowski K., Krause J., Lisiecka A., 1986. Rośliny ozdobne, rozmnażanie roślin
ozdobnych część I, PWN, Warszawa, s. 118
3. Kopcewicz J., Lewak S., 2002. Fizjologia roślin, PWN, Warszaw, s. 806
4. Michalik S., 1975. Storczyki-ginąca grupa roślin, Wiadomości Botaniczne 19 ( 4): 231-243
5. Mróz L., 1994. Ekologia Dactylorhiza sambucina (L.) Soó w Sudetach. Acta Universitatis
Wratislaviensis 1605, Prace Botaniczne LXXVI: 103-157
6. Piękoś- Mirkowa H., 2003. Atlas roślin chronionych , Multico Oficyna Wydawnicza,
Warszawa, s. 270-271
7. Szeląg Z., Zarzycki K., 1992. Czerwona lista roślin naczyniowych zagrożonych w Polsce.
[w:] K. Zarzycki, W. Wojewoda &Z. Heinrich (red.). Lista roślin zagrożonych w Polsce. IB
im. W. Szafera, PAN, Kraków, ss. 87-98.
8.Szlachetko D., Skakuj M., 1996. Storczyki Polski, Wydawnictwo Sorus, Poznań, s.245
9. Szlachetko D., 2001. Storczyki, Multico Oficyna Wydawnicza, Warszawa, s.168
10.Van der Cingel 1995. An atlas of Orchid pollination, A.A Bakkema Publishers, Rotterdam,
s. 175
11.Zając A., Zając M., 2001. Atlas rozmieszczenia roślin naczyniowych w Polsce, Kraków, s.
188
12.Znaniecka J., Wojkowska E., 2008. Zastosowanie hodowli in vitro w ochronie ex situ
storczyków, Problemy badawcze i perspektywy ochrony storczykowatych w Polsce, OsowiecTwierdza, s.96-103