dr hab. Tadeusz Dobosz
PRAKTIKUM Z BIOLOGII MOLEKULARNEJ
Materiały pomocnicze do zajęć z biologii molekularnej, diagnostyki molekularnej i
medycyny molekularnej dla studentów Akademii Medycznej we Wrocławiu.
Wydanie internetowe.
Data ostatniej aktualizacji - 15 lutego 2005
Katedra Medycyny Sądowej Akademii Medycznej we Wrocławiu
Zakład Technik Molekularnych
Spis treści:
1. Wykaz skrótów i objaśnienie terminów użytych w pracy
2. Co zagraża pracownikowi laboratorium
3. Materiał genetyczny człowieka
4. Izolacja DNA i RNA
5. Enzymy restrykcyjne
6. Elektroforeza i detekcja DNA i RNA
7. Blotting i hybrydyzacja
8. Odwrotna transkrypcja
9. Reakcja PCR
10. Sekwencjonowanie DNA
11. Zastosowanie biologii molekularnej w medycynie sądowej
12. Zastosowanie biologii molekularnej w seroantropologii
13. Zastosowanie biologii molekularnej w medycynie (terapia genetyczna)
14. Klonowanie DNA
15. Przewidywane kierunki rozwoju biologii molekularnej
1. Wykaz skrótów i objaśnienie terminów użytych w tekście.
A - adenina
Agaroza - polimer węglowodanowy, uzyskiwany z wodorostów, służy do łatwego
(poprzez rozgotowywanie) sporządzania żeli do elektroforezy
Autoklaw - ciśnieniowy sterylizator parowy
Blot - folia nylonowa, na którą przeniesiono analizowane fragmenty DNA
Blotting - przenoszenie fragmentów DNA z żelu na folię nylonową
C - cytozyna
cDNA - ang. Cloned Deoxyrybonucleic Acid - klonowany DNA, kwas
deoksyrybonukleinowy, uzyskany z nici mRNA za pomocą techniki odwrotnej
transkrypcji
Cis - po tej samej stronie (w odróżnieniu od trans - po drugiej stronie)
DNA - ang. Deoxyrybonucleic Acid - kwas deoksyrybonukleinowy
DTT - ang. Dithiotreitol - ditiotreitol, odczynnik redukujący mostki siarkowe w białkach
Dygestorium - wyciąg, szafka z wymuszoną wentylacją ("wciąga" szkodliwe opary)
Elektroforeza - metoda rozdziału naładowanych elektrycznie cząsteczek w polu
prądu elektrycznego stałego lub zmiennego (wprowadzona w 1937
roku przez Tiseliusa, nagroda Nobla w 1948 roku)
G - guanina
Genom - DNA zawarty w pojedynczym jądrze komórkowym zygoty
Glovesbox - komora do pracy z materiałem niebezpiecznym (z zamontowanymi na
stałe gumowymi rękawicami w przedniej szybie lub bocznych ściankach)
Helisa - struktura przestrzenna, złożona z dwu owiniętych wokół siebie łańcuchów
Kancerogen - substancja rakotwórcza
Kapilara - wypełniona rzadkim żelem cienka rurka szklana lub kwarcowa, ostatnio
coraz częściej stosowana do elektroforezy produktów reakcji PCR lub
reakcji sekwencjonowania DNA
Klenow'a fragment - polimeraza DNA strawiona tak dobraną proteazą, aby produkt
trawienia zachował aktywność enzymatyczną
Laminar - komora, do której poprzez filtry jest nawiewane sterylne powietrze
MALDI - TOF - ang. Matrix Associated Laser Desorption Ionization - Time Of Flight –
technika analizy spektralnej, polegająca na odparowaniu laserem
próbki i pomiarze czasu, w którym sublimująca substancja dociera do
detektora
mg - miligram, 10-3 grama
Mg++ - jon magnezowy, aktywator polimeraz DNA, najczęściej dostarczany w postaci
soli chlorkowej, rzadziej siarczanowej
Mitochondrium - "siłownia" komórki, oraganellum w którym zachodzą intensywne
procesy energetyczne, prowadzące do wytwarzania dużych ilości
ATP
Multi loci - próba (sonda) molekularna hybrydyzująca z wieloma fragmentami
restrykcyjnymi, dająca charakterystyczny wzór prążkowy, podobny do
kreskowego kodu towarowego
Mutagen - substancja powodująca mutacje (zmiany w DNA)
mpz - megapary zasad, odcinki DNA mierzone w jednostkach wyrażonych w
milionach par
mRNA - ang. Messenger Rybonuleic Acid - informacyjny RNA, wzorzec do syntezy
białek, kwas nukleinowy uzyskany z przepisania informacji z nici DNA na nić
RNA, poddany enzymatycznej obróbce polegającej na wycięciu
niepotrzebnych fragmentów (np. intronów)
N - którakolwiek z zasad (A, U, T, G, C)
ng - nanogram, 10-9 grama
Organellum - struktura komórkowa, odpowiedzialna za daną funkcję biologiczną (np.
mitochondria są głównym miejscem syntezy ATP w komórce)
Patogen - czynnik zakaźny
Palindrom - tekst, który można czytać jednakowo od początku i od końca (np. "kobyła
ma mały bok")
PCR - ang. Polymerase Chain Reaction - reakcja polimerazowa, namnażanie DNA in
vitro, (metoda wprowadzona w 1986 roku przez Mullisa, nagroda Nobla w
1993 roku)
pg - pikogram, 10-12 grama
plazmid - niewielki zamknięty (kolisty) łańcuch DNA w cytoplazmie bakterii,
replikujący się samodzielnie, często determinuje odporność na antybiotyk
pmRNA - ang. Prematured Rybonuleic Acid - świeżo wytworzony RNA, jeszcze przed
wycięciem niepotrzebnych fragmentów, potocznie także zwany "surowym
transkryptem", w szeregu podręczników błędnie nazywany "mRNA"
Poli A - sekwencja kilkunastu adenin, charakterystyczna dla mRNA
Poli T - sekwencja komplementarna do poli A, wykorzystywana przy uzolacji mRNA
Prąd przemienny - prąd elektryczny, w którym biegunowość oscyluje (plus co chwila
zamienia się miejscami z minusem)
Prąd stały - prąd elektryczny o stałej biegunowości (elektroda podłączona do
dodatniego źródła takiego prądu to anoda, do ujemnego to katoda)
Prąd zmienny - prąd elektryczny o stałej biegunowości, lecz o zmiennym (najczęściej
regularnie falującym) napięciu
Primer - odcinek DNA o długości na ogół od 15 do 30 pz, stosowany w reakcji PCR
do "oflankowania" fragmentu DNA który ma być powielony w wyniku reakcji
Promotor - sekwencja DNA będąca sygnałem do rozpoczęcia syntezy pmRNA
pz - pary zasad, miara długości łańcucha DNA
Restryktaza - enzym restrykcyjny, bakteryjna nukleaza specyficznie rozcinająca
łańcuch DNA w ściśle określonym miejscu
RNA - ang. Ribonucleic Acid - kwas rybonukleinowy
RT-PCR - ang. Reverse Transcriptase Polymerase Chain Reaction - reakcja
polimerazowa, namnażanie DNA in vitro przy użyciu jako wzorca nici nie
DNA, lecz RNA
Starter - patrz "primer"
T - tymina
Termocycler - amplifikator DNA, mechaniczne urządzenie będące w istocie
sterowaną mikroprocesorowo cieplarką, służące do namnażania in
vitro odcinka DNA o długości wyznaczonej przez primery
hybrydyzujące z obiema niciami DNA
Teratogen - substancja powodująca zaburzenia w rozwoju płodu
Transiluminator - stolik, emitujący poprzez filtr w blacie promieniowanie UV o
długości fali około 305 – 315 nm
Transkrypt - RNA zsyntetyzowane na macierzystej nici DNA
U - uracyl
UV - ang. Ultra Violet - promieniowanie nadfioletowe
V - wolt, jednostka napięcia prądu elektrycznego
v - łac. versus - oznacza "lub" względnie "albo"
wektor - przenośnik, "koń trojański", środek za pomocą którego dokonujemy
transfekcji (przenosimy do jądra komórki obce jej DNA (np. plazmid z
wklonowanym genem)
g - mikrogram, 10-6 grama
- znak oznaczający miejsce, w którym łańcuch DNA jest rozcinany przez restryktazę
- znak oznaczający kierunek działania enzymu
* - znak używany na oznaczenie allelu (np. CYP2D6*3 oznacza trzeci allel w układzie
grupowym cytochromu)
2. Co zagraża pracownikowi laboratorium
Zagrożenia czyhające na biologa molekularnego można podzielić na zakaźne,
chemiczne i fizyczne. Zostaną one kolejno omówione.
Zagrożenia zakaźne.
Związane są z zakaźnością badanego materiału biologicznego. Podczas pracy
należy "na wszelki wypadek" traktować każdy dostarczony materiał biologiczny jako
potencjalnie zakaźny, potencjalnie bardzo groźnym błędem jest dzielenie materiału a
priori na "bezpieczny" i "niebezpieczny". Materiał genetyczny obecny w próbce
biologicznej zwykle nie jest niszczony w wysokiej temperaturze, a więc próbki które
zawierają mało białka teoretycznie można przed badaniem autoklawować, co w
praktyce wydatnie zmniejsza niebezpieczeństwo zakażenia. Jeżeli takie
postępowanie jest niemożliwe, bo próbka ulega koagulacji cieplnej, wówczas
opakowanie należy przenieść pod włączone dygestorium, założyć rękawiczki i gogle i
bardzo ostrożnie otworzyć (uwaga - czasami zawartość fiolki bywa pod ciśnieniem i
potrafi "trysnąć"!). Pobrać część odpowiednią do badań, resztę zamknąć w zgrzanym
foliowym worku i zamrozić do ewentualnej powtórki /po zakończonym badaniu spalić,
lub po otwarciu worka i fiolki wrzucić do wiadra z rozcieńczonym podchlorynem sodu
albo, w przypadku materiału w najwyższym stopniu zakaźnego - zasypać wapnem
chlorowanym/. Przed izolacją kwasów nukleinowych z próbki skrzepłej krwi lub
fragmentu tkanki często należy ją rozdrobnić, dobrze jest robić to za pomocą
narzędzi jednorazowego użytku. Podczas izolacji materiału genetycznego klasyczną
metodą (z użyciem m.in. fenolu i etanolu) zakaźność materiału znika i praca z
wyizolowanym materiałem genetycznym bakterii i wirusów jest już całkowicie
bezpieczna.
Zagrożenia chemiczne.
Najpoważniejszym zagrożeniem jest praca z odczynnikami do wybarwiania kwasów
nukleinowych (np. z bromkiem etydyny - ethidium bromide). Praktycznie każda
substancja wiążąca się z DNA ma działanie muta- lub kancerogenne. Nie należy
dopuszczać do kontaktu tych substancji ze skórą ani wdychać pyłu lub oparów.
Problemem ekologicznym jest pozbycie się resztek takiej substancji. W przypadku
bromku etydyny sposób powszechny na świecie (kolumny jonowymienne) w Polsce
jest bezużyteczny, ponieważ, jak dotąd, nie ma służb utylizujących wypełnione
kolumny. Pozostaje sposób prymitywny i mniej skuteczny, polegający na dodawaniu
łyżeczki nadmanganianu potasu na każdy litr roztworu bromku etydyny i po kilku
godzinach wlewaniu niewielkiej ilości stężonego kwasu solnego - w takim środowisku
zdecydowana większość mutagennej substancji ulega rozpadowi i można
stosunkowo mało szkodząc środowisku po całonocnej inkubacji spuścić ciecz do
kanalizacji.
Inna niebezpieczna mieszanina, odczynnik fenolowy, jest żrąca, silnie korodująca,
mutagenna i trująca, a czysty gorący fenol używany do jej wytworzenia dodatkowo
jest łatwopalny. Podczas sporządzania odczynnika fenolowego i późniejszej z nim
pracy należy zachować najwyższą ostrożność. Chloroform, używany
komplementarnie z fenolem ma działanie karcynogenne.
Sól sodowa siarczanu dodecylu (SDS, sodium dodecyl sulphate) jest bardzo silnym
detergentem w dużym stężeniu rozpuszczającym błony komórkowe, zwłaszcza
"cienkościennych" komórek nabłonka układu oddechowego. Dodatkowo jest to
substancja bardzo lekka, pylista i elektryzująca się (łatwo "odskakuje" od łopatki
podczas nabierania). Unikać wdychania pyłu! W czasie ważenia należy zakładać
maseczkę!
Obecnie odczynniki chemiczne, zwłaszcza sprowadzane z zagranicy, są dobrze
opisane. Czytajmy ulotki dołączone do odczynników, studiujmy napisy na
opakowaniach, nauczmy się międzynarodowych znaków ostrzegawczych (patrz ryc.
1.)
Zagrożenia fizyczne.
Najpoważniejsze do niedawna zagrożenie fizyczne w pracowni biologii molekularnej,
czyli promieniowanie jonizujące izotopów radioaktywnych obecnie w praktyce prawie
przestało istnieć. Nie ma już konieczności stosowania izotopów, znakowania
radioaktywne prawie całkowicie zostały wyparte przez nie radioaktywne (biotyną,
antygenem lub enzymem). Izotopy są (i pewnie jeszcze długo będą) stosowane w
"starych" laboratoriach, w których po latach owocnej pracy ciężko zarzucić rutynową,
sprawdzoną technologię i przestawić się na nową, nie radioaktywną. Należy to
uszanować, ale nowo tworzone pracownie powinny unikać stosowania izotopów od
początku swojej działalności. Szczególnie niebezpieczny jest radioaktywny fosfor,
paradoksalnie dlatego, że "krótko żyje". Zwykle w pracowni mamy naskładane całe
sterty blotów, a gdy przyjdzie wreszcie wytęskniona dostawa izotopu to pracujemy
cały dzień i jeszcze długo w nocy, a o drugiej nad ranem jakże łatwo o nieostrożność,
nieuwagę i wypadek.
Niedocenianym zagrożeniem jest promieniowanie ultrafioletowe, którego źródła w
pracowni to lampy sterylizujące podsufitowe i w laminarach oraz transiluminatory.
Należy chronić całą twarz przesłoną (a już koniecznie co najmniej oczy specjalnymi
okularami), zakładać rękawiczki. Wietrzyć pracownię z nadmiaru tworzącego się pod
wpływem UV ozonu! Rozpada się on na tlen cząsteczkowy i osławiony wolny rodnik
tlenowy (anionorodnik ponadtlenkowy).
Pracownia biologii molekularnej to nieprzeliczone mrowie aparatów podłączonych do
sieci elektrycznej, co zwiększa możliwość porażenia prądem. Zastosowanie
nowoczesnych anty porażeniowych instalacji elektrycznych (z wyłącznikami
różnicowo-prądowymi) jest wskazane, ale nie zawsze zdaje egzamin ponieważ taki
zabezpieczenia są bardzo czułe i bywa, że działają bez potrzeby, a spowodowane
odłączeniami prądu awarie są niezmiernie przykre w skutkach, a bywa, że i
niesłychanie kosztowne. Absolutne minimum bezpieczeństwa to wszystkie gniazdka
elektryczne w pracowni ze sprawnym zerowaniem (są to gniazdka z wystającymi
metalowymi "kołkami").
Środki ochrony.
Fartuch laboratoryjny to nie fason ani moda. To nasza najważniejsza obrona przed
zabrudzeniem odzieży chemikaliami i patogenami. Mniej twarzowe, ale
skuteczniejsze są fartuchy wiązane z tyłu. W czasie przebywania w laboratorium ręce
płuczemy dosłownie co chwila, ale mydła używamy tylko przed posiłkiem i przed
wyjściem z pracy. Jeżeli ktoś "nie może" myć rąk samą wodą, to niech używa kremu
natłuszczającego, bo odtłuszczona ludzka skóra to istne sito... Pracujemy w
rękawiczkach, to chroni nas przed badanym materiałem i ... badany materiał
(zwłaszcza RNA) przed nami. Wyciąg (dygestorium) jest po to, aby chronić
pracownika przed robotą (próbkami). Komora z laminarnym przepływem powietrza
jest po to, aby chronić robotę (tzn. próbki, zwłaszcza podczas nastawiania testu
PCR) przed pracownikiem (zanieczyszczenie). Komora sterylna (glovesbox) służy do
bezpiecznej pracy z wyjątkowo niebezpiecznym materiałem, chroni więc skutecznie
"obie strony".
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z powyższego
wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na konsultację.
1. Wszystko, co biologiczne, i tak wcześniej lub później zgnije, a na śmietniku leżą i
w kanalizacji pływają wszelkie możliwe odpadki. Czy w związku z tym resztki
przebadanych próbek śmiało możemy wyrzucić na śmietnik lub wylać do kanalizacji?
2. Wirus, biologicznie rzecz biorąc, to, z niewielką przesadą, prawie czysty materiał
genetyczny. Czy to znaczy, ze wyizolowany wirusowy DNA lub RNA też jest
zakaźny?
3. Bromek etydyny jest szkodliwy. Ale są znane także inne, nowocześniejsze i
znacznie czulsze barwniki do kwasów nukleinowych. Czy one też są szkodliwe?
4. SDS w substancji to okropne paskudztwo. A w roztworze, kilku- lub
kilkunastoprocentowy?
5. Czy "ciernista koniczynka" to znak ostrzegający przed radioaktywnością?
6. Nowe technologie znakowania prób /sond/ molekularnych są może i dobre, ale
jeszcze długo nie zastąpią izotopów fosforu i siarki, bo radioaktywne znakowania są
tańsze i czulsze, nieprawdaż?
7. Ozon to zdrowy, orzeźwiający gaz który na wakacjach czujemy w powietrzu po
burzy. Jest więc oczywistością, że dobrze działa na nasze zdrowie także wtedy, gdy
codziennie wdychamy go w naszym laboratorium, prawda?
8. Prawdziwa higiena jest wtedy, gdy nie żałujemy mydła, czy z tego wynika, że
mycie rąk samą wodą nie ma żadnego sensu?
9. Do czego w pracowni biologii molekularnej służą dygestorium, laminar i
glovesbox?
3. Materiał genetyczny człowieka.
W chwili pisania tych słów zastosowanie diagnostyczne w medycynie człowieka
znalazły dwa rodzaje DNA, pochodzący z jądra komórkowego (zwany także DNA
genomowym) oraz pochodzący z mitochondriów. W tym miejscu należy się
lingwistyczna dygresja: DNA to kwas, czyli rodzaj męski. Studenci jednak często
mówią o nim w rodzaju nijakim, „to DNA”. Jest to błąd gramatyczny, ale mnie on się
podoba. W końcu DNA jest bezpłciowy (bezpłciowe!) i dobrze służy obu płciom, a
więc ta gramatycznie błędna forma jest za to bardzo politycznie poprawna.
Ludzki genomowy DNA w pojedynczym jądrze komórkowym ma łączną długość
około 3 miliardów nukleotydów i waży około 7 pg. Wypreparowany z jednej gamety
utworzyłby helisę o całkowitej długości około 1 metra (a po jej rozwinięciu i
naciągnięciu nitek do granic fizycznej wytrzymałości około półtora metra). Około 95%
tego DNA nie pełni żadnej znanej nam funkcji, istnieją hipotezy że jest to regulator
aktywności genów, "wypełniacz" chromosomów, pamiątka po prastarych
przemianach ewolucyjnych a nawet... plan ewolucyjnych zmian które dopiero zajdą w
przyszłości. Kodująca część genomu człowieka ma więc długość zaledwie około 150
mpz i zawiera ponad 30.000 genów. Ludzki DNA podzielony jest na 46 "kawałków",
każdy odcinek tworzy jeden chromosom, największy z nich (nr 1) jest około sześć
razy większy od każdego z najkrótszych (21, 22 i Y).
W porównaniu z DNA genomowym, DNA mitochondrialne na pierwszy rzut oka
wygląda bardzo niepozornie, ponieważ obejmuje tylko około 16.000 pz. Jeżeli jednak
uwzględnimy, że w komórce jest tylko jedno jądro ze 150 milionami kodujących
zasad, natomiast kilkaset, a nawet więcej, mitochondriów, to niespodziewanie okaże
się, że komórkowy kodujący DNA mitochondrialny to równoważnik wagowy ponad
10% kodującego DNA genomowego.
W każdej komórce organizmu ludzkiego posiadającej jądro komórkowe możemy
znaleźć dwa rodzaje materiału genetycznego: DNA, czyli kwas
deoksyrybonukleinowy (charakteryzujący się zdolnością do tworzenia regularnej
helikoidalnej struktury przestrzennej, cukrem deoksyrybozą i jednopierścieniowymi
zasadami pirymidynowymi tyminą i cytozyną) oraz RNA, czyli kwas rybonukleinowy,
znamienny długimi odcinkami jednoniciowości, cukrem rybozą i pirymidynami
uracylem i cytozyną. Oba kwasy zawierają takie same dwupierścieniowe zasady
purynowe, adeninę i guaninę. Guanina ma zdolność do łączenia się z cytozyną
trzema wiązaniami wodorowymi, a adenina dwoma takimi wiązaniami z tyminą (lub
uracylem). Uwaga: w piśmiennictwie używane są czasami inne chemiczne nazwy
związków wyżej wymienionych zasad: nukleozydy (zasady plus cukier), np. tymidyna,
cytydyna, adenozyna i guanozyna, a czasami nawet precyzyjne określenia w rodzaju
"nukleotydy" (zasada plus cukier plus reszta lub reszty fosforanowe), np. fosforan
deoksyguanidyny, trójfosforan deoksyguanidyny itp.
Kwas deoksyrybonukleinowy ludzkiej komórki prawie zawsze występuje w swojej
"naturalnej" postaci, którą jest dwuniciowa prawoskrętna helisa typu B. Oba łańcuchy
helisy są przeciwbieżne ( "odwrotnie spolaryzowane" albo "antyrównoległe"), tam,
gdzie jeden z nich ma koniec 5', drugi ma 3' i odwrotnie. Jest to bardzo istotne,
niezrozumienie tego faktu prowadzi do pospolitego w podręcznikach genetyki błędu,
polegającego na podawaniu informacji, że sekwencją komplementarną do np.
sekwencji 5'AATGGTAACA3' jest sekwencja TTACCATTGT. Jest to oczywiście
nieprawda, ponieważ końce tej rzekomo komplementarnej sekwencji są odwrotne, a
więc prawdziwa sekwencja komplementarna (po uporządkowaniu końców) będzie
wyglądać następująco: 5'TGTTACCATT3'. Powyższy wywód nie jest wcale, jak by
się mogło na pierwszy rzut oka wydawać, nieistotnym mędrkowaniem, bez jego
dogłębnego zrozumienia nie jest możliwe samodzielne konstruowanie primerów
(starterów) niezbędnych do przeprowadzania reakcji PCR - patrz rozdział 9.
DNA ulega odwracalnej denaturacji cieplnej (topnieniu) w tym wyższej temperaturze,
im większy odsetek zasad w topionym łańcuchu to pary G-C. Alkalizacja środowiska i
dodatek niektórych substancji (np. mocznika, siarczanu dekstranu, glicerolu lub
formamidu; uwaga: najczęściej stosowany formamid jest teratogenem!) wydatnie
obniżają temperaturę topnienia, zwaną także często temperaturą hybrydyzacji (DNA
ogrzewany się topi, schładzany - hybrydyzuje). Trzeci używany termin, denaturacja,
nie jest najszczęśliwszy, ponieważ określenie to oznacza także w biochemii
nieodwracalne uszkodzenie, podczas gdy topnienie nie uszkadza helisy DNA.
Normalny (najczęściej spotykany) układ organizacji procesów życiowych żywej
komórki to DNA - RNA - białko. Początek syntezy RNA (kwasu rybonukleinowego) w
jądrze ludzkiej komórki może być rozpoczęty na wiele sposobów, najczęstszy z nich
polega na wykorzystaniu promotorowej sekwencji (boksu, czyli kasety) TATA,
położonej około 25 pz przed miejscem rozpoczęcia syntezy RNA. Inna nazwa kasety
TATA to Hogness Box, sekwencja ta może być znacznie dłuższa i najczęściej jest
oskrzydlona sekwencjami bogatymi w G i C. Początek syntezy białka jest z reguły
rozpoczynany od kodonu ATG, kodującego metioninę, i dlatego ten aminokwas jest
zwykle pierwszym aminokwasem bardzo wielu rodzajów ludzkiego białka. Ludzkie
geny są podzielone na eksony (exon, expressed region) i introny (intron, intervented
region). Podczas syntezy pmRNA (prematured RNA, czyli surowego transkryptu)
przepisywane są i eksony, i introny, a następnie w czasie dojrzewania mRNA
(messenger RNA) introny są wycinane, często z wykorzystaniem autokatalitycznych
właściwości cząsteczki RNA. Początek intronu jest zwykle rozpoznawany po
sekwencji GT, koniec po sekwencji AG, poprzedzonej ciągiem bogatym w pirymidyny
(T i C). Ostatnio ewolucjoniści powszechnie uważają, że geny poprzedzielane
intronami oraz RNA są ewolucyjnie wcześniejsze od genów bez intronów i od
powstania DNA.
Transkrypcja ludzkiego genu może być zakończona na szereg różnych sposobów, z
których najpowszechniejszy polega na syntezie sekwencji
AAGCGCCGxxxxxCGGCGCUUn - proszę zwrócić uwagę na palindromiczną
komplementarność sekwencji tych zasad, powoduje ona samorzutne uformowanie
się struktury "pętelki" względnie "spinki do włosów", a szereg Un powoduje łatwe
oderwanie transkryptu od macierzystej nici DNA.
Obecnie czynione są intensywne wysiłki zaprzęgnięcia systemu replikacyjnego do
użytecznej dla biologa molekularnego pracy, polegającej na amplifikacji materiału
genetycznego bez wykorzystania klonowania genów lub reakcji PCR.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z powyższego
wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na konsultację.
1. Czy genom ludzki jest modelowym przykładem bardzo oszczędnej i celowej
organizacji biologicznej, w której nie ma nic zbędnego i niepotrzebnego?
2. Czy DNA mitochondrialny to zaledwie bardzo drobny, wręcz nieistotny odsetek
całego DNA obecnego w ludzkiej komórce? A właściwie to ile tego DNA jest w
jednym jądrze?
3. Czym się różni DNA od RNA?
4. Czy adenina może wchodzić w skład RNA?
5. Jaki ciąg nukleotydów jest komplementarny do sekwencji 5'TGCAATGGAC3'?
6. Jak obniżyć temperaturę hybrydyzacji DNA?
7. Jaka jest sekwencja głównego promotora i głównego terminatora syntezy mRNA w
ludzkich komórkach?
8. Co to jest ekson? A intron?
9. Jak można zwielokrotnić /namnożyć/ posiadaną przez nas niewielką ilość DNA?
4. Izolacja DNA i RNA
Jednym z niewielu truizmów, wartych ciągłego powtarzania jest stwierdzenie, że
wszelka praca z materiałem genetycznym człowieka bezwzględnie wymaga przed jej
rozpoczęciem... posiadania, a więc wyizolowania tego materiału. Od tego zdawałoby
się mało istotnego, wstępnego etapu jakże często zależy końcowy spektakularny
sukces eksperymentu. Wbrew pozorom, izolacja materiału genetycznego wysokiej
jakości nie jest wcale prosta.
DNA występuje w ludzkich komórkach głównie w dwu organellach : jądrze i w
mitochondriach. Do wyizolowania DNA mitochondrialnego wcale nie trzeba najpierw
izolować mitochondriów, preparuje się on "przy okazji", jako spora, kilkuprocentowa
domieszka w czasie izolacji DNA jądrowego /genomowego/.
DNA genomowe występuje w komórkach jądrzastych, bezskuteczna byłaby więc
próba izolacji DNA np. z odpłukanej masy erytrocytarnej, aczkolwiek pewne
niewielkie ilości DNA można uzyskać i z tego źródła, pochodzi on z mitochondriów
oraz z niedojrzałych, jeszcze jądrzastych krwinek czerwonych /retikulocytów/, w
świeżo pobranej krwi średnio co setny erytrocyt ma jeszcze przez pewien czas jądro
komórkowe.
DNA można izolować z praktycznie każdej ludzkiej tkanki, aczkolwiek z niektórych
tkanek nie warto tego robić, z różnych powodów. I tak na przykład z tkanki płucnej
uzyskuje się "brudne", ciemne preparaty z zawiesiną koloidalnych cząsteczek kurzu.
Tkanka tłuszczowa jest trudna do homogenizacji, ponieważ "maże się", natomiast
tkanka kostna jest bardzo twarda. Wątroba zawiera nukleazy, które degradują DNA,
a śledziona duże ilości hemu /inhibitora reakcji PCR/. Niektóre komórki /np. plemniki,
niektóre guzy nowotworowe, tkanki z formaliny/ źle się trawią proteinazą K, trzeba
dodawać jej bardzo dużo i aktywować odczynnikiem tiolowym /DTT/. Wybrane tkanki
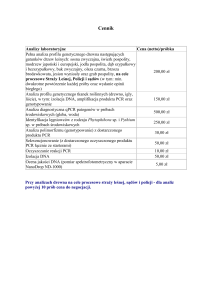
ciała ludzkiego jako źródło izolacji DNA są wymienione w poniższej tabeli.
Tkanka g DNA/1 g tkanki Tkanka g DNA/1 g tkanki
Krew
30
Ślinianka 270
Mózg
125
Serce
270
Mięsień 200
Wątroba 750
Tarczyca 250
Gonada 1950
Z tabeli wynika, że najlepszym źródłem izolacji DNA ze zwłok ludzkich są bez
wątpienia gonady /jajniki i jądra/, i to niezależnie od wieku zmarłej osoby. W
przypadku osób żywych najwygodniejszym, a więc najczęściej używanym materiałem
do izolacji jest krew lub ślina, a ściślej wymaz nabłonków z jamy ustnej z domieszką
śliny, najczęściej pobierany specjalną bibułową „skrobaczką”.
Izolacja DNA może być przeprowadzona na bardzo wiele sposobów, a metody
stosowane w laboratoriach prawie zawsze są kompilacją możliwie dużej liczby
technik źródłowych. Wykaz technik źródłowych jest przedstawiony na poniższym
schemacie.
KOMÓRKA
JĄDRO KOMÓRKOWE
BIAŁKO
- strawienie proteazą
- wysalanie
- ekstrakcja fenolowa
- wytrącanie chloroformem
DNA
- ultrawirowanie
- jonowymiana
- mikrosączenie
- elektroforeza preparatywna
- jonowymiana
- absorpcja
- wiązanie z przeciwciałem
- absorpcja na silikonie
- formowanie potrójnej helisy
- wiązanie z przeciwciałem
- strącanie sperminą
-wytrącanie alkoholem
W tej chwili najbardziej rozpowszechnione techniki izolacji DNA w laboratoriach
biologii molekularnej to metoda fenolowa i metoda solna /"nietoksyczna"/.
Jeszcze lepsze wyniki osiągnąć można łącząc elementy obu tych metod.
Wschodzącą gwiazdą wśród technik preparacji DNA jest metoda opierająca się
na wykorzystaniu wiązania DNA przez pył silikonowy (krzemowy lub szklany) i
następnie elucję (poprzez zmianę składu buforu, jego stężenia lub pH)
związanego z pyłem DNA. W zastosowaniach medyczno - sądowych często
stosuje się technikę cheleksową Bardzo dobry preparat DNA powinien mieć dużą
lepkość, stężenie około 1mg/1ml, czystość spektrofotometryczną (iloraz
absorbancji mierzonej przy A260nm/A280nm) zawartą pomiędzy wartością 1,6 a 1,8 a
ponadto brak inhibitorów reakcji PCR oraz dużą trwałość, która umożliwia
wieloletnie przechowywanie takiego preparatu.
RNA izoluje się do badań wówczas, gdy organizm który badamy nie zawiera DNA
(np. jest retrowirusem), względnie wtedy, gdy nie interesuje nas czy dany gen jest
obecny w genomie badanego organizmu, lecz to, czy ten gen jest aktywny, co
przejawia się poprzez wytwarzanie odpowiedniego mRNA. RNA można izolować
całościowo (za pomocą kwaśnego odczynnika fenolowego zwanego Trizolem) lub
w postaci mRNA, wykorzystuje się wówczas fakt, że każda cząsteczka mRNA
posiada strukturę poliA. Do izolacji używa się oligonukleotydów poliT, związanych
z nośnikiem (celulozą, kulkami magnetycznymi itp).
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Czym preparacja DNA mitochondrialnego różni się od preparacji DNA
genomowego?
2. Czy z erytrocytów można wyizolować DNA? Z leukocytów? Z płytek krwi? A z
surowicy?
3. Których tkanek nie warto /jeżeli mamy wybór/ brać do izolacji ludzkiego DNA?
4. Która tkanka ze zwłok człowieka jest najodpowiedniejsza do izolacji DNA?
5. Jak wypreparować DNA z tkanki, która źle się trawi proteinazą K?
6. Jakie drogi izolacji DNA są możliwe do zastosowania?
7. Jakie metody izolacji DNA są najbardziej rozpowszechnione?
8. Jakimi parametrami charakteryzuje się dobry preparat DNA?
9. Jak wyizolować całościowy RNA? A jak jego najważniejszą frakcję, mRNA?
5. Enzymy restrykcyjne.
Enzymy te, zwane skrótowo restryktazami, czynnościowo są bakteryjnym
"układem immunologicznym" - chronią przed zakażeniem wirusowym poprzez
rozcinanie materiału genetycznego wirusa w krótkim momencie pomiędzy
wstrzyknięciem materiału genetycznego wirusa a przestawieniem metabolizmu
zaatakowanego mikroorganizmu na potrzeby agresora.
Terminologia restryktaz zwykle jest odzwierciedleniem łacińskiej nazwy bakterii,
pierwsza litera pochodzi od rodzaju, dwie następne - od gatunku. I tak restryktaza
Eco pochodzi z Escherichia coli, Alu z Anthrobacter luteus, Pst z Providencia
stuarti itd.
Restryktazy rozcinają DNA mniej lub bardziej swoiście, rozpoznając przed
cięciem określoną sekwencję nukleotydów. Rozpoznawany odcinek może być
różnej długości, od 4 nukleotydów (restryktaza AluI, 5'AG CT3') do 32 - 33
nukleotydów (restryktaza AloI, 5' N7GAACN6TCCN12-13 3'). Sekwencja
rozpoznawana może być ściśle określona (restryktaza Bsp143l, 5' GATC3') lub z
dopuszczalnymi niewielkimi (restryktaza MvaI, 5'CC AvTGG3'), sporymi
(restryktaza SduI, 5'GGvAvTGCCvAvT C3') lub dużymi wariancjami (restryktaza
Eco81l, 5'CC TNAGG3').
DNA może zostać przecięte równo (niczym sznurek spleciony z dwu włókien
przecięty nożem), czyni to np. restryktaza SmiI, 5'ATTT AAAT3' lub z
przesunięciem miejsca cięcia na obu łańcuchach o jeden /restryktaza MvaI,
pierwszy łańcuch 5'CC AvTGG3', drugi łańcuch 5'CC TvAGG3'/, dwa /restryktaza
Bsp119l, pierwszy łańcuch 5'TT CGAA3', drugi łańcuch 5'TT CGAA3'/, trzy
/restryktaza Eco81l, pierwszy łańcuch 5'CC TNAGG3', drugi łańcuch 5'CC
TNAGG3'/, cztery /restryktaza CfrI, pierwszy łańcuch 5'Py GGCCPu3', drugi
łańcuch 5'Py GGCCPu3'/ a nawet pięć nukleotydów /restryktaza Eco91l, pierwszy
łańcuch 5'G GTNACC3', drugi łańcuch 5'G GTNACC3'/. W przypadku równego
cięcia mówimy o "tępych" a w przypadku nierównego o "lepkich" końcach
rozciętego łańcucha DNA. Pojawianie się lepkich końców jest bardzo użyteczne w
manipulacjach genetycznych, ponieważ możemy sztucznie łączyć ze sobą obce
fragmenty DNA, cięte tą samą restryktazą, fragmenty te na zasadzie hybrydyzacji
przytrzymane zostaną przy sobie na krótki czas potrzebny do zadziałania ligazy enzymu naprawczego który łączy przerwane łańcuchy DNA.
Znane są restryktazy które tną wewnątrz rozpoznawanej sekwencji DNA /np.
Eco105l, 5'TAC GTA3'/, na zewnątrz tej sekwencji w bliskiej /restryktaza
Mva1269l, 5'GAATGCN 3'/ odległości, daleko od niej /restryktaza HphI,
5'GGTGAN8 / lub dwukrotnie, po jej obu stronach /PpiI, 5' N7GAACN5CTCN13 /.
Powstaje pytanie, skąd restryktaza bakteryjna "wie" które DNA jest "obce" a które
"własne", a więc nie powinno być cięte? Mechanizmem ochronnym może być
metylacja własnego DNA, wiele restryktaz występuje w parze z odpowiednią
metylazą /np. restryktaza PstI, 5'CTGCA G3' oraz metylaza PstI,
5'CTGCA(CH3)G3'/. Od tej reguły są jednak wyjątki, i tak np. restryktaza DpnI
rozcina wyłącznie zmetylowany łańcuch DNA 5'GA(CH3) TC3', oszczędzając
niezmetylowany. Wydaje się więc, że najpewniejszym mechanizmem ochronnym
jest po prostu taka sekwencja nukleotydów rozpoznawana przez restryktazę,
która w ogóle nie występuje w DNA danej bakterii, natomiast mechanizm
metylacji gra główną rolę w wyciszaniu zbędnych genów.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Jaka jest biologiczna funkcja enzymów restrykcyjnych? Czy restryktazy
występują u kręgowców?
2. Jak tworzy się nazwy restryktaz?
3. Co to jest sekwencja rozpoznawana przez restryktazę? Jakie mogą być rodzaje
takiej sekwencji?
4. Co to są "lepkie końce" i do czego je można wykorzystać?
5. Gdzie może leżeć miejsce cięcia względem sekwencji rozpoznawalnej przez
restryktazę?
6. Jak bakteria chroni się przed pocięciem własnego DNA?
6. Elektroforeza i detekcja DNA i RNA
Kwasy nukleinowe można analizować za pomocą elektroforezy, czyli wędrówki
cząsteczek w polu elektrycznym prądu stałego (dotyczy to krótkich łańcuchów, od
30 do 20000 pz) lub prądu zmiennego (łańcuchy do 1,5 mpz), ale nie prądu
przemiennego.
Szybkość wędrówki cząsteczki zależy wprost proporcjonalnie od jej ładunku (a
ten z kolei od pH środowiska) i od siły pola elektrycznego wyrażanej zazwyczaj w
woltach na centymetr nośnika, oraz odwrotnie proporcjonalnie od wielkości
cząsteczki (a ściślej od jej kształtu) i od oporu, stawianego przez nośnik (opór ten
rośnie wraz ze wzrostem lepkości oraz ze zmniejszaniem się porów nośnika).
Parametrami powyższymi można manipulować, ale w umiarkowanych granicach,
np. ekstremalne wartości pH mogą uszkodzić rozdzielaną substancję, nadmierne
zwiększanie napięcia powoduje przegrzewanie się nośnika, a zmniejszanie
lepkości i powiększanie porów powoduje wzrost konwekcyjnych prądów w buforze
oraz zanik efektu sita molekularnego.
Elektroforeza kwasów nukleinowych obecnie przeprowadzana jest głównie na
żelach agarozowym i akryloamidowym oraz w tzw. płynnych (nisko
spolimeryzowanych) żelach akryloamidowych w kapilarach. Elektroforeza
akryloamidowa jest powszechnie, chociaż niesłusznie uważana za bardziej
precyzyjną od agarozowej oraz (słusznie) za tańszą. Zaletami żelu
poliakryloamidowego są niskie koszta oraz możliwość wybarwiania rozdzielonych
frakcji DNA poprzez srebrzenie, które daje wyraźne, widoczne gołym okiem i
trwałe obrazy. Wady, to trudność w opanowaniu przez osoby początkujące
techniki polimeryzacji akryloamidu, jednorazowe użycie żelu, silna
neurotoksyczność monomerów oraz słabsze niż w przypadku żelu agarozowego
wybarwianie DNA przy pomocy bromku etydyny. Zaletami agarozy są łatwość
sporządzania żelu, możliwość jego wielokrotnego wykorzystania i silne
wybarwianie DNA z bromkiem etydyny, natomiast wady to stosunkowo wysoki
koszt i brak możliwości srebrzenia.
Wybarwianie DNA elektroforetycznie rozdzielonego na żelu może być
przeprowadzane za pomocą bromku etydyny lub innego, podobnego barwnika
/np. SYBR Gold, który jest o wiele czulszy i mniej ekologicznie szkodliwy, lecz
znacznie droższy/, natomiast w przypadku elektroforezy kapilarnej szczególnie
popularne jest wielokolorowe barwienie fluorescencyjne, wykorzystujące
wzbudzoną laserem fluorescencję wbudowanych w łańcuch DNA fluorochromów.
Coraz rzadziej jest stosowana detekcja poprzez srebrzenie żeli
poliakryloamidowych.
Przy użyciu bromku etydyny RNA wybarwia się znacznie słabiej niż DNA, i
dlatego w ostatnim okresie coraz powszechniej stosowane są specjalne barwniki
do barwienia RNA, np. "Radiant Red RNA stain" albo "SYBR Green II RNA gel
stain".
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Jaki rodzaj prądu elektrycznego można zastosować w elektroforezie kwasów
nukleinowych?
2. Od czego zależy szybkość wędrówki rozdzielanej substancji?
3. Na jakich podłożach rozdziela się kwasy nukleinowe?
4. Wymień zalety i wady żeli - poliakryloamidowego i agarozowego.
5. Jak wybarwić żel w celu uwidocznienia rozdzielonych frakcji DNA? Lub RNA?
7. Blotting i hybrydyzacja
Po zakończeniu elektroforezy żel, zwłaszcza agarozowy, można wysuszyć na
specjalnym próżniowym stoliku i przeprowadzić bezpośrednio na żelu hybrydyzację,
ale jest to trudny i kapryśny zabieg, i dlatego hybrydyzacja zwykle jest poprzedzona
przeniesieniem frakcji rozdzielonego kwasu nukleinowego z żelowego placka na
arkusz folii. Zabieg ten nosi nazwę blotingu (transferu, plamienia, stemplowania). Na
początku używano folii z azotanu celulozy, ale ze względu na słabe wiązanie kwasów
nukleinowych i niebezpieczeństwo zapłonu (azotan celulozy jest głównym
składnikiem prochu strzelniczego) obecnie prawie wyłącznie stosuje się folie
nylonowe. Bloting może być kapilarny, próżniowy, elektryczny mokry lub elektryczny
półsuchy (popularny kiedyś bloting odśrodkowy został już zaniechany). Bloting
kapilarny fragmentów DNA został wymyślony w 1975 roku przez dr Southerna z
Oxfordu i dlatego nosi nazwę "southern blotting". Nazwa ta dała powód do
językowych krotochwili, i tak transfer RNA pospolicie nosi nazwę "northern blotting",
transfer białek "western blotting" a transfer białek po elektroforezie dwukierunkowej
nazywany bywa "eastern blottingiem".
Po zakończeniu blotingu należy dać przeniesionemu materiałowi genetycznemu czas
na trwałe związanie się z folią, w tym celu należy folię wysuszyć i pozostawić w
spokoju w temperaturze pokojowej na dwa tygodnie. Jeżeli nie można czekać, folię
można zapiec przez 2 godziny w +80o C, względnie przez 3 minuty na
transiluminatorze albo przez kilkanaście sekund używając specjalnego
ultrafioletowego pieca do zapiekania.
Zapieczoną folię można hybrydyzować. Przebieg hybrydyzacji przedstawia rysunek.
Hybrydyzacja polega na połączeniu jednoniciowego kwasu nukleinowego na blocie
(jednoniciowość zapewniamy poprzez użycie RNA lub prowadzenie blotingu w
alkalicznym środowisku) z sondą (próbą) molekularną którą jest jednoniciowy
fragment kwasu nukleinowego o sekwencji komplementarnej do sekwencji, którą
chcemy wykryć i o długości zapewniającej wiązanie się tylko z tą właśnie sekwencją.
Pierwszy udany zabieg hybrydyzacji DNA-RNA wykonali Hall i Spiegelman w 1961
roku. Obecnie jako hybrydyzującej próby prawie wyłącznie używa się sztucznie
zsyntetyzowanych łańcuchów oligonukleotydowych, najczęściej wyznakowanych już
w trakcie ich syntezy (np. w testach typu "ASO Dot Blot").
W czasie przeprowadzania hybrydyzacji musimy zadbać o to, aby odbyła się ona we
właściwej temperaturze. Temperaturę tę wstępnie ustala się korzystając z różnych
wzorów, np. ze wzoru t = 69,3oC + 0,41[%G+C] - 650/n (n oznacza ilość par zasad w
hybrydyzującej części próby molekularnej), ale zwykle jest to tylko ustalenie wstępne
i ostateczną temperaturę ustala się metodą prób i błędów. UWAGA: tego wzoru nie
należy stosować do obliczania temperatury hybrydyzacji primera w czasie
przeprowadzania reakcji PCR - do tego celu służą inne wzory, które zostaną podane
w rozdziale o przeprowadzaniu reakcji PCR. Jednym ze składników mieszaniny
hybrydyzacyjnej jest bardzo często roztwór Denhardta, drugim zaś substancja
blokująca folię w miejscach, w których hybrydyzacja nie zachodzi (bez niej próba
łączyłaby się z folią i tło byłoby bardzo ciemne). Substancją tą zwykle jest bardzo
czysta kazeina, ale można w tym celu użyć także... zwykłego odtłuszczonego mleka
w proszku!
Po zakończeniu hybrydyzacji należy uwidocznić połączenie kwasu nukleinowego z
próbą (sondą) molekularną. Można tego dokonać za pomocą autoradiografii (przy
użyciu radioaktywnych prób) albo bez użycia izotopów, metodą
chemiluminescencyjną albo wykorzystując reakcję barwną enzymu, połączonego
bezpośrednio lub pośrednio z sondą.
Technika radioaktywna jeszcze niedawno była bardzo popularna, lecz obecnie z
powodów BHP i ekologicznych bardzo szybko traci popularność na korzyść technik
nie izotopowych.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z powyższego
wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na konsultację.
1. Jaką czynność należy wykonać po zakończeniu elektroforezy, przed
hybrydyzacją?
2. Jakie znasz rodzaje transferu (blotingu)?
3. Co to jest zapiekanie folii (blotu) i jak można je wykonać?
4. Jak wyznaczyć właściwą temperaturę hybrydyzacji?
5. Po co blokuje się folię w czasie hybrydyzacji? Jak to zrobić?
6. Jak uwidocznić miejsca w których na blocie zaszła hybrydyzacja?
8. Odwrotna transkrypcja
Technikę odwrotnej transkrypcji stosuje się podczas pracy z RNA. Wykorzystuje się
tu zdolność niektórych polimeraz do syntezy potomnej nici DNA na macierzystej nici
RNA. DNA wytworzone za pomocą tej techniki nosi nazwę cDNA i może być badane
technikami badania DNA (np. klonowania, PCR, restrykcji enzymatycznej lub
hybrydyzacji). Obecnie do przeprowadzania reakcji odwrotnej transkrypcji
wykorzystuje się szereg enzymów, których właściwości ujmuje poniższa tabela.
Nazwa i pochodzenie enzymu
Tth Polymerase z Thermus
thermophilus
Jon
Uwagi
aktywujący
Termostabilna odwrotna transkryptaza,
Mn++
która z jonami magnezu wykazuje
aktywność zwyczajnej polimerazy DNA
MMuLV Rewerse Transkryptase
z Moloney Murine
Mg++
LeucemiaVirus
AMV Reverse Transkryptase z
Mg++
Avian Myeloblastosis Virus
Cth Polymerase Klenow
Fragment z Carbohydrothermus Mg++
hydrogenoformans
Obecnie najpowszechniej stosowana
odwrotna transkryptaza
Coraz powszechniej stosowana
odwrotna transkryptaza
Stosowana w mieszaninie z Taq
polimerazą do jednostopniowej reakcji
RT-PCR
Ostatnia z polimeraz wymienionych w tabeli jest o tyle ciekawa, że może być
zastosowana do jednostopniowej reakcji RT-PCR. Typowa reakcja RT-PCR
składa się z dwu etapów: odwrotnej transkrypcji polegającej na uzyskaniu cDNA i
właściwej reakcji PCR przeprowadzonej z wykorzystaniem jako wzorca
uzyskanego cDNA. Przy użyciu termostabilnych fragmentów Klenow'a Cth
polimerazy zmieszanych z Taq polimerazą można od razu przystąpić do reakcji
PCR, cDNA będzie wówczas produkowane w postępie arytmetycznym a
następnie amplifikowane w postępie geometrycznym.
Reakcję RT-PCR stosuje się najczęściej wtedy, gdy chcemy się przekonać nie
tyle o tym, czy w genomie badanego organizmu dany gen jest, ale o tym, czy ten
gen jest aktywny (czy działa, czyli czy wytwarzany jest odpowiedni mRNA).
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Jak w laboratorium przepisać informację zawartą w nici RNA na nić DNA?
2. Jakie enzymy stosuje się do tego celu?
3. Czy reakcję PCR można przeprowadzić używając jako wzorzec nie DNA, ale
RNA?
4. Kiedy stosuje się reakcję RT-PCR?
9. Reakcja PCR
Reakcja PCR obecnie jest uważana za najważniejsze narzędzie w pracowni biologa
molekularnego. Do przeprowadzenia reakcji potrzebne jest odpowiednie
oprzyrządowanie (patrz koniec tego rozdziału), zestaw odczynników który można
kupić w wielu firmach oraz primery (startery) czyli dwa oligonukleotydy których
syntezę można zamówić w dowolnej, wyspecjalizowanej firmie biotechnologicznej.
Samodzielne konstruowanie primerów opiera się na następujących zasadach:
1. Z banku genów uzyskujemy sekwencję genu.
2. Wybieramy taki fragment genu, który ma długość od 21 do 27 nukleotydów,
rekomendowane jest 24, stosunek zasad C+G do A+T powinien być jak
najbliższy 50%. Przepisujemy ten fragment i nadajemy mu zrozumiałą dla nas
krótką nazwę z dodatkiem na końcu litery F ("forward"). Przykładowo, dla genu
amylazy nazwa ta może brzmieć „AMYF”.
3. W odległości od 150 do 450 nukleotydów od końca primera F szukamy
odcinka o takiej samej długości i takim samym procentowym stosunku zasad
GC do AT, jeżeli możliwe, to zaczynającego się od litery G lub C (względnie
dwu takich liter, ale nie więcej). Przepisujemy go "od końca" i
"komplementarnie", nazywając tak samo jak primer F, ale z dodatkiem na
końcu litery R ("reverse"). Przykład: wybrana według powyższych wskazówek
sekwencja genu amylazy 5’GTG CAC TTA GGT CAT GCA TTC TGC3’ ,
przetłumaczona na zapis primeru R będzie miała postać „AMYR 5'GCA GAA
TGC ATG ACC TAA GTG CAC 3'”.
4. Sprawdzamy, czy ostatnie trzy (lub więcej) nukleotydy każdego z primerów nie
są komplementarne do czytanej wspak sekwencji drugiego primera. Przykład:
w primerze F nie może w żadnym miejscu być sekwencji GTG, GTGC,
GTGCA itd.
5. Jeżeli primery konstruujemy nie do reakcji PCR, ale RT-PCR, musimy
sprawdzić czy wybrane przez nas startery nie leżą w sekwencji intronowej
oraz czy pomiędzy nimi nie znajduje się intron.
Schemat reakcji PCR jest przedstawiony na poniższej ilustracji (po kliknięciu rysunku
otwiera się powiększenie).
zielony - primer F
czerwony - primer R
kolejne strzałki - numery 110
CYKL I
CYKL II
CYKL III
1 - macierzysty dwuniciowy DNA
2 - pierwsza denaturacja (rozdzielenie na dwie nici)
3 - wiązanie z primerami
4 - synteza nowych nici, zaczynająca się od odpowiedniego primera
5 - druga denaturacja
6 - wiązanie produktów pierwszego cyklu z primerami
7 - synteza w drugim cyklu
8 - trzecia denaturacja
9 - wiązanie z primerami
10 - synteza specyficznych produktów reakcji
Do przedstawionego schematu można dodać następujące uwagi:
1. Primery (startery) przyłączają się do obu nici, każdy z nich do innej i łącznie
wyznaczają długość dwuniciowego fragmentu DNA, który będzie
amplifikowany.
2. Synteza DNA biegnie od końca 3' primera, a ponieważ łańcuchy DNA są
przeciwbieżne, więc synteza nowych łańcuchów na obu niciach biegnie
pozornie w odwrotne strony.
3. W drugim cyklu reakcji PCR powstają niespecyficzne ("za długie") łańcuchy,
których ilość przyrasta w kolejnych cyklach w postępie arytmetycznym.
4. W trzecim i następnych cyklach reakcja PCR tworzy specyficzne łańcuchy, o
długości zdeterminowanej przez primery, a ich ilość przyrasta w postępie
geometrycznym.
5. Prawdopodobieństwo przyłączenia się primerów do nowo zsyntetyzowanego
DNA, a nie do DNA macierzystego jest tym większe, im więcej zaszło cykli.
Taka zależność ma znaczenie praktyczne, ponieważ termiczna denaturacja
krótszych fragmentów DNA jest łatwiejsza. Temperatura topnienia
("denaturacji") w miarę upływu czasu może być więc obniżana. Można w ten
sposób zwiększyć trwałość polimerazy, termostabilnej z nazwy, ale w
rzeczywistości posiadającej ograniczoną wytrzymałość na temperaturę
przekraczającą +80oC.
6. Temperatura hybrydyzacji (ang. annealing) zależy głównie od budowy
primerów, tzn. im więcej jest G/C w stosunku do A/T, tym jest ona wyższa.
Inne czynniki wpływające na tę temperaturę to długość startera oraz skład
buforu reakcyjnego. Przy długości primera 14-19 oraz 36-70 bp temperaturę tę
można obliczyć zgodnie z wzorem Tm = 81,5 + 16,6 [log10(J+)] + 0,41 (%GC) (600/L) - 0,63(%F) gdzie J+ to stężenie jonów jednowartościowych, L to
długość primera w bp a F to procentowe stężenie formamidu (przy braku
formamidu ten człon równania wynosi 1). Przy długości primera 20-35 bp
wygodniej jest stosować uproszczoną formułę Tm = [0,5 x (TmF + TmR)] - 7o C,
gdzie TmF i TmR to temperatury podane na "metryczkach" przez wytwórcę
primerów. Niestety, czasami może się okazać, że rzeczywista temperatura
hybrydyzacji różni się od wyliczonej nawet o 12o C. Z tego powodu w praktyce
laboratoryjnej najlepiej jest ustalać temperaturę hybrydyzacji doświadczalnie,
przy użyciu termocyclera z termogradientowym blokiem grzewczym.
7. Optymalna temperatura syntezy ("elongacji") produktu reakcji PCR zależy od
pochodzenia termostabilnej DNA polimerazy. Dla najczęściej stosowanej Taq
polimerazy wynosi ona około +72o C.
8. Niezgodność na końcu 5' sekwencji startera z macierzystym DNA nie ma
większego znaczenia dla przebiegu reakcji PCR.
Reakcję PCR zazwyczaj przeprowadza się w specjalnych urządzeniach zwanych
termocyclerami (amplifikatorami), ale można ją przeprowadzić także ręcznie, z
zegarkiem w ręku, używając trzech termostatów nastawionych na trzy temperatury
cyklu. Reakcja PCR składa się zazwyczaj z 30 cykli i trwa w zależności od programu
i rodzaju amplifikatora od 2 do 4 godzin, ale najszybsze dostępne obecnie
termocyclery potrafią uporać się z zadaniem w czasie poniżej 30 minut. Kluczowym
odczynnikiem w reakcji PCR jest termostabilna polimeraza DNA. Obecnie na rynku
znajduje się szereg różnych polimeraz, najważniejsze z nich zostały wymienione w
poniższej tabeli.
Nazwa (pochodzenie)
Taq polymerase
(Thermus aquaticus)
Taq Klenow Fragment
(Thermus aquaticus)
Taq Stoffel Fragment
(Thermus aquaticus)
Uwagi
Pierwsza termostabilna polimeraza na
rynku, obecnie produkowana głównie
metodami inżynierii genetycznej
Taq polimeraza częściowo strawiona
proteazą, ma zwiększoną termostabilność
Cząsteczka Taq polimerazy pozbawiona
289 aminokwasów, o zwiększonej
termostabilności, wymaga więcej
magnezu
Producent
Pierwszy: Cetus
Obecnie : wiele
firm
Wiele firm
Applera
Z jonami manganu ma aktywność
Tth polymerase
odwrotnej transkryptazy, magnezu (Thermus thermophilus)
polimerazy DNA
Cth polymerase
Fragment Klenow'a tej DNA polimerazy
(Carbohydrothermus
ma aktywność odwrotnej
hydrogenoformans)
magnezozależnej transkryptazy.
Tma polymerase
Zwiększona termostabilność, duża
(Thermatoga maritima) dokładność
Pfu polymerase
Zwiększona dokładność
(Pyrococcus furiosus)
Tfl polymerase
(Thermus flavus)
Bst polymerase
(Bacillus
stearothermophilus)
Tgo polymerase
(Thermococcus
Bardzo duża dokładność
gorgonarius)
Tli polymerase
Ekstremalna termostabilność, duża
(Thermococcus litoralis) dokładność
Wiele firm
Roche
Applera
Stratagene
Bioline
Biorad
Roche
BioLabs
Niektóre z zawartych w powyższej tabeli termostabilnych polimeraz
charakteryzują się zwiększoną dokładnością syntezy "dorabianego" łańcucha
DNA. Na ogół jest to skorelowane z posiadaniem przez enzym dodatkowej
aktywności ezgonukleazy 3'-->5'. Jeżeli enzym przyłącza błędny nukleotyd, to
wskutek niesparowania "odstaje" on od macierzystej nici i natychmiast zostaje
odcięty, po czym polimeraza na nowo podejmuje swoją działalność.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Ile primerów (starterów) jest potrzebnych do przeprowadzenia reakcji PCR?
2. Jak samemu skonstruować primery do reakcji PCR? RT-PCR?
3. Dlaczego przy konstruowaniu primerów do reakcji RT-PCR należy wystrzegać
się sekwencji intronowych?
4. W którym kolejnym cyklu reakcji PCR po raz pierwszy otrzymamy produkty
syntezy o żądanej długości?
5. Który koniec primera jest wydłużany przez polimerazę?
6. Czy można przeprowadzić reakcję PCR bez dostępu do termocyclera?
7. Dlaczego polimeraza DNA użyta w reakcji PCR musi pochodzić z termofilnego
organizmu?
8. Czy temperaturę hybrydyzacji można w przybliżeniu ustalić za pomocą
obliczeń arytmetycznych?
9. Jaką wspólną cechę mają wszystkie polimerazy DNA używane w reakcji PCR,
niezależnie od źródła pochodzenia?
10. Sekwencjonowanie DNA
Pierwsze udane próby sekwencjonowania DNA podjęto w 1965 roku.
Sekwencjonowanie polega na ustaleniu kolejności nukleotydów. Jeżeli chcemy
ustalić kolejność nukleotydów w RNA, należy najpierw uzyskać cDNA za pomocą
odwrotnej transkrypcji. Wynik sekwencjonowania na ogół wieńczy dzieło zazwyczaj jest końcowym etapem wszelkich badań przeprowadzanych w
pracowni biologii molekularnej. Z dwu, niedawno prawie równie popularnych
technik sekwencjonowania, Maxama-Gilberta i Sangera ostatnio stosowana jest
wyłącznie ta druga. Wprowadzony przez firmę Perkin-Elmer (obecnie Applera)
system znakowania trójfosforanów czterech dideoksynukleotydów fluorochromami
w czterech różnych kolorach okazał się bezkonkurencyjny i w szybkim tempie
wypiera wszelkie inne techniki sekwencjonowania oparte na technice Sangera.
Spośród trzech konkurencyjnych wariantów tej metody (ze znakowanymi
primerami i kolejno z każdym z nieznakowanych trójfosforanów
deoksynukleotydów "Dye Primer Sequencing", kolejno z każdym ze
znakowanych trójfosforanów deoksynukleotydów "Cycle Sequencing" i z
mieszaniną nieznakowanych trójfosforanów deoksynukleotydów i znakowanych
trójfosforanów dideoksynukleotydów "Dye Terminator Sequencing") ta ostatnia
wygrała nieformalne lecz zażarte współzawodnictwo, ponieważ była stosowana
przez oba konkurujące zespoły naukowe, które z sukcesem zakończyły
sekwencjonowanie genomu człowieka. W technice tej używa się pojedynczego
startera. Jeżeli do nici oligonukleotydowej losowo przyłączy się deoksynukleotyd,
nić ta może być dalej wydłużana. Jeżeli natomiast los zrządzi, że przyłączy się
dideoksynukleotyd, to następuje zakończenie (terminacja) wydłużania, a kolor
fluorochromu daje informację który z dideoksynukleotydów zakończył łańcuch. W
wyniku reakcji uzyskuje się więc kilkaset produktów reakcji dłuższych jeden od
drugiego o pojedynczy znakowany dideoksynukleotyd, a elektroforeza kapilarna o
wysokiej rozdzielczości pozwala na ustalanie koloru piętna, jednego po drugim.
Dla pewności, że reakcja sekwencjonowania przebiegła prawidłowo, równolegle
sekwencjonuje się drugą nić z drugim primerem, i porównuje się, czy uzyskane
sekwencje są komplementarne na całej długości.
W fazie eksperymentów znajdują się inne, zupełnie nowe techniki
sekwencjonowania, np. technika z wykorzystaniem lucyferazy i apyrazy, technika
mikromatrycowa i inne.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Jakie są możliwości ustalenia kolejności nukleotydów w DNA?
2. Jak przebiega sekwencjonowanie najczęściej stosowaną technika „Dye
Terminator
Sequencing”?
11. Zastosowanie biologii molekularnej w medycynie sądowej
W medycynie sądowej techniki biologii molekularnej znalazły zastosowanie przy
identyfikacji osób i próbek krwi oraz przy badaniu śladów biologicznych.
Identyfikacja osób. Z tym zagadnieniem mamy do czynienia w przypadku podejrzenia
zamiany noworodków w szpitalach oraz przy ustalaniu pokrewieństwa do celów
spadkowych lub emigracyjnych. Zbliżonym zagadnieniem jest identyfikacja
nieznanych zwłok w sytuacji, w której inne metody identyfikacji indywidualnej
(okazanie zwłok rodzinie, daktyloskopia, odontologia lub superprojekcja) nie mogą
być przeprowadzone. Możliwość wydania opinii zależy od zakresu wykonanego
badania. Przy wąskim zakresie często nie można wydać użytecznej opinii, natomiast
po zbadaniu polimorfizmu DNA w szerokim zakresie dość często można wydać
opinię "twardą", o bardzo wysokim stopniu prawdopodobieństwa prawdziwości
konkluzji.
Identyfikacja próbek krwi. Badanie to przeprowadza się w przypadku podejrzenia
zamiany próbek krwi pobranej w celu stwierdzenia obecności niedozwolonych
substancji (alkoholu, narkotyków, leków) lub, rzadziej, pobranej do dochodzenia
ojcostwa. Praktyka wykazała, że spotykane są cztery rodzaje zamiany: a/ na krew
zwierzęcą, b/ na krew ludzką bez dobierania grupy, c/ na krew ludzką zgodną w
zakresie AB0 i Rh oraz d/ na krew tego samego człowieka (po pozbyciu się
inkryminowanej substancji). Zamiany typu "a", "b" i "c" są (przy użyciu technologii
DNA) wykrywane w 100%. Zamiany typu "d" są niewykrywalne, jednakże prawidłowa
organizacja pracy w laboratoriach alkoholowych i toksykologicznych może bardzo
utrudnić tego typu przestępczą działalność.
Badanie śladów biologicznych. Najczęściej do badania są przysyłane ślady krwi. W
badaniu kryminalistycznym można określić, czy jest to krew ludzka, a jeżeli tak, to
czy "zwykła" względnie miesiączkowa albo połogowa.
Śladami biologicznymi są też, spotykane w przestępstwach seksualnych, ślady
nasienia. Nasienie jest często wymieszane z wydzielinami ciała ofiary przestępstwa, i
dlatego (jeżeli ofiara była kobietą) szczególnie wartościowe wyniki osiąga się
oznaczając w takich śladach jedynie cechy genetyczne determinowane przez geny
obecne na chromosomie Y.
Innym rodzajem śladów biologicznych są tkanki. Badane są po znalezieniu
szczątków ludzkich względnie narzędzi, którymi dokonano zabójstwa lub
uszkodzenia ciała ofiary. Znajdywane też bywają na pojazdach mechanicznych.
Oprócz oznaczenia przynależności gatunkowej i badań genetycznych tkanki można
badać histologicznie.
Ciekawym rodzajem śladu biologicznego są włosy. Jeżeli włosy są obcięte, urwane
lub odłamane, to można w nich określić jedynie cechy morfologiczne, grupę krwi w
układzie AB0 i niekiedy cechy DNA mitochondrialnego. Obecność cebulki umożliwia
określenie płci oraz polimorficznych cech genomowego DNA.
Kolejnym rodzajem rutynowo badanych śladów biologicznych są ślady śliny. Bada się
je głównie na niedopałkach papierosów, znaczkach, kopertach, gumie do żucia i ciele
lub odzieży osób gryzionych przez napastnika.
Ostatnim rodzajem rutynowo badanych śladów biologicznych są próbki moczu, w
którym znajduje się zwykle wystarczająco dużo komórek nabłonkowych, aby można
było przeprowadzić badanie polimorfizmu DNA.
Badania dowodów rzeczowych powinny być przeprowadzone w zakresie
zapewniającym szansę przypadkowego powtórzenia oznaczonego zbiegu cech
rzadziej niż raz na dziesięć tysięcy.
W ostatnich latach coraz wyraźniej odchodzi się od badań śladów biologicznych w
kierunku stwierdzenia tradycyjnych cech grupowych (np. grup w układzie AB0). Jest
to coraz powszechniej uważane za "marnowanie materiału" i zastępowane
badaniami polimorfizmu DNA. Przed wykonaniem badania śladów krwi można je
ocenić pod kątem przydatności w dostarczeniu informacji o przebiegu zdarzenia, np.
o ilości, sile i kierunku zadanych ciosów, przebiegu zdarzenia, lokalizacji ofiary w
pomieszczeniu itp.
Niektóre z technik badawczych stosowanych w kryminalistyce znalazły zastosowanie
w archeologii. Prowadzone są badania zmumifikowanych zwłok, a nawet
pojedynczych kości, zwłaszcza czaszki i kości kończyn. Nie wiek szczątków ludzkich,
ale warunki środowiska, w których przebywały, decydują o sukcesie tych badań.
W medycynie sądowej techniki biologii molekularnej zastąpiły metody stosowane
wcześniej i umożliwiły spełnienie stuletniego marzenia genetyków sądowych indywidualnej identyfikacji krwi ludzkiej i wszelkiego innego materiału biologicznego.
Dochodzenie spornego ojcostwa. W Polsce badania kontynuuje się do uzyskania
prawdopodobieństwa ojcostwa nie mniejszego niż 99,9999%. Z pomocą oznaczania
tradycyjnych grup krwi osiągnięcie tego stopnia prawdopodobieństwa w zasadzie też
było możliwe, ale zdarzało się to raz na kilkaset badań, a nie w każdym badaniu, jak
obecnie. Do ustalania spornego ojcostwa można zastosować:
1. Badanie DNA restrykcyjno - hybrydyzacyjne (bardzo skuteczne ale kosztowne,
pracochłonne i długotrwałe, obecnie w wyraźnym zaniku)
2. Badanie DNA mikrosatelitarne zwane także badaniem PCR względnie
multipleksowym (prawie tak skuteczne jak poprzednie, obecnie dominujące)
3. Badanie DNA sekwencyjne (bardzo skuteczne badanie przyszłościowe, obecnie
znajduje się we wstępnym stadium rozwojowym, nie wiadomo, czy rozwinie się w
kierunku sekwencjonowania DNA, czy raczej stwierdzania punktowych zmian typu
SNP przy użyciu technologii mikrochipowej)
Niekiedy sporne dzieci, badane w sprawie o ustalenie ojcostwa są wieloraczkami,
najczęściej bliźniętami. Bliźnięta mogą być dwujajowe z jednego cyklu jajeczkowania
(ang. superfecundation) lub z dwu kolejnych cykli (ang. superfetation). W obu
przypadkach mogą mieć tego samego ojca lub dwu różnych ojców. Mogą też być
jednojajowe i wtedy zwykle powstają z jednego jaja i jednego plemnika, tzn. w wyniku
podziału zygoty na dwa płody. Możliwe są jednak także bliźnięta jednojajowe lecz
dwuplemnikowe. Z taką osobliwą sytuacją mamy do czynienia wówczas, gdy
zostanie zapłodnione nie jajo, ale jeszcze oocyt, który się jeszcze raz podzieli,
tworząc zygotę i dodatkowe jajo, które może zostać zapłodnione przez inny plemnik,
pochodzący od tego samego lub nawet innego mężczyzny (ostatnia możliwość jest
czysto teoretyczna, nie znaleziono jeszcze takiego przypadku).
Najogólniej, badanie DNA dla potrzeb medycyny sądowej można podzielić na trzy
rodzaje:
1. Badanie "zwykłych" cech grupowych (np. AB0 lub HLA), przeprowadzane nie
na poziomie antygenu, lecz na poziomie genu.
2. Badania uzupełniające, mające zwiększyć "moc dowodową" ekspertyzy
wykonanej w zakresie tradycyjnym lub mające doprowadzić wydawaną opinię
do wymaganej „siły dyskryminacyjnej”.
3. Badania molekularne wykonane w specjalnie wyznaczonym zakresie
(najczęściej ustalanym przez organizacje międzynarodowe, chodzi o
możliwość porównania wyników badań wykonanych w różnych krajach,
ponieważ przestępczość międzynarodowa nie jest już wyjątkiem, stała się
raczej regułą).
Polimorfizm kwasu deoksyrybonukleinowego.
Polimorfizm DNA można z grubsza podzielić na trzy główne rodzaje: polimorfizm
typu VNTR (Variable Number Tandem Repeats), mikrosatelitarny czyli STR
(Short Tandem Repeat) i typu SNP (Single Nucleotide Polymorphism).
Polimorfizm VNTR. W ludzkim DNA około 95% nie koduje białek. W tej masie
DNA o niejasnej funkcji występują powtarzalne sekwencje, a powtarzalność ta
realizuje się na trzy sposoby: "high" od 10.000 do 1.000 kopii, "medium" od 1.000
do 100 kopii i "low" od 100 do 2 kopii. Główna strefa wysokopowtarzalnego DNA
znajduje się na chromosomach w okolicach centromerów. Ten rodzaj DNA jest
odpowiedzialny za wystąpienie polimorfizmu typu VNTR. Genetycy sądowi
uważają, że polimorfizm ten daje bardzo wartościową informację, ale koszt,
pracochłonność i długotrwałość badań sprawiają, że badania tego typu prawie już
całkowicie zanikły.
Polimorfizm mikrosatelitarny. W obrębie niekodujących wstawek zawartych w
genach (sekwencje intronowe) możemy natrafić na polimorfizm mikrosatelitarny,
inaczej STR, polegający na różnej ilości powtórzeń 2 - 5 nukleotydowego motywu.
Oznacza się go za pomocą techniki PCR (Polymerase Chain Reaction).
Omówienie tej techniki znajduje się w następnym rozdziale. Fragment
polimorficzny "oflankowuje" się z obu stron starterami (primerami) i po
przeprowadzeniu reakcji porównuje się długość uzyskanego produktu z wzorcem,
czyli tak zwaną "drabinką alleliczną". Wynik badania z reguły podaje się w
ilościach powtórzeń motywu mikrosatelitarnego, np. zapis TH01 6/6 oznacza, że
w obrębie systemu mikrosatelitarnego TH01 (Tyrosine Hydroxylase intron 1)
badana osoba jest homozygotą allelu 6, a zapis TH01 6/9.3 oznacza, że jest
heterozygotą allelu 6 i niedoskonałego allelu 9.3, składającego się z dziewięciu
powtórzeń czteronukleotydowego motywu AATG plus skrócony motyw ATG (trzy
nukleotydy).
Polimorfizm typu SNP. Szacuje się, że w obrębie DNA kodującego średnio raz na
200 zasad występuje mutacyjna różnica, będąca wynikiem tranzycji (podstawienia
jednej zasady przez inną), albo znacznie rzadziej insercji (wstawienia jednej lub
wielu zasad), delecji (wypadnięcia jednej lub wielu zasad) albo inwersji
(przestawienia kolejności nukleotydów). Tego typu różnice są wykrywane jako
polimorfizm SNP. Polimorfizm ten jest o tyle ciekawy, że m. in. może objąć na
poziomie genu większość polimorfizmów grup krwi, ponieważ o poszczególnych
allelach nader często decydują punktowe, jednonukleotydowe mutacje (tranzycje)
w obrębie genu warunkującego daną grupę krwi. Polimorfizm typu SNP
najczęściej jest wykrywany za pomocą reakcji PCR lub techniki mikromatrycowej.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Jakie znasz sądowo - lekarskie zastosowania technik biologii molekularnej?
2. Czy za pomocą tych technik można ustalać sporne ojcostwo, a jeżeli tak, to w
czym te badania są lepsze od tradycyjnych oznaczeń grup krwi?
3. Jakie rodzaje badań DNA można zastosować do potrzeb medycyny sądowej?
12. Zastosowanie biologii molekularnej w seroantropologii
Seroantropologia jest działem antropologii badającym polimorfizm genetyczny
człowieka w celu wyciągnięcia wniosków dotyczących pochodzenia naszego
gatunku, jego pozycji systematycznej wśród hominidów, ustalenia prehistorycznych
szlaków migracji, pokrewieństwa poszczególnych odmian etnicznych i narodowości
oraz innych, podobnych informacji. Twórcą seroantropologii był Ludwik Hirszfeld,
badający i porównujący grupy krwi u rannych żołnierzy różnych narodowości w
czasie I Wojny Światowej. Z porównania częstości genów, warunkujących grupy krwi
wynika, że Polacy najbliżej spokrewnieni są z, co nie zaskakuje, innymi narodami
słowiańskimi, ale także, co można wytłumaczyć meandrami naszej historii, z
Niemcami, Irańczykami i ludami Syberii. Rozpatrując pokrewieństwo należy
oddzielnie rozpatrywać pokrewieństwo "po mieczu", wynikające z badania cech
obecnych na chromosomie Y i pokrewieństwo "po kądzieli", czyli dziedziczenie DNA
mitochondrialnego.
Badania seroantropologiczne w zasadzie rozstrzygnęły stary spór antropologów
dotyczący pochodzenia Homo sapiens. Wywodzimy się z Afryki i jesteśmy gatunkiem
stosunkowo młodym, luźno spokrewnionym z innymi gatunkami hominidów. Drugi z
ogólnie znanych gatunków człowieka, Homo neandertalis nie był naszym przodkiem,
lecz oddzielną, równoległą linią ewolucyjną rodzaju Homo. Naszymi najbliższymi
żyjącymi krewnymi są w kolejności: bonobo (Pan paniscus), szympans (Pan
troglodytes), goryl (Gorilla gorilla), orangutan (Pongo pigmaeus) i gibbon (Hylobates
lar). Szokująca jest informacja, że genomy człowieka i bonobo są tożsame w prawie
99%. Inne ciekawostki seroantropologiczne to ustalenia że:
1. Współczesny Homo sapiens miał pochodzenie afrykańskie, pierwsze "wyjście z
Afryki" miało miejsce ponad 200.000 lat temu, a ostatnie (w tej grupie znajdowała się
słynna "Ewa mitochondrialna") 130.000 - 170.000 lat temu.
2. Najbardziej archaiczną (zbliżoną do pnia) grupą etniczną są Buszmeni i Pigmeje.
3. Najbardziej genetycznie izolowaną grupą etniczną do niedawna byli Aborygeni
australijscy.
4. Ameryki zostały zasiedlone drogą lądowa od północnego krańca, a Euroazja z
południowego krańca kontynentu.
Badania seroantropologiczne doprowadziły do wykrycia szeregu markerów
charakteryzujących konkretną populację. Najbardziej znane przykłady to gen
hemoglobiny sierpowatej HBS oraz gen kwaśnej fosfatazy ACP*R, charakterystyczne
dla odmiany negroidalnej albo geny C4*A12 i HLA*Bw48 charakterystyczne dla ras
orientalnych. Markery takie mają poważne znaczenie kryminalistyczne, ponieważ
wykrycie takiej cechy w śladzie biologicznym z miejsca przestępstwa może
ukierunkować śledztwo.
Od początku powstania seroantropologii poszukiwano biologicznego
(przystosowawczego) sensu stwierdzonego zróżnicowania genetycznego. Sensu
tego nie znaleziono, co sprowokowało następne pytanie, skąd się ten polimorfizm w
ogóle wziął. Spośród różnych hipotez, tłumaczących przyczyny powstania
obojętnego pod względem przystosowawczym polimorfizmu genetycznego człowieka
najpopularniejsze są następujące:
1. Hipoteza mutacyjna. Mutacje są bezkierunkowe (ściślej wielokierunkowe) i z reguły
szkodliwe, a przez to eliminowane przez dobór naturalny. Natomiast jeżeli mutacja
jest neutralna pod względem przystosowawczym to nie jest eliminowana, a więc w
tym samym miejscu może zachodzić wielokrotnie i powoli się akumulować.
2. Hipoteza katastrof. Jest ona uzupełnieniem hipotezy mutacyjnej. Zakłada, że po
katastrofie demograficznej (zaraza, głód, migracja itp.) następuje odbudowa populacji
z niewielkiej wyjściowo grupy osobników. Jeżeli wśród nich przypadkowo znajdzie się
nosiciel zmutowanego genu, to w odbudowanej populacji ten gen będzie
rozprzestrzeniony o wiele częściej niż w populacji pierwotnej. Zjawisko to nazywane
jest czasami "dryftem genetycznym".
3. Hipoteza krzyżowania czystych linii. Jeżeli dwie linie genetyczne (różniące się w
obrębie jakiegoś genu) zostaną zmieszane np. w wyniku napływu jednej na
terytorium drugiej, może to doprowadzić do wytworzenia dwuallelicznego modelu
dziedziczenia, a stopień polimorfizmu będzie zależał od ilościowego stosunku obu
form wyjściowych. Hipoteza ta jest zgodna z głoszonym przez niektórych
seroantropologów poglądem o polifiletycznym pochodzeniu rodzaju ludzkiego.
4. Hipoteza fetalizacji. Genom ssaka ma dwa komplety genów: czynnych w czasie
rozwoju płodu oraz czynnych później, po zakończeniu embriogenezy. Geny
pierwszego kompletu po wypełnieniu swojej funkcji powinny zostać "wyłączone", ale
jeżeli wskutek błędu tak się nie stanie, to czynne geny "płodowe" zachowują się jak
allele względem genów "dorosłych", co może spowodować wytworzenie się
polimorfizmu.
Ze względu na łatwość oznaczania, markery w postaci genów warunkujących
polimorfizm grupowy są bardzo cenne w wielu badaniach genetycznych. Poniższe
zestawienie podaje przybliżoną lokalizację chromosomalną najważniejszych
seroantropologicznych markerów genetycznych.
A1 - Rh, Fy, PGM1, FUC, PGD, AMY, C8, F13B
A2 - ACP, TPOX, CRY, D2S1338
A3 - Tf, D3S1358
A4 - MNSs, PGM2, PLG, Do, Gc, FGA, FABP
A5 - C6, CSF1PO, D5S818
A6 - HLA (A, B, C. DR, DQA1), Bf, PLG, GLO, PGM3, Lp(a), SE, C4, F13A, SE33
A7 - Kell, D7S820
A8 - GPT, LPL, D8S347, D8S1179
A9 - AB0, Ii, ALD, AK, ORM, GALT, D9S926
A10 - D10S608
A11 - TH01, UGB, APO
A12 - VWA, CD4, PLA
A13 - ESD, D13S317
A14 - Pi, Gm, D14S306
A15 - FES/FPS, CYP19, PENTA E
A16 - Hp, PGP, D16S539
A17 - ACE, D17S1358
A18 - Jk, MBP, D18S51
A19 - Lu, Le, Se, C3, D19S433, D19S235
A20 - ADA, D20S85
A21 - D21S11, PENTA D
A22 - P, D22S264
X - Xg, G6PDH, HPRT, AR, AMEL(X)
Y - DYS19, DYS385, DYS389(I,II), DYS390, DYS391, DYS393, AMEL(Y)
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z powyższego
wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na konsultację.
1. Kto był twórcą seroantropologii?
2. Na jakim kontynencie powstał nasz gatunek?
3. Jakie gatunki zwierząt są najbliższe genetycznie człowiekowi?
4. Czy znane są ludzkie chromosomy, na których nie ma ważnych markerów
seroantropologicznych?
13. Zastosowanie biologii molekularnej w medycynie (diagnostyka i terapia
genetyczna)
Rozwój diagnostyki molekularnej datuje się od 1978 roku, w którym w dwu
niezależnych ośrodkach wykonano oznaczenie mutacji w szóstym kodonie betaglobiny, warunkującej powstanie hemoglobiny HbS, odpowiedzialnej za anemię
sierpowatą. Diagnostyka molekularna może być bezpośrednia - badanie wtedy
polega na wykryciu konkretnej mutacji, określonego allelu lub materiału
genetycznego patogenu mikrobiologicznego. Diagnostyka ta może też być
pośrednia, polegająca na analizie sprzężeń genetycznych, im bliżej oznaczana
cecha znajduje się względem genu powodującego chorobę, tym mniejsza możliwość
pomyłki.
Najgłośniejsze zastosowanie medyczne metod opartych na zdobyczach biologii
molekularnej to, oczywiście, próby terapii genetycznej. Próby te można podzielić na
sześć głównych nurtów:
A. Próby wykorzystania materiału genetycznego jako szczepionki. Z techniką tą
wiązano bardzo duże nadzieje, sądzono, że jest to najlepsza z możliwości
zmniejszenia nadprodukcji białek powodujących chorobę lub zablokowania
zmutowanego, dominującego patologicznego genu. Okazało się jednak, że w
praktyce ciągle zbyt mało wiemy o strukturze DNA. Szczepionka DNA, aby
była w pełni skuteczna, powinna być pozbawiona niektórych ważnych
biologicznie sekwencji ( dla przykładu - elementów cis-aktywnych, tzn.
obecnych na drugiej nici DNA), za to wzbogacona o sekwencje
immunostymulujące (wyspy CpG). W praktyce bardzo trudno jest spełnić te
wymagania.
B. Próby terapii genem za pomocą wektorów wirusowych. Pierwszy ujawniony
przypadek tego typu terapii to podjęta w 1990 roku próba terapii SCID
(wrodzonego braku odporności immunologicznej) za pomocą wprowadzenia
genu dezaminazy adenozynowej do limfocytów chorego dziecka. Używane
wektory wirusowe, jak do tej pory, należą do grupy retrowirusów,
adenowirusów lub herpeswirusów. Terapia taka ma dwie bardzo poważne
wady, pierwsza to sam pomysł terapii poprzez zakażenie (a chorzy bywają
bardzo słabi i miewają obniżoną odporność), a druga to problemy związane z
immunogennością białek wirusowego wektora. Największe trudności sprawia
opanowanie zakaźności wirusowych wektorów, przenoszących leczący gen.
Wynika to z możliwości nieoczekiwanego odbudowania sztucznie obniżonej
zjadliwości dobroczynnego wirusa drogą rekombinacji z dzikimi wirusami,
mało zjadliwymi lecz spokrewnionymi z naszym wektorem.
C. Próby terapii genem za pomocą wektorów nie będących wirusami. Polegają
one na "ukrywaniu" terapeutycznego genu w kapsule wiążącej się
bezpośrednio z celem - błoną jądrową. Przykładem tej techniki jest ukrycie
genu w kapsule, złożonej z białka - receptora progesteronu oraz samego
progesteronu w emulsji olejowej, taka kapsuła może być podana doustnie, bez
trudności penetruje błony komórkowe i po dotarciu do jąder (niestety komórek każdej tkanki, a nie tylko tej, którą obraliśmy za cel) wiąże się ze
steroidowym receptorem błony jądrowej, uwalniając ukryty wewnątrz gen.
D. Próby terapii za pomocą sekwencji antysensownych. Stosuje się ją wtedy, gdy
choroba polega na nadprodukcji jakiegoś białka. Technika polega na syntezie
oligonukleotydu komplementarnego do kluczowych biologicznie sekwencji
mRNA lub, jeszcze lepiej, pmRNA. Oligonukleotyd ten wiąże się z pmRNA
utrudniając prawidłowy proces składania (splicing'u) lub z mRNA, wydatnie
zmniejszając produkcję niepożądanego białka. Jedyna, ale największa
trudność tej pomysłowej terapii polega na braku dobrej metody dostarczania
antysensownego oligonukleotydu do wnętrza komórki. Ostatnio próbuje się
wiązać (blokować) mRNA także przy pomocy niebiałkowych molekuł
organicznych - niemniej problem ich transportu do miejsca przeznaczenia
pozostaje ten sam co w przypadku terapii antysensownym polinukleotydem.
E. Wykorzystanie zjawiska interferencji RNA. W ostatnich kilku latach okazało
się, że dwuniciowy RNA ma ciekawą właściwość – uruchamia kaskadę
zdarzeń prowadzących do strawienia mRNA komplementarnego do sekwencji
wspomnianego dwuniciowego RNA. Mechanizm ten pozwala na silne,
wybiórcze blokowanie aktywności dowolnie wybranego genu i w chwili pisania
tych słów jest juz stosowany w klinicznych próbach wyłączania genów
wirusowych, kluczowych w procesie namnażania wirusów w trakcie choroby.
F. Próby terapii genu, tzn. naprawa uszkodzeń nieczynnego lub zmutowanego
genu. Próby te, niewątpliwie przyszłościowe, obecnie ciągle jeszcze znajdują
się na etapie laboratoryjnych manipulacji in vitro.
Wszelkie manipulacje na kodzie genetycznym człowieka muszą być dokonywane
z wielką roztropnością, z trzech zasadniczych powodów. Po pierwsze, coraz
więcej danych genomiki porównawczej świadczy o tym, że "człowieczeństwo"
polega nie na posiadaniu przez nasz gatunek specyficznych "ludzkich" genów, ale
na specyficznej tylko dla Homo sapiens organizacji (zestrojenia) genomu.
Majstrowanie na oślep przy tym precyzyjnym mechanizmie może doprowadzić do
ponurych skutków. Po drugie, ostatnio wykryto liczne "dobroczynne" skutki wielu
złowrogich mutacji, a więc próby ich całkowitego wyeliminowania z puli genowej
człowieka mogą przynieść więcej szkody niż pożytku. Dla przykładu - nosiciele
genu anemii sierpowatej oraz osoby z nieczynnym genem glukozo 6fosfodehydrogenazy wykazują dużą odporność na zakażenie malarią, nosiciele
genu choroby Tay-Sachsa i mutanci wydzielający za dużo pepsynogenu do soku
żołądkowego są odporni na zakażenie prątkami gruźlicy, a nosiciele genu
powodującego mukowiscydozę są odporni na toksynę przecinkowca cholery.
Takich zaskakujących korelacji wykrywa się coraz więcej. Drugi powód do
zachowania ostrożności to brak należytej wiedzy jak nasze manipulacje
genetyczne wpłyną na zdrowie przyszłych pokoleń. Z powyższych powodów
wszelkie działania terapeutyczne na poziomie ludzkiego materiału genetycznego
muszą bezwzględnie podlegać jednej żelaznej zasadzie - możemy z naszym
pacjentem robić co chcemy (oczywiście po uzyskaniu jego świadomej zgody i w
granicach wiedzy lekarskiej oraz zasad etyki) lecz pod warunkiem, że zmieniamy
wyłącznie materiał genetyczny komórek somatycznych, a nie rozrodczych. Jeżeli
zachowanie tej zasady jest z jakichkolwiek powodów niemożliwe, należy
zrezygnować z próby terapii na poziomie genu lub bardzo poważnie rozważyć
możliwość sterylizacji pacjenta (jego interes reprodukcyjny można przecież
zabezpieczyć pobierając i zamrażając komórki rozrodcze).
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Czy można szczepić pacjenta używając do tego celu DNA?
2. Czy możliwe jest leczenie poprzez chorobę (zakażenie wirusowe)?
3. Jak można wprowadzić do wnętrza jądra komórkowego gen bez użycia
wektora wirusowego?
4. Co to jest terapia genu i czym się różni od terapii genem?
5. Jaka jest główna, naczelna zasada terapii genowej u człowieka i dlaczego
należy ją stosować?
14. Klonowanie DNA
Klonowanie DNA w zasadzie nie jest ani metodą badawczą, ani analityczną. Jest
to po prostu przemysłowy sposób na amplifikację in vivo wybranego fragmentu
DNA. Sposób ten jest technicznie prosty: plazmid zapewniający odporność na
antybiotyk rozcina się enzymem restrykcyjnym dającym lepkie końce cięcia, i tym
samym enzymem wycina się fragment DNA który ma ulec powieleniu. Po
zmieszaniu produktów cięcia i połączeniu ich enzymem ligującym uzyskuje się
między innymi plazmid z wklonowanym obcym fragmentem DNA. Następnie
dodaje się ten plazmid do hodowli drobnoustrojów w warunkach, w których mogą
przeżyć tylko te komórki, które pobiorą plazmid. Po wyhodowaniu ogromnej
biomasy drobnoustrojów izoluje się z nich plazmidy używane do terapii lub
odzyskuje się z nich DNA plazmidowe, z którego wycina się enzymami
restrykcyjnymi interesujący nas, sklonowany fragment DNA. Klonowanie DNA
opisaną metodą najłatwiej przeprowadzić korzystając z usług wyspecjalizowanej
firmy biotechnologicznej lub we własnym zakresie, przy użyciu gotowych
zestawów do klonowania. Od czasu opracowania technik amplifikacji dłuższych
niż 10.000 bp odcinków DNA za pomocą techniki PCR, popularność klonowania
DNA w plazmidach znacznie zmalała i, pominąwszy zastosowania przemysłowe,
klonowanie jest techniką coraz rzadziej stosowaną.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Na czym polega klonowanie DNA?
2. Do czego jest stosowana ta technika?
15. Przewidywane kierunki rozwoju biologii molekularnej
Trudno przewidzieć przyszłość, zwłaszcza odleglejszą. Dlatego w tym rozdziale
zostaną omówione tylko takie nowe techniki badawcze, które już istnieją, ale są
stosunkowo mało znane i ciągle bardzo mało rozpowszechnione.
Wiele przesłanek wskazuje na to, że stoimy w przededniu wynalezienia nowej,
trzeciej po klonowaniu i reakcji PCR techniki amplifikacji DNA, polegającej na
wykorzystaniu znanych enzymów do namnażania DNA w stałej temperaturze, bez
użycia termocyclerów.
W zakresie hybrydyzacji szerokim frontem wchodzą różne techniki
mikromatrycowe („mikroczipowe", „mikromacierzowe” wzglednie
„mikroczujnikowe”). Obserwuje się walkę dwu wariantów metodycznych: kwas
nukleinowy może być syntetyzowany albo na specjalnej płytce krzemowej, albo
nakrapiany na odpowiednio przygotowanym szkiełku mikroskopowym. Na
mikromatrycę można nakrapiać DNA wielu pacjentów (i hybrydyzować z próbą
molekularną) lub nakrapiać cDNA (nawet kompletu genów danego organizmu, bo
na niektórych mikromatrycach mieści się kilkadziesiąt tysięcy „kropek”), w tym
drugim przypadku hybrydyzuje się do związanych z podłożem "kropek" DNA lub
cDNA badanego pacjenta. Pojawiają się także pierwsze prace z wykorzystaniem
reakcji polimerazy, która na mikromatrycy dobudowuje znakowany fluorochromem
nukleotyd. Techniki mikroczipowe są bardzo tanie w wykonaniu, ale wymagają
niesłychanie drogiego oprzyrządowania (głównie niesłychanie precyzyjnego
skanera laserowego).
W dziedzinie sekwencjonowania może niedługo nastąpić rozwój technik
sekwencjonowania bezpośredniego, poprzez fizykochemiczną analizę DNA, bez
użycia reakcji PCR.
W technice PCR coraz powszechniej stosuje się odmianę reakcji zwaną
potocznie "real time", charakteryzującą się trzema cechami: miniaturyzacją testu,
bardzo wydatnym skróceniem czasu jej przebiegu oraz analizą produktów
przebiegającą w czasie trwania reakcji a nie, jak do tej pory, dopiero po jej
zakończeniu. Inną nowością są bloki termocyclerów przeznaczone już nie na
mikropłytki 96 miejscowe, ale 384 miejscowe ( w przyszłości zapewne będą także
i na 1536 miejscowe). Do ładowania takich mikropłytek stosowane będą roboty
nakrapiające, ponieważ jest to praca przekraczająca możliwości nawet
najstaranniejszego i najsprawniejszego manualnie człowieka.
REPETYTORIUM
Jeżeli potrafisz odpowiedzieć na zadane pytania, opanowałeś materiał z
powyższego wykładu. Jeżeli masz wątpliwości, zgłoś się do wykładowcy na
konsultację.
1. Czy obecnie możliwy jest także inny, trzeci (obok klonowania molekularnego i
reakcji PCR) sposób amplifikacji czyli namnażania DNA?
2. Co to jest "technika mikromatrycowa"?
3. Co to jest "real time PCR"?