Pewna Justyna rozpoczynając naukę chemii prosiła mnie o pomoc. Chciała szkolną wiedzę
wykorzystać do rzeczywistego zrozumienia podstaw chemii. Oto co jej odpisałem – moŜe i Tobie coś
się z tego przyda w skutecznym uczeniu się chemii.
Podstawowe informacje o chemii
Rozpoczynając szkolną naukę chemii dobrze wiedzieć o paru sprawach, które w szkolnej nauce nie
są podawane w ogóle, albo mówi się o nich zdecydowanie za późno i za mało.
Pod pojęciem chemii rozumiemy naukę o procesach przebiegających z wytworzeniem lub
zerwaniem wiązania chemicznego. Najczęściej mamy do czynienia z procesami, w których
następują oba te zjawiska. Przemiany, w których nie ma zmian w obrębie wiązań, naleŜą do fizyki.
Skoro o chemii decydują wiązania, naleŜałoby zacząć naukę od ich opisania. Ale tu „zaczynają się
schody”. Aby choć trochę pojąć istotę wiązań chemicznych, naleŜy poznać budowę i właściwości
atomów. Natomiast Ŝeby poznać i wyjaśnić właściwości chemiczne atomów i ich skłonność do tworzenia wiązań, trzeba posłuŜyć się mechaniką kwantową, która do prostych i łatwych niestety nie
naleŜy. Dochodzi więc do paradoksalnej sytuacji, Ŝe aby ułatwić poznanie i zrozumienie chemii,
trzeba by zacząć od arcytrudnej mechaniki kwantowej oraz budowy materii (teŜ niezbyt łatwej, o
czym za chwilę). I to zapętlenie jest prawdopodobnie powodem, Ŝe w dydaktyce chemii od stulecia
nic nie drgnęło. Początki nauki są dokładnie takie same jak w ubiegłym wieku, mimo Ŝe o podstawach chemii wiemy o niebo więcej niŜ wówczas, gdy te zręby chemicznej dydaktyki powstawały.
śeby przeciąć ten gordyjski węzeł, proponuję zapoznanie się z naprawdę niezbędnym minimum
wiedzy dotyczącej świata atomów. Ze względu na trudności w wyjaśnianiu tego świata mikro za
pomocą prostych i jasnych sformułowań, musisz na początek wiele twierdzeń przyjąć na wiarę.
Czas na rzetelne wyjaśnienie problemów związanych z mechanika kwantową przyjdzie ewentualnie
później, po przebyciu całego kursu chemii. A skoro nie będziemy w sposób pełny wyjaśniać praw
świata atomów, to przynajmniej naleŜy Ci się wyjaśnienie, czemu jest to takie trudne.
Od urodzenia poznajemy otaczający nas świat za pomocą zmysłów, a więc poznajemy zjawiska,
procesy, które są skutkami, a nie przyczynami. Później zaczyna się wyjaśnianie przyczyn tych znanych nam juŜ skutków, ale umysł wyćwiczony w poznawanie skutków, często właśnie przez ich
pryzmat próbuje widzieć przyczyny (a nie odwrotnie). To, Ŝe Ziemia przyciąga nas i wszystkie
przedmioty grawitacją przyjmujemy za prawdę dość łatwo (bo takie są nasze doświadczenia) ale to,
Ŝe my równieŜ przyciągamy Ziemię z taką samą siłą, juŜ tak łatwo nas nie przekonuje. Na temat
tego, co się dzieje w świecie cząsteczek i atomów bezpośrednio naszymi zmysłami nie jesteśmy w
stanie dowiedzieć się nic. Wszystko (a jest tego sporo) co o tym świecie wiemy, pochodzi z obserwacji pośrednich, skutków makroskopowych i wyciąganych na tej podstawie wniosków. A sprawa
jest jeszcze bardziej pogmatwana, bo nie dość, Ŝe nie widzieliśmy ani nie dotknęliśmy nigdy pojedynczej cząsteczki czy atomu (o elektronach nie wspominając) to jeszcze wnioski, które wyciągamy z obserwacji pośrednich, są tak zaskakujące i nieprzystające do naszego obrazu makroświata, Ŝe
„zwykłego” człowieka przyprawiają o ból głowy. No ale w końcu inni sobie z tym poradzili (przynajmniej niektórzy) - spróbujmy i my!
Budowa atomu:
Jądra atomów, z których zbudowana jest cząsteczka związku chemicznego, składają się z dodatnio
naładowanych protonów i obojętnych elektrycznie neutronów. Siły elektrostatycznego odpychania
jednoimiennych ładunków powinny powodować nietrwałość takiego tworu - jądro powinno
„eksplodować” a odpychające się dodatnie protony z duŜą prędkością powinny oddalać się od
siebie. PoniewaŜ tak się nie dzieje, wnioskujemy stąd, Ŝe w jądrze atomowym działają jeszcze
jakieś siły utrzymujące jego spójność, mimo owych destrukcyjnych sił odpychania. Są to tzw. siły
bliskiego zasięgu, działające na bardzo krótkich odległościach. JeŜeli przyjmiemy, Ŝe średnica
protonu czy neutronu wynosi około 1 fermi (10-15 m) to zasięg działania sił krótkiego zasięgu,
spajających jądro, wynosi około 2-3 fermi. Tak więc siły te działają wyłącznie na najbliŜsze sobie
nukleony i praktycznie zasięg ich działania ogranicza się do jądra. Odpychanie elektrostatyczne
protonów jądra działa na odległości znacznie większe (maleje z kwadratem odległości między
protonami) lecz jest o wiele słabsze, najczęściej pomijalnie małe w porównaniu z siłami spójności.
Jednak przy odległościach między protonami rzędu 0,5 fermi (protony sąsiadujące ze sobą)
wielkość sił odpychania elektrostatycznego zaczyna równowaŜyć siły przyciągania nukleonów.
Mamy tu do czynienia z przykładem stabilnej równowagi między dwiema przeciwstawnymi siłami
(stan w przyrodzie bardzo często spotykany).
Tak więc w jądrze atomowym „zmagazynowana” jest olbrzymia ilość energii (olbrzymia w
porównaniu do masy jądra). MoŜemy porównać jądro atomowe do butli z gazem pod duŜym
ciśnieniem, gdzie zmagazynowaną energię moŜemy wyzwalać powoli, pod kontrolą, spalając gaz w
kuchence (reaktor atomowy, kontrolowany rozpad jąder) lub moŜe nastąpić niekontrolowane
wyzwolenie energii (wybuch butli), co w odniesieniu do jąder atomowych oznacza wybuch jądrowy
(bomba atomowa). Poza dość wąską dziedziną chemii jądrowej, chemików ten zakres opisu materii
interesuje mniej niŜ inne - jest to raczej dziedzina pracy fizyków.
Orbitale atomowe:
Chemik jądro atomowe najczęściej traktuje jako monolityczny twór o określonych właściwościach
(nie wolno jednak zapominać, Ŝe te właściwości to wypadkowa właściwości i zachowań
składowych) i bardziej niŜ „wnętrze” interesują go relacje jądra z pozostałymi składowymi atomu,
czyli z elektronami. Tu znów znajdujemy równowagę między siłami elektrostatycznego
przyciągania (dodatnie jądro - ujemne elektrony) i elektrostatycznego odpychania (elektrony
między sobą). Im elektrony są bliŜej jądra, tym mniejsze odległości między nimi i silniejsze
odpychanie - zarówno przez elektrony powłok bliŜszych jądra, jak i elektronów danej powłoki. Przy
pewnej odległości następuje zrównowaŜenie sił przyciągania przez dodatnie jądro i odpychania
przez pozostałe elektrony atomu.
Pojawia się tu jednak problem, trudny do wyjaśnienia na gruncie elektrostatycznych oddziaływań dlaczego elektrony powłoki najbliŜszej jądra (1s), które są spychane przez inne elektrony w
kierunku jądra, i które przez to jądro są przyciągane, utrzymują się jednak w pewnej, dość ściśle
określonej odległości od niego? I tu koniecznym staje się zastosowanie zasad i praw mechaniki
kwantowej, która wykaŜe, Ŝe tak musi być, ale nie wyjaśni nam niestety w prosty sposób, dlaczego
tak musi być.
Zdajemy juŜ sobie sprawę, jak skomplikowany układ sił działa na elektron w atomie. Siły te
(elektryczne, magnetyczne) sumując się wektorowo, powodują powstanie wokół jądra atomowego
obszarów, w obrębie których na umieszczony tam elektron oddziałują bardzo małe siły. Taki obszar,
gdzie elektron poddawany jest działaniu bardzo małych sił, nazywamy orbitalem. PoniewaŜ
w przestrzeni wokół jądra, nie naleŜącej do orbitali, na elektron działają znaczne siły, elektrony są
„zaganiane” do obszarów orbitali. JeŜeli jednak w obrębie orbitala znajdą się choćby dwa elektrony,
zaczynają oddziaływać na siebie odpychająco, a więc „wypychają się” nawzajem z tej pozycji.
PoniewaŜ jednak elektrony prócz pól elektrycznych oddziałują na siebie takŜe polami
magnetycznymi, powstającymi jako konsekwencja ich ruchu wirowego (spin), dwa elektrony na
jednym orbitalu niwelują odpychanie elektryczne przyciąganiem magnetycznym (przeciwne spiny
to przeciwny układ biegunów magnetycznych). Stąd jeden orbital moŜe pomieścić najwyŜej dwa
elektrony o przeciwnych spinach. Wyobraźmy sobie tacę, której np. jedna czwarta powierzchni to
łagodne zagłębienia. Nasypmy na tę tacę garść grochu i potrząsając delikatnie, obserwujmy, gdzie
będą lokalizować się ziarna grochu. Nie jest dla nas Ŝadnym zaskoczeniem, Ŝe za kaŜdym razem
zdecydowana większość grochu ulokuje się w zagłębieniach. Te zagłębienia to model orbitali.
Często orbitale w podręcznikach są definiowane jako miejsca, gdzie prawdopodobieństwo
znalezienia elektronu jest największe. Czasem nawet precyzują, Ŝe owo największe oznacza 90%
lub 95%. Kształt orbitala określa (fizycznie nie istniejąca !!) granica zamykająca ów obszar 95%
prawdopodobieństwa znalezienia elektronu.
Podręczniki, pokazując graficzny obraz orbitali, mówiąc o ich kształcie, wyrabiają w nas
podświadome przekonanie o fizycznym, wręcz materialnym charakterze orbitala. Jeszcze bardziej
utwierdzają nas w tym podświadomym przekonaniu, mówiąc o „napręŜeniach” wiązań, jeśli
orbitale tworzące wiązanie chemiczne nakładają się pod innymi kątami niŜ ich „naturalne” ułoŜenie
w przestrzeni. Są to bardzo wygodne, ale bardzo nieprawdziwe modele. Co prawda często
przekonująco wyjaśniające pojedyncze zjawisko (np. nietrwałość cyklopropanu) ale jednocześnie
wprowadzające zamieszanie w zrozumieniu ogólnych pojęć (np. wiązania chemicznego).
Tak więc nie wchodząc zbyt głęboko w skomplikowaną materię wszelkich sił działających w
obrębie atomu i wzajemnych relacji między nimi wystarczyć nam musi, Ŝe skomplikowana gra sił
grawitacji (masa), elektrycznych (ładunek) i magnetycznych (spin) powoduje, Ŝe jądro atomowe
jest tworem bardzo trwałym (do pewnej masy - atomy promieniotwórcze) a w pewnych obszarach
wokół jądra atomowego siły te dla konkretnego elektronu praktycznie się znoszą. JeŜeli elektron
przez przypadek znalazł się poza tym obszarem, działa zawsze na niego jakaś siła wypadkowa,
kierująca go w konsekwencji właśnie do tego obszaru o najniŜszej energii. Obszary te (orbitale)
układają się w pewnych konkretnie określonych odległościach od jądra (powłoki elektronowe
opisane główną liczbą kwantową), a w obrębie tych powłok tworzą obszary o róŜnym kształcie i
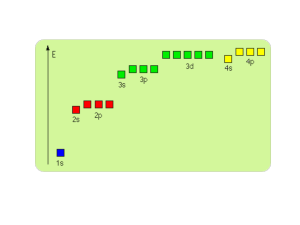
energii (orbitale opisane poboczną liczbą kwantową - patrz rysunek niŜej) oraz ukierunkowaniu w
przestrzeni (opisane magnetyczna liczbą kwantową). Tak więc „adres” konkretnego elektronu
w atomie musi składać się z podania numeru powłoki (główna liczba kwantowa, w starszych
podręcznikach stosowano teŜ oznaczenia literowe K, L, M, N), typu orbitalu (poboczna liczba
kwantowa l - poszczególnym jej wartościom przypisujemy oznaczenia literowe typów orbitali: s, p,
d, f... - patrz rysunek niŜej) i jego usytuowania w przestrzeni (np. px, py, pz) - magnetyczna liczba
kwantowa. Warto tu wspomnieć, Ŝe istnienie orbitala wynika z budowy danego atomu, tak więc
dany orbital istnieje, bez względu na to czy są elektrony mogące go wypełnić (orbital obsadzony)
czy teŜ nie (orbital nieobsadzony).
Wiązania:
Jeśli juŜ przeanalizowaliśmy budowę atomu i pojęcie orbitali, moŜemy zacząć rozpatrywać problem
wiązań chemicznych. Tu mamy jeszcze bardziej skomplikowany układ sił przyciągania
i odpychania elektrostatycznego, bierze w nim udział bowiem kilka atomów (a dwa co najmniej).
Wiązania chemiczne na ogół są tworzone przez orbitale naleŜące do ostatniej, walencyjnej powłoki
elektronów. JeŜeli dwa orbitale dwóch atomów („czerwony” i „niebieski” na rysunkach poniŜej)
zbliŜą się do siebie (rysunek pierwszy), to elektron „niebieski” znajdzie się w zasięgu działania
silnych sił „czerwonego” i odwrotnie (odpychanie elektronów). Jeśli jednak przezwycięŜymy te siły
i jeszcze bardziej zbliŜymy atomy do siebie, tak by przestrzeń orbitalu „niebieskiego” i przestrzeń
orbitalu „czerwonego” były w duŜej części toŜsame, to oba elektrony znajdą się w sytuacji
minimalnych oddziaływań (mechanika kwantowa) - wspólna przestrzeń to teraz orbital
cząsteczkowy, wiąŜący. Tak w duŜym skrócie wygląda tworzenie najpopularniejszego wiązania
typu sigma, powstające przez współosiowe nałoŜenie się orbitali.
Teraz w rozwaŜania o wiązaniach wtrąćmy informacje o bardzo waŜnej cesze atomów elektroujemności ...
Elektroujemność:
Elektroujemność jest jednym z istotniejszych parametrów opisujących właściwości pierwiastków.
Elektroujemność najłatwiej wytłumaczyć na prostym układzie dwóch atomów połączonych
wiązaniem chemicznym. Wspólna para elektronów tworzących wiązanie moŜe znajdować się w
środku między dwoma atomami, naleŜąc jednocześnie do obydwu atomów (wiązanie atomowe,
patrz rysunek powyŜej) lub w całości naleŜeć do jednego tylko atomu, który przyjmuje wówczas
ładunek ujemny i z drugim atomem (który oczywiście przyjmuje wówczas ładunek dodatni) łączy
go wyłącznie siła przyciągania elektrostatycznego (wiązanie jonowe).
Prócz tych dwóch skrajnych połoŜeń wspólnej pary elektronowej, w rzeczywistości występuje całe
spektrum wiązań, w których wspólna para elektronów zajmuje pozycję pośrednią między
wiązaniem atomowym a jonowym. To przesunięcie elektronów wiąŜących jest wynikiem róŜnicy w
sile przyciągania elektronów przez poszczególne atomy, a siłę tę nazywamy elektroujemnością.
Elektroujemność jest to zatem pewna tendencja atomu pierwiastka do przyciągania
(„zawłaszczania”) elektronów walencyjnych innych atomów. Na wielkość elektroujemności główny
wpływ mają dwa czynniki: odległość powłoki walencyjnej od jądra atomowego oraz dąŜenie
kaŜdego atomu do stworzenia sytuacji, w której ostatnia obsadzona elektronami powłoka będzie
zawierać osiem elektronów. Zatem wyŜszą elektroujemnością będą charakteryzować się pierwiastki
początkowych okresów (mały promień atomowy, silniejsze przyciąganie przez dodatnie jądro) i
końcowych grup (duŜa ilość elektronów walencyjnych ułatwia osiągnięcie oktetu). Zgodnie z tą
regułą najbardziej elektroujemnym pierwiastkiem jest fluor (drugi okres, siódma grupa).
Siłę elektroujemności pierwiastka określamy poprzez wartość półempirycznego parametru.
Wartości tego współczynnika dla poszczególnych pierwiastków pierwszy obliczył (i przede
wszystkim zaproponował sposób ich wyliczania) Pauling. Później, stosując nieco inne podejście i
sposób liczenia wartości parametru elektroujemności podali Rochow i Allred. Istnieje równieŜ inna
metoda liczenia zastosowana przez Mullikena. W kaŜdej z tych metod otrzymuje się nieco róŜne
wartości dla tego samego pierwiastka, z czego wynika prosty wniosek, Ŝe nie naleŜy do wartości
parametru elektroujemności przywiązywać zbyt duŜej wagi i traktować go naleŜy jako parametr
wyłącznie pólilościowy. RóŜnice pomiędzy elektroujemnością obliczoną róŜnymi metodami
zazwyczaj nie przekraczają wartości 0,3, choć w pojedynczych przypadkach róŜnica ta moŜe nawet
przekroczyć wartość 1. Zakres wartości współczynnika elektroujemności zawiera się z reguły
między wartościami 1 (metale) a 4 (fluor).
Elektroujemność zaleŜy w głównej mierze od promienia atomu oraz dąŜenia do uzyskania trwałej
konfiguracji oktetu elektronowego (osiem elektronów na ostatniej powłoce).
Pierwszy czynnik związany jest z siłą oddziaływania dodatnio naładowanego jądra atomowego,
która głównie zaleŜy od wielkości ładunku jądra i promienia atomu - praktycznie moŜna przyjąć, Ŝe
siła ta słabnie wraz ze wzrostem promienia atomu.
Drugi czynnik - chęć uzyskania oktetu elektronowego, naleŜy rozwaŜać w układzie dwóch atomów
połączonych wiązaniem. Tu decydującą rolę odgrywa prawdopodobieństwo. Dla przykładu - w
połączonych w cząsteczkę MgO atomach większe jest prawdopodobieństwo uzyskania oktetu
przez atom tlenu, który zawierając juŜ sześć elektronów, potrzebując przyłączenia tylko dwóch, niŜ
przez atom magnezu, który w tym celu musiałby przyłączyć aŜ sześć elektronów (ma tylko dwa
walencyjne). Magnezowi łatwiej (istnieje większe prawdopodobieństwo takiego zachowania)
uzyskać oktet przez oddanie dwóch elektronów z walencyjnej powłoki M (pozostanie mu oktet na
niŜej połączonej powłoce L). Stąd czasem mówimy o pierwiastkach elektrododatnich, dla
podkreślenia, Ŝe łatwiej przechodzą w postać z oktetem elektronowym przez oddanie elektronów i
uzyskanie ładunku
elektroujemność).
dodatniego
niŜ
przez
przyłączenie
elektronów
(taka
„odwrotna”
Elektroujemność pierwiastków (a dokładniej róŜnice elektroujemności między pierwiastkami połączonymi wiązaniami chemicznymi) wpływając na wielkość polaryzacji poszczególnych wiązań, powoduje powstawanie, w elektrycznie obojętnej cząsteczce, miejscowych ładunków dodatnich i
ujemnych, co z kolei ma znaczący wpływ na reaktywność związków chemicznych (wytwarzają się
swoiste „punkty zaczepienia” dla drugiej cząsteczki substratu). Ładunki te determinują takŜe w
znacznym stopniu właściwości fizyczne związku (np. rozpuszczalność czy temperaturę topnienia
lub wrzenia). Są teŜ podstawowym czynnikiem określającym charakter wiązania między dwoma
atomami (kowalencyjne, jonowe ...).
Znajomość elektroujemności i jej wpływu na reaktywność i właściwości związków
chemicznych jest podstawową wiedzą, konieczną do zrozumienia chemicznych przemian i
fizykochemicznych właściwości związków.
... i wróćmy do sprawy wiązań:
W bardzo duŜym uproszczeniu moŜna powiedzieć, Ŝe cząsteczka to atomy i wiązania. O ile atomy
nie ulegają jakimś zasadniczym zmianom, o tyle wiązania łączące atomy w cząsteczkę są bardzo
róŜne i mogą ulegać zmianom pod wpływem innych elementów cząsteczki. Wiązanie chemiczne
jest realizowane przez elektrony ostatniej powłoki elektronowej danego pierwiastka, która nosi
nazwę powłoki walencyjnej. KaŜdy atom, poprzez tworzenie wiązań stara się uzyskać konfiguracje
oktetu (osiem elektronów) na swojej powłoce walencyjnej. „Klasyczne” wiązanie chemiczne polega
na takim zbliŜeniu dwóch atomów, Ŝe odpowiednie ich orbitale powłok walencyjnych nakładają się
na siebie (część przestrzeni między atomami jest wspólna dla obydwu orbitali tworzących wiązanie)
a znajdujące się na orbitalach elektrony (po jednym na kaŜdym orbitalu) tworzą parę o przeciwnych
spinach i znajdują się w przestrzeni wspólnej dla obu atomów. Takie wiązanie nazywamy
wiązaniem atomowym, kowalencyjnym. W praktyce spotykamy je dość rzadko - takie wiązanie
występuje między atomami tego samego pierwiastka, a więc najczęściej w przypadku pierwiastków
gazowych N2, Cl2 czy I2.
Drugim typem wiązań, najczęściej chyba spotykanym, (szczególnie w chemii organicznej) jest wiązanie atomowe spolaryzowane. RóŜni się ono od opisanego powyŜej jedynie tym, Ŝe poniewaŜ w
wiązaniu biorą udział dwa atomy róŜnych pierwiastków, o róŜnych elektroujemnościach, „środek
cięŜkości” ładunku elektronów wiązania jest przesunięty w kierunku atomu o większej elektroujemności, przez co zatraca się równowaga elektryczna i w obrębie wiązania powstaje układ biegunowy
(dipol). Jeden z atomów przyjmuje ładunek δ- a drugi δ+ i choć cząsteczka jako całość nadal jest
elektrycznie obojętna, to przesunięcia ładunku w jej obrębie powodują powstanie miejsc bardziej
podatnych na reakcje chemiczne. PoniewaŜ powstałe ładunki nie są równe elementarnemu ładunkowi, zaznaczamy je symbolem δ .
W duŜym uproszczeniu moŜna powiedzieć, Ŝe aktywność chemiczna cząsteczki, jej podatność na
przemiany chemiczne zaleŜy głównie od wielkości polaryzacji wiązań, choć nie wolno nam zapominać, Ŝe znaczna rolę odgrywa tu takŜe przestrzenne usytuowanie poszczególnych atomów.
JeŜeli róŜnica wartości elektroujemności dwóch atomów tworzących wiązanie jest większa niŜ 1,4
dochodzi do powstania wiązania jonowego. Wiązanie jonowe tym się róŜni od atomowego
spolaryzowanego, Ŝe siłą wiąŜącą dwa atomy nie jest juŜ wspólnota pary elektronowej, lecz siły
przyciągania elektrostatycznego dodatniego ładunku kationu (który oddał swój elektron, lub
dokładniej, któremu elektron został zabrany) i ujemnego ładunku anionu (który z kolei powstał
przez zabranie całego elektronu z kationu). Tak więc wiązanie jonowe sensu stricto nie jest
wiązaniem chemicznym, a jedynie czystym, elektrostatycznym oddziaływaniem między jonami.
Takie „czyste” wiązanie jonowe występuje równie rzadko co czyste wiązanie kowalencyjne.
Zdecydowana większość wiązań chemicznych to mniej lub bardziej spolaryzowane wiązania
kowalencyjne.
Ze względu na to, Ŝe w wiązaniu jonowym następuje przeniesienie elektronu (przesunięcie całego
ładunku elementarnego), kationy i aniony zaznaczamy znakiem plus lub minus, juŜ bez symbolu
delty. Wiązania typu sigma silnie spolaryzowane i jonowe dość łatwo doprowadzić do dysocjacji.
Wiązania jonowe wymagają tylko niewielkiego wkładu energii potrzebnego do odsunięcia jonów
od siebie (pokonania jedynie sił elektrostatycznego przyciągania odmiennych ładunków). Zupełnie
inna jakość wiązania jonowego powoduje, Ŝe reakcje między związkami o charakterze jonowym
przebiegają wyraźnie inaczej niŜ reakcje między związkami o wiązaniach atomowych.
Dysocjacja wiązania
„prawie” jonowego
Wiązanie „czysto” jonowe
PoniewaŜ wiązania atomowe spolaryzowane moŜemy uznać za stan pośredni, między wiązaniem
atomowym (brak polaryzacji wiązania) a wiązaniem jonowym („pełna”, maksymalna polaryzacja)
czasem w róŜnych opracowaniach moŜemy spotkać się z określaniem procentowego udziału
wiązania jonowego w wiązaniu atomowym, dla bardziej precyzyjnego określenia charakteru
wiązania spolaryzowanego. Z wiązaniem jonowym mamy do czynienia przede wszystkim w chemii
nieorganicznej.
Specyficznym rodzajem wiązania chemicznego jest wiązanie koordynacyjne, inaczej donorowoakceptorowe. Ta druga nazwa dokładnie oddaje charakter wiązania. Jest to wiązanie pozornie takie
jak atomowa - wspólna para elektronów łączy dwa atomy - lecz róŜni się tym, Ŝe oba elektrony
pochodzą od jednego atomu (donora) i są wykorzystywane takŜe przez drugi atom (akceptor).
Tego typu wiązania spotykamy w związkach, gdzie występują atomy na stopniu utlenienia większym od +4.
PoniewaŜ generalnie elektronów walencyjnych wokół kaŜdego atomu moŜe być tylko osiem (w
przypadku wodoru dwa), to np. dla kwasu siarkowego(VI), trzymając się formalnych wartościowości, uzyskamy wzór, w którym wokół atomu siarki znajduje się aŜ 12 elektronów walencyjnych
(sześć wiązań po 2 elektrony). Jest to niezgodne z podanym wcześniej warunkiem, więc musimy
przyjąć, Ŝe dwa wiązania siarki z atomami tlenu są wiązaniami donorowo (siarka daje) akceptorowymi (tlen przyjmuje), co oznaczamy strzałkami od donora do akceptora. W takim układzie wokół
wszystkich atomów jest odpowiednia ilość elektronów walencyjnych (po osiem, przy wodorach po
dwa). Związki o takiej strukturze wiązań są najczęściej silnymi utleniaczami (kwas azotowy(V),
nadmanganiany, kwas chlorowy(VII) itp.)
Istnieje jeszcze jeden typ wiązań, bardzo podobny do wyŜej omówionego - wiązania powstające
przez nałoŜenie się orbitala zawierającego parę elektronów (tzw. wolną parą elektronów) i orbitala
nieobsadzonego („pustego”) drugiego atomu (p lub d). Tego typu wiązania donorowo-akceptorowe
występują np. w kompleksach.
Ostatnim typem wiązania jest tzw. wiązanie wodorowe. Jest to nazwa nieco myląca, wiązanie
wodorowe bowiem nie jest wiązaniem stricte chemicznym, nie wiąŜe atomów w cząsteczce, jest
raczej pewnym typem oddziaływania między atomem wodoru w cząsteczce a elektroujemnym
atomem innego pierwiastka, lecz ze względu na charakter tego oddziaływania otrzymało ono nazwę
wiązania. Jest to dość słabe oddziaływanie występujące pomiędzy atomem wodoru połączonego z
atomem silnie elektroujemnego pierwiastka (np. tlenu lub azotu) a elektroujemnym atomem,
posiadającym tzw. wolne pary elektronowe, tzn. elektrony z powłoki walencyjnej, niebiorące
udziału w wiązaniu. „Siłą napędową” powstania takiego wiązania jest częściowy ładunek dodatni
na atomie wodoru, który powstaje wskutek polaryzacji wiązania wodór - atom elektroujemny
(najczęściej tlen, np. w grupie –O–H) i związany z tym cząstkowy ładunek ujemny na atomie
elektroujemnego pierwiastka. Jednak charakter sił wiąŜący atom wodoru z atomem
elektroujemnego pierwiastka nie ma charakteru oddziaływań elektrostatycznych, tak jak ma to
miejsce między dipolami, lecz posiada dość wyraźnie zaznaczony charakter wiązania chemicznego
(wspólnota elektronów), aczkolwiek niezmiernie słabego. Udział w nim biorą wolne pary
elektronowe atomu silnie elektroujemnego pierwiastka. Mimo niewielkiej siły wiązanie wodorowe
jest przyczyna wielu waŜnych zjawisk fizykochemicznych. Jemu zawdzięczamy istnienie naszego
Ŝycia, gdyby bowiem nie wiązania wodorowe, woda (podstawa Ŝycia na Ziemi) nie byłaby cieczą o
znanych nam właściwościach, lecz podobnie jak metan byłaby gazem, na co wskazuje jej formalna
masa cząsteczkowa (metan 16, woda 18, amoniak 17, azot 28, tlen 32). W rzeczywistości wiązania
wodorowe między cząsteczkami wody powodują, Ŝe zachowuje się ona jak substancja o masie o
wiele większej (100-150). Silnie elektroujemny atom tlenu powoduje polaryzację wiązań H–O,
umoŜliwiając powstanie oddziaływań o charakterze wiązań wodorowych, tak jak podano na
rysunku poniŜej.
Dotychczas mówiliśmy o wiązaniach typu sigma, gdy orbitale wiąŜące nasuwają się na siebie
współosiowo. Istnieją jeszcze wiązania typu pi, gdzie orbitale wiąŜące nakładają się bokami:
Tego typu wiązania pojawiają się jako drugie lub trzecie wiązanie w tzw. wiązaniach wielokrotnych
- podwójnych (np. CO2; O=C=O) lub potrójnych. Znajomość ich właściwości i powstawania będzie
miała duŜe znaczenie w trakcie poznawania chemii organicznej. Np. w
iązania typu π (boczne nałoŜenie orbitali p) łatwiej niŜ σ ulegają rozerwaniu, bowiem część
wspólna orbitali składowych jest mniejsza, średnia energia elektronów wiąŜących jest zatem
większa i niewiele energii potrzeba, by rozsunąć elektrony (kaŜdy na "swój" orbital (rysunek
poniŜej).
http://www.mlyniec.gda.pl/~chemia/ogolna/atom.htm
(budowa i elektroujemność)
http://www.mlyniec.gda.pl/~chemia/ogolna/substancje/substancja.htm (wstęp)
I na koniec jeszcze parę ogólniejszych uwag, które mogą przyczynić się do lepszego pojmowania i
łatwiejszego uczenia się chemii (i nie tylko).
KaŜda przemiana - tak reakcja chemiczna, jak i zjawisko fizyczne ("fizykochemiczne") - odbywa
się z pewnym efektem energetycznym. Jedne wiązania czy oddziaływania muszą zostać pokonane,
rozerwane (potrzeba energii) by mogły powstać nowe (odzysk energii). Zatem, czy i jak
przebiegnie zjawisko (reakcja), decydować będą etapy uwalniające lub pobierające energię. śeby
jakiś etap wymagający energii mógł zaistnieć, układ musi mieć dostęp do "zapasu" energii. Ten
zapas mógł być stworzony w poprzednim etapie, wyzwalającym energię, lub takiego zapasu nie ma
i proces się zatrzymuje. Tak więc o reakcji nie decyduje reguła, np. tlenki niemetali z wodą dają
kwas, lecz siła wiązań i oddziaływań. Dla CO2 ta reguła jest prawdziwa, dla SiO2 - juŜ nie (siły
wiązań tworzących krystaliczną strukturę krzemionki - kwarcu na to nie pozwolą w „zwykłych”
warunkach). Tak więc wiedza chemiczna to nie znajomość regułki tylko zrozumienie istoty
zachowania się materii.
Następne przyzwyczajenie, od którego dobrze jest się wyzwolić, to traktowanie symboli związków i
samych związków jako bytów toŜsamych. Bardzo często zapominamy, Ŝe H2O to tylko symboliczny zapis cząsteczki wody, a nie woda jako taka. Informacje płynące z takiego zapisu nic nam nie
mówią o rzeczywistości i na przykład niezrozumiałym jest, dlaczego cząsteczki o masie molowej
18 tworzą ciecz a nie gaz, tak jak inne substancje o podobnej masie i strukturze - NH3 CH4 czy
H2S. Bardzo mało w czasie nauczania chemii mówi się o wpływie formy, postaci, w jakiej występują reagenty na reaktywność substancji. Wyjątkiem, zazwyczaj jedynym, jest węgiel, na przykładzie którego nieco szerzej omawia się wpływ struktury na reaktywność i właściwości chemiczne
(grafit i diament). Omawia się jednak wówczas te róŜnice z punktu widzenia alotropii pierwiastków i mało kto uogólnia i przenosi te wiadomości na inne pierwiastki i związki chemiczne. Nie
moŜna, z praktycznego punktu widzenia, kaŜdej reakcji opisywać pełną, wyczerpująca informacją,
bo zagmatwalibyśmy tak jej zapis, Ŝe stałby się całkowicie nieczytelny - ale trzeba ciągle pamiętać
o symboliczności zapisu równania reakcji.