Transplantacje komórek
i tkanek – rola układu odpornościowego
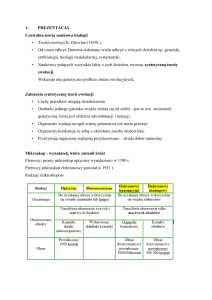
Rozwój strategii wytwarzania substytutów tkanek in vitro
typ tkanki
rola substytutu
przykład
fizyczny
biomechaniczna
kość
naczynia krwionośne
fizjologiczny
fizjologiczna
wątroba, nerka
chemiczny
produkcja rozpuszczalnych,
dyfundujących substancji
wysepki Langerhansa
kombinacja
złożona
skóra
Sposób działania implantu
fizyczne - biomechanika zależy od składu macierzy i zdolności
żywych komórek w obrębie tego implantu do utrzymania takiej
struktury- naczynia
- „wypełniacze” tkankowe - mastektomia
fizjologiczne i chemiczne - hepatocyty
złożone - skóra
Rola gospodarza w implantacji
Odrzucanie przeszczepu – reakcja niespecyficzna, wrodzona
Korzystny wpływ odpowiedzi immunologicznej – integracja z
tkanką gospodarza
Niekontrolowany stan zapalny- zwłóknienie, uszkodzenie
architektury konstruktu (enkapsulacja implantu)
Źródła komórek
Kryteria wyboru:
- łatwość pozyskiwania
- funkcjonalność
- przeżywalność w implancie
Źródła komórek
Komórki autologiczne
proliferacja in vitro – krytyczny czas oczekiwania na kmórki
biopsja tkanki pacjenta, namnożenie poza organizmem, reimplantacja
-
aktywowanie zasiedlania nośnika in vivo
manipulacja in vivo czynnikami mobilizującymi właściwe komórki do migracji
w obszar implantu
-
Źródła komórek
Komórki allogeniczne – bankowanie komórek
wystandaryzowanie źródło komórek
- unieśmiertelnione linie komórkowe
możliwość modyfikacji genetycznych, często utrata zdolności do różnicowania,
niektóre cechy komórek nowotworowych – bezpieczeństwo stosowania
Źródła komórek
Komórki ksenogeniczne
Komórki macierzyste
embrionalne
izolowane z dojrzałego organizmu
izolowane z krwi pępowinowej
Komórka macierzysta
zdolność do nieograniczonych podziałów
daje początek co najmniej jednemu typowi zróżnicowanych
komórek
Ektoderma
Gastrulacja
Mezoderma
Endoderma
Tkanka nerwowa / NSCs
Skóra / SSCs
HSCs, MSCs
Szpik kostny i krew /
tkankoweSCs
Mięśnie i kości/
narządowo-specyficzneSCs
Płuca, wątroba, trzustka /
jelitoweSCs
Przełyk, żołądek, jelito/
Embrionalne
komórki macierzyste
Pierwotne komórki
rozrodcze
Mezoderma
Tkanka nerwowa
Skóra
Szpik kostny i krew
Mięśnie i kości
Endoderma
Płuca,wątroba, trzustka
Przełyk, żołądek, jelito
Ektoderma
Gastrulacja
Embrionalne
komórki macierzyste
Pierwotne komórki rozrodcze
NSCs/ SSCs
Multipotencjalne komórki macierzyste
HSCs/MSCs/tkankoweSCs
NarządoweSCs/jelitoweSCs
totipotencjalne
komórki zygoty
pluripotencjalne
komórki zarodkowe
pluripotencjalne
zarodkowe
komórki rozrodcze
multipotencjalne
komórki macierzyste
multipotencjalne
komórki macierzyste
tkankowo-specyficzne
organy i tkanki
komórki macierzyste
układu krwiotwórczego
komórki macierzyste
centralnego układu nerwowego
komórki macierzyste
skóry
komórki macierzyste
mięśni
gonady
Pluripotencjalne komórki
wewnętrznej masy komórkowej ludzkiej blastocysty
-zdolne do różnicowania w komórki z 3 warstw germinalnych
- różnicują in vitro pod nieobecność czynników wzrostu warunkujących samoodnawianie
komórek macierzystych
- niski poziom spontanicznego różnicowania podczas pasaży
- aktywność alkalicznej fosfatazy
- markery powierzchniowe: SSEA-3(stage specyfic embryonic antigen) SSEA-4, TRA-1-60,
TRA-1-81, GCTM-2
- ekspresja telomerazy
- ekspresja czynnika transkrypcyjnego Oct4 regulującego ekspresję genów
Charakterystyka
embrionalnych komórek macierzystych
niezdefiniowany potencjał proliferacyjny
stabilny diploidalny kariotyp
zdolność do wzrostu klonalnego
formowanie potworniaków
wielokierunkowe różnicowanie in vitro
możliwość manipulacji genetycznych
James A. Thomson, Univ. Wisconsin
John D. Gearhart, Roger Pedersen, John Hopkins Univ.
Gerard Bain i David I Gottlieb, Washington Univ.
School of Medicine
Meri Firpo, Gordon Keller’s Laboratory
Loren J. Field, Indiana Univ.
Terrence Deacon, Harvard Medical School
Embrionalne komórki macierzyste - sektor komercyjny
GERON
PLURION
INFIGEN
Advanced Cell Technology
Origen Therapeutics
Stem Cell Sciences
MIDAS
AVIGENICS
Biotechnology
Rsrch&Development
Melno Park, Calif.
White Plains, New York
DeForest, Wisc.
Worcester, Mass.
San Francisco, Calif.
Monash, Australia
North Grafton, Mass.
Athens, Georgia
Peoria, III.
ludzkie, małpie
ludzkie
bydlęce
bydlęce, świńskie,
ludzkie
kurze, bydlęce
świńskie, szczurze
świńskie
kurze
świńskie
Days
Embryonic stem
(ESC) cells
cultivated
on feeder layer
d0
Cultivation
of ESC in
Formation of
hanging drops
embryoid bodies
d3
Transfer of
plates
d5
Plating
embryoid bodies
and
cultivation
to bacteriological
in suspension
of embryoid bodies
day 5 and 7)
into endo
mesodermal cells
d5 + 16
( between
- , ecto - and
Perspektywy badań komórek macierzystych
Badanie rozwoju,
kontroli genów
Badanie leków,
testy cytotoksyczności
Pluripotencjalne komórki macierzyste
w hodowli in vitro
Komórki/tkanki dla celów terapeutycznych
szpik kostny
komórki nerwowe
komórki mięśnia
serca
komórki trzustki
w dojrzałym organizmie tkankowo swoiste komórki macierzyste
posiadają zdolność do różnicowania w komórki tego narządu
lub tkanki, dla której stanowią tzw. pulę komórek rezerwowych
komórki macierzyste obecne w różnych narządach
mogą różnicować w komórki innych tkanek –
wykazywać tzw. plastyczność
alternatywna teoria tłumacząca plastyczność współzawodnictwo o wspólne nisze w tkankach
Źródła somatycznych komórek macierzystych
Szpik kostny – hematopoetyczne komórki macierzyste, mezenchymalne
komórki macierzyste
Skóra– epidermalne komórki macierzyste, komórki macierzyste mieszka
włosowego
Mięśnie szkieletowe – komórki satelitarne, komórki macierzyste mięśnia
Żołądek – komórki macierzyste nabłonka
Serce– komórki macierzyste kardiomiocytów
Mózg – neuronalne komórki macierzyste
Wątroba- komórki owalne
Schofield 1978 –
zaproponował hipotezę występowania „niszy” jako fizjologicznie
ograniczonego mikrośrodowiska (komórki, macierz, sygnały) regulujące
i chroniącego komórki macierzyste
Nisze warunkują właściwości komórek macierzystych
i przejściowo namnażających się
skóra
nabłonek
jelita
zarodek
szpik
kostny
tkankowo-specyficzne
komórki macierzyste
embrionalne
komórki
macierzyste
przejściowo
namnażające się
komórki
Kontrola transdukcji
sygnału w niszy
proliferacja
terminalnie
zróżnicowane
komórki
różnicowanie
Figure 1. Stem cell hierarchy
Rizvi, A. Z. et al. Stem Cells 2005;23:150-165
Copyright ©2005 AlphaMed Press
Figure 2. Rapidly renewing stem cell niches
Rizvi, A. Z. et al. Stem Cells 2005;23:150-165
Copyright ©2005 AlphaMed Press
Standaryzacja hodowli komórek do
przeszczepów
1. Liczenie wyizolowanych komórek, testy żywotności, wydajność tworzenia kolonii
(liczba kolonii utworzonychx100/liczba wysianych komórek)- %CFE
2. Identyfikacja komórek- analiza morfologiczna (mikroskopia elektronowa), antygeny
markerowe – metoda immunologiczna, kariotypowanie
3. Monitorowanie kontaminacji:
Sprawdzenie materiału do izolacji
Monitoring w trakcie hodowli
Źródła zakażeń:
tkanka
Niewłaściwa izolacja
W trakcie hodowli
Z materiałów stosowanych do hodowli
Ze środowiska
Niewłaściwy układ hodowlany
Immunologia nie autologicznych komórek
Profesjonalne i nieprofesjonalne komórki prezentujące antygeny
MHCII i białka kostymulujące B7 i CD40
Bezpieczeństwo stosowania komórek nie autologicznych :
Badanie komórek donorowych na obecność:
wirusa HIV, żółtaczki, adenowirusy, badania kariotypu,
tumorogenność, zmiany fenotypowe
IMMUNOMODULACJA
Projektowanie tkanek i organów
- eliminacja komórek limfoidalnych dawcy
- maskowanie lub eliminacja antygenów odpowiadających
za reakcję immunologiczną
IMMUNOMODULACJA
Projektowanie tkanek i organów /modyfikacja antygenów
komórek donorowych/
Źródła koncepcji projektowania tkanek:
Spits et al. Science 1986 „Alloantigen recognition is preceded by nonspecific ahhesion of
cytotoxic T cells and target cells”
kompleks MHC I na powierzchni komórek przeszczepianych (allo- lub
kseno-) jest zaangażowany w adhezję i aktywację limfocytów T
cytotoksycznych
Badania nad projektowaniem tkanek
Maskowanie przeciwciałami
antygen MHC I maskowany fragmentami F(ab’)2
- cukrzyca
- choroby neurodegeneracyjne – choroba Parkinsona i pląsawica Huntingtona
Badania nad projektowaniem tkanek
Maskowanie przeciwciałami
Dodawanie genów
Usuwanie RNA
Usuwanie enzymatyczne (papaina)
Usunięcie lub maskowanie MHC I - mechanizmy
przetrwania przeszczepu
delecja b2-mikroglobuliny
Odtwarzanie na powierzchni komórek dawcy antygenów
MHC I z wykorzystaniem b2-mikroglobuliny biorcy- ochrona
przed komórkami NK, powodującymi lizę komórek bez MHC I
IMMUNOIZOLACJA – terapia biohybrydowa
enkapsulacja
technologia
- rodzaje kapsuł (mikro-, makro-)
- komórki stosowane do enkapsulacji
Próby kliniczne
Cukrzyca - implantacja komórek wysp trzustkowych w
kapsułach alginianowych
Próby kliniczne
Cukrzyca
Chroniczny ból
ALS (amyotrophic lateral sclerosis) – stwardnienie
zanikowe boczne
Wyzwania inżynierii w rozwoju narzędzia
immunoizolacji
Dostarczenie tkanek z z hodowli pierwotnej bądź komórkowej
Ochrona przed immunologicznym odrzutem przeszczepu
Utrzymanie żywotności komórek i ich funkcji
gradient O2
Wyspy komórek
Langerhansa
błona
immunoizolacyjna
O2
tkanka
komórki
białka insulina metabolity:
Kwas mlekowy
CO2
H+
Utrzymanie żywotności komórek i ich funkcji
dostarczanie składników odżywczych i tlenu
Preferowane miejsca implantacji wysp
trzustkowych:
jama otrzewnej
jama opłucnej
wątroba