Podstawy Fizyki
Wykład II
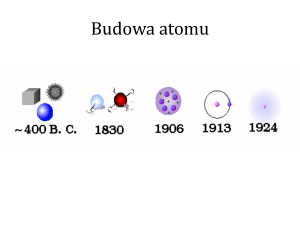
Model Bohra atomu
Rzeszów, 2011r.
Plan wykładu
1. Model Bohra atomu:
– serie widmowe atomów;
– postulaty Bohra;
– kwantowanie energii;
– orbity bohrowskie.
2. Zjawisko Comptona:
– rozpraszanie fotonu na elektronie;
– comptonowska długość fali elektronu.
2
Serie widmowe atomów
Do roku 1913 w fizyce do opisu atomu stosowano
model Rutherforda. Model ten miał jednak dość
poważne braki:
1. Nie potrafił wyjaśnić struktury promieniowania
atomów :
1 1
1
const 2 2
n1 n2
2. Nie potrafił wyjaśnić stabilności atomów –
elektron po czasie rzędu 10-11s powinien „spaść”
na jądro na skutek wypromieniowania energii.
Serie widmowe atomów
Serie widmowe atomów
Serie widmowe atomów
Znane do roku 1913 fakty doświadczalne
dotyczące serii widmowych atomu wodoru:
1. W 1885r. Balmer podał wzór empiryczny
n
3646 2
A , n 3, 4, 5, ...
n 4
2. W 1890r. Rydberg przeprowadził serię
eksperymentów poświęconych widmom
atomowym. Korzystał on z pojęcia liczb falowych
1
1 1 n 3, 4, ....
RH 2 2
1
2 n RH 10967757 .6 m
2
Serie widmowe atomów
3. Dla atomów pierwiastków alkalicznych:
1
1
1
R
2
2
m a n b
gdzie R to stała Rydberga dla danego pierwiastka,
zaś a i b są stałymi dla poszczególnych serii.
4. W 1908r. Ritz sformułował zasadę kombinacji
(tzw. zasada kombinacji Rydberga-Ritza):
Liczby falowe dowolnych linii spektralnych mogą być wyrażone
jako różnice odpowiednich termów, które z kolei przez
kombinację z innymi termami służyć mogą do obliczania liczb
falowych innych linii tego samego widma.
Model atomu Bohra
Niels Bohr (1886-1962)
Nagroda Nobla – 1922r.
Model atomu Bohra
W 1913r. Niels Bohr opublikował słynne postulaty
dotyczące budowy atomu:
1. Elektrony w atomie poruszają się po orbitach
o promieniu r takich, aby ich moment pędu był
całkowitą wielokrotnością stałej Plancka
(podzielonej przez 2)
h
mvr n
n
2
2. Elektrony poruszając się po orbitach nie
wypromieniowują energii (stany stacjonarne).
Model atomu Bohra
3. Elektrony mogą dokonywać przejść (nieciągłych)
z jednej (dozwolonej) orbity na drugą
wypromieniowując różnicę energii w postaci
fotonu o częstości
E E
h
4. Atom może absorbować energię, dzięki czemu
jego elektrony „przechodzą” na wyższą
(energetycznie) orbitę.
Model atomu Bohra
Wyniki teorii Bohra (atom wodoropodobny):
- promień n-tej orbity atomu:
0h 2 2
rn
n
2
me Z
- energia dla n-tej orbity:
4
2
me Z 1
En 2 2 2
8 0 h n
- liczba falowa:
1
1
2 1
RZ 2 2
n1 n2
me 4
R 3 2 stała Rydberga
8h c 0
Serie widmowe atomów
Efekt Comptona
Zgodnie z fizyką „klasyczną” fala
elektromagnetyczna padając na np. metalową
folię wywołuje drgania elektronów, które stają się
źródłem wtórnego promieniowania. Intensywność
promieniowania wtórnego zmienia się jak
I ~ 1 cos
i nie zależy od długości fali padającego
promieniowania.
2
Efekt Comptona
Arthur Compton zauważył, że promieniowanie
rozproszone pod wybranym kątem składa się
z dwóch składników. Pierwszego o długości fali
zgodnej z długością fali promieniowania
padającego, oraz z drugiego – o długości fali
przesuniętej w stosunku do długości fali
promieniowania padającego o wartość zależną od
kąta .
Compton wyjaśnił ten efekt zakładając, że światło
to strumień cząstek o energii h.
Efekt Comptona
0.7078Å
0.7314Å
1
0
foton
padający
Spektrum promieniowania rozproszonego
przez grafit. Długość fali promieniowania
padającego: 0.7078Å.
foton
rozproszony
odrzucony
elektron
Efekt Comptona
Wyniki teorii Comptona:
1 0 C 1 cos
gdzie Comptonowska długość fali elektronu:
h
C
0.0243A
m0 c