Zawadzka
Alergia
Astma
P, Szczepañski
ImmunologiaM,
2006,
£ykowska-Szuber
11(3): 155-161L i wsp. Rola autoprzeciwcia³ w diagnostyce i ró¿nicowaniu
155
Rola autoprzeciwcia³ w diagnostyce i ró¿nicowaniu
nieswoistych zapaleñ jelit
The role of autoantibodies in diagnosing and identifying inflammatory
bowel diseases
PATRYCJA ZAWADZKA 1/, MIROS£AW SZCZEPAÑSKI 2/, LILIANA £YKOWSKA-SZUBER 1/, HUSAM SAMARA 2/,
KRZYSZTOF LINKE 1/, JAN ¯EROMSKI 2/
1/
2/
Katedra i Klinika Gastroenterologii, ¯ywienia Cz³owieka i Chorób Wewnêtrznych Akademii Medycznej im. Karola
Marcinkowskiego w Poznaniu
Katedra i Zak³ad Immunologii Klinicznej Akademii Medycznej im. Karola Marcinkowskiego w Poznaniu
Streszczenie
Summary
Wprowadzenie. Nieswoiste zapalenia jelit to przewlek³e zapalne
choroby przewodu pokarmowego, do których nale¿¹ wrzodziej¹ce
zapalenie jelita grubego oraz choroba Leniowskiego-Crohna. W oko³o
5 do 15% przypadków trudno jest postawiæ rozpoznanie na podstawie
przyjêtych kryteriów klinicznych oraz badañ obrazowych
i histologicznych. Markerami serologicznymi we wrzodziej¹cym
zapaleniu jelita grubego s¹ przeciwcia³a przeciw cytoplazmie neurtofili
z oko³oj¹drowym typem wiecenia (pANCA) oraz przeciwcia³a przeciw
komórkom kubkowym jelita (GAB), natomiast w chorobie
Leniowskiego-Crohna przeciwcia³a przeciw Saccharomyces
cerevisiae (ASCA) oraz przeciw czêci zewn¹trzwydzielniczej
trzustki (PAB).
Introduction. Inflammatory bowel diseases are chronic diseases of
gastrointestinal tract which include ulcerative colitis and Crohns
disease. About 5 to 15% of the cases are difficult to diagnose using
conventional clinical, radiological, endoscopic and microscopic criteria.
Antibodies pANCA and GAB are serologic markers of ulcerative colitis,
while antibodies ASCA and PAB are characteristic for Crohns disease.
Cel pracy. Celem pracy jest ocena wartoci diagnostycznej
autoprzeciwcia³ pANCA, GAB, ASCA oraz PAB w rozpoznawaniu
i ró¿nicowaniu nieswoistych zapaleñ jelit.
Materia³ i metody. Badanie przeprowadzono u 20 chorych
z wrzodziej¹cym zapaleniem jelita grubego, 20 chorych z chorob¹
Leniowskiego-Crohna, a grupê kontroln¹ stanowi³o 20 zdrowych
ochotników. Autoprzeciwcia³a oznaczano metod¹ immunofluorescencji
poredniej.
Wyniki. We wrzodziej¹cym zapaleniu jelita grubego pANCA
wystêpowa³y u 65% chorych, a GAB u 25% chorych. W chorobie
Leniowskiego-Crohna ASCA wystêpowa³y w 65% chorych, a PAB
u 50% chorych. We wrzodziej¹cym zapaleniu jelita grubego czu³oæ
i swoistoæ pANCA wynosi³a odpowiednio 65% i 90% natomiast GAB
25% i 95%. W chorobie Leniowskiego-Crohna czu³oæ i swoistoæ
ASCA wynosi³a odpowiednio 68% i 95%, natomiast PAB 47% i 95%.
Wnioski. Oznaczanie przeciwcia³ pANCA, ASCA, PAB oraz GAB
³¹cznie stanowiæ mo¿e panel serologiczny przydatny w diagnostyce
i ró¿nicowaniu nieswoistych zapaleñ jelit.
Aim of the study. Evaluate the role of pANCA, GAB, ASCA and PAB
in diagnosing and identifying inflammatory bowel diseases.
Material and methods. Serum samples were obtained from 20
patients with diagnosed Crohns disease, 20 patients with ulcerative
colitis and 20 healthy controls. Autoantibodies were assessed using
the indirect immunofluorescence technique.
Results. In ulcerative colitis, pANCA were present in 65% and GAB
in 25% patients. In Crohns disease, ASCA were present in 65% and
PAB in 50% subjects. In ulcerative colitis the sensitivity and specificity
of pANCA was 65 and 95% and that of GAB was 25% and 95%
respectively. In Crohns disease, the sensitivity and specificity of ASCA
was 68% and 95% and that of PAB was 47% and 95%, respectively.
Conclusions. Assessment of pANCA, GAB, ASCA and PAB together
can be used as a serologic panel for diagnosing and identifying
inflammatory bowel diseases.
Key words: ulcerative colitis, Crohns disease, autoatibodies
pANCA, GAB, ASCA, PAB
S³owa kluczowe: wrzodziej¹ce zapalenie jelita grubego, choroba
Leniowskiego-Crohna, przeciwcia³a pANCA, ASCA, GAB, PAB
© Alergia Astma Immunologia, 2006, 11(3): 155-161
Adres do korespondencji / Address for correspondence
www.mediton.pl/aai
Patrycja Zawadzka
Katedra i Klinika Gastroenterologii, ¯ywienia Cz³owieka i Chorób
Wewnêtrznych Akademii Medycznej im. Karola Marcinkowskiego
w Poznaniu, SPSK nr 2 ul. Przybyszewskiego 49, 60-355Poznañ
tel. (61) 869 13 43, fax (61) 869 16 86
e-mail: [email protected]
Nades³ano: 10.01.2006
Zakwalifikowano do druku: 12.07.2006
156
WSTÊP
Nieswoiste zapalenia jelit (nzj) to przewlek³e choroby
zapalne przewodu pokarmowego przebiegaj¹ce z okresami remisji i zaostrzeñ, do których zalicza siê chorobê
Leniowskiego-Crohna (chL-C) oraz wrzodziej¹ce zapalenie jelita grubego (wzjg). Mimo znacznych postêpów
w badaniach nad patogenez¹ nzj ich etiologia nadal pozostaje niejasna [1-7]. Wykazano, ¿e wiele zwi¹zków wchodz¹cych w sk³ad ciany komórkowej bakterii jelitowych
mo¿e pe³niæ rolê antygenów lub wp³ywa moduluj¹co na
uk³ad immunologiczny b³ony luzowej przewodu pokarmowego [3,7]. Wiele badañ wskazuje, ¿e u pod³o¿a nzj
le¿¹ zaburzenia odpowiedzi uk³adu immunologicznego jelit [8,9]. U chorych z nzj dochodzi do produkcji autoprzeciwcia³ skierowanych przeciwko komórkom wystêpuj¹cym w nab³onku jelitowym, a których obecnoæ stwierdza siê w surowicy krwi i b³onie luzowej jelit [10]. Nieprawid³owa supresja komórek autoreaktywnych oraz niew³aciwa aktywacja limfocytów B i T le¿y u podstawy
utrzymywania siê autoprzeciwcia³ i jest charakterystyczna dla chorób autoimmunologicznych [6,7,10].
W surowicy chorych na wzjg wykrywa siê m.in. przeciwcia³a przeciwko cytoplazmie neutrofili z oko³oj¹drowym typem wiecenia (perinuclear anti-neutrophil cytoplasmic antibodies pANCA) oraz przeciwcia³a przeciwko komórkom kubkowym jelita (goblet cells antibodies GAB), natomiast u pacjentów z chL-C przeciwcia³a przeciwko Saccharomyces cerevisiae (anti-Saccharomyces cerevisiae antibodies ASCA) oraz przeciwcia³a przeciwko czêci zewn¹trzwydzielniczej trzustki
(pancreatic exocrine antibodies PAB) [1,6,7,11]. Sugeruje siê, ¿e u chorych z nzj wystêpuje nieprawid³owa
odpowied immunologiczna skierowana przeciwko endogennej florze wystêpuj¹cej w przewodzie pokarmowym.
Zwi¹zki wchodz¹ce w sk³ad ciany komórkowej lub wydzielane przez bakterie jelitowe mog¹ pe³niæ funkcjê antygenów dla wielu przeciwcia³ oraz mog¹ wp³ywaæ moduluj¹co na uk³ad immunologiczny b³ony luzowej jelit [7].
W chL-C wykrywa siê przeciwcia³a przeciwko dro¿d¿om
Saccharomyces cerevisiae, Mycobacterium, Bacteroides, Listeria oraz Escherichia coli, natomiast u chorych na wzjg stwierdza siê przeciwcia³a pANCA przeciwko Bacteroides ceccae, Mycobacterium oraz Pseudomonas [1,6,11,12]. Targan i wsp. wykazali, ¿e przeciwcia³a pANCA s¹ produkowane przez limfocyty B obecne w lamina propria b³ony luzowej jelita i s¹ markerem
serologicznym odpowiedzi immunologicznej luzówki jelit
we wzjg [13]. Przeciwcia³a ASCA charakteryzuj¹ siê
wysok¹ swoistoci¹ dla chL-C, dlatego uznano je za marker serologiczny tej choroby. Przez wiele lat budowa antygenu przeciwko któremu skierowane s¹ przeciwcia³a
ASCA pozostawa³a nieznana. Dopiero wykrycie cz¹steczki PPM (phosphopeptidomannan) zbudowanej z polimerów mannozowych po³¹czonych z czêci¹ bia³kow¹
w cianie komórkowej dro¿d¿y Saccharomyces cerevi-
Alergia Astma Immunologia 2006, 11(3): 155-161
siae i jej dalsze badania chemiczne ujawni³y, ¿e determinanty antygenowe dla przeciwcia³ ASCA sk³adaj¹ siê z polisacharydów [14].
U chorych na nzj stwierdza siê nie tylko przeciwcia³a
przeciwko florze komensalnej, ale równie¿ przeciwko
w³asnym komórkom i tkankom. S¹ to przeciwcia³a GAB
wystêpuj¹ce we wzjg oraz przeciwcia³a PAB w chL-C
[1,10,12,15]. Mechanizm immunologiczny doprowadzaj¹cy do powstania przeciwcia³ GAB i PAB pozostaje niejasny. Wykazano, ¿e antygenem, z którym reaguj¹ przeciwcia³a PAB mo¿e byæ bia³ko zlokalizowane pocz¹tkowo w cytozolu komórek pêcherzyków trzustkowych,
a nastêpnie wydzielane z sokiem trzustkowym [15,16]. Nie
wykazano zwi¹zku miêdzy obecnoci¹ przeciwcia³ PAB
a uszkodzeniem czêci egzokrynnej trzustki [15,17]. Hahm
i wsp. wykazali, ¿e przeciwcia³a GAB reaguj¹ z mukopolisacharydami pochodz¹cymi z komórek kubkowych jelita grubego [10].
Mimo obecnoci autoprzeciwcia³ oraz autoreaktywnych limfocytów u chorych na nzj wydaje siê, ¿e uszkodzenie ciany jelita nie jest spowodowane bezporednio
przez reakcje immunologiczne zale¿ne od autoprzeciwcia³. Wiele badañ potwierdza fakt, ¿e odpowied autoimmunologiczna w nzj jest spowodowana poprzez reakcje
krzy¿owe z antygenami wystêpuj¹cymi w wietle jelita [15].
Wspó³czesna diagnostyka i ró¿nicowanie nzj opiera
siê na objawach klinicznych oraz charakterystycznych
zmianach morfologicznych ocenianych w badaniach endoskopowych i radiologicznych. Istotne znaczenie w potwierdzeniu rozpoznania ma badanie histopatologiczne
wycinka z jelita. Jednak u 5 do 15% chorych trudno jest
jednoznacznie postawiæ diagnozê, a co za tym idzie wdro¿yæ leczenie. S¹ to przypadki przebiegaj¹ce z objawami
nietypowymi lub sk¹poobjawowe, u których wynik badañ
endoskopowych, histologicznych i obrazowych pozostaje
niejednoznaczny. Trudnoci diagnostyczne nastrêcza równie¿ tzw. colitis nondeterminata, kiedy w obrazie mikroskopowym nie ma pe³nych wyk³adników wzjg czy chL-C
[18,19].
Celem pracy by³a ocena wartoci diagnostycznej autoprzeciwcia³ pANCA, GAB, ASCA oraz PAB w rozpoznawaniu i ró¿nicowaniu nzj. Oceniano czu³oæ i swoistoæ
autoprzeciwcia³ dla chL-C i wzjg. W badaniu sprawdzano równie¿ czy istnieje zale¿noæ miêdzy obecnoci¹ autoprzeciwcia³ a wiekiem i p³ci¹ chorych oraz aktywnoci¹ choroby i lokalizacj¹ zmian zapalnych w obrêbie przewodu pokarmowego.
MATERIA£ I METODY
Pacjenci
W badaniu bra³o udzia³ 40 chorych na nzj, w tym 20
chorych na wzjg i 20 pacjentów z chL-C. W grupie chorych na wzjg by³o 12 kobiet w wieku 27 do 74 lat (rednia
wieku 52 lata) i 8 mê¿czyzn w wieku 24 do 77 lat (rednia
Zawadzka P, Szczepañski M, £ykowska-Szuber L i wsp. Rola autoprzeciwcia³ w diagnostyce i ró¿nicowaniu
157
wieku 48 lat). U chorych na wzjg aktywnoæ choroby
oceniano za pomoc¹ skali Truelovea i Wittsa, a zasiêg
zmian oceniano na podstawie wlewu doodbytniczego
dwukontrastowego i/lub kolonoskopii. W grupie pacjentów z chL-C by³o 8 kobiet w wieku 20 do 56 lat (rednia
wieku 35 lat) oraz 12 mê¿czyzn w wieku 21 do 40 (rednia wieku 31 lat). U pacjentów z chL-C aktywnoæ choroby oceniano za pomoc¹ skali CDAI (Crohns Disease
Activity Index), a lokalizacjê zmian oceniano na podstawie pasa¿u jelita cienkiego oraz kolonoskopii. U wszystkich chorych rozpoznanie postawione zosta³o na podstawie przyjêtych kryteriów klinicznych, laboratoryjnych,
endoskopowych i radiologicznych. W ka¿dym przypadku
rozpoznanie potwierdzono histopatologicznie. Grupê kontroln¹ stanowi³o 20 zdrowych ochotników (honorowi dawcy krwi).
Krew obwodow¹ pobierano na skrzep, nastêpnie krew
odwirowano, a uzyskan¹ surowicê przechowywano
w temperaturze -70°C do czasu wykonania badañ immunofluorescencyjnych.
Obecnoæ autoprzeciwcia³ wykrywano przy zastosowaniu immunofluorescencji poredniej. W tym celu u¿yto
mozaiki tkankowe firmy EUROIMMUN (Lubeck, Germany), w sk³ad których wchodzi³y mro¿akowe skrawki
z ma³piej w¹troby, trzustki, jelita grubego oraz rozmazy
ludzkich granulocytów utrwalonych etanolem, a tak¿e rozmazy z Saccharomyces cerevisiae. Stosowano wtórne
Tabela I. Rodzaje u¿ytych tkanek i wykrywane na nich autoprzeciwcia³a
Tkanka
Wykrywane autoprzeciwcia³a:
Rozcieñczenie
surowicy
W¹troba ma³py
Przeciwj¹drowe (do ró¿nicowania
1:10
z pANCA)
Trzustka ma³py
Przeciw wyspom trzustki (PAB)
1:10
Jelito grube ma³py Przeciw komórkom kubkowym jelita
1:10
(GAB)
Granulocyty ludzkie Przeciw mieloperoksydazie (pANCA) 1:10
S. cerevisiae
Przeciw Saccharomyces cerevisiae
1:100
(ASCA)
przeciwcia³a mysie anty-ludzkie znakowane fluorescein¹.
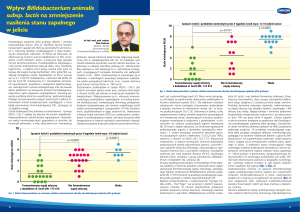
Preparaty oceniono jakociowo w mikroskopie fluorescencyjnym (ryc. 1). W tabeli I przedstawiono u¿yte tkanki
i wykrywane na nich autoprzeciwcia³a, a tak¿e rozcieñczenie badanych surowic.
Czu³oæ zdefiniowano jako zdolnoæ wykrywania
wszystkich osób istotnie chorych (dodatni wynik testu
u osób chorych), natomiast swoistoæ zdefiniowano jako
zdolnoæ wykrywania osób ca³kowicie zdrowych (ujemny wynik testu u osób zdrowych).
Do oceny statystycznej zale¿noci miêdzy wystêpowaniem autoprzeciwcia³ a parametrami klinicznymi zastosowano test χ2 oraz test Fishera. Przyjêto poziom istotnoci p≤0,05.
WYNIKI
W grupie chorych na wzjg stwierdzono rzut lekki
u 4 pacjentów, rzut rednio-ciê¿ki u 6 pacjentów oraz u rzut
ciê¿ki u 10 chorych. W grupie tej zmiany zapalne obejmowa³y odbytnicê i esicê u 5 pacjentów, lew¹ po³owê jelita
grubego (do zagiêcia ledzionowego) u 10 chorych oraz
praw¹ po³owê jelita grubego (powy¿ej zagiêcia ledzionowego) u 5 chorych. W grupie pacjentów z chL-C
stwierdzono rzut lekki u 4 chorych, rzut rednio-ciê¿ki u 10
chorych oraz rzut ciê¿ki u 6 chorych. W grupie tej stwierdzono zajêcie koñcowego odcinka jelita krêtego u 8 chorych, zajêcie tylko jelita grubego u 7 chorych oraz lokalizacjê w obrêbie jelita cienkiego i jelita grubego (koñcowy
odcinek jelita krêtego oraz zmiany w prawej po³owie jelita grubego) u 7 pacjentów.
Wystêpowanie autoprzeciwcia³ pANCA, ASCA,
GAB oraz PAB w surowicy chorych na wzjg, chL-C oraz
w grupie kontrolnej przedstawiaj¹ ryciny 2-5.
We wzjg czu³oæ i swoistoæ przeciwcia³ pANCA
wynosi³a
odpowiednio 65% i 90% natomiast przeciwcia³
Ryc. 1. Obecnoæ autoprzeciwcia³ wykazana metod¹ immunoGAB 25% i 95%. W grupie chorych na wzjg obecnoæ
fluorescencji poredniej
przeciwcia³ pANCA przy jednoczesnym braku przeciwA przeciwcia³a przeciw cytoplazmie neutrofili (pANCA);
cia³ ASCA (pANCA+/ASCA-) stwierdzono u 12 chorych
B przeciwcia³a przeciw Saccharomyces cerevisiae (ASCA);
C przeciwcia³a przeciw czêci zewn¹trzwydzielniczej trzustki (60%). Czu³oæ i swoistoæ kombinacji pANCA+/ASCA(PAB); D przeciwcia³a przeciw komórkom kubkowym jelita u tych pacjentów wynosi³a 100%. W grupie tej jednocze(GAB)
sna obecnoæ przeciwcia³ pANCA i GAB oraz brak ASCA
158
Alergia Astma Immunologia 2006, 11(3): 155-161
(pANCA+/GAB+/ASCA-) stwierdzono zaledwie
u 3 chorych (15%). W chL-C czu³oæ i swoistoæ przeciwcia³ ASCA wynosi³a odpowiednio 68% i 95%, natomiast przeciwcia³ PAB 47% i 95%. W grupie pacjentów
z chL-C obecnoæ przeciwcia³ ASCA przy jednoczesnym
braku przeciwcia³ pANCA (ASCA+/pANCA-) wykazano u 12 chorych (60%). Czu³oæ i swoistoæ kombinacji
ASCA+/pANCA- u tych chorych wynosi³a odpowiednio
92% i 100%. W grupie pacjentów z chL-C jednoczesn¹
obecnoæ przeciwcia³ ASCA i PAB oraz brak pANCA
(ASCA+/PAB+/pANCA-) stwierdzono u 6 chorych
(30%). Czu³oæ i swoistoæ kombinacji ASCA+/PAB+/
pANCA- u tych pacjentów wynosi³a odpowiednio 75%
oraz 100%.
Nie wykazano korelacji miêdzy p³ci¹ chorych a wystêpowaniem autoprzeciwcia³ we wzjg oraz chL-C.
Nie wykazano korelacji miêdzy wiekiem chorych na
wzjg a wystêpowaniem autoprzeciwcia³. Wiek chorych
w czasie postawienia rozpoznania by³ istotnie ni¿szy u pacjentów z chL-C ASCA-negatywnych i wynosi³ 7 do 29
lat (wartoæ rednia 23 lata) w porównaniu z pacjentami
ASCA-pozytywnymi, u których wynosi³ 16-41 lat (wartoæ rednia 28,4 roku) (p<0,05).
Wykazano dodatni¹ korelacjê miêdzy aktywnoci¹
wzjg a wystêpowaniem przeciwcia³ pANCA (na granicy
istotnoci statystycznej, p=0,08), natomiast nie zaobserwowano zale¿noci miêdzy aktywnoci¹ wzjg a obecnoci¹ przeciwcia³ GAB. Nie wykazano korelacji miêdzy
wystêpowaniem przeciwcia³ ASCA oraz PAB a aktywnoci¹ chL-C.
Ryc. 2. Wystêpowanie przeciwcia³ przeciw cytoplazmie neutrofili (pANCA) w surowicy pacjentów z chorob¹ LeniowskiegoCrohna (chL-C), wrzodziej¹cym zapaleniem jelita grubego (wzjg)
oraz w grupie kontrolnej (GK)
Ryc. 4. Wystêpowanie przeciwcia³ przeciw Saccharomyces cerevisiae (ASCA) w surowicy pacjentów z chorob¹ Leniowskiego-Crohna (chL-C), wrzodziej¹cym zapaleniem jelita grubego (wzjg) oraz w grupie kontrolnej (GK)
Ryc. 3. Wystêpowanie przeciwcia³ przeciw komórkom kubkowym jelita (GAB) w surowicy pacjentów z chorob¹ Leniowskiego-Crohna (chL-C), wrzodziej¹cym zapaleniem jelita grubego (wzjg) oraz w grupie kontrolnej (GK)
Ryc. 5. Wystêpowanie przeciwcia³ przeciw czêci zewn¹trzwydzielniczej trzustki (PAB) w surowicy pacjentów z chorob¹ Leniowskiego-Crohna (chL-C), wrzodziej¹cym zapaleniem jelita
grubego (wzjg) oraz w grupie kontrolnej (GK)
DYSKUSJA
Na podstawie danych literaturowych przeciwcia³a
pANCA wystêpuj¹ w surowicy chorych z wzjg w 45 do
80%, co zgadza siê z wynikiem przeprowadzonego badania. Mog¹ one wystêpowaæ równie¿ w 5 do 10% w grupie pacjentów z chL-C, u których zmiany zlokalizowane
s¹ w jelicie grubym (tzw. ulcerative colitis-like Crohns
disease), natomiast w populacji ogólnej wystêpuj¹ od 0 do
4%, co zgadza siê z naszymi wynikami. W wielu badaniach wykazano, ¿e wystêpowanie przeciwcia³ pANCA
nie korelowa³o z wiekiem, p³ci¹, czasem trwania choroby
oraz lokalizacj¹ zmian, co potwierdzi³y wyniki naszego
badania [3,5,21,22-24]. Natomiast dane literaturowe dotycz¹ce korelacji miêdzy obecnoci¹ przeciwcia³ pANCA
w surowicy pacjentów z wzjg a aktywnoci¹ choroby s¹
Zawadzka P, Szczepañski M, £ykowska-Szuber L i wsp. Rola autoprzeciwcia³ w diagnostyce i ró¿nicowaniu
159
rozbie¿ne niektóre prace sugerowa³y taki zwi¹zek,
a niektórzy badacze go nie wykazali [5,25-27]. W naszym
badaniu stwierdzono dodatni¹ zale¿noæ miêdzy wystêpowaniem przeciwcia³ pANCA a aktywnoci¹ wzjg. Jednak korelacja ta nie by³a statystycznie istotna (na granicy
istotnoci statystycznej, p=0,08), co mo¿e wi¹zaæ siê ze
zbyt ma³¹ liczb¹ pacjentów z wzjg w podgrupach (np.
w podgrupie z rzutem lekkim by³o 4 pacjentów). Czu³oæ
przeciwcia³ pANCA we wzjg wynosi 38 do 73%, a swoistoæ 83 do 97%, co potwierdzi³ wynik przeprowadzonego przez nas badania [26-30].
Przeciwcia³a ASCA wystêpuj¹ w surowicy chorych
z chL-C w 50 do 80%, rzadko stwierdza siê ich obecnoæ
we wzjg (poni¿ej 10%), a w populacji ogólnej wystêpuj¹
od 0 do 5%, co zgadza siê z przeprowadzonymi przez nas
badaniami [5,30]. W wiêkszoci prac nie wykazano korelacji miêdzy p³ci¹, wiekiem chorych oraz lokalizacj¹ zmian
w obrêbie przewodu pokarmowego u pacjentów z chL-C
a wystêpowaniem przeciwcia³ ASCA, co zgadza siê z naszymi wynikami [4,5,15,38,39]. W jednej pracy stwierdzono dodatni¹ korelacjê miêdzy m³odym wiekiem pacjentów z chL-C w momencie rozpoznania choroby (chorzy
ACSA-pozytywni w wieku 10-59 lat, rednia 21 lat; chorzy ASCA-negatywni w wieku 15-47 lat, rednia 24 lata)
a obecnoci¹ przeciwcia³ ASCA [24]. W naszym badaniu
wykazano przeciwn¹ zale¿noæ wiek chorych w czasie
postawienia diagnozy by³ istotnie ni¿szy u pacjentów
z chL-C ASCA-negatywnych (chorzy w wieku 7-29 lat,
rednia 23 lata) w porównaniu z pacjentami ASCA-pozytywnymi, (chorzy w wieku16-41 lat, rednia 28,4 roku).
Mo¿e to t³umaczyæ fakt, i¿ w patogenezie chL-C wa¿n¹
rolê ogrywaj¹ czynniki rodowiskowe (m.in. sk³adniki pokarmowe, leki oraz sk³ad flory jelitowej), które mog¹ dzia³aæ
moduluj¹co na uk³ad immunologiczny przewodu pokarmowego oraz na produkcjê przeciwcia³ ASCA. Ponadto
stwierdzenie dodatniej zale¿noci miêdzy obecnoci¹ przeciwcia³ ASCA a starszym wiekiem pacjentów z chL-C
mo¿e byæ zwi¹zane z d³u¿szym okresem ekspozycji na
antygeny jelitowe (polisacharydy Saccharomyces cerevisiae). Dane literaturowe nie s¹ zgodne, co do zale¿noci miêdzy aktywnoci¹ chL-C a obecnoci¹ przeciwcia³
ASCA niektóre prace wykaza³y tak¹ korelacjê, a inne
nie [2-5,14,15,40,41]. W naszym badaniu nie potwierdzono takiej zale¿noci. Na podstawie danych z pimiennictwa szacuje siê, ¿e w chL-C czu³oæ przeciwcia³ ASCA
wynosi 39 do 71%, a swoistoæ oko³o 90%, co zgadza siê
z uzyskanymi przez nas wynikami [28-30,43,44,47].
Wed³ug danych literaturowych przeciwcia³a PAB
wystêpuj¹ u oko³o 40% chorych z chL-C, co potwierdzono w naszym badaniu [15-17,37,46,47]. Nie wykazano
zwi¹zku miêdzy wystêpowaniem przeciwcia³ PAB a p³ci¹,
wiekiem chorych, lokalizacj¹ zmian oraz aktywnoci¹
choroby, co równie¿ odzwierciedli³y uzyskane przez nas
wyniki [15,45]. Badanie Klebla i wsp. [15] przeprowadzone na du¿ej populacji chorych z chL-C wykaza³o wy-
sok¹ swoistoæ przeciwcia³ PAB dla tej choroby, co zgadza siê z przeprowadzonym przez nas badaniem [15].
Przeciwcia³a GAB wystêpuj¹ w oko³o 30% u pacjentów z wzjg oraz s¹ swoiste dla tej choroby, co zgadza siê
z wynikami naszego badania [15]. Przeciwcia³ GAB nie
wykryto u chorych z infekcyjnym zapaleniem jelit, zapaleniem uchy³ków czy inn¹ nie autoimmunologiczn¹ chorob¹ jelit. GAB nie s¹ wiêc wynikiem niespecyficznej reakcji immunologicznej wystêpuj¹cej w zwi¹zku z zapaleniem b³ony luzowej jelita grubego [5,10,15]. W jednej
pracy badano zwi¹zek przeciwcia³ GAB we wzjg z p³ci¹,
wiekiem chorych, zasiêgiem zmian oraz aktywnoci¹ choroby i nie wykazano takich zale¿noci, co potwierdzi³o
nasze badanie [Lawrance I i wsp, 2005].
Odpowiadaj¹c na pytanie: Czy badanie wybranych
przeciwcia³ u chorych z nzj ma wartoæ diagnostyczn¹?,
odpowied brzmi tak. Testy charakteryzuj¹ce siê nisk¹
czu³oci¹ i wysok¹ swoistoci¹ dla danych jednostek chorobowych mog¹ byæ pomocne w ich ró¿nicowaniu [15].
Natomiast parametr o wysokiej czu³oci mo¿e byæ u¿yteczny w badaniach diagnostycznych. Na podstawie przeprowadzonego badania wykazano nisk¹ czu³oæ przeciwcia³ GAB (25%) i PAB (47%) odpowiednio dla wzjg
i chL-C. Choæ czu³oæ przeciwcia³ pANCA oraz ASCA
odpowiednio dla wzjg i chL-C by³a istotnie wy¿sza (oko³o
65%) ni¿ GAB i PAB dla tych chorób, uwa¿a siê, ¿e wartoæ ta nie jest wysoka. Natomiast wykazano wysok¹
swoistoæ autoprzeciwcia³ pANCA (90%) i GAB (95%)
dla wzjg oraz ASCA i PAB (95%) dla chL-C. Oceniaj¹c
obecnoæ przeciwcia³ pANCA przy braku ASCA czu³oæ i swoistoæ testu we wzjg wzros³a do 100%. Z kolei
oceniaj¹c obecnoæ ASCA przy braku pANCA czu³oæ
testu w chL-C wzros³a do 92%, a swoistoæ do 100%.
Do³¹czenie do tej kombinacji przeciwcia³ PAB (ASCA+/
PAB+/pANCA-) spowodowa³a spadek czu³oci do 75%,
ale swoistoæ testu pozosta³a wysoka 100%, co u³atwia³o ró¿nicowanie wzjg i chL-C i zgadza³o siê z danymi
z pimiennictwa [Lawrance i wsp.]. Uwa¿a siê, ¿e w niejasnych przypadkach nzj, w których wystêpuj¹ trudnoci
w postawieniu diagnozy i zró¿nicowaniu wzjg oraz chL-C
na podstawie kryteriów klinicznych, endoskopowych, histologicznych i radiologicznych, za rozpoznaniem wzjg
przemawia stwierdzenie w surowicy krwi przeciwcia³
pANCA przy jednoczesnym braku przeciwcia³ ASCA.
Natomiast za rozpoznaniem chL-C przemawia obecnoæ
przeciwcia³ ASCA lub ASCA i PAB przy braku przeciwcia³ pANCA [15, Jaskowski i wsp.]. Rola przeciwcia³
GAB i PAB w diagnostyce odpowiednio wzjg i chL-C
pozostaje ograniczona ze wzglêdu na ich nisk¹ czu³oæ.
Ich rola jako markera serologicznego w ró¿nicowaniu nzj
mimo wysokiej swoistoci równie¿ wydaje siê niewielka
ze wzglêdu na rzadkie wystêpowanie tych przeciwcia³
w odpowiednich podtypach nzj (GAB u oko³o 30% chorych na wzjg, a PAB u oko³o 40% chorych na chL-C).
Testy serologiczne zwiêkszaj¹ szansê prawid³owego
160
rozpoznania oraz minimalizuj¹ zastosowanie badañ inwazyjnych u chorych prezentuj¹cych niespecyficzne objawy sugeruj¹ce nzj. Uwa¿a siê, ¿e testy serologiczne maj¹
uzasadnienie w tych przypadkach nzj, w których wystê-
Alergia Astma Immunologia 2006, 11(3): 155-161
puj¹ trudnoci w postawieniu w³aciwego rozpoznania na
podstawie przyjêtych kryteriów oraz, ¿e potrzebne s¹ dalsze badania dotycz¹ce oznaczania autoprzeciwcia³ w nzj
[20, Canai R i wsp 2006].
Pimiennictwo
1. Nakamura R, Matsutani M, Barry M. Advances in clinical
laboratory tests for inflammatory bowel disease. Clin Chim Acta.
2003; 335(1-2): 9-20.
2. Peeters M, Cortot A, Vermeire S i wsp. Familial and sporadic
inflammatory bowel disease: different entities? Inflamm Bowel
Dis. 2000; 6(4): 314-320.
3. Sutton C., Yang H., Li Z. i wsp.: Familial expression of antiSaccharomyces cerevisiae mannan antibodies in affected and
unaffected relatives of patients with Crohns disease. Gut. 2000;
46: 58-63.
4. Annese V, Lombardi G, Perri F i wsp. Variants of CARD15 are
associated with an aggressive clinical course of Crohns diseasean IG-IBD study. Am J Gastroenterol. 2005; 100(1):84-92.
5. Lerner A, Shoenfeld Y. Serological markers in inflammatory bowel
disease: the pros and cons. Eur J Gastroenterol Hepatol. 2002;
14(2): 103-105.
6. Wen Z, Fiocchi C. Inflammatory bowel disease: autoimmune or
immune-mediated pathogenesis? Clin Dev Immunol. 2004;
11(3-4): 195-204.
7. Cohavy O, Harth G, Horwitz M i wsp. Identification of a novel
Mycobacterial histon H1 homologe (HupB) as an antigenic target
of pANCA monoclonal antibody and serum immunoglobulin A
from patients with Crohns disease. Inf and Immun. 1999; 67(12):
6510-6517.
8. Balish E, Warner T. Enterococcus faecalis induces inflammatory
bowel disease in interleukin-10 knockout mice. Am J Pathol.
2002, 160: 2253-2257.
9. Kullberg M, Ward J, Gorelick P i wsp. Helicobacter hepaticus
triggers colitis in specific-pathogen-free Interleukin-10 (IL-10)deficient mice through an IL-12-and gamma interferon-dependent
mechanism. Inf and Immun. 1998; 66(11): 5157-5166.
10. Hahm K, Im Y, Parks S i wsp. Loss of transforming growth
factor â signalling in the intestine contributes to tissue injury in
inflammatory bowel disease. Gut. 2001; 49: 190-198.
11. Nakamura R, Barry M. Serologic markers in inflammatory bowel
disease (IBD). Med Lab Obs. 2001; 33(11): 8-15.
12. Beaven S, Abreu M. Biomarkers in inflammatory bowel disease.
Curr Opin Gastroenterol. 2004; 20(4): 318-327.
13. Targan S, Landers C, Cobb L i wsp. Perinuclear anti-neutrophil
cytoplasmic antibodies are spontaneously produced by mucosal
B cells of ulcerative colitis patients. J Immunol. 1995; 155(6):
3262-3267.
14. Sendid B, Colombel J, Jacquinot P i wsp. Specific antibody
response to oligomannosidic epitopes in Crohns disease. Clin
Diagn Lab Immunol. 1996; 3(2): 219-226.
15. Török H, Folwaczny C. Pancreatic antibodies in Crohns disease:
a feasible diagnostic tool? Eur J Gastroenterol Hepatol. 2005;
17(1): 37-39.
16. Joossens S, Vermeire S, Van Steen K i wsp. Pancreatic
autoantibodies in inflammatory bowel disease. Inflamm Bowel
Dis. 2004; 10(6): 771-777.
17. Seibold F, Scheurlen M, Muller A i wsp. Impaired pancreatic function
in patients with Crohns disease with and without pancreatic
autoatibodies. J Clin Gastroenterol. 1996; 22(3): 202-206.
18. Monatelli A, Mainardi E, Vagni A i wsp. Immunological markers
anti-Saccharomyces cerevisiae antibodies (ASCA) and antineutrophil cytoplasmic antibodies (ANCA) in inflammatory
bowel disease: a helpful diagnostic tool. Minerva Gastroenterol
Dietol. 2005; 51(2): 201-207.
19. Odze R. Pathology of indeterminate colitis. J Clin Gastroenterol.
2004; 38(Suppl.5): 36-40.
20. Dubinsky M, Ofman J, Urman M i wsp. Clinical utility of
serodiagnostic testing in suspected pediatric inflammatory bowel
disese. Am J Gastroenterol. 2001; 96(3): 758-765.
21. Lindgren S, Floren C, Lindhagen T i wsp. Low prewalence of
anti-neutrophil cytoplasmic antibodies in ulcerative colitis
patients with long-term remission. Eur J Gastroenterol Hepatol.
1995; 7(6): 563-568.
22. Patel R, Stokes R, Birch D i wsp. Influence of total colectomy on
serum antineutrophil cytoplasmic antibodies in inflammatory
bowel disease. Br J Surg. 1994; 81(5): 724-726.
23. ZholudevA, Zurakowski D, Young W i wsp. Serologic testing
with ANCA, ASCA and anti-OmpC in children and young adults
with Crohns disease and ulcerative colitis: diagnostic value and
correlation with disease phenotype. Am J Gastroenterol. 2004;
99(11): 2235-2241.
24. Quinton J, Sendid B, Reumaux D i wsp. Anti-Saccharomyces
cerevisiae mannan antibodies combined with antineutrophil
cytoplasmic autoantibodies in inflammatory bowel disease:
prevalence and diagnostic role. Gut. 1998; 42: 788-791.
25. Saibeni S, Folli C, de Franchis R i wsp. Diagnostic role and
clinical correlates of anti-Saccharomyces cerevisiae atnibodies
(ASCA) and anti-neutrophil cytoplasmic antibodies (p-ANCA)
in Italian patients with inflammatory bowel diseases. Dig Liver
Dis. 2003; 35(12): 862-868.
26. Abad E, Tural C, Mirapeix E i wsp. Relationship between ANCA
and clinical activity in inflammatory bowel disease: variation in
prevalence of ANCA and evidence of of heterogeneity.
J Autoimmun. 1997; 10(2): 175-180.
27. Frenzer A, Fierz W, Rundler E i wsp. Atypical, cytoplasmic and
perinuclear antineutriphil cytoplasmic antibodies in patients with
inflammatory bowel disease. J Gastroenterol Hepatol. 1998;
13(9): 863-864.
28. Kim J, Kim K, Seo J. Diagnostic role of anti-Saccharomyces
cerevisiae and antineutrophil cytoplasmic antibodies in pediatric
inflammatory bowel disease. Korean J Gastroenterol. 2003; 42(4):
297-302.
29. Gupta S, Fitzgerald J, Croffie J i wsp. Comparison of serological
markers of inflammatory bowel disease with clinical diagnosis in
children. Inflamm Bowel Dis. 2004; 10(3): 240-244.
30. Peeters M, Joossens S, Vermeire S i wsp. Diagnostic value of
anti-Saccharomyces cerevisiae and antineutrophil cytoplasmic
autoanibodies in inflammatory bowel disease. Am J Gastroenterol. 2001; 96(3): 730-734.
31. Ooi C, Lim B, Cheong W i wsp. Antineutrophil cytoplasmic
antibodies (ANCAs) in patients with inflammatory bowel disease
show no correlation with proteinase 3, lectoferrin, myeloperoxidase,
elastase, cathepsin G and lyzozyme: a Singapore study. Ann Acad
Med Singapore. 2000; 29(6): 704-707.
Zawadzka P, Szczepañski M, £ykowska-Szuber L i wsp. Rola autoprzeciwcia³ w diagnostyce i ró¿nicowaniu
161
32. Wei B, Dalwadi H, Gordon L i wsp. Molecular cloning of
a Bacteroides caccae TonB-linked outer membrane protein
identified by an inflammatory bowel disease marker antibody.
Infect Immun. 2001; 69(10): 6044-6054.
33. Sandborn W. Serologic markers in inflammatory bowel disease:
state of the art. Rev Gastroenterol Disord. 2004; 4(4): 167-174.
34. Vernier G, Sendid B, Poulain D i wsp. Relevance of serologic
studies in inflammatory bowel disease. Curr Gastroenterol Rep.
2004; 6(6): 482-487.
35. Terjung B, Herzog V, Worman H i wsp. Atypical antineutrophil
cytoplasmic antibodies with perinuclear fluorescence in chronic
inflammatory bowel diseases and hepatobiliary disorders
colocalize with nuclear lamina proteins. Hepatology. 1998; 28(2):
332-340.
36. Schinke S, Fellermann K, Herlyn K i wsp. Autoantibodies against
the bactericidal/permeability-increasing protein from
inflammatory bowel disease patients can impair the antibiotic
activity of bactericidal/permeability-increasing protein. Inflamm
Bowel Dis. 2004; 10(6): 763-770.
37. Muller-Ladner U, Gross V, Andus T i wsp. Distinct patterns of
immunoglobulin classes and IgG subclasses of autoantibodies in
patients with inflammatory bowel disease. Eur J Gastroenterol
Hepatol. 1996; 8(6): 579-584.
38. Walker L, Aldhous M, Drummond H i wsp. Anti-Saccharomyces
cerevisiae antibodies (ASCA) in Crohns disease are associated
with disease severity but not NOD2/CARD15 mutations. Clin
Exp Immunol. 2004; 135(3): 490-496.
39. Preda C, Diculescu M, Mirea V i wsp. Significance of antiSaccharomyces cerevisiae antibodies (ASCA) in patients with
inflammatory bowel diseases in Romania. Rom J Gastroenterol.
2005; 14(1): 23-26.
40. Vermeire S, Peeters M, Vlietinck R i wsp. Anti-Saccharomyces
cerevisiae antibodies (ASCA), phenotypes of IBD, and intestinal
permeability: a study in IBD families. Inflamm Bowel Dis. 2001;
7(1): 8-15.
41. Halme L, Turunen U, Helio T i wsp. Familial and sporadic
inflammatory bowel disease: comparison of clinical features and
serological markers in a genetically homogenous population. Scand
J Gastroenterol. 2002; 37(6): 692-698.
42. Oshitani N, Matsumoto T, Jinno Y i wsp. Decreased antiSaccharomyces cerevisiae antibodies titer by mesalazine in
patients with Crohns disease. J Gastroenterol Hepatol. 2000;
15(12): 1400-140.
43. Vermeire S, Joossens S, Peeters M i wsp. Comparative study of
ASCA (Anti-Saccharomyces cerevisiae antibody) assays in
inflammatory bowel disease. Gastroenterology. 2001; 120(4):
827-83.
44. Kountroubakis I, Petinaki E, Mouzas I i wsp. Anti-Saccharomyces
cerevisiae manna antibodies and antineutrophil cytoplasmic
autoantibodies in Greek patients with inflammatory bowel
disease. Am J Gasroenterol. 2001; 96(2): 449-454.
45. Sandborn W, Loftus E, Colombel J i wsp. Evaluation of serologic
disease markers in a population-based cohort of patients with
ulcerative colitis and Crohns disease. Inflamm Bowel Dis. 2001;
7(3): 192-201.
46. Folwarczny C, Noehl N, Endres S i wsp. Antineutrophil and
pancreatic autoantibodies in first-degree relatives of patients with
inflammatory bowel disease. Scand J Gastroenterol. 1998; 33(5):
523-528.
47. Jedynak-W¹sowicz U, Fyderek K, Kowalska-Duplaga K i wsp.
Profil autoprzeciwcia³ narz¹dowych w nieswoistych zapaleniach
jelit u dzieci. Pediatria Wspó³czesna 2004; 6/3: 273-277.