Rekombinacja in vitro i
wprowadzanie
zrekombinowanego DNA do
komórek
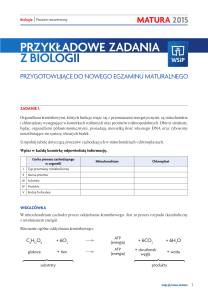
Jak otrzymać zrekombinowane DNA-schemat
klonownia molekularnego
Schemat doświadczenia
pozwalającego na
rekombinację DNA w
wektorze np. plazmidowym:
1.
Przygotowanie fragmentu DNA
2.
Przygotowanie wektora do
klonowania (etapy 1 i 2 zwykle
odbywają się równocześnie)
3.
Ligacja wektora i wstawki
4.
Wprowadzenie
zrekombinowanego DNA do
odpowiedniego gospodarza
np. transformacja bakterii
zrekombinowanym DNA
5.
Selekcja i analiza transformantów
(screening)
I. Przygotowanie fragmentu DNA
1. DNA do klonowania najczęściej jest trawione odpowiednim
enzymem restrykcyjnym (ale możemy także rekombinować
w wektorach fragmenty DNA powielone wcześniej
techniką PCR)
2. Elektroforetyczna kontrola jakości, poprawności i wydajności
trawienia (lub amplifikacji, jeśli fragment DNA powielamy w
PCR), ewentualne oczyszczenie produktu trawienia przez izolację
fragmentu DNA z żelu agarozowego
OPCJONALNIE:
a) Dodanie nowego miejsca restrykcyjnego po trawieniu enzymem
generującym tępe końce - poprzez ligację linkerów DNA np.
wyposażonych w miejsce restrykcyjne
b) Zamiana lepkiego 5’ końca na koniec tępy (np. egzonukleazą,
polimerazą Klenowa)
c) Zamiana lepkiego 3’ końca na koniec tępy
d) dodanie ogonków homopolimerowych np. w klonowaniu cDNA
Opcjonalne manipulacje na fragmencie DNA do klonowania
a) zamiana końca
tępego na lepki poprzez
dodanie linkerów
wyposażonych w
miejsca restrykcyjne
b) dodawanie ogonków homopolimerowych w klonowaniu cDNA
W niektórych eksperymentach (dotyczy to np. rekombinowania w wektorach
eukariotycznego cDNA) nie można użyć do klonowania enzymów restrykcyjnych.
Wyposaża się je wtedy w sztuczne lepkie końce (co może również dotyczyć
wektorów). Technika ta polega na wyposażeniu końców 3’ DNA w łańcuchy
identycznych nukleotydów (ang. Homopolymer tailing).
Syntezę homopolimerowych jednoniciowych zakończeń DNA dokonuje terminalna
transferaza nukleotydowa.
Zaletą tej techniki jest to że na zasadzie komplementarności mogą się ze sobą skleić jedynie
fragmenty obcego DNA i DNA wektora, a nie ma możliwości autoligacji wektora. W
wyniku ligacji cząsteczek wyposażonych w sztuczne lepkie końce powstają więc jedynie
cząsteczki zrekombinowanego DNA
II. Przygotowanie wektora np. plazmidowego
1. Wektor do klonowania musi być zlinearyzowany odpowiednim
enzymem (enzymami) restrykcyjnym (najczęściej takim samym jak
klonowany fragment*)
*
BamHI
BglII
5'-G^G A T C C-3
3'-C C T A G^G-5'
5'-A^G A T C T-3‘
3'-T C T A G^A-5'
2. Elektroforetyczna kontrola jakości, poprawności i wydajności trawienia
– szczególnie istotna w przypadku wektora!!!
a) Opcjonalnie defosforylacja 5’
końców wektora, która zapobiega
autoligacji DNA wektora!!! (tylko
przy trawieniu pojedynczym
enzymem)
III. Ligacja wektora i wstawki – właściwa rekombinacja in vitro
W rekombinacji in vitro wykrzystuje się ligazę DNA uzyskiwaną z komórek E. coli
zakażonych fagiem T4 (ligaza ta wymaga ATP i skleja poza lepkimi także tępe
końce DNA)
Optymalna temp. działania ligazy T4 od 4 (dla końców lepkich), 15-25 (dla
końców tępych)
W mieszaninie ligacyjnej wstawka
(insert, rekombinowany fragment
DNA) powinna stanowić molowy
nadmiar względem ilości
cząsteczek wektora
•Przy małym stężeniu DNA wstawki najbardziej
prawdopodobne jest połączenie końców tej
samej cząsteczki DNA (recyrkularyzacja).
•Wzrost stężenia DNA w reakcji ligacji zwiększa
prawdopodobieństwo połączenia dwóch różnych
cząsteczek DNA
•Dla większości aplikacji można przyjąć
stosunek molarny wstawka : wektor - 3:1
•W reakcji ligacji prawie nigdy nie powstaje 100% zrekombinowanego
DNA, dlatego wektory wyposaża się w systemy wizualnej selekcji
zrekombinowanych klonów, poddaj się je defosforylacji itp.
IV. Wprowadzanie zrekombinowanego DNA do bakterii
1. Transformacja
Zjawisko transformacji – czyli pobierania nagiego DNA z podłoża do komórek
wykazano po raz pierwszy w bakteriach G+ Streptococcus pneumoniae
(a
potem także w Pneumonococcus czy Diplococcus) - Fred Griffiths 1928.
•Zdolność transformacji bakterii zależy
od tzw. stanu kompetencji
•Stan naturalnej kompetencji
uwarunkowany jest genetycznie.
•W takiej transformacji najlepiej
pobierany jest liniowy natywny ds DNA.
Jedna nić ulega degradacji, druga
rekombinacji do genomu gospodarza.
•Naturalną zdolność wchodzenia w stan
kompetencji wykazują głównie bakterie
Gramdodatnie (Streptococcus,
Staphylococcus, Bacillus).
•Bakterie Gram-ujemne zwłaszcza te z
rodziny Enterobacteriaceae (m.in. E.
coli) podlegają tego typu transformacji
ze znacznie mniejsza wydajnością.
Sztuczna kompetencja –
•transformacja E. coli plazmidowym DNA z użyciem metody chemicznej
•podstawowy sposób wprowadzania zrekombinowanego DNA do bakterii
Procedura transformacji E. coli plazmidowym DNA metodą chemiczną:
1.
Przygotowanie hodowli biorcy we wczesnej fazie logarytmicznej (OD600 0.3-0.4)
2.
Otrzymanie komórek kompetentnych przez traktowanie bakterii zimnym (0 st.
C) roztworem 50 lub 100mM chlorku wapnia (w niektórych modyfikacjach
stosuje się dodatek innych jonów np. Mg lub Rb). Roztwory chlorków sprawiają ze
osłona komórkowa staje się przepuszczalna np. dla plazmidu
3.
Zmieszanie komórek kompetentnych z preparatem DNA (plazmid adsorbuje się na
powierzchni komórki) i poddanie krótkotrwałemu działaniu szoku cieplnego.
Szybkie podwyższanie temperatury (do 42 st. C na ok. 3 min.)
powoduje zmiany w powłokach komórkowych bakterii (podwyższona temperatura
wpływa na stan fizyczny lipidów w błonie powodując powiększenie
porów) pozwalające na wniknięcie cząsteczek DNA do wnętrza komórek
4.
Pozostawienie komórek w podłożu nieselekcyjnym na okres umożliwiający
powrót komórek do normalnego stanu fizjologicznego i wyrażenie się genów
zawartych na wprowadzanym plazmidzie lub wektorze fagowym (co najmniej 1
godz. W pożywce bez antybiotyku z napowietrzaniem)- bardzo ważne!!!
5.
Wysiew komórek na podłoża selekcyjne lub w przypadku transformacji z
wykorzystaniem wektora fagowego (np. M13) na płytki bez selekcji z agarem
miękkim – „top agarem”
Od czego zależy wydajność transformacji bakterii metodą chemiczną?
1.
Szczep biorcy powinien być bezplazmidowy (wrażliwy na antybiotyki), mieć nieaktywny system
restrykcyjny (Res-) zapobiega degradacji obcego DNA oraz system rekombinacji (RecA-) co
zapewnia stabilność wprowadzanych plazmidów w komórce (ważne np. przy klonowaniu
genów chromosomalnych. Takie cechy mają np. szczepy E. coli DH5 i XL1-Blue
rekomendowane jako biorcy w transformacji
2.
DNA plazmidowy powinien być oczyszczony – nadmiar soli, enzymów restrykcyjnych, resztek
fenolu, obniża lub hamuje wydajność transformacji
3.
Najbardziej efektywną formą transformacji jest forma ccc DNA plazmidu, transformacja
formą liniową jest mało wydajna i stosowana tylko w szczególnych wypadkach
4.
Wydajność transformacji zależy od wielkości cząsteczki plazmidu, duże cząsteczki
transformują się trudniej
5.
Nadmiar DNA nie wpływa na wzrost wydajności, optymalna ilość dla E. coli powinna wynosić
od 20-200 ng na reakcję
6.
Komórki kompetentne są bardzo wrażliwe i należy się z nimi obchodzić bardzo delikatnie,
zwłaszcza podczas wirowania, mieszania z DNA. Wszystkie etapy preparatyki należy
przeprowadzać w lodzie.
Wydajność podaje się jako liczbę transformantów w przeliczeniu na 1 mikrogram DNA.
Dla E. coli wydajność ta w metodzie wapniowej (z chlorkiem wapnia) waha się od
104 do 106 (max. 107 na 1 g plazmidowego DNA).
2. Elektrotransformacja (elektroporacja )
Istotą metody jest przepuszczenie przez
zawiesinę komórek krótkiego (5-10 msek)
impulsu prądu o bardzo wysokim napięciu (12502500 V). Prowadzi do powstawania porów
(wielkości do 2 nm) w błonie (impuls elektryczny
przejściowo i odwracalnie przerywa ciągłość
błony), przez które do komórek może wnikać
DNA.
Po raz pierwszy zastosowana przez Dovera i
wsp. 1988 roku dla bakterii, zyskała wielką
popularność, ponieważ pozwala transformować
gatunki, które trudno uzyskują kompetencję
metodami chemicznymi.
Zalety elektroporacji w porównaniu z metodą chemiczną :
•można uzyskać bardzo wysoką wydajność transformacji (109-1010
transformantów na g DNA, to co najmniej dwa rzędy wielkości więcej niż w
metodzie chemicznej),
•można wprowadzać bardzo duże cząsteczki DNA (np. plazmidy z
insertami wielkości setek kpz) np. zrekombinowane wektory do
konstrukcji bibliotek genowych z dużymi wstawkami.
Pewną wadą jest to że łatwo można zniszczyć (zabić) komórki
bakteryjne w zawiesinie
V. Selekcja transformantów na odpowiednich
podłożach selekcyjnych
Analiza transformantów:
• Namnożenie bakterii niosących zrekombinowane DNA
w płynnym podłożu selekcyjnym
• Izolacja plazmidowego DNA
• Trawienie plazmidowego DNA – analiza obecności wstawki
Metody wprowadzania DNA (np. zrekombinowanego)
do innych (niż bakterie) typów komórek
Zwykle nie służy to klonowaniu molekularnemu!!!
Problem z nomenklaturą!!!
Jeżeli wprowadzamy zrekombinowane DNA do:
1. Bakterii i drożdży to mówimy o transformacji
2. Komórek roślin – także mówimy o transformacji genetycznej roślin
choć to zupełnie inny proces niż w przypadku bakterii
3. Komórek zwierzęcych lub ludzkich mówimy o transfekcji
(ponieważ używamy wtedy głownie wektorów pochodzenia wirusowego).
W tym wypadku pojęcie transformacji dotyczy transformacji
nowotworowej tych komórek
Wprowadzanie zrekombinowanego DNA do drożdży:
•
Transformacja metodami chemicznymi komórek drożdży
odbywa się na zasadach podobnych jak w przypadku
transformacji komórek bakteryjnych
•
zrekombinowane DNA możemy też wprowadzać do drożdży
przez elektrotransformację
•
z wykorzystywaniem odpowiednich wektorów np. typu YAC
Wprowadzanie zrekombinowanego DNA do roślin
•Wykorzystuje się bakterie z rodzaju Rhizobium: Agrobacterium tumefaciens i
Agrobacterium rhizogenes, które posiadają naturalną zdolność do wprowadzania
swojego DNA do roślin.
•Posiadają w swojej komórce plazmid, kodujące geny niezbędne do infekcji rośliny.
Jeden z fragmentów tego plazmidu, nazwany odcinkiem T (T-DNA), integruje się z
materiałem genetycznym komórki gospodarza.
•Dzięki usunięciu części sekwencji wewnątrz plazmidu T, w to miejsce
można stawić dowolny fragment obcego DNA
•Metoda ta ma poważne ograniczenie - można ja stosować wyłącznie do roślin
dwuliściennych, ponieważ tylko one ulegają infekcji przez Agrobacterium
Transformacja genetyczna roślin dwuliściennych
1)
2)
3)
4)
5)
6)
7)
8)
Wybór odcinka DNA mającego stanowić „transgen” w roślinie i
wstawienie go w odpowiednie miejsce wektora będącego
pochodną plazmidu T - rekombinacja w E. coli
(transformacja I)
Wprowadzeniu zrekombinowanego wektora do
Agrobacterium (transformacja II),
Inkubacja bakterii niosących wektor z fragmentem tkanki
roślinnej (kokultywacja) – umieszczenie eksplantatów w
roztworze bakterii
Przeniesienie fragmentów tkanki na pożywkę selekcyjnoregeneracyjną z odpowiednim antybiotykiem (czynnik
eliminujący Agrobacterium i czynnik selekcyjny
transformantów)
Indukcja podziałów komórkowych i powstanie bezkształtnej
masy dzielących się komórek zwanej kalusem,
Regeneracja roślin z komórek kalusa za pomocą pożywek
zawierających hormony roślinne,
Ukorzenianie rośliny w odpowiedniej pożywce,
Przeniesienie roślin do ziemi, hartowanie; analizy molekularne,
fizjologiczno-biochemiczne
Sposoby transformacji genetycznej czyli wprowadzania
np. zrekombinowanego DNA do roślin jednoliściennych
(zboża, trawy i cebulowate)
-Mikrowstrzeliwanie – biobalistyka (nie wymaga tworzenia
protoplastów z komórek roślinnych)
Inne metody są stosowane raczej rzadko – w większości
wymagają uzyskania protoplastów
Metody wprowadzania zrekombinowanego DNA do
komórek zwierzęcych i ludzkich:
•
Dominują metody biologiczne, które są najbardziej skuteczne transfekcja z użyciem zrekombinowanych wektorów wirusowych tj.
inkubacja linii odpowiednich komórek z zawiesiną zrekombinowanego
wirusa w odpowiednich warunkach (pożywka, temp. itd.)
Inne metody (rzadziej stosowane)
•
Lipofekcja (najczęściej wprowadzane jest DNA bezwektorowe
•
Mikroiniekcja dojądrowa - DNA bezwektorowe
Wykorzystanie liposomów i
lipopleksów – lipofekcja
Liposomy to drobne syntetyczne pęcherzyki lipidowe.
Powstają one spontanicznie, jeżeli pewne typy
lipidów zawiesi się w roztworze wodnym. Ich błonę
stanowi podwójna warstwa lipidowa, tak więc
budową przypominają np. błonę komórki.
Liposomy wiążą i kondensują DNA spontanicznie,
tworząc komleksy o wysokim powinowactwie do błon
komórkowych.
Zwykle mają dość niewielką pojemność wewnętrzna
średnica liposomu (0,025-0,1 mikrometrów) jest
zazwyczaj znacznie mniejsza niż długość
plazmidowego DNA, który może mierzyć nawet do 2
mikrometrów. Oznacza to że tylko nieliczne ciasno
zwinięte cząsteczki DNA mogą być otaczane w
liposomach
Problemem jest także ukierunkowane lipososmów
do konkretnych tkanek
Lipofekcja c.d.
•Liposomy powinny być także wyposażone w peptydy, zdolne niszczyć
błony endosomalne i zapobiegać lizosomalnej degradacji DNA, a także w
rekombinazy, wspomagające rekombinację między wprowadzonym DNA
a DNA komórki, oraz białka i RNA, które mogą służyć ekspresji
wprowadzonego DNA.
Ciągle próbuje się ulepszać tego typu niewirusowe nośniki pozwalające
wprowadzać DNA do komórek zwierzęcych i ludzkich
Dość obiecujące są rożnego rodzaju lipidy kationowe i polimery kationowe
tzw. lipopleksy.
Na ich korzyść przemawia
•brak ryzyka rekombinacji genetycznych i mutacji typu insercji występujących w
przypadku stosowania nośników wirusowych
•stosunkowo duża pojemność (większa niż liposomów) dla terapeutycznego DNA
•możliwość wielokrotnych iniekcji (lipidy oraz polimery kationowe nie są
bowiem immunogenne) co umożliwia ich bezpieczniejsze stosowanie
także in vivo (czyli w tym przypadku np. u pacjenta)
Mikroiniekcja dojądrowa (głównie
komórki zwierzęce np. w
transgenezie zwierząt rzadziej
kom. ludzkie)
•Polega na wstrzykiwaniu DNA
bezpośrednio do jąder komórek za
pomocą szklanych mikroigieł,
kontrolowanych przez sterowane
hydraulicznie mikromanipulatory, przy
równoczesnej obserwacji pod
mikroskopem o wysokiej
rozdzielczości.
•Metoda ta jest bardzo wydajna
•Doświadczenie wykonywanie jest
przez ręcznie człowieka.
Metoda praco- i czasochłonna.
Obszary współczesnej biotechnologii, na które
inżynieria genetyczna ma największy wpływ:
zielona biotechnologia obejmująca rolnictwo i szeroko
pojęty przemysł rolno-przetwórczy
czerwona biotechnologia — związana z różnymi aspektami
ochrona zdrowia ludzi i zwierząt (włącznie z diagnostyką,
farmacją, jak również weterynarią)
Podstawą współczesnej zielonej biotechnologii
jest transgeneza – przeniesienie na stałe do jakiegoś
organizmu jednego lub więcej genów pochodzących z
innej komórki lub innego organizmu – GMO
Podstawą transgenezy jest
rekombinacja in vitro - łączenie dowolnych
cząsteczek DNA
Transgeniczne rośliny bardziej odporne na choroby i
czynniki środowiska
Transgeniczne rośliny - poprawione cechy jakościowe:
pszenica – więcej glutelin = lepsza wartość wypiekowa mąki
ananas – białko utrudniające zamarzanie = mniejsze straty przy
przechowywaniu w chłodniach
pomidor – więcej karotenu = lepsze wybarwianie owoców
ryż – zwiększenie zawartości prowitaminy A
kawa – usunięcie enzymów zaangażowanych w syntezę kofeiny
Rośliny GM jako „bioreaktory” - agrofarmaceutyka
(agropharming)
wykorzystanie roślin transgenicznych jako bioreaktorów do produkcji
białek, które mogą być wykorzystane w terapii lub diagnostyce medycznej
somatotropina
ziemniak – bulwa
kolagen
tytoń – liście
podj. hemoglobiny
tytoń – nasiona
interleukina-2
ziemniak – bulwy
interferon alfa
ziemniak
Transgeniczne zwierzęta - poprawione cechy użytkowe
•Szybszy wzrost zwierząt hodowlanych
•Większa wydajność produkcji np.
mleka albo mięsa - (mleko specjalnie
przystosowane do produkcji serów)
•Transgeniczne zwierzęta w medycynie i badaniach
biomedycznych – badania podstawowe - transgeniczne
myszy są niezastąpionym modelem w badaniu chorób
człowieka, np. nowotworów, otyłości, starzenia, chorób układu
krążenia, cukrzycy itp.
•Genetycznie modyfikowane zwierzęta np. świnie jako
dawcy narządów albo ksenogenicznych komórek i
tkanek do przeszczepów
Czerwona biotechnologia - ochrona zdrowia ludzi i zwierząt
Produkcja rekombinowanych białek (leków, hormonów, białek
wykorzystywanych w biologii molekularnej) w
mikroorganizmach i komórkach eukariotycznych
Transformation
Rekombinowane biofarmaceutyki:
• Do chwili obecnej na świecie do użytku dopuszczonych jest ok 650 leków
białkowych, z czego 400 to leki oparte na białkach rekombinowanych
• Kolejne 1300 rekombinowanych biofarmaceutyków jest w fazach testów, z
wyraźną tendencją wzrostu udziału w ich produkcji komórek
eukariotycznych, choć niektóre typy tych leków np. przecinowotworowe,
są w dużej mierze produkowane w bakteriach
Lista rekombinowanych biofarmaceutyków przeciwnowotworowych
dopuszczonych do stasowania w jednym miesiącu 2015
Jakiego typu schorzenia próbujemy leczyć za
pomocą rekombinowanych biofarmaceutyków
Zysk ze sprzedaży rekombinowanych biofarmaceutyków
przeciwnowotworowych przewyższa zyski ze sprzedaży leków chemicznych
Terapia genowa - leczenie chorób genetycznych np. przez
wprowadzenie terapetucznego DNA albo wprowadzenie tzw. genu
samobójczego – zniszczenie chorych komórek np. nowotworowych
wektor AAV
wektor
retrowirusowy
•
•
•
Unia Europejska dopuściła na swój rynek pierwszą terapię genową
•
Stężenie tłuszczów we krwi chorych poddawanych terapii ulega wyraźnemu
zmniejszeniu, znacząco zmniejsza się ryzyko wystąpienia zapalenia trzuski, które
stanowi główne powikłanie w tej chorobie
•
Glybera jest obecnie jednym z najdroższych leków świata. Koszt
terapii jednego pacjenta wynosi ponad 1,2 mln euro
Glybera jest przeznaczona dla osób cierpiących na rzadką (jedna-dwie
osoby na milion) chorobę związaną z niemożnością właściwego
trawienia tłuszczów (wrodzony niedobór lipazy lipoproteinowej (LPLD
– lipoprotein lipase deficiency)
Technologia oparta na wiedzy o DNA umożliwia ponadto
•rozwój precyzyjnej, szybkiej i taniej diagnostyki
• projektowanie osobistych leków “custom drugs” (spersonalizowana
medycyna)