Biochemia 3 koło.doc
(90 KB) Pobierz
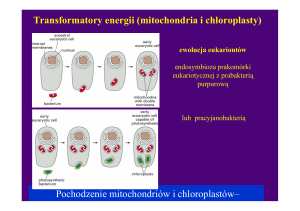
BUDOWA ŁAŃCUCH ODDECHOWEGO- inaczej łańcuch transportu elektronów. Układ białek umiejscowiony w wewnętrznej błonie mitochondriom. Jego rola polega na przeniesieniu elektronów na cząsteczkę tlenu, jest to ostatni etap oddychania wewnątrzkomórkowego, przebiegający na wewnętrznych błonach mitochondrium i polegający na przenoszeniu
elektronów i protonów na kolejne przenośniki. Kolejnym etapom tej wędrówki elektronów towarzyszy wydzielanie się energii, która zostaje wykorzystana do syntezy ATP z ADP. Ostatecznym akceptorem elektronów i protonów jest tlen, a reakcja ta prowadzi do utworzenia cząsteczki wody. Tworzenie wody jest podstawową reakcją dostarczającą energii komórkom w
warunkach tlenowych.W reakcje łańcucha oddechowego wchodzą cząsteczki NADH i FADH, Przejściu jednej cząsteczki NADH w NAD i przebiegowi elektronów przez łańcuch oddechowy towarzyszy synteza 3 cząsteczek ATP. Głównymi składnikami łańcucha oddechowego są poza tym: dwa kompleksowe enzymy flawoproteinowe zawierające żelazo niehemowe dehydrogenaza nukleotydów pirydynowych i dehydrogenaza bursztynianowa, ubichinon (Q) oraz cytochromy b, c1, c i a. Ostatnim ogniwem łańcucha oddechowego jest enzym oksydaza cytochromowa, odpowiedzialny za wytworzenie jonu tlenowego O2, który łączy się z dwoma protonami i tworzy cząsteczkę wody Błona mitochondralna- główną rolą jest uzyskiwanie
energii w formie ATP wskutek przekształcania związków organicznych, ale biorą również udział w innych procesach metabolicznych, takich jak: Apoptoza - programowana śmierć komórki Regulacja stanu redoks komórki, Synteza hemu, Synteza sterydów, Wytwarzanie ciepła, Cykl mocznikowy - w mitochondriach wątroby ubichinon (CoQ)- mała cząsteczka rozpuszczalna
w tłuszczach, znajduje się w zewnętrznej błonie ,mitochondrialnej, cząsteczka ta funkcjonuje jako przenośnik elektronów mogący przyjąć aż dwa elektrony i dwa jony H+, w ten sposób przekształca się w ubichinon(CoQH2) zajmuje centralne miejsce w strukturze łańcucha, w kompleksie występuje z białkami błonowymi. Zespala kompleks I i II dokonując pierwotnego
utlenienia NADH z kompleksami III i IV na które przekazuje elektrony. Na nim tez protony są zawracane do matrix, a następnie pompowane do strefy międzybłonowej. Przenośnik dwuelektrodowy cytochromy- jest białkiem mającym grupę hemową zawierająca atom żelaza, różne cytochromy mają różne grupy hemowe ale mimo to mogę funkcjonować jako przenośniki
elektronów, jest to przenośnik jednoelektrodowy cytochrom c – jest peryferycznym białkiem błonowym luźno związanym z zew powierzchnią wew blony mitochondrialnej, wiąże się kompleksem cytochromów bc1 i odbiera elektron przechodząc ze stanu Fe3+ do Fe2+, następnie cytochrom c wiąże się z oksydazą cytochromową i przekazuje jej elektron z atomu żelaza
hemowego cytochrom a – stanowi parę z atomem miedzi Cu a cytochrom a3- występuje w parze z odmiennym atomem miedzi ATP-aza- Pompa sodowo-potasowa, inna często używana nazwa to Na+/K+ ATP-aza to ważny enzym uczestniczący w aktywnym transporcie kationów sodu i potasu. Ma on podstawowe znaczenie dla każdego rodzaju komórek żywych,
utrzymując potencjał błonowy i objętość komórki. Koenzym A – wewnątrz komórkowe oddychanie zachodzi w mitochondriach, to jest jeden z kompleksów enzymatycznych łańcucha oddechowego. Koenzym przenosi jony H+. Związane jest to z uwalnianiem energii łącznie z syntezą ATP. Uczestniczy w aktywacji reszt kwasów karboksylowych.
OMOW ETAPY PRZENOSZENIA ELEKTRONÓW W ŁAŃCUCHU ODDECHOWYM, W JAKI SPOSÓB PRZENOSZENIE ELEKTRONÓW SPRĘŻONE JEST Z POWSTAWANIE GRADIENTU JONÓW WODOROWYCH – kolejność przepływu elektonów: substrat NADHNAD+ <=> FpCoQCyt bCyt cCyt a+at3O2. –1 etap- NADHdehydrogenaza NADH- wiąże ona NADH i utlenia go do NAD+ odbierając dwa elektrony które następnie przechodzą do grupy prostetycznej FMN (mononukleotyd flawinowy) i tworzy się FMNH2. Każdy z elektronów jest odbierany razem z jonem wodoru H+, dalej elektrony są przenoszone do centrów żelazowo-siarkowych umiejscowionych w białkach żelazosiarkowych. W centrum Fe-S elektron jst przenoszony przez atom żelaza który przyjmując elektrony przechodzi ze stanu Fe3+ do Fe2+, gdy elektron przejdzie do następnego przenośnika elektronów atom żelaza w centrum Fe-S znowu powraca do stanu Fe3+ 2 etap-Dehydrogenaza NADH- ubichinon (CoQ) elektrony z centrów żelazowo-siarkowych dehydrogenazy
NADH przechodzą do ubichinonu(CoQ) ta cząsteczka funkcjonuje jako przenośnik elektronów mogący przyjąć aż dwa elektrony i dwa jony H+ i w ten sposób CoQ przekształca się u ubichinon CoQH2 3 etap- ubichinon- kompleks bc1- jony H+ zostają uwolnione jeszcze raz, w skład kompleksu bc1 wchodza :cytochrom b i cytochrom c1 i białko Fe-S. Atom żelaza z
grupy hemowej przyjmujący elektron przyjmujący elektron przechodzi ze stanu Fe3+ do stanu 2+ .Ubichinol najpierw uwalnia jeden elektron i jon H+ wskutek czego staje się ubisemichinonem ( CoQH2) a po odłaczeniu drugiego elektronu i jonu H+ przechodzi w ubichinon CoQ 4 etap- kompleks cytochromów bc1- cytochrom c – oksydaza cytochromowa. Cytochrom c
wiąże się z kompleksem cytochromów bc1 i odbiera elektron przechodząc ze stanu Fe3+ do Fe2+, potem cytochrom c wiąże się z oksydazą cytochromowi i przekazuje jej elektron z atomu żelaza hemowego przechodzącego wówczas do stanu Fe3+ 5etap- oksydaza cytochromowa- tlen. Zawiera dwa cytochromy w czasie przenoszenia elektronów atomy żelaza oscylują
między stanem Fe3+ a Fe2+ atomy miedzi oscylują między Cu2+ a Cu+. Zachodzi tu przeniesienie czterech elektronów z czterech cząsteczek cytochromu c oraz czterech jonów H+ do tlenu cząsteczkowego z wytworzeniem dwóch cząsteczek wody. Zmiana potencjału redoks obserwowana w łańcuch oddechowym jest miarą zmiany energii swobodnej, potencjał spada od
początku do końca łańcucha ale największe spadki odpowiadają trzem kompleksom: kompleksowi dehydrogenazy NADH, kompleksowi cytochromów bc1 i kompleksowi oksydazy cytochromowej, zmiana energii w tych miejscach jest wystarczająco duża do wypompowania jonów H+ z matrix mitochondrialnej, poprzez wew błonę mitochndrialną do przestrzeni
międzybłonowej. Czyli każdy z tych kompleksów jest pompą H+ napędzaną przez transport elektronów, czyli podczas transportu elektronów z NADH uwalnia się energia która zostaje wykorzystana do tworzenia gradientu H+.
AKTYWACJA KW. TŁUSZCZOWYCH. Rozpad kwasów tłuszczowych zachodzi w cytozolu komórek prokariotycznych i w matriks mitochondrialnej komórek eukariotycznych. Zanim kwas tłuszczowy dotrze do matriks, ulega aktywacji przez utworzenie wiązania tioestrowego z CoA. RCOO-+ATP+HS-CoAsynteza acylo-CoAR-C(=O)-S-CoA+AMP+PPi.
Reakcja ta zużywa cząsteczkę ATP i katalizowana jest przez syntezę acylo-CoA, umiejscowioną na zewnętrznej błonie mitochondrialnej. Na skutek zachodzącej nastepnie hydrolizy PPi do dwóch cząsteczek Pi napisana reakcja przez mnie jest nieodwracalna. β-OKSYDACJA TŁUSZCZÓW (UTLENIANIE KWASÓW TŁUSZCZOWYCH). Kwasy tłuszczowe ulegają
spalaniu w procesie β-oksydacji. Polega na cyklicznym odłączeniu reszty kwasu octowego połaczonej z koenzymem A, która zostaje rozłożona w cyklu Krebsa. Łańcuch jest w ten sposób krótszy o dwa atomy węgla za każdym razem. Proces zachodzi w mitochondriach w komórkach eukariotycznych głównie w wątrobie. W pierwszym etapie kwas tłuszczowy łączy się z
CoA i w obecności dehydrogenazy acylo-koenzymu A ulega odwodornieniu przez FAD. Powstaje kwas o wiązaniu podwójnym, połączony z CoA. W drugim etapie podwójne wiazanie ulega rozerwaniu w wyniku przyłączenia wody w obecności enzymu hydratazy enoilo-CoA. Powstaje kwas hydroksyacylowy połączony z CoA. Ten z kolei ulega dehydratacji w reakcji
katalizowanej przez dehydrogenazę 3-hydroksy-ksyacylo-CoA. W wyniku działania enzymu acylotransferazy acetylo-CoA następuje odłączenie acetylo-CoA od dotychczasowego kwasu, w wyniku czego łańcuch kwasu tłuszczowego jest o dwa atomy węgla krótszy i do którego ponownie przyłączony CoA. Proces się powtarza. Końcowym produktem β-oksydacji jest
bytyrylo-CoA, który rozkładany jest na dwie cząsteczki acetylo-CoA. CECHY ATP-( ADENOZYNOTRIFOSFORAN) jest przenośnikiem energii swobodnej w większości procesów zużywających energię, ATP jest nukleotydem składającym się z adeiny, rybozy i trifosforanu. Aktywna formą ATP jest przeważnie kompleks z Mg+2 lub Mn+2. ATP jest czasteczką
bogatą w energię ponieważ jego jednostka trifosforanowa zawiera dwa bezwodnikowe wiązania fosforanowe. Duża ilość energi swobodnej jest uwalniana gdy ATP ulega hydrolizie do ADP i ortofosforanu(Pi) lub gdy jest on hydrolizowany do AMP (adenozynomonofosforanu) i pirofosforanu(PPi) ATP+H2O=ADP+Pi+H+ ATP+H2O=AMP+PPi+H+ ATP,ADP,AMP
mogą ulegać wzajemnym przemianom, enzym kinaza adenylanowa(miokinaza) katalizuje reakcje ATP+AMP=ADP+ADP energia swobodna uwalniana w czasie hydrolizy ATP jest wykorzystywana do przeprowadzenia reakcji wymagających jej dostarczenia np. skurcz mięśni. ATP służy jako bezpośredni donor energii swobodnej w układach biologicznych. ATP jest
stabilny nie rozpada się samorzutnie potrzebny jest enzym. Synteza ATP odbywa się głównie w mitochondriach, jest wykorzystywana w reakcjach glikolizy, cyklu Krebsa. Cząsteczki ATP są dawcami grup fosforanowych w procesach fosforylacji . do rys (adeina połączona wiązaniem N-glikozydowym z rybozą, reszty fosforanowe połączone wiązaniami bezwodnikowymi).
CYKL ATP-ADP jest podstawowym sposobem wykorzystania energii w organizmach żywych ATP+H2O=ADP+P (rys) . Druga droga hydrolizy ATP- odłączenie od ATP cząsteczki difosforanu (rys) Duża energii pochodzi z hydrolizy wiązanie bezwodnikowego ATP oraz produkty tworzą tzw system adenylowany uczestniczący w przekształcaniu i magazynowaniu
energii i stanowiący jej główne źródło dla procesów komórkowych. Proces ten trwa ustawicznie dzięki regeneracji która odbywa się w wyniku fosforylacji. Hydroliza ATP jest procesem samorzutnym a zatem dostarcza energie bez jej uprzedniego pochłaniania. Duża ilość energii jest uwalniana gdy ATP ulega hydrolizie do ADP i AMP. ATP jest cząsteczką bogatą w
energie ponieważ jego jednostka trifosforanowa zawiera dwa bezwodnikowe wiązania fosforanowe.
SZLAK GLIKOLIZY – Etap I 1)Fosforylacja glukozy do glukozo-6-fosforanu – enzym heksokinaza, enzym allosferyczny wymaga Mg+2 lub Mn+2, metal tworzy kompleks z ATP wiązanie glukozy katalizuje przeniesienie grupy fosforanowej na akceptor( sześć węglowy) jest regulowana przez glukozo-6-fosforan, kiedy fosfofruktokinaza jest nieaktywna wzrasta
sprężenie fruktozo-6-fosforanu, jednocześnie wzrasta poziom glukozo-6-fosforanu będącego w równowadze z fruktozo-6-fosforanem,dlatego hamowanie fosfofruktokinazy prowadzi do hamowania heksokinazy 2)Izomeryzacja glukozo-6-fosforanu do fruktozo-6-fosforanu- enzym izomeraza glukozofosforanowa 3) Fosforylacja fruktozo-6-fosforanu do fruktozo-1,6difosforanu, enzym: fosforuktokinaza: podlega regulacji enzym allosferyczny, szybkość glikozy zależy od jego aktywności, jego aktywność jest kontrolowana allosferycznie przez niektóre metabolity. Występuje w wątrobie jest hamowana przez wysoki poziom ATP który zmniejsza powinowactwo enzymu do fruktozo-6-fosforanu Hamujące działanie ATP jest znoszone
przez AMP tak więc aktywność fosfofruktokinazy wzrasta w momencie obniżania stosunku ATP/AMP, spadek ładunku energetycznego stymuluje glikolizę. Fosfofrukinaza jest hamowana przez cytrynian, wysoki poziom cytrynianu oznacza że nie jest potrzebne rozkładanie dodatkowych ilości glukozy 4)Rozszczepienie fruktozo-1,6-difosforanu do aldehydu 3fosfoglicerynowego i fosfodihydroksyacetonu, enzym: aldonaza fruktozodifosforanowa 5) Izomeryzacja fosfodihydroksyacetonu do aldehydu 3-fosfoglicerynowego , enzym: izomeraza trifosforanowa ETAP II 6) Utlenianie ald 3-fosfoglicerydu do 1,3-difosfoglicerynianu, enzym: dehydrogenaza aldehydu-3-fosfoglicerynowego 7) Defosforylacja 1,3difosfoglicerynianu do 3-fosfoglicerynianu z wytworzeniem ATP , enzym: kinaza fosfoglicerynianowa 8) Izomeryzacja 3-fosfoglcerynianu do 2-fosfoglicerynianu, enzym: fosfoglicerolomutaza 9)Dehydratacja 2-fosfoglicerynianu do fosfoendopirogronianu, enzym: enolaza 10) Defosforylacja fosfoendopirogronianu do pirogronianu z wytworzeniem ATP,
enzym: kinaza pirogronianowa – kontroluje wypływ związków ze szlaku glikolitycznego. ATP hamuje allosferycznie kinazę pirogronianową zwalniając szybkość glikolizy w sytuacji, gdy ładunek energetyczny w komórce jest duży. Alanina (syntetyzowana z pirogronianu w pojedyńczej reakcji) również hamuje allosferycznie kinaze pirogronianową sygnalizując obfitość
składników budulcowych, jest aktywowana przez fruktozo-1,6-bifosforanu.. CYKL KREBSA (kw. CYTRYNOWEGO)- 1. Tworzenie cytrynianu w nieodwracalnej reakcji kondensacji acetylo-CoA ze szczawiooctanem katalizowanej przez syntezę cytrynianową. 2. Przekształcanie cytrynianu w izocytrynian. Enzym: akonitaza. W rzeczywistości jest to reakcja
dwustopniowa, w której powstaje intermedia, cis-akonitan. 3. Utlenianie izocytrynianu do α-ketoglutaranu i CO2 przez dehydrogenazę izocytrynianową. Ten mitochondrialny enzym współpracuje z NAD+ redukowanym do NADH. 4. Oksydacyjna dekarboksylacja α-ketoglutaranu do buerztynylikoenzymu A. Enzym: kompleks dehydrogenazy α-ketoglutaranowej. Podobnie
jak w przypadku dehydrogenazy pirogronowej, jest to kompleks złożony z trzech enzymów, wykorzystujący NAD+ jako kafaktor. 5. Przekształcenie Bursztynylokoenzymu A w bursztynian w wytworzeniem GTP. Enzym: syntetaza bursztynyloCoA. E reakcji tej energia uwalniana podczas rozerwania w bursztynylo-CoA jest wykorzystywana do syntezy albo GTP(głównie
u zwierząt) albo ATP (wyłącznie u roślin) z Pi i odpowiednio DGP lub ADP..6. Utlenianie Bursztynianu do fumaranu. Enzym: dehydrogenaza bursztynianowa. Z enzymem ściśle związany jest FAD, który po redukcji przechodzi w FADH2.. 7.Uwodornianie Fumaranu do L-Jabłczanu. Enzym: hydrataza fumaranowa.. 8. Utlenianie Jabłczanu do szczawiooctanu. Enzym:
dehydrogenaza jabłczanowa
BUDOWA ŁAŃCUCH ODDECHOWEGO- inaczej łańcuch transportu elektronów. Układ białek umiejscowiony w wewnętrznej błonie mitochondriom. Jego rola polega na przeniesieniu elektronów na cząsteczkę tlenu, jest to ostatni etap oddychania wewnątrzkomórkowego, przebiegający na wewnętrznych błonach mitochondrium i polegający na przenoszeniu elektronów i protonów
na kolejne przenośniki. Kolejnym etapom tej wędrówki elektronów towarzyszy wydzielanie się energii, która zostaje wykorzystana do syntezy ATP z ADP. Ostatecznym akceptorem elektronów i protonów jest tlen, a reakcja ta prowadzi do utworzenia cząsteczki wody. Tworzenie wody jest podstawową reakcją dostarczającą energii komórkom w warunkach tlenowych.W reakcje
łańcucha oddechowego wchodzą cząsteczki NADH i FADH, Przejściu jednej cząsteczki NADH w NAD i przebiegowi elektronów przez łańcuch oddechowy towarzyszy synteza 3 cząsteczek ATP. Głównymi składnikami łańcucha oddechowego są poza tym: dwa kompleksowe enzymy flawoproteinowe zawierające żelazo niehemowe - dehydrogenaza nukleotydów pirydynowych i
dehydrogenaza bursztynianowa, ubichinon (Q) oraz cytochromy b, c1, c i a. Ostatnim ogniwem łańcucha oddechowego jest enzym oksydaza cytochromowa, odpowiedzialny za wytworzenie jonu tlenowego O2, który łączy się z dwoma protonami i tworzy cząsteczkę wody Błona mitochondralna- główną rolą jest uzyskiwanie energii w formie ATP wskutek przekształcania związków
organicznych, ale biorą również udział w innych procesach metabolicznych, takich jak: Apoptoza - programowana śmierć komórki Regulacja stanu redoks komórki, Synteza hemu, Synteza sterydów, Wytwarzanie ciepła, Cykl mocznikowy - w mitochondriach wątroby ubichinon (CoQ)- mała cząsteczka rozpuszczalna w tłuszczach, znajduje się w zewnętrznej błonie ,mitochondrialnej,
cząsteczka ta funkcjonuje jako przenośnik elektronów mogący przyjąć aż dwa elektrony i dwa jony H+, w ten sposób przekształca się w ubichinon(CoQH2) zajmuje centralne miejsce w strukturze łańcucha, w kompleksie występuje z białkami błonowymi. Zespala kompleks I i II dokonując pierwotnego utlenienia NADH z kompleksami III i IV na które przekazuje elektrony. Na nim tez
protony są zawracane do matrix, a następnie pompowane do strefy międzybłonowej. Przenośnik dwuelektrodowy cytochromy- jest białkiem mającym grupę hemową zawierająca atom żelaza, różne cytochromy mają różne grupy hemowe ale mimo to mogę funkcjonować jako przenośniki elektronów, jest to przenośnik jednoelektrodowy cytochrom c – jest peryferycznym białkiem
błonowym luźno związanym z zew powierzchnią wew blony mitochondrialnej, wiąże się kompleksem cytochromów bc1 i odbiera elektron przechodząc ze stanu Fe3+ do Fe2+, następnie cytochrom c wiąże się z oksydazą cytochromową i przekazuje jej elektron z atomu żelaza hemowego cytochrom a – stanowi parę z atomem miedzi Cu a cytochrom a3- występuje w parze z odmiennym
atomem miedzi ATP-aza- Pompa sodowo-potasowa, inna często używana nazwa to Na+/K+ ATP-aza to ważny enzym uczestniczący w aktywnym transporcie kationów sodu i potasu. Ma on podstawowe znaczenie dla każdego rodzaju komórek żywych, utrzymując potencjał błonowy i objętość komórki. Koenzym A – wewnątrz komórkowe oddychanie zachodzi w mitochondriach, to
jest jeden z kompleksów enzymatycznych łańcucha oddechowego. Koenzym przenosi jony H+. Związane jest to z uwalnianiem energii łącznie z syntezą ATP. Uczestniczy w aktywacji reszt kwasów karboksylowych.
OMOW ETAPY PRZENOSZENIA ELEKTRONÓW W ŁAŃCUCHU ODDECHOWYM, W JAKI SPOSÓB PRZENOSZENIE ELEKTRONÓW SPRĘŻONE JEST Z POWSTAWANIE GRADIENTU JONÓW WODOROWYCH – kolejność przepływu elektonów: substrat NADHNAD+ <=> FpCoQCyt bCyt cCyt a+at3O2. –1 etap- NADH- dehydrogenaza
NADH- wiąże ona NADH i utlenia go do NAD+ odbierając dwa elektrony które następnie przechodzą do grupy prostetycznej FMN (mononukleotyd flawinowy) i tworzy się FMNH2. Każdy z elektronów jest odbierany razem z jonem wodoru H+, dalej elektrony są przenoszone do centrów żelazowo-siarkowych umiejscowionych w białkach żelazo-siarkowych. W centrum Fe-S elektron
jst przenoszony przez atom żelaza który przyjmując elektrony przechodzi ze stanu Fe3+ do Fe2+, gdy elektron przejdzie do następnego przenośnika elektronów atom żelaza w centrum Fe-S znowu powraca do stanu Fe3+ 2 etap-Dehydrogenaza NADH- ubichinon (CoQ) elektrony z centrów żelazowo-siarkowych dehydrogenazy NADH przechodzą do ubichinonu(CoQ) ta cząsteczka
funkcjonuje jako przenośnik elektronów mogący przyjąć aż dwa elektrony i dwa jony H+ i w ten sposób CoQ przekształca się u ubichinon CoQH2 3 etap- ubichinon- kompleks bc1- jony H+ zostają uwolnione jeszcze raz, w skład kompleksu bc1 wchodza :cytochrom b i cytochrom c1 i białko Fe-S. Atom żelaza z grupy hemowej przyjmujący elektron przyjmujący elektron przechodzi
ze stanu Fe3+ do stanu 2+ .Ubichinol najpierw uwalnia jeden elektron i jon H+ wskutek czego staje się ubisemichinonem ( CoQH2) a po odłaczeniu drugiego elektronu i jonu H+ przechodzi w ubichinon CoQ 4 etap- kompleks cytochromów bc1- cytochrom c – oksydaza cytochromowa. Cytochrom c wiąże się z kompleksem cytochromów bc1 i odbiera elektron przechodząc ze stanu
Fe3+ do Fe2+, potem cytochrom c wiąże się z oksydazą cytochromowi i przekazuje jej elektron z atomu żelaza hemowego przechodzącego wówczas do stanu Fe3+ 5etap- oksydaza cytochromowa- tlen. Zawiera dwa cytochromy w czasie przenoszenia elektronów atomy żelaza oscylują między stanem Fe3+ a Fe2+ atomy miedzi oscylują między Cu2+ a Cu+. Zachodzi tu przeniesienie
czterech elektronów z czterech cząsteczek cytochromu c oraz czterech jonów H+ do tlenu cząsteczkowego z wytworzeniem dwóch cząsteczek wody. Zmiana potencjału redoks obserwowana w łańcuch oddechowym jest miarą zmiany energii swobodnej, potencjał spada od początku do końca łańcucha ale największe spadki odpowiadają trzem kompleksom: kompleksowi dehydrogenazy
NADH, kompleksowi cytochromów bc1 i kompleksowi oksydazy cytochromowej, zmiana energii w tych miejscach jest wystarczająco duża do wypompowania jonów H+ z matrix mitochondrialnej, poprzez wew błonę mitochndrialną do przestrzeni międzybłonowej. Czyli każdy z tych kompleksów jest pompą H+ napędzaną przez transport elektronów, czyli podczas transportu elektronów
z NADH uwalnia się energia która zostaje wykorzystana do tworzenia gradientu H+.
AKTYWACJA KW. TŁUSZCZOWYCH. Rozpad kwasów tłuszczowych zachodzi w cytozolu komórek prokariotycznych i w matriks mitochondrialnej komórek eukariotycznych. Zanim kwas tłuszczowy dotrze do matriks, ulega aktywacji przez utworzenie wiązania tioestrowego z CoA. RCOO-+ATP+HS-CoAsynteza acylo-CoAR-C(=O)-S-CoA+AMP+PPi. Reakcja ta zużywa
cząsteczkę ATP i katalizowana jest przez syntezę acylo-CoA, umiejscowioną na zewnętrznej błonie mitochondrialnej. Na skutek zachodzącej nastepnie hydrolizy PPi do dwóch cząsteczek Pi napisana reakcja przez mnie jest nieodwracalna. β-OKSYDACJA TŁUSZCZÓW (UTLENIANIE KWASÓW TŁUSZCZOWYCH). Kwasy tłuszczowe ulegają spalaniu w procesie β-oksydacji.
Polega na cyklicznym odłączeniu reszty kwasu octowego połaczonej z koenzymem A, która zostaje rozłożona w cyklu Krebsa. Łańcuch jest w ten sposób krótszy o dwa atomy węgla za każdym razem. Proces zachodzi w mitochondriach w komórkach eukariotycznych głównie w wątrobie. W pierwszym etapie kwas tłuszczowy łączy się z CoA i w obecności dehydrogenazy acylokoenzymu A ulega odwodornieniu przez FAD. Powstaje kwas o wiązaniu podwójnym, połączony z CoA. W drugim etapie podwójne wiazanie ulega rozerwaniu w wyniku przyłączenia wody w obecności enzymu hydratazy enoilo-CoA. Powstaje kwas hydroksyacylowy połączony z CoA. Ten z kolei ulega dehydratacji w reakcji katalizowanej przez dehydrogenazę 3-hydroksy-ksyacyloCoA. W wyniku działania enzymu acylotransferazy acetylo-CoA następuje odłączenie acetylo-CoA od dotychczasowego kwasu, w wyniku czego łańcuch kwasu tłuszczowego jest o dwa atomy węgla krótszy i do którego ponownie przyłączony CoA. Proces się powtarza. Końcowym produktem β-oksydacji jest bytyrylo-CoA, który rozkładany jest na dwie cząsteczki acetylo-CoA.
CECHY ATP-( ADENOZYNOTRIFOSFORAN) jest przenośnikiem energii swobodnej w większości procesów zużywających energię, ATP jest nukleotydem składającym się z adeiny, rybozy i trifosforanu. Aktywna formą ATP jest przeważnie kompleks z Mg+2 lub Mn+2. ATP jest czasteczką bogatą w energię ponieważ jego jednostka trifosforanowa zawiera dwa bezwodnikowe
wiązania fosforanowe. Duża ilość energi swobodnej jest uwalniana gdy ATP ulega hydrolizie do ADP i ortofosforanu(Pi) lub gdy jest on hydrolizowany do AMP (adenozynomonofosforanu) i pirofosforanu(PPi) ATP+H2O=ADP+Pi+H+
ATP+H2O=AMP+PPi+H+ ATP,ADP,AMP mogą ulegać wzajemnym przemianom, enzym kinaza adenylanowa(miokinaza) katalizuje
reakcje ATP+AMP=ADP+ADP energia swobodna uwalniana w czasie hydrolizy ATP jest wykorzystywana do przeprowadzenia reakcji wymagających jej dostarczenia np. skurcz mięśni. ATP służy jako bezpośredni donor energii swobodnej w układach biologicznych. ATP jest stabilny nie rozpada s...
Plik z chomika:
tospg2012
Inne pliki z tego folderu:
2.jpg (35 KB)
Biochemia 3 koło.doc (90 KB)
III koło.doc (21 KB)
TOS-matabolizm10.pdf (161 KB)
Inne foldery tego chomika:
Zgłoś jeśli naruszono regulamin
Strona główna
Aktualności
Kontakt
Dział Pomocy
Opinie
Regulamin serwisu
Polityka prywatności
Copyright © 2012 Chomikuj.pl