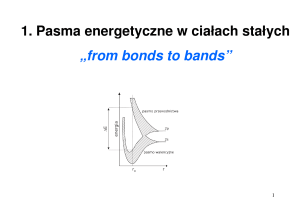
BUDOWA ATOMU cd.
MECHANIKA KWANTOWA
∗ zajmuje się opisem ruchu cząstek elementarnych,
∗ układ można opisywać posługując się współrzędnymi określającymi położenie bądź pęd,
∗ współrzędne określa się z pewnym przybliżeniem,
np. współrzędną x z dokładnością do Δx, a pęd cząstki z dokładnością do Δp,
tak więc: mechanika kwantowa zakłada istnienie prawdopodobieństwa Ρ
napotkania cząstki w danym miejscu dv w przestrzeni
Teoria Bohra (1913 r.)
Postulat I:
Elektron w atomie może przebywać w jednym z wielu możliwych stanów
energetycznych (tzw. stanów stacjonarnych). W stanie stacjonarnym elektron nie wypromieniowuje ani nie pochłania energii.
Postulat II:
Elektron może pobrać kwant energii docierającej do atomu z zewnątrz i
przejść do stanu stacjonarnego o wyższej energii lub może oddać kwant
energii w formie fali elektromagnetycznej i przejść do stanu stacjonarnego
o niższej energii.
Niels Bohr (1885-1962)
Nagroda
Nobla w 1922 r.
Zmiana orbity może nastąpić tylko w wyniku absorpcji lub emisji kwantu
promieniowania hν: EII − EI = h · ν
Całkowita energia elektronu na n-tej orbicie: E = Ek + Ep
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
PODSTAWY WSPÓŁCZESNEJ TEORII KWANTOWEJ
(1) Elektron w atomie może przebywać w jednym z wielu możliwych
stanów kwantowych, określonych wartościami:
- energii → główna liczba kwantowa n
- momentu pędu → orbitalna (poboczna) liczba kwantowa l
- rzutu momentu pędu na wyróżniony kierunek → magnetyczna liczba kwantowa m
- spinu → spinowa liczba kwantowa s
(2) W żadnym stanie kwantowym elektron nie wypromieniowuje ani nie pochłania
energii, tzn. nie zmienia wartości momentu pędu i spinu ani ich orientacji
przestrzennej.
(3) Elektron może absorbować kwant energii docierający do atomu z zewnątrz
i przejść do stanu kwantowego o wyższej energii lub może emitować do otoczenia
kwant energii w formie fali elektromagnetycznej przechodząc równocześnie
do stanu kwantowego o niższej energii.
(4) Nie można określić równocześnie dokładnego położenia i pędu elektronu w danej
chwili (zasada nieoznaczoności Heisenberga).
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
(5) Ruch elektronu w atomie opisuje się równaniem różniczkowym zwanym
równaniem Schrödingera (1926 r.), którego rozwiązaniami nie są liczby,
lecz funkcje zwane funkcjami falowymi i odpowiadające im wartości energii.
∂ 2Ψ ∂ 2Ψ ∂ 2Ψ 8 π2 ⋅ me
+
+
+
(E − Ep )Ψ = 0
∂x 2 ∂y 2 ∂z 2
h2
Ψ - amplituda fali de Broglie’a, funkcja falowa
Ψ2 - gęstość prawdopodobieństwa napotkania elektronu
ρ = ρ (x, y, z) = |Ψ (x, y, z)|2
Równanie Schrödingera można całkowicie rozwiązać
dla atomu wodoru i jonów pokrewnych zawierających
tylko jeden elektron, takich jak: He+ i Li2+.
Erwin Schrödinger
(1887-1961)
Nagroda Nobla w 1933 r.
(6) Dla każdego stanu kwantowego można obliczyć prawdopodobieństwo przebywania elektronu w danej odległości od
jądra, określić kształt i rozmiary tzw. orbitalu atomowego.
Orbital to przestrzeń, w której prawdopodobieństwo
znalezienia elektronu jest największe.
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
0,3
0,1
0,03
(7) Zbiór stanów kwantowych o wspólnej wartości głównej liczby kwantowej n nosi
nazwę powłoki (warstwy) elektronowej.
Główna liczba kwantowa n określa energię elektronu w atomie.
Maksymalna liczba stanów kwantowych w danej powłoce, tj. maksymalna
liczba elektronów na danej powłoce wynosi 2n2.
wartość n:
1
symbol powłoki:
K
max. liczba elektr.: 2
2
L
8
3
M
18
4
5
N O
32
6
P
7
Q
itd.
itd.
itd.
(8) Zbiór stanów kwantowych, z których wszystkie mają wspólną wartość n oraz
wspólną wartość orbitalnej (pobocznej) liczby kwantowej l (ale nigdy n = l)
nazywa się podpowłoką elektronową.
Poboczna liczba kwantowa l określa rodzaj orbitalu w danej powłoce.
Liczba kwantowa l, dla danej wartości głównej liczby kwantowej n, przyjmuje
wartości: l = 0, 1, 2 ... (n-1), np. jeżeli n = 3 to l = 0, 1, 2.
Liczba elektronów w danej podpowłoce (orbitalu) wynosi: 4·l + 2
wartość l:
0
symbol podpowłoki:
s
max. liczba elektronów: 2
1
p
6
2
d
10
3
f
14
4
g
itd.
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
(9) Zbiór stanów kwantowych o wspólnych wartościach liczb kwantowych:
głównej n, pobocznej l i magnetycznej m nosi nazwę poziomu orbitalnego
(także zwanego orbitalem, lecz oznaczanego np. px, py, pz
Liczba poziomów orbitalnych w powłoce (warstwie) wynosi n2,
natomiast w podpowłoce 2·l + 1.
Magnetyczna liczba kwantowa m przyjmuje wartości: -l ≤ m ≤ +l
Magnetyczna liczba kwantowa m (lub ml) określa zachowanie się
orbitalu w polu magnetycznym.
Do każdego poziomu orbitalnego należą dwa elektrony różniące się orientacją
przestrzenną wektora spinu, s = ± 1/2
Tak więc:
powłoka – zawiera elektrony o tej samej wartości n
podpowłoka – to zbiór elektronów o tej samej wartości n i l
orbital – zawiera elektrony o tej samej wartości n, l i m
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
(10) Spinowa liczba kwantowa s (lub ms) określa w uproszczeniu tzw. kręt elektronu.
Do każdego poziomu orbitalnego należą dwa elektrony różniące się orientacją
przestrzenną wektora spinu, s = ± 1/2
symbol podpowłoki:
liczba poziomów orbitalnych:
symbol orbitalu:
s
1
s
px
p
3
py p z
dxz
d
5
dxy dyz
d x2 −y 2 d z 2
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
n
l
Orbital
m
s
Maksymalna liczba
elektronów
podpowłoka
powłoka
2
1 (K)
0
1s
0
± 1/2
2
2 (L)
0
1
2s
2p
0
-1, 0, +1
± 1/2
± 1/2
2
3 (M)
0
1
2
3s
3p
3d
0
-1, 0, +1
-2, -1, 0, +1, +2
± 1/2
± 1/2
± 1/2
2
6
10
18
4 (N)
0
1
2
3
4s
4p
4d
4f
0
-1, 0, +1
-2, -1, 0, +1, +2
-3, -2, -1, 0, +1, +2, -3
± 1/2
± 1/2
± 1/2
± 1/2
2
6
10
14
32
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
6
8
z
x
s
y
z
z
z
x
y
x
px
z
dxy
z
x
y
dxz
z
x
x
y
pz
y
z
x
y
py
y
z
x
dyz
y
dx2-y2
kształt orbitali i równania funkcji falowych
http://winter.group.shef.ac.uk/orbitron/index.html
y
Orbitale.url
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Orbital 1s
Orbital 2s
Orbitale 2p
Orbitale 3p
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
x
dz2
Orbitale 3d
Orbitale 4f
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
http://winter.group.shef.ac.uk/
orbitron/index.html
Orbitale.url
Orbital atomowy 3p - funkcja falowa Ψ oraz gęstość elektronowa Ψ2
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
1H
2He
K1
K2
1s1
1s2
1s
3Li
K2L1
1s22s1
4Be
K2L2
1s22s2
2s
2p
5B
...
10Ne
K2L3
1s22s22p1
3s
3p
3d
K2L8
1s22s22p6
11Na
K2L8M1
1s22s22p63s1
4s
4p
4d
K2L8M3
1s22s22p63s23p1
5s
5p
5d
K2L8M8
1s22s22p63s23p6
19K
K2L8M8N1
1s22s22p63s23p64s1
6s
6p
6d
20Ca
K2L8M8N2
K2L8M9N2
1s22s22p63s23p64s2
1s22s22p63s23p64s23d1
7s
7p
...
13Al
...
18Ar
21Sc
...
4f
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
ZAKAZ PAULIEGO − w atomie nie mogą znajdować się
elektrony o jednakowych czterech liczbach kwantowych.
REGUŁA HUNDA − najkorzystniejsze energetycznie
jest takie zapełnianie orbitali, przy którym liczba
elektronów o niesparowanych spinach w obrębie
danej podpowłoki jest największa.
↑↓
↑ ↓ ↑↓ ↑↓
s
p
↑↑
↑↓
↑
↑↓ ↑↓
↑
↑
↑
d
↓
↑
↓
↓
↓↓ ↑↓
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Wolfgang Pauli
(1900-1958)
Nagroda Nobla w 1945 r.
PROMIENIE KOWALENCYJNE ATOMÓW PIERWIASTKÓW
Pierwiastek
Li
Be
B
C
N
r [Å]
ładunek jądra
(liczba protonów)
1,23
0,89
0,80
0,77
0,74
0,74 0,72
+3
+4
+5
+6
+7
+8
+9
liczba elektronów
na powłoce K
liczba elektronów
na powłoce L
2
2
2
2
2
2
2
1
2
3
4
5
6
7
Li
Na
K
Rb
Cs
r [Å]
1,23
1,57
2,03
2,16
2,35
ładunek jądra
+3
+ 11
+ 19
+ 37
+ 55
O
elektrony walencyjne
1
1
1
1
1
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
F
Promienie kowalencyjne pierwiastków (w Å)
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
POTENCJAŁ JONIZACYJNY (ENERGIA JONIZACJI – Ej )
Me → Me+ + e
( Me + hν → Me+ + e )
Energia jonizacji - energia, jakiej należy dostarczyć, aby od izolowanego
atomu w stanie gazowym oderwać najluźniej związany elektron.
Pierwiastek
Na
Mg
Al
Si
P
S
Cl
Ar
Ej (I) (kJ/mol)
496
737
577
786
1012
999
1255
1521
1600
2500
Ne
2000
↑↓
Be, Mg
Ar
1400
Cl
1200
1500
F
N
1000
↑↓
O
C
Be
Li
0
Li
Be
B
↑
↑
N, P
B
500
↑
C
N
O
F
Ne
↑↓
↑↓ ↑↓ ↑↓
Ne, Ar
P
1000
S
800
Mg
Si
600
Al
Na
400
200
0
Na
Mg
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Al
Si
P
S
Cl
Ar
Be
Ej (I)
(kJ/mol)
899
Ej (II) Ej (I+II)
(kJ/mol) (kJ/mol)
1760
2659
Mg
737
1450
2187
Ca
Sr
590
549
1150
1060
1740
1609
Ba
503
960
1463
3000
Be
Ej (I)
2500
Ej (II)
Ej (I+II)
Mg
2000
Be
Ca
Sr
Mg
1500
Ba
Ca
1000
Sr
Be
Ba
Mg
Ca
Sr
Ba
500
0
Be
↑↓
Ej (I)
(kJ/mol)
Ej (II)
(kJ/mol)
Ej (III)
(kJ/mol)
Li
520
7300
Na
496
4560
Be
Mg
899
737
1760
1450
14850
7740
Al
577
1810
2750
Mg
Ca
Sr
Ba
Ej (IV)
(kJ/mol)
11580
W wyniku oderwania jednego lub więcej elektronów z ostatniej powłoki powstają kationy.
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Pierwsze energie jonizacji pierwiastków (w kJ/mol)
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
POWINOWACTWO ELEKTRONOWE
(ELEKTRONOPOWINOWACTWO – Pe )
X + e → X–
( X + e → X– + hν)
Powinowactwo elektronowe - energia, jaka się wydziela podczas przyłączania
pierwszego elektronu do izolowanego atomu w stanie gazowym.
Pierwiastek
Li
Be
B
C
N
O
F
Liczba elektronów walencyjnych
1
2
3
4
5
6
7
Pe (kJ/mol)
60
- 241
27
122
0
141
328
Pe (kJ/mol)
Pe (kJ/mol)
O
141
F
328
S
200
Cl
347
Se
195
Br
325
Te
190
I
295
W wyniku przyłączenia jednego lub dwóch elektronów do obojętnego atomu powstają aniony.
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
PROMIENIE ATOMOWE I JONOWE
Pierwiastek
Na
Mg
Al
Si
P
r [Å]
1,57
1,36
1,25
1,17
1,10
Jon
Na+
Mg2+
Al3+
Si
P
r [Å]
1,02
0,72
0,54
r [Å]
r [Å]
S
Cl
Ar
1,04 0,99 1,91
S2–
Cl–
1,84 1,81
r [Å]
r [Å]
r [Å]
Be
0,89
Be2+
0,45
F
0,72
F–
1,33
Fe
1,17
Mg
1,36
Mg2+
0,72
Cl
0,99
Cl–
1,81
Fe2+
0,76
Ca
1,74
Ca2+
1,00
Br
1,14
Br–
1,96
Fe3+
0,64
1,33
I–
2,20
Zn
1,25
Zn2+
0,74
Sr
1,91
Sr2+
1,18
Ba
1,98
Ba2+
1,35
I
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Porównanie promieni atomów i jonów
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
ELEKTROUJEMNOŚĆ (χ)
Elektroujemność - tendencja (dążność) atomu w cząsteczce związku
chemicznego do przyciągania do siebie elektronów.
skale elektroujemności: - Pauling (1932 r.)
- Mullikan (1935 r.)
- Allred i Rochow (1958 r.)
cząsteczka: A – A ⇒ EA-A
B – B ⇒ EB-B
dla EA-B Pauling zaproponował średnią geometryczną:
E A −B = E A − A ⋅ E B −B
np.
Δχ = 0,088 Δ
Δ = 125,9 kJ/mol
Δ χ = χN - χH = 1,0
dla wiązania N – H
więc:
Linus Carl Pauling
(1901-1994)
Nagroda Nobla
w 1954 r. z chemii
i w 1962 pokojowa
Zał.: w celu otrzymania dla C i F wartości,
odpowiednio 2,5 i 4,0 przesunięto początek
skali z χH = 0 do χH = 2,1
Pierwiastek
Li
Be
B
C
N
O
F
χ
1,0
1,5
2,0
2,5
3,0
3,5
4,0
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
Elektroujemność pierwiastków według Paulinga
dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii