2. WIĄZANIA CHEMICZNE,
BUDOWA CZĄSTECZEK
Irena Zubel
Wydział Elektroniki Mikrosystemów i Fotoniki
Politechnika Wrocławska
(na prawach rękopisu)
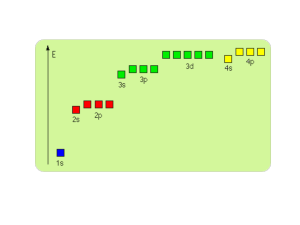
Wiązania chemiczne
Podstawowe stany skupienia materii (w temp. otoczenia):
• gazy - cząsteczki (H2, O2, CO2), atomy (He, Ar) – brak oddziaływań
• ciecze – cząsteczki (H2O, CH3OH)- oddziaływania słabe
- jony (stopione sole)
- atomu lub skupiska atomów (stopione metale)
• ciała stałe – atomy, cząsteczki, jony połączone silnymi oddziaływaniami
w strukturę ciągłą
Typy oddziaływań miedzy atomami:
• wiązania chemiczne – oparte na wymianie elektronów walencyjnych
• oddziaływania o charakterze fizycznym – siły van der Waalsa
Typy wiązań:
• wiązania kowalencyjne (atomowe) -uwspólnienie elektronów
walencyjnych sąsiadujących atomów
• wiązana jonowe – przeniesienie elektronów walencyjnych od jednego
rodzaju atomów do drugiego
• metaliczne – uwspólnienie części elektronów walencyjnych bardzo wielu
atomów
Wiązania chemiczne
Przy zbliŜaniu się do siebie atomów mogą zachodzić między nimi róŜnego
typu oddziaływania, zaleŜne od rodzaju tych atomów:
- siły odpychające związane są z efektami kwantowymi, wynikającymi
z nakładanie się powłok elektronowych i z oddziaływaniami kulombowskimi
- siły przyciągające wynikają z oddziaływań między elektronami
walencyjnym, z fluktuacji rozkładu gęstości ładunku itp.
DąŜenie układu do osiągnięcia min. energii jest
przyczyną tworzenia się wiązań chemicznych.
H + H → H2 + 436 kJ/mol ← energia wiązania
Klasyczna teoria wiązań chemicznych to
elektronowa teoria wiązań Levis’a (1916):
KaŜdy atom dąŜy do takiej zmiany zewnętrznej
powłoki elektronowej, aby uzyskać najtrwalszą
konfigurację, tzn. minimum energii. Trwałe
konfiguracje to: s2, s2p6, s2p6d10.Teoria ta dotyczy
zarówno wiązań kowalencyjnych jak i jonowych.
F odpychające
E↑
F przyciągające
E↓
Wiązania kowalencyjne
Wiązanie kowalencyjne – powstaje między atomami posiadającymi
niesparowane elektrony walencyjne. Polega ono na utworzeniu wspólnej
pary elektronowej, naleŜącej jednocześnie do obu atomów.
H: s1
H:
s1
H2:
O: s2p4
O:
s2p4
O2 :
dąŜenie do uzyskania trwałej konfiguracji s2 lub s2p6
Cząsteczki z wiązaniami kowalencyjnymi opisuje się za pomocą wzorów
elektronowych lub kreskowych, tzw. wzorów Levisa:
H2:
O2:
H H
O O
H¯ H
¯ ¯O
¯
O
¯
¯ ¯
W przyrodzie gazy te występują w postaci cząsteczek
dwuatomowych, co potwierdza teorię Levise’a
Wiązania kowalencyjne
Powstawanie orbitali molekularnych
Przy dostatecznie małej odległości dwóch atomów ich chmury elektronowe
przenikają się wzajemnie, tworząc wiązania kowalencyjne między atomami.
Kształty orbitali powstających cząsteczek (orbitali molekularnych) wynikają
z nakładania się funkcji falowych poszczególnych atomów.
W przypadku najprostszej cząsteczki H2 mogą zaistnieć dwa przypadki:
- funkcje falowe dotyczą elektronów o spinach zgodnych
- funkcje falowe dotyczą elektronów o spinach przeciwnych
Na gruncie mechaniki kwantowej moŜna udowodnić, Ŝe gdy elektrony mają
spiny zgodne, to wypadkowa funkcja falowa (molekularna) ma dwa maksyma
rozsunięte względem osi cząsteczki (prawdopodobieństwa znalezienia
elektronu między jądrami jest małe). Gdy mają spiny przeciwne, gęstość
prawdopodobieństwa jest największa w obszarze między jądrami atomów, co
wskazuje na istnienie wiązania.
Dodatkowy warunek powstania wiązania kowalencyjnego (oprócz istnienia
niesparowanych elektronów):
Spiny elektronów tworzących wiązanie muszą być skierowane przeciwnie.
Wiązania kowalencyjne
Powstawanie orbitali molekularnych
orbital antywiąŜący
E(R)
R
Emin
Gęstość chmury elektronowej
między jądrami atomów mała,
poniewaŜ zgodnie z zakazem
Pauliego dwa elektrony nie mogą
znajdować się w tym samym
stanie kwantowym (na tym samym
orbitalu). Jądra się odpychają.
Energia układu wzrasta.
orbital wiąŜący
- Gęstość chmury elektronowej między jądrami atomów duŜa.
- Oddziaływania elektrostatyczne jądro - elektrony rosną.
- Powstają siły przyciągająca (Emin), powstaje stabilne wiązanie
Wiązania kowalencyjne
Klasyczna teoria Levis’a nie wystarcza do opisu wszystkich cząsteczek
występujących w przyrodzie, np: BeF2, B3, CH4. Dodatkowe postulaty
wprowadzono w wyniku zastosowania mechaniki kwantowej (Pauling 1931).
Hybrydyzacja orbitali:
•atomy podczas łączenia się w cząsteczki dąŜą do ujednolicenia orbitali
elektronowych ostatniej powłoki,
•orbitale shybrydyzowane są róŜne od orbitali s, p, d,
•w powstałej cząsteczce wszystkie orbitale są równocenne, są one kombinacją
liniową funkcji falowych s2, p6,d10, nazywane są orbitalami molekularnymi.
Reguła maksymalnej odległości - przestrzenie orbitalne orbitali
shybrydyzowanych są tak rozmieszczone, aby odległości między nimi były jak
największe.
s2p2
hybrydyzacja
sp3
http://www.kurssikory.pl/contents/pliki/materialy/KM9DCH000.pdf
Wiązania kowalencyjne
Hybrydyzacja
Przykłady hybrydyzacji
Be: s2p0
➞
sp
B: s2p
➞
sp2
C: s2p2
➞
sp3
F: s2p5
➞ nie hybrydyzuje
Etap I
stan
wzbudzenia
Etap II - powstawanie cząsteczki
F
F
BeF2:
BF3:
Be
F
B
F
F
F
F
B
F ― Be ― F
F
Wiązania kowalencyjne
Orientacja przestrzenna orbitali:
atomowych
shybrydyzowanych
Orbitale molekularne
sp 180°
F ― Be ― F
F
sp2 120°
F
B
F
sp3 109,4°
C: 2s2 2p2
N: 2s2 2p3
O: 2s2 2p4
Wiązania kowalencyjne
Kształty cząsteczek
trygonalna
BF3
s↷ p
liniowa
BeCl2
s↷ d
p↷d
Kształty cząsteczek powstałych w oparciu o przestrzenną
orientację orbitali molekularnych
tetraedryczna
CH4
oktaedryczna
bipiramidalna
SF6
PCl5
Na podstawie kształtów
orbitali molekularnych
moŜna przewidywać
kształty cząsteczek.
Wiązania kowalencyjne
Kształty cząsteczek
Ukształtowanie
przestrzenne
Rodzaj
hybryd.
Struktura pierwiastka
Związek
liniowe
sp
Be:1s2 2s2➞ sp
BeF2
trygonalno płaskie
sp2
B: 1s2 2s22p ➞sp2
BF3
tetraedryczne
sp3
C: 1s2 2s22p2 ➞sp3
CH4
kwadratowo
płaskie
sp2d
Ni: 1s2 2s22p63s23p6 4s23d8
[Ni(CN)4]2-
trygonalno
dwupiramidowe
sp3d
P: 1s2 2s22p6 3s23p3 ➞ sp3d
PCl5
oktaedryczne
sp3d2
S: 1s2 2s22p6 3s23p4 ➞sp3d2
SF6
pentagonalno
dwupiramidalne
sp3d3
I: 1s2 2s22p6 3s23p6 4s23d104p6
5s24d105p5 ➞ sp3d3
IF7
Czyste wiązania kowalencyjne
Wiązania kowalencyjne tzw. „czyste” to wiązania czysto kowalencyjne.
Występują między atomami homojądrowymi (atomami tego samego
pierwiastka). Tworzą się zgodnie ze wszystkimi poznanymi regułami.
Wiązania te mogą być pojedyncze (jak w cząsteczkach H2, O2, Cl2 lub
wielokrotne- podwójne, potrójne (jak w cząsteczkach S2, N2 oraz w wielu
cząsteczkach związków organicznych między atomami węgla)
N
IN≡NI
S
Cl: 1s2 2s2 2p3 3s2 3p5
S
Cl Cl
S¯ = S̄
¯ ¯
¯
C̄l ¯ Cl
¯
¯
¯
N
S: 1s2 2s2 2p6 3s2 3p4
¯
N: 1s2 2s2 2p3
Czyste wiązania kowalencyjne
Wiązania wielokrotne
Nakładanie się orbitali atomowych podczas tworzenia orbitali cząsteczkowych
moŜe zachodzić na dwa sposoby. W wyniku osiowego nałoŜenia się orbitali
atomowych tworzących orbitel molekularny powstają wiązania typu σ (sigma).
W wyniku bocznego nakładania się orbitali atomowych powstają wiązania typu
π (pi).
Wiązanie σ moŜe powstać w wyniku nałoŜenia się dwóch orbitali typu s, dwóch
orbitali p oraz orbitali s i p. Skierowane jest ono wzdłuŜ prostej łączącej jądra
dwóch atomów. Powstają orbitale molekularne s-s, p-p lub s-p. JeŜeli
występuje nakładanie się tylko dwóch orbitali, w cząsteczce powstaje
wiązanie pojedyncze.
Wiązania typy π powstają zawsze po utworzeniu wiązania σ. Stanowią drugie
albo trzecie wiązanie między dwoma atomami (wiązania wielokrotne). Wiązanie
podwójne złoŜone jest z wiązania σ i wiązania π, wiązanie potrójne z wiązania
σ i dwóch wiązań π. Wiązania π są słabsze od wiązania σ. PoniewaŜ
cząsteczka ma kształt określony kształtem orbitali molekularnych, wiązania typu
π nie mogą leŜeć w tej samej linii co wiązania σ.
Czyste wiązania kowalencyjne
Wiązania wielokrotne
H
|
H―C―H
|
H
Metan
CH4
Etan
C2H6
Eten
C2H4
s-p (HCl)
H H
| |
H―C―C―H
| |
H H
H
H
C =C
H
Etyn
C2H2
s-s (H2)
p-p (Cl2)
( S2 )
H
H―C Ξ C―H
( N2 )
Sposób tworzenia się
wiązania π
Czyste wiązania kowalencyjne
Energia wiązania
Energia wiązania - jest to energia niezbędna do rozerwania wiązania między
atomami tworzącymi cząsteczkę.
Długość wiązania – odległość między jądrami związanych atomów.
Wraz ze wzrostem krotności wiązania rośnie energia wiązania i maleje długość
wiązania.
Typ wiązania
| |
―C―C―
| |
Energia wiązania
[kJ/mol ] (eV)
343 (3,43)
Długość wiązania
[pm]
154
C =C
―C Ξ C―
615 (6,15)
802 (8,02)
133
120
Wiązania kowalencyjne to wiązania silne i krótkie.
Długości wiązania
wybranych cząsteczek
[pm]
H2
F2
Cl2
N2
O2
HF
72
142
199
109,4
120,7
92
Wiązania kowalencyjne spolaryzowane
W cząsteczkach homojądrowych prawdopodobieństwo znalezienia elektronów
wokół obu atomów jest jednakowe. Gdy wiązanie tworzą dwa róŜne atomy –
wspólna para elektronowa jest przyciągana przez atom pierwiastka bardziej
elektroujemnego. Takie wiązanie nazywamy spolaryzowanymi.
Moment dipolowy (wektor skierowany od „-” do „+” dipola):
µ =|q | d
gdzie q- ładunek jednego bieguna, d- odległość biegunów
Moment dipolowy układu atomów tworzących wiązanie - moment dipolowy
grupy. Moment dipolowy cząsteczki – wypadkowa momentów grupowych.
+
-
+
+
¯
H ¯ F¯
¯
-
Cząsteczki polarne: CO, HF, H2O, NH3 (µ≠0)
Wiązania kowalencyjne spolaryzowane cd.
Cząsteczki niepolarne: - homojądrowe H2, N2, Cl2 (µ = 0)
- CH4, CO2, BF3 (Σ µ = 0 )
F
F
¯ = C = Ō
O
¯
¯
B
F
+
+
-
-
+
-
-
+
+
+
+
-
-
+
(Σ µ = 0 )
(Σ µ = 0 )
(Σ µ = 0 )
-
+
Wiązania kowalencyjne
koordynacyjne, donorowo- akceptorowe
Wiązanie donorowo – akceptorowe (wiązanie koordynacyjne) powstaje wtedy,
gdy wiąŜąca para elektronowa pochodzi od jednego z atomów.
Donor – atom, który dostarcza wolną parę elektronową
Akceptor – atom, który przyjmuje parę elektronową na swój wolny orbital
H
+
|
H―N→H
|
H
H ¯F
| |
¯
= H―N →B―F
| | ¯
H F
amoniak NH3
rozpuszczony w
wodzie
N: 1s2 2s22p3
¯
¯
¯
¯
¯
¯
¯
¯
¯F
H
|
|
¯
H―N Ι + B―F
| ¯
|
F
H
¯
¯
H
¯
H
H
|
H―N Ι + H+ =
|
H
¯
H
B: 1s2 2s2p1
Wiązania kowalencyjne
koordynacyjne, donorowo- akceptorowe
Przykłady jonów z wiązaniami koordynacyjnymi
O: 1s2 2s22p4
III okres: P, S, Cl (H3PO4, H2SO4, HClO4)
¯
¯
¯
¯
¯
3-
¯
↑
¯ ← P→
O←
→¯ O
¯ ↓ ¯
O
II okres: B, C, N (HNO3, H2CO3, H3CO3)
¯
O
¯
¯
¯
¯
O
¯
N
ΙΙ
¯
¯
O
S2-: 1s2 2s22p6 3s23p6
¯
¯
¯
¯
¯
¯
¯
↑
¯ ←S →¯ O
O←
¯ ↓ ¯
O
¯
¯
¯
¯
¯
↑
¯O
¯O←
←Cl →
¯ ↓ ¯
O
¯O
2-
¯
¯O
-
¯
¯
¯O
Cl-: 1s2 2s22p6 3s23p6
- krotność wiązania: 4/3
- długość wiązania: 121,8pm
dla N―O : 146pm
dla N = O : 115pm
P3-: 1s2 2s22p6 3s23p6
N-: 1s2 2s22p4
Wiązania kowalencyjne
Podsumowanie
Wiązania kowalencyjne wykazują następujące właściwości:
•powstają między atomami o duŜej elektroujemności (blok p)
•mają charakter kierunkowy
•mogą występować w dowolnym stanie skupienia:
gazy (H2, N2, O2, NH3)
ciecze (H2O, CH3OH, H3PO4, HNO3)
ciała stałe (kryształy kowalencyjne: Si, SiO2, GaAs, SiC,
kryształy molekularne: lód, cukier, CO2 zestalony)
•tworzą wiązania pojedyncze i wielokrotne
•energia wiązania i długość wiązania zaleŜą od krotności wiązania
Istotną cechą w klasyfikacji wiązań jest róŜnica elektroujemności tworzących je
atomów. Gdy róŜnica elektroujemności jest < 0,4 – wiązania kowalencyjne
1,4 – 1,7 – kowalencyjne spolaryzowane
> 1,7 - wiązania jonowe
Wiązania kowalencyjne
Podsumowanie
Jak określić udział charakteru
ZaleŜność między udziałem charakteru
jonowego w wiązaniu?
jonowego w wiązaniu a róŜnicą
elektroujemności.
µ – wyznaczono na podstawie przenikalności
XA –XB Udział charakteru
elektrycznej (stałej dielektrycznej) związku
jonowego [%]
0,2
0,4
0,6
1,2
1,4
1,7
1,8
2,2
2,6
3,2
1
4
15
30
39
50
55
70
82
92
µmax =|q|d – obliczono przy załoŜeniu, Ŝe cały
ładunek zgromadzony jest w odległości równej
długości wiązania (wiązanie czysto jonowe)
Moment dipolowy Długość
Związek µ [D] q·d [D] wiązania
[pm]
HF
HCl
HBr
HI
1,98
1,08
0,79
0,38
4,42
6,07
6,82
7,74
92
128
143
162
µ/q·d [%]
45
18
12
5
Wiązania jonowe
Wiązanie jonowe jest wynikiem maksymalnej polaryzacji wiązania
kowalencyjnego. Polega ono na przeniesieniu elektronu od atomu mniej
elektroujemnego do atomu bardziej elektroujemnego
• występuje tylko w związkach chemicznych, nigdy miedzy atomami tego
samego pierwiastka
•
tworzą je atomy o duŜej róŜnicy elektroujemności
•
skłonność atomów do tworzenia wiązania jonowego jest tym większa, im
większa jest róŜnica elektroujemności
•
atomy pierwiastków początkowych grup układu okresowego oddają
elektrony, tworzą kationy
•
atomy pierwiastków końcowych grup układu okresowego uzupełniają
brakujące elektrony, tworzą aniony
•
nie mają charakteru kierunkowego, mają zapełnione zewnętrzne powłoki,
co daje symetrię sferyczną, analogiczną do gazu szlachetnego
•
polega głównie na oddziaływaniu elektrostatycznym
•
występuje wyłącznie w ciałach stałych o ciągłej strukturze krystalicznej
Wiązania jonowe
Powstawanie wiązania jonowego
zachodzi w kilku etapach:
•jonizacja atomów sodu – dostarczenie
energii (energia jonizacji)
•jonizacja atomów chloru – wydzielenie
energii (powinowactwo elektronowe)
•połączenie się jonów – wydzielenie
energii (energia sieci)
Bilans energetyczny
prowadzi do wyznaczenia
energii wiązania
Energia potencjalna układu Na + Cl
Wiązania jonowe
Wiązania metaliczne
Wiązania metaliczne występują miedzy atomami metali tworzących sieć
krystaliczną, a więc w ciele stałym. Dotyczą duŜej liczby pierwiastków (85 ze100).
• zjonizowane dodatnio atomy metali (kationy) tworzą gęsto upakowaną sieć
krystaliczną
• uwolnione w wyniku jonizacji elektrony walencyjne są zdelokalizowane (nie
są przypisane do określonych jonów) i poruszają się swobodnie w obrębie
całej sieci krystalicznej, tworząc tzw. gaz elektronowy
• wiązania metalicznego są wynikiem równowagi dwóch sił: elektrostatycznego
oddziaływania dodatnich jonów metalu z „chmurą elektronową” i sił
odpychania między jednoimiennymi jonami w sieci.
• wiązania metaliczne nie są kierunkowe; dobre przewodnictwo ciepła i prądu
W oparciu o fizykę kwantową:
Funkcje falowe elektronów walencyjnych atomów pierwiastków
metalicznych są bardzo rozległe, porównywalne z odległościami między
atomami w sieci. Występuje więc „zachodzenie na siebie” funkcji falowych, w
wyniku czego gęstość prawdopodobieństwa znalezienia elektronu jest stała w
całej objętości kryształu. Elektrony zachowują się jak elektrony swobodne.
Wiązania metaliczne
Właściwości mechaniczne
sieć metaliczna
przemieszczenie się względem
siebie atomów nie powoduje
naruszenia struktury sieci
sieć jonowa
plastyczność
przemieszczenie się jonów
skutkuje pojawieniem się
sił odpychających
sieć kowalencyjna
wiązania sztywne, kierunkowe,
następuje ich zerwanie
Oddziaływania o charakterze fizycznym
- siły van der Waalsa
Oddziaływania międzycząsteczkowe
(siły van der Waalsa, wiązania
drugiego rzędu) – słabe oddziaływania elektrostatyczne miedzy atomami lub
cząsteczkami, nie mają charakteru wiązania chemicznego
• mają wpływ na stan skupienia materii (topnienie, wrzenie, kondensacja,
krystalizacja gazów CO2, N2, skraplanie gazów szlachetnych)
• są odpowiedzialne za adsorpcję fizyczną
• ujawniają się szczególnie w niskiej temperaturze, gdy słabną drgania
termiczne cząsteczek i atomów
• są bardzo słabe, 4-40kJ/mol (ok.10% energii typowego wiązania chemicznego)
• występują zawsze, odgrywają jednak rolę tylko wtedy, gdy inne wiązania nie
są moŜliwe
• źródłem wiązania jest trwały lub indukowany moment dipolowy cząsteczek lub
fluktuacje ładunku w atomach (cząsteczkach) obojętnych
Siły van der Waalsa
Rodzaje
Siły dyspersyjne: występują między atomami lub cząsteczkami, które nie mają
trwałych momentów dipolowych Polegają na wzajemnym przyciąganiu się dipoli
szybkozmiennych powstających wskutek chwilowych fluktuacji ładunku
(chwilowej polaryzacji). Są to oddziaływania bardzo bliskiego zasięgu (E~1/r6),
wskazane jest zwiększone ciśnienie.
+
+
-+
+
-+
-+
Siły indukcyjne: występują w układzie
dipol-cząsteczka obojętna. Wskutek
indukcji powstaje oddziaływanie dipol- dipol indukowany.
Siły orientacji: oddziaływania dipoldipol (woda, amoniak, skroplony HCl).
-+
-+
+
-+
+
-
+
+
-
+
-
+
-
+
Wiązania wodorowe
Wiązanie wodorowe powstaje między atomem wodoru związanym z atomem o
duŜej elektroujemności, a atomem posiadającym wolne pary elektronowe.
Np. w silnie spolaryzowanej cząsteczce wody atom wodoru jest prawie zupełnie
pozbawiony elektronu. Jest on przyciągany przez atom tlenu sąsiedniej
cząsteczki wody, który ma dwie wolne pary elektronowe.
Wiązanie to moŜe być traktowane jako: -elektrostatyczne (dipol – dipol)
- kowalencyjne (donorowo- akceptorowe )
Wskutek tych wiązań w wodzie powstają grupy cząsteczek wody (asocjaty),
złoŜone średnio z 6 cząsteczek wody, połączonych tzw. mostkami wodorowymi.
Wiązanie
wodorowe
O – H…O
O – H…N
N – H …O
N – H …N
F – H …F
Energia
[kJ/mol]
12,5 – 33,4
16,7 – 29,3
12,5 – 16,7
5,4 – 20,9
20,9 – 33,4
Wiązania wodorowe
Energia wiązań wodorowych jest większa od energii oddziaływań van der Waalsa.
Wiązania wodorowe są przyczyną wysokiej temperatury wrzenia wody i topnienia
lodu.
T wrzenia
T topnienia
Elektroujemność
Grupa 15 Grupa 16
N : 3,0
O: 3,5
P:
S:
2,1
2,5
As: 2,0
Se: 2,4
Sb: 1,9
Te: 2,1
H: 2,1
Temperatura wrzenia i topnienia zawiązków
wodoru z tlenowcami i azotowcami
Bez wiązań wodorowych nie
byłoby Ŝycia na Ziemi - woda
istniałaby w postaci pary!
Układ okresowy pierwiastków