Plan metodyczny lekcji chemii w klasie drugiej gimnazjum
1. Imię i nazwisko prowadzącego zajęcia
Dorota Bęben
2. Typ szkoły
Gimnazjum
3. Przedmiot
chemia
4. Klasa
2
5.Temat lekcji/ dwie jednostki lekcyjne/
Wiązania chemiczne.
6. Cele lekcji:
główny:
A/Uczeń wie na czym polega wiązanie jonowe i atomowe.
B/Uczeń zna zależność właściwości związku chemicznego od rodzaju wiązania chemicznego
pomiędzy atomami tworzącymi cząsteczkę.
szczegółowe:
A.Dla wiązania jonowego
Uczeń ma wiedzieć:
jak powstają wiązania jonowe/A/,
jakie pierwiastki biorą udział w wiązaniu jonowym/B/,
Uczeń ma umieć:
przedstawiać schematy tworzenia związków jonowych/C/,
zapisywać proces powstawania wiązania jonowego za pomocą równania/C/,
pisze wzory prostych jonów/C/,
podaje nazwy prostych kationów i anionów/C/,
podaje cechy substancji jonowych/D/.
B. Dla wiązania kowalencyjnego
Uczeń ma wiedzieć:
jakie pary pierwiastków tworzą wiązania kowalencyjne/A/,
co to jest wiązanie kowalencyjne spolaryzowane/A/.
Jak tworzą się asocjaty.
Uczeń ma umieć:
przedstawiać schematy wiązań atomowych dla cząsteczek pierwiastków i prostych związków
typu NH3, CH4, H2O, CO2 /C/,
podawać przykłady substancji kowalencyjnych/C/,
podawać przykłady wiązania kowalencyjnego pojedynczego, podwójnego i potrójnego/D/.
7. Wiadomości i umiejętności wyjściowe:
Uczeń zna budowę układu okresowego,
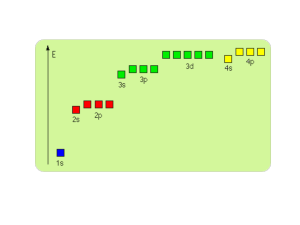
Zna budowę atomu (jądro, elektrony, protony powłoka elektronowa rdzeń atomowy ,
elektrony walencyjne),
Zna pojęcie wartościowości i potrafi tą wielkość wykorzystać przy tworzeniu wzorów
sumarycznych związków chemicznych,
Potrafi korzystać z układu okresowego ( okres i grupa), czyta niezbędne informacje( liczba
atomowa, liczba masowa),
Potrafi rysować modele atomów z grup głównych,
Pisze wzory sumaryczne związków chemicznych.
8. Dominujące metody kształcenia :
Prezentacja,
Metoda podająca,
Ćwiczenia uczniów.
9. Formy pracy uczniów;
Praca zbiorcza / aktywny udział uczniów w przedstawianiu pierwszego wiązania/
Praca w grupach – zapis schematów powstawania prostych związków chemicznych z
wiązaniem jonowym i wiązaniem kowalencyjnym,
Indywidualna praca ucznia / chętnego do rozwiązania trudniejszego wiązania/.
10. Środki i materiały dydaktyczne;
Zestaw komputerowy z rzutnikiem,
Układ okresowy,
Karty pracy ucznia.
11. Scenariusz lekcji:
A. Powitanie uczniów.
B. Sprawy organizacyjne.
C. Przedstawienie tematu lekcji .
D. Zapoznanie z głównymi celami lekcji.
E. Przypomnienie wiadomości z poprzednich lekcji niezbędnych do zrozumienia tematu i
osiągnięcia celów lekcji bieżącej:
Powtórzenie budowy układu okresowego,
Czym różnią się metale od niemetali,
Model atomu sodu, chloru, tlenu i wodoru,
Przypomnienie zapisu skróconego rozkładu elektronów za pomocą oznaczeń
powłok głównych (K,L,M,N,O,P),
F. Przedstawienie prezentacji umożliwiającej zrozumienie wiązania jonowego.
G. Ćwiczenia uczniów w pisaniu równań reakcji otrzymywania związków z wiązaniem
jonowym – karty pracy( KCl, MgS, CaCl2, AlBr3 ),
H. Dalszy ciąg prezentacji umożliwiającej zrozumienie zasad powstawania wiązania
kowalencyjnego.
I. Ćwiczenia uczniów w pisaniu schematów powstawania wiązań kowalencyjnych w
cząsteczkach pierwiastków i związkach chemicznych ( N2 , Br2,H2O, CO2, CH4, H2S),
J. Prezentacja – polaryzacja cząsteczek, asocjaty.
K. Prezentacja – wiązanie a właściwości substancji chemicznych,
L. Kontrola kart pracy uczniów i ocena ich pracy.
M. Rekapitulacja – krótki test sprawdzający wiadomości i umiejętności uczniów.
N. Podziękowanie za aktywny udział w lekcjach.