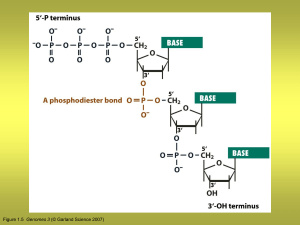
Transformacja pośrednia
składa się z trzech etapów:
1. Otrzymanie pożądanego odcinka DNA
z materiału genetycznego dawcy
2. Wprowadzenie obcego DNA do
wektora
3. Wprowadzenie wektora, niosącego w
sobie DNA dawcy do komórek biorcy,
w taki sposób by DNA dawcy połączył
się trwale z DNA biorcy
Wektor transformacji
- niewielka cząsteczka DNA
mająca zdolność przenoszenia
obcego DNA oraz zdolność do
autonomicznej replikacji.
Cechy dobrego wektora:
1.
2.
3.
4.
5.
6.
7.
Dobrze poznany biologicznie i genetycznie
Zawiera pojedyncze miejsce restrykcyjne
rozpoznawane przez przynajmniej jeden enzym
restrykcyjny
Posiada geny tzw. markerów selektywnych
Miejsce restrykcyjne nie może znajdować się w
pobliżu genów markerów selektywnych
Posiada co najmniej jedną sekwencję startu
replikacji
Posiada gen tzw. replikacji luźnej
Nie zawiera genów stanowiących zagrożenie dla
człowieka lub środowiska
Figure 2.17 Genomes 3 (© Garland Science 2007)
Figure 2.18 Genomes 3 (© Garland Science 2007)
Przygotowanie wektora transformacji
– rekombinacja in vitro
DNA
wektora
1. Trawienie tym samym
enzymem restrykcyjnym
DNA dawcy
2. Ligacja
3. Namnażanie
Wektor zrekombinowany z
insertem
Figure 2.15 (part 2 of 3) Genomes 3 (© Garland Science 2007)
Figure 2.15 (part 3 of 3) Genomes 3 (© Garland Science 2007)
Metoda transformacji roślin
za pomocą Agrobacterium
• Agrobacterium tumefaciens
– plazmid Ti (tumor inducing)
– choroba – guzowatość korzeni (crown-gall)
• Agrobacterium rhizogenes
– plazmid Ri (root inducing)
– choroba – włosowatość korzeni (hairy-gall)
Guzowate narośla (tumory)
wywołane infekcją Agrobacterium
tumefaciens
Schemat budowy plazmidu Ti
LB i RB
T-DNA
Rejon vir
ori
KO
tra
Cechy charakterystyczne T-DNA:
1.
2.
3.
4.
Ma zdolność trwałej integracji z genomem
rośliny
Za przeniesienie i integrację T-DNA
odpowiedzialne są sekwencje graniczne (LB i
RB), które mają identyczną budowę i wyróżniają
się zachowawczą lokalizacją we wszystkich
typach plazmidów Agrobacterium
Usunięcie fragmentu DNA plazmidowego z
obszaru między sekwencjami granicznymi i
wstawienie w to miejsce DNA dawcy, nie
zakłóca procesów przeniesienia i integracji TDNA z DNA rośliny
Stanowi 5-10% DNA plazmidu
Markery
• Marker genetyczny – gen występujący
przynajmniej w dwóch łatwo
rozróżnialnych postaciach (allelach),
dziedziczenie którego można śledzić w
czasie krzyżówki genetycznej, co umożliwia
ustalenie pozycji genu na mapie
Cechy dobrego markera:
1. Silny polimorfizm (obecność wielu form
allelicznych)
2. Dziedziczenie kodominujące
3. Wysoka frekwencja i równomierne
rozłożenie w genomie
4. Neutralność selekcyjna (brak sprzężenia z
genami obniżającymi płodność)
5. Wysoka powtarzalność
6. Prosta i szybka metoda wykrywalności
Rodzaje markerów
1. Markery cech morfologicznych
2. Markery molekularne
•
•
Izoenzymy
Markery DNA
Izoenzymy
• rozmaite molekularne formy enzymów
o podobnej bądź identycznej
specyficzności wobec substratu,
występujące w tym samym organiźmie.
• Wg. Merket`a i Moller`a są to odmienne
formy molekularne enzymów
otrzymanych podczas separacji
różnymi technikami rozdzielczymi.
Typy A i E reprezentują dwie
homozygotyczne formy
rodzicielskie izozymów
o różnej ruchliwości
elektroforetycznej.
A
B
D
E
Typy B i D przedstawiają możliwe
formy heterozygotyczne izozymów.
Typ B otrzymujemy
Typ C spotykamy w przypadku, gdy
w przypadku, gdy
badany enzym jest dimerem. Pośredni
badany enzym jest
prążek powstaje z jednej podjednostki
monomeryczny.
typu A i z jednej typu E oraz wykazuje
pośrednią ruchliwość
Typ D obrazuje cetramer. Trzy
elektroforetyczną.
pośrednie prążki powstają przez
połączenie w różnych
kombinacjach podjednostek typu A
i E.
Marker DNA
Sekwencja DNA występująca w dwóch lub
większej liczbie łatwych do rozróżnienia
wersji i której z tego powodu można użyć do
zaznaczenia pozycji na mapie
Rodzaje markerów DNA
Oparte na procesie hybrydyzacji:
RFLP (Restriction Fragment Length
Polymorphism)
Fingerprinting na bazie oligonukleotydów
Rodzaje markerów DNA
Oparte na PCR (Polymerase Chain
Reaction)
•
•
•
•
RAPD
STS
CAPS
AFLP
RAPD - random amplified polymorphic
DNA
(losowo amplifikowany polimorficzny
DNA)
• reakcja PCR z jednym tylko starterem (12
nukleotydowy lub krótszy), który przyłącza
się w sposób losowy do
komplementarnych miejsc w
zdenaturowanym DNA
• rezultat - wiele odcinków DNA, które
rozdzielane są elektroforetycznie, a
każdemu odcinkowi odpowiada jeden
locus
STS ( sequence-tagged site) miejsce znaczone sekwencyjnie
• stanowi unikatową w obrębie genomu, krótką
sekwencję (ok. 200-300 pz) identyfikującą
specyficzny locus
• amplifikacja STS wymaga zastosowania
dwóch starterów długości ok. 20
nukleotydów
• produkt - jeden prążek na żelu
elektroforetycznym (unikatowy region
genomu), odpowiadający wielkością
wyznaczonemu do amplifikacji fragmentowi
RFLP - polimorfizm długości fragmentów
restrykcyjnych
Trawienie genomowego DNA
enzymem restrykcyjnym o
specyficznym miejscu
rozpoznania
Rozdział elektroforetyczny
produktów trawienia
RFLP
RFLP - polimorfizm długości
fragmentów restrykcyjnych
• znakowanie radioaktywnymi cząstkami
lub fluorochromami specyficznych
sekwencji nukleotydów (sond)
• hybrydyzacja w celu identyfikacji
genów lub określonych sekwencji