Alergia
Strona 1 z 4
ALERGIA 4/15 2002 E P I D E M I E
Dr n. med.
Anna
Muszyńska
X X I
W I E K U
Zakażenie HIV - co nowego?
W pracy przedstawiono najnowsze ustalenia w zakresie mechanizmu zakażania
Jerzy komórek przez HIV, z wykorzystaniem różnych receptorów błonowych komórek.
Kruszewski
Szczególnie dużo uwagi poświęcono receptorom dla chemokin prozapalnych które
stanowią ważny system koreceptorów wykorzystywanych przez HIV. Omówiono tez
Klinika Chorób
Infekcyjnych i znane mutacje tych receptorów i ich wpływ na zdolność zakażania komórek przez HIV.
Prof. dr hab. n. med.
Alergologii
Wojskowego
Instytutu
Medycznego w
Warszawie
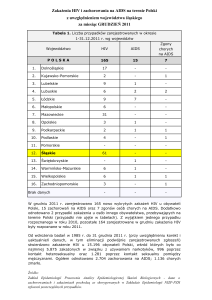
Wbrew wcześniejszym prognozom, liczba nowo wykrywanych zakażeń HIV w ostatnich
latach w Polsce jest mniejsza niż oczekiwano. W 2000 r. do Zakładu Epidemiologii PZH
zgłoszono 630 nowych przypadków, podczas gdy w 1990 r. stwierdzono 809 nowych
zakażeń (1). Przyczyn może być wiele, od skuteczności propagowanych działań
profilaktycznych (prezerwatywy), poprzez dostępność badań przesiewowych,
bezpieczeństwo procedur medycznych i przetaczanej krwi, aż do zmian zachowań
seksualnych Polaków. Natomiast liczba zachorowań na AIDS w Polsce rośnie, osiągając
liczbę 1024 stwierdzonych w latach 1986-2000. Jest to zapewne efektem upływu ok. 10 lat
- czasu koniecznego do rozwoju AIDS, od okresu, w którym notowano najwięcej
przypadków nowych zakażeń HIV.
Badania nad patogenezą zakażenia HIV podkreślają znaczenie warunków koniecznych do
interakcji między wirusem HIV i zakażanymi komórkami. Istotnym odkryciem ostatnich lat
było stwierdzenie, że komórki dendrytyczne obecne w skórze i na śluzówkach są w stanie
zachować zdolne do zakażania cząsteczki wirusa HIV przez okres kilku dni po ekspozycji.
Może to mieć znaczenie w zakażaniu drogą kontaktów seksualnych (2). Podobnie jak
wiele innych wirusów, wirus HIV w procesie fuzji i zakażania komórek, oprócz cząsteczki
CD4+, wykorzystuje inne struktury błonowe, np. receptory, które fizjologicznie pełnią
określone role. Te dodatkowe struktury błonowe konieczne do fuzji określa się mianem
koreceptorów. Występowanie określonych koreceptorów decyduje, które z komórek mogą
stać się obiektem jego ataku, zatem może decydować o osobniczej podatności na
zakażenie HIV. Z tym kierunkiem badań wiązane są nadzieje na opracowanie nowej
i skutecznej strategii profilaktyki zakażeń HIV. Są one o tyle ciekawe dla alergologa, że
dotyczą również struktur uczestniczących w mechanizmach alergicznych, m. in. chemokin
prozapalnych. Problemy te były przedmiotem naszego wcześniejszego opracowania (3),
a obecne jest uzupełnieniem o nowe informacje z ostatnich lat.
Ogólnie biorąc, rozważania autorów
w tym zakresie nadal dotyczą
głównie takich koreceptorów, jak
receptory dla chemokin CCR5
i CXCR4 oraz wpływu
spontanicznych mutacji w obrębie
genów dla tych receptorów na
zdolności HIV do zakażania
komórek.
CCR5 jest głównym koreceptorem
dla makrofagotropowych szczepów
HIV-1 (NSI-HIV/R5-tropowe HIV),
dominujących we wczesnej fazie
zakażenia HIV. W przypadku
pierwszej z opisanych mutacji
w obrębie genu dla CCR5 (delecja
32 nukleotydów - CCR5D32),
w zależności od tego, czy osoby
pod względem tej mutacji są
homozygotyczne, czy
heterozygotyczne, wykazano, że
może mieć ona istotne znaczenie
ochronne przed zakażeniem HIV (4, 5), jak również wpływ na szybkość progresji zakażenia (6, 7).
file://K:\www\alergia\archiwum\02_04\TMPdy8hkp9uyh.htm
2003-12-02
Alergia
Strona 2 z 4
Inna mutacja w obrębie genu dla CCR5, polegająca na zastąpieniu tymidyny w 303
nukleotydzie na adeninę (CCR5 m303), w skojarzeniu z CCR5D32 również wydaje się
chronić przed zakażeniem HIV (8).
Kolejna mutacja w zakresie genu dla receptora CCR5 (zastąpienie adeniny na guaninę
w pojedynczej parze nukleotydów 59029 obszaru promotora CCR5 - CCR5 59029G/G),
występująca z wysoką częstością, bo od 43 do 68% w zależności od rasy (9), również
może mieć znaczenie w infekcji HIV. Sugeruje się, że komórki osób homozygotycznych
pod względem tej mutacji mogą wykazywać mniejszą ekspresję receptora CCR5
w porównaniu z komórkami osób bez tej mutacji (10). W jednym z badań wykazano, że
osoby specjalnie wyselekcjonowane pod kątem braku mutacji CCR5D32 i CCR2-64I
(mutacja, w której walina pozycji 64 pierwszej domeny transmembralnej kodowanego
łańcucha białkowego zostaje zastąpiona izoleucyną) z towarzyszącą mutacją CCR5
59029G/G rozwijają znacznie później AIDS w porównaniu z osobami bez tej mutacji (9).
Jednym z wyjaśnień zjawiska dominacji wykorzystania koreceptora CCR5 podczas
transmisji zakażenia HIV może być fakt liczebnej przewagi komórek wykazujących
ekspresję tego receptora w lamina propria błony śluzowej odbytu i narządów płciowych
(11).
Rozważano także wpływ stężeń chemokin na możliwości zakażania makrofagów przez
szczepy NSI-HIV. Wyniki badań nie są jednoznaczne, bowiem w niektórych wykazano
efektywność hamowania tego procesu przez chemokiny RANTES, MIP-1a, MIP-1b
(chemokiny prozapalne, naturalne ligandy dla CCR5) (12, 13, 14, 15), a w niektórych jego
brak (16, 17, 18, 19).
W innego typu badaniach obserwowano jednak spontaniczną niezdolność szczepów HIV-1
do zakażania makrofagów posiadających receptory CCR5, co sugeruje, że wykorzystanie
koreceptora przez poszczególne szczepy HIV-1 może różnić się w zależności od typu
wirusa, typu komórki docelowej oraz stopnia ekspresji tego koreceptora.
Mutacja w zakresie genu dla SDF-1b, białka będącego naturalnym ligandem dla receptora
CXCR4 (zamiana w pojedynczym nukleotydzie guaniny na adeninę w pozycji 801),
również wydaje się mieć pewien wpływ na zakażenie HIV. Stwierdzana jest ona z różną
częstością: 6% u Afroamerykanów, 21% u Kaukazoidów i 26% u Azjatów (20). Jej wpływ
na zakażenie HIV ciągle pozostaje niejasny, gdyż w niektórych pracach stwierdzono, że
osoby homozygotyczne pod względem tej mutacji (SDF1-3 A/3 A) nieco później
rozwijają AIDS w porównaniu z osobami bez tej mutacji (20), ale opublikowano też
badania sugerujące coś zupełnie przeciwnego (21). Rozbieżności mogą wynikać z różnic
w doborze osób badanych lub zbyt małej liczby osób homozygotycznych pod względem tej
mutacji w grupach. Inną przyczyną mogą być również różne czynniki środowiskowe
modulujące poziom SDF-1 i mające w efekcie wpływ na aktywność CXCR4 jako
koreceptora dla HIV-1.
Badanie oceniające łączny wpływ mutacji SDF1-3 A/3 A i CCR5/Dr5 u dzieci wykazało
szybszą progresję zakażenia HIV w porównaniu z osobami bez tej mutacji (22). Osoby
homozygotyczne pod kątem mutacji SDF-1-3 A wykazują większą ekspresję SDF-1, co
może hamować zakażanie komórek przez szczepy limfocytotropowe HIV dominujące
w poźniejszym okresie zakażenia (SI-HIV), a promować replikację szczepów NSI-HIV.
Z kolei osoby heterozygotyczne pod kątem mutacji CCR5D32, wykazując mniejszą
ekspresję koreceptorów CCR5 promują zakażanie komórek przez SI-HIV. Połączenie tych
obu mutacji mogłoby nasilać replikację wirusa, szczególnie w dziewiczych limfocytach
TCD4+, co odbija się w sposób niekorzystny na niedojrzałym układzie odpornościowym.
Opisywana już wcześniej mutacja punktowa w zakresie genu dla CCR2 (CCR2-64I),
występująca u 10% Kaukazoidów, 15% Afroamerykanów i 25% Azjatów (21, 23), wydaje
się mieć wpływ na szybkość rozwoju AIDS. Występuje ona istotnie częściej u osób, które
wolniej rozwijają AIDS, w porównaniu z osobami bez tej mutacji (10, 23). Stwierdzono też,
że osoby z mutacją CCR2-64I cechują się znacząco mniejszą wiremią w okresie 9-12
miesięcy po serokonwersji, w porównaniu z osobami bez tej mutacji (23). Poza tym łączne
występowanie mutacji CCR5D32 i CCR2-64I wydaje się jeszcze bardziej hamować
szybkość progresji zakażenia HIV (10, 23).
Oprócz dotychczas omówionych receptorów dla HIV również inne receptory - CCR2b
(występuje na komórkach mikrogleju), CCR3, CCR8 (występuje na monocytach
i limfocytach CD4+), CX3CR1 (występuje na komórkach limfatycznych i układu
nerwowego), Bonzo/STRL33 (występuje na komórkach grasicy, śledziony, węzłów
chłonnych) lub BOB/GPR15 (24, 25, 26, 27, 28, 29, 30) - mogą być wykorzystywane przez
wirus jako koreceptory.
Ostatnie badania wykazują, że koreceptorem dla HIV-1 może być też receptor dla
leukotrienu B4 (31) lub cząsteczka US28 kodowana przez cytomegalowirusy (CMV),
file://K:\www\alergia\archiwum\02_04\TMPdy8hkp9uyh.htm
2003-12-02
Alergia
Strona 3 z 4
a będąca homologiem receptora chemokinowego (jego ligandy to RANTES, MIP-1a i b,
MCP-1) (27, 32). Być może zakażenie CMV powoduje, że komórki początkowo oporne na
infekcję HIV stają się na nią podatne. W jednej z prac stwierdzono, że świeże zakażenie
CMV zwiększa ponadtrzykrotnie ryzyko rozwoju AIDS u zakażonych HIV (33). Sugeruje
się, że zakażone CMV komórki jednojądrzaste mogą produkować cytokiny, które stymulują
replikację HIV.
Kontakt komórek docelowych z HIV
w większości wypadków wymaga
udziału cząsteczki CD4+, ale opisano
również możliwość interakcji domen
w otoczce wirusa z koreceptorami przy
braku obecności CD4+. Wydaje się
jednak, że taki sposób zakażania nie
jest wydajny i w związku z tym ma
małe znaczenie in vivo (34, 35).
Opisywane są również szczepy HIV-1
będące w stanie zainfekować komórki
posiadające na swojej powierzchni
cząsteczkę CD8+ nawet bez
współudziału koreceptorów CCR5 czy
CXCR4 (36). Potwierdza to
wcześniejsze obserwacje sugerujące
ogromne możliwości dostosowawcze
HIV-1 w tym zakresie, będące
prawdopodobnie wynikiem dużej
plastyczności białek otoczki wirusa.
Taki sposób zakażania mógłby
tłumaczyć gwałtowny spadek liczby
limfocytów w późniejszych stadiach
AIDS, być może w wyniku rozwoju
szczepów HIV-1 zdolnych do zakażania cytotoksycznych limfocytów T CD8+, które
w początkowych etapach zakażenia nie mogły być komórkami docelowymi wirusa (36).
W niektórych pracach wykazano, że w koncentratach ludzkich immunoglobulin stwierdza
się przeciwciała skierowane przeciwko różnym powierzchniowym cząsteczkom, m. in.
przeciwko cząsteczkom CCR5. Wykazano hamujące działanie koncentratów
immunoglobulin na zakażanie makrofagów i limfocytów CD4+ przez szczepy NSI-HIV (37).
Ponieważ w tych preparatach stwierdza się również przeciwciała skierowane przeciwko
cząsteczkom CD4+ (38), rozważa się ich zastosowanie terapeutyczne.
W jednej z prac wykazano istotną korelację między stężeniem naturalnych przeciwciał
anty-CCR5 i brakiem serokonwersji u osób często eksponowanych na HIV i nie
ulegających zakażeniu (39). Jednak poznanie ochronnej roli tego rodzaju przeciwciał
w mechanizmie zakażenia HIV in vivo wymaga dalszych badań.
Podsumowując należy zaznaczyć, że mimo ciągłego postępu wiedzy nad patogenezą
zakażenia HIV, a zwłaszcza mechanizmem zakażania komórek, możliwości praktycznego
wykorzystania tych informacji są ciągle kwestią przyszłości. •
Piśmiennictwo:
1. Szata W., AIDS i zakażenie HIV w 2000 r. Przegl. Epidemiol. 2002; 56: 363-373. 2. Geitenbeek T. B., Kwon D.
S., Torensma R. i wsp., DC-SIGN, a dendritic cell-specific HIV-1-binding protein that enhances transinfection of T
cells. Cell 2000; 100: 587-597. 3. Kruszewski J., Naturalne mechanizmy oporności organizmu na zakażenie HIV.
Med. Sci. Rev. 1997, 1, 13-17. 4. Huang Y., Paxton W. A., Wolinsky S. M. i wsp., The role of a mutant CCR5
allele in HIV-1 transmission and disease progression. Nat. Med. 1996; 2 (11): 1240-1243. 5. O Brien T. R.,
Winkler C., Dean M. i wsp., HIV-1 infection in a human homozygous for CCR5D32. Lancet 1997; 349: 1219. 6.
Dean M., Carrington M., Winkler C. i wsp., Genetic restriction of HIV-1 infection and progression to AIDS by
a deletion allele of the CKR5 structural gene. Science 1996; 273: 1856-1862. 7. Eugen-Olsen J., Iversen A. K. N.,
Garred P. i wsp., Heterozygosity for a deletion in the CKR-5 gene leads to prolonged AIDS-free survival and
slower CD4 T-cell decline in a cohort of HIV seropositive individuals. AIDS 1997; 11: 305-310. 8. Quillent C.,
Oberlin E., Braun J. i wsp., HIV-1-resistance phenotype conferred by combination of two separate inherited
mutations of CCR5 gene. Lancet 1998; 351: 14-18. 9. Zimmerman P. A., Guignard F., Kleeberger C. A. i wsp.,
CCR5 promoter polymorphism and HIV-1 disease progression. Lancet 1998; 352: 866-870, 10. Smith M. W.,
Dean M., Carrington M. i wsp., Contrasting genetic influence of CCR2 and CCR5 variants on HIV-1 infection and
disease progression. Science 1997; 277: 959-964. 11. Zhang L., He T., Talal A. i wsp., In vivo distribution of the
human immunodeficiency virus/simian immunodeficiency virus coreceptors: CXCR4, CCR3, CCR5. J. Virol. 1998;
72: 5035-5045. 12. Scarlati G., Tresoldi E., Bjorndal A., In vivo evolution of HIV-1 co-receptor usage and
sensitivity to chemokine-mediate supression. Nat. Med. 1997; 3: 1259-1265. 13. Verani A., Scarlati G., Comar M.,
C-C chemokines released by lipopolysaccharide (LPS) -stimulated human macrophages suppress HIV-infection
in both macrophages and T-cells. J. Exp. Med. 1997; 185: 805-816. 14. Alkhatib G., Combadiere C., Broder C. C.
i wsp., CC CKR5: RANTES, MIP-a, MIP- 1b receptor as a fusion cofactor for macrophage-tropic HIV-1. Science
1996; 272: 1955-1958. 15. Trkola A., Dragic T., Arthos J. i wsp., CD4-dependent antibody-sensitive interactions
between HIV-1 and its co-receptors CCR-5. Nature 1996; 384: 179-183. 16. Deng H. K., Liu R., Ellmeier W.
i wsp., Identification of a major co-receptor for primary isolates of HIV-1. Nature 1996; 381: 661-666. 17. Dragic
file://K:\www\alergia\archiwum\02_04\TMPdy8hkp9uyh.htm
2003-12-02
Alergia
Strona 4 z 4
T., Litwin V., Allaway G. P. i wsp., HIV-1 entry into CD4+ cells is mediated by the chemokine receptor CC-CKR5.
Nature 1996; 381: 667-673. 18. Moriuchi H., Moriuchi M., Combadiere C. i wsp., CD8+ T-cell-derived soluble
factor (s), but not b- chemokines RANTES, MIP-a, MIP-1b suppress HIV-1 replication in monocyte/macrophages.
Proc. Natl. Acad. Sci. USA 1996; 93: 15341-15345. 19. Schmidtmayerowa H., Sherry B., Burkinsky M.,
Chemokines and HIV replication. Nature 1996; 382: 762. 20. Winkler Ch., Modi W., Smith M. W. i wsp., Genetic
restriction of AIDS pathogenesis by an SDF-1 chemokine gene variant. Science 1998; 279: 389-392. 21.
Mummidi S., Ahuja S. S., Gonzales E. i wsp., Genealogy of the CCR5 locus and chemokine system gene variants
associated with altered rates of HIV-1 disease progression. Nature Med. 1998; 4 (7): 786-793. 22. Sei S., Boler A.
M., Nguyen G. T. i wsp., Protective effect of CCR5D32 heterozygosity is restricted by SDF-1 genotype in children
with HIV-1 infection. AIDS 2001; 15: 1343-1352. 23. Kostrikis L. G., Huang Y., Moore J. P. i wsp., A chemokine
receptor CCR2 allele delays HIV-1 disease progression and is associated with CCR5 promoter mutation. Nature
Med. 1998; 4: 350-353. 24. Martin J. C., Bandres J. C., Cells of the monocyte-macrophage lineage and
pathogenesis of HIV-1 infection. JAIDS 1999; 22 (5): 413-429. 25. Doranz B. J., Rucker J., Yi Y. J. i wsp., A dualtropic primary HIV-1 isolate that uses fusin and the beta-chemokine receptors CKR-5, CKR-3, and CKR2b as
fusion cofactors. Cell 1996; 85: 1149-1158. 26. Choe H., Farzan M., Sun Y. i wsp., The b-chemokine receptors
CCR3 and CCR5 facilitate infection by primary HIV-1 isolates. Cell 1996; 85 (7): 1135-1148. 27. Rucker J.,
Edinger A. L., Sharron M. i wsp., Utilization of chemokine receptors, orphan receptors, and herpesvirus-encoded
receptors by diverse human and simian immunodeficiency viruses. J. Virol. 1997; 71 (12): 8999-9007. 28. Horuk
R., Hesselgesser J., Zhou Y. i wsp., The cc-chemokine J-309 inhibits CCR-8-dependent infection by diverse HIV1 strains. J. Biol. Chem. 1998; 273: 386-391. 29. Jinno A., Shimizu N., Soda Y. i wsp., Identification of the
chemokine receptor TER/CCR8 expressed in brain-derived cells and T cells as a new coreceptor for HIV1infection. Biochem. Biophys. Res. Commun. 1998; 243: 497-502. 30. Combadiere C., Salzwedel K., Smith E. D.
i wsp., Identification of CX3CR1 a chemotactic receptor for the human CX3C chemokine fractalkine, and a fusion
coreceptor for HIV-1. J. Biol. Chem. 1998; 273: 23799-23804. 31. Owman C., Garzino-Demo A., Cocchi F. i wsp.,
The leukotriene B-4 receptor functions as a novel type of coreceptor mediating entry of primary HIV-1 isolates
into CD4-positive cells. Proc. Natl. Acad. Sci. USA 1998; 95: 30-34. 32. Pleskoff O., Treboute C., Brelot A. i wsp.,
Identification of a chemokine receptor encoded by human cytomegalovirus as a cofactor for HIV-1 entry. Science
1997; 276: 1874-1878. 33. Robain M., Boufassa F., Hubert J. -B. i wsp., Cytomegalovirus seroconversion as
a cofactor for progression to AIDS. AIDS 2001; 15: 251-256. 34. Hesselgesser J., Halks-Miller M., Del-Vecchio V.
i wsp., CD4-independent association between HIV-1 gp 120 and CXCR4 functional chemokine receptors are
expressed in human neurons. Curr. Biol. 1997; 7: 112-121. 35. Dumonceaux J., Nisole S., Chanel C. i wsp.:
Spontaneous mutation in the env gene of the human immunodeficiency virus type 1 NDK isolate are associated
with a CD4-independent entry phenotype. J. Virol. 1998; 72: 512-519. 36. Cullen B. R., A new entry route for HIV.
Nature Med. 2001; 7 (1): 20-21. 37. Bouhlal H., Hocini H., Quillent-Gregoire C. i wsp., Antibodies to C-C
chemokine receptor 5 in normal human IgG block infection of macrophages and lymphocytes with primary R5tropic strains of HIV-1. J. Immunol. 2001; 166 (12): 7606-7611. 38. Hurez V., Kaveri S. V., Moutiub A. i wsp., AntiCD4 activity of normal human immunoglobulin for therapeutic use. Ther. Immunol. 1994; 1 (5): 269-277. 39.
Ditzel H. J., Rosenkilde M. M., Garred P. i wsp., The CCR5 receptor acts as an alloantigen in CCR5 Delta 32
homozygous individuals: identification of chemokine and HIV-1-blocking human antibodies. Proc. Natl. Acad. Sci
USA 1998; 95 (9): 5241-5245.
HIV infection
The following work presents the latest outcomes regarding a mechanizm of the cell infection
by HIV, with the use of different cell membrane receptors. Particular attention was paid to the
receptors for proinflammatory chemokines, which form an important system of co-receptors
allowing HIV to enter cells. Moreover, the study discusses the mutations of these receptors
and their influence on the HIV's ability to infect cells.
file://K:\www\alergia\archiwum\02_04\TMPdy8hkp9uyh.htm
2003-12-02