MGR 4
4. Analiza energetyczna przejść fazowych.
• Pojęcie trzech stanów skupienia na przykładzie wody.
• Topnienie i krzepnięcie ciał. Przemiany energii podczas topnienia i
krzepnięcia.
• Ciepło topnienia i krzepnięcia. Stałość i równość temperatury topnienia i
krzepnięcia.
• Parowanie i skraplanie. Czynniki wpływające na szybkość parowania i
skraplania.
• Wrzenie. Temperatura wrzenia.
• Temperatura krytyczna.
• Zjawisko rozpuszczania. Czynniki wpływające na szybkość rozpuszczania.
• Krzepnięcie i wrzenie roztworów.
Ćw.
1. Wyznaczanie ciepła topnienia i krzepnięcia lodu.
2. Wrzenie wody pod kloszem pompy próżniowej.
3. Pokaz wrzenia wody pod zmniejszonym ciśnieniem.
4. Wyznaczanie ciepła właściwego ciała stałego.
5. Przyrząd do demonstracji punktu krytycznego eteru
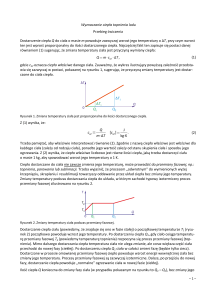
Wyznaczanie ciepła topnienia lodu
•
Ważymy kolorymetr wraz z mieszadełkiem ( niech jego masa
wynosi mk), nalewamy do niego wody i ważymy powtórnie
( jego masa będzie teraz wynosiła więcej, m1 ). Masa mw wynosi
więc
m w = m1 − mk
•
Mierzymy następnie temperaturę wody. Niech wyniesie ona t1.
Jeżeli wrzucimy teraz do kalorymetru kawałek dobrze
osuszonego za pomocą bibuły lodu, który znajdował się przez
dłuższy czas w wodzie, to będzie się on zamieniał na wodę
o temperaturze 00C.Powstała z lodu woda o tej temperaturze
ogrzewa się w dalszym ciągu oziębiając przy tym wodę w
kalorymetrze. Temperatury wody powstałej z lodu i wody w
kalorymetrze w końcu się wyrównają, co poznamy po tym, że
temperatura wody w kalorymetrze się ustali. Oznaczmy tę
końcową temperaturę przez t. Dla jej dokładnego uchwycenia
notujemy w tabelce wyniki obserwacji temperatury
w kalorymetrze po wrzuceniu do wody lodu.
Czas t, min
Temperatura
T,0C
•
Temperatura przechodzi przez minimum, po czym zaczyna się
podwyższać. Po osiągnięciu temperatury końcowej ważymy
jeszcze kalorymetr. Jeżeli jego masa wyniesie m2, to masa
stopionego lodu wyniesie
ml = m2 − m1
Podczas doświadczenia mieszamy nieustannie wodę dla
uniknięcia lokalnych ochłodzeń.
•
Wszystkie części kalorymetru są wykonane z aluminium,
którego ciepło właściwe wynosi 849
J
kg ⋅ 0 C
•
W celu otrzymania dokładniejszego pomiaru należy uwzględnić
ciepło pobrane przez część termometru zanurzoną
w kalorymetrze. Można obliczyć, że do ogrzania 1cm3 szkła lub
rtęci o 10C potrzeba średnio 1,93 J. Ciepło pobrane przez
termometr wynosi
Qt = V ⋅ r (t p − t )
gdzie: V-objętość
części
w kalorymetrze
termometru
zanurzonej
tp - temperatura otoczenia
r = 1,93
•
J
cm ⋅ C
3 o
Korzystając z bilansu cieplnego obliczamy wartość ciepła
topnienia lodu ( wartość tablicowa 334 700
•
J
)
kg
Określamy błąd względny pomiaru ciepła topnienia lodu
i zapisujemy ostateczny wynik
Wrzenie wody pod kloszem pompy próżniowej
Zlewkę z letnią wodą ( około 500C) ustawiamy
po kloszem pompy próżniowej. W trakcie
wypompowywania powietrza spod klosza woda
w zlewce zaczyna wrzeć. ( rys.3.165). W celu
odczytania temperatury wrzenia wody pod
zmniejszonym ciśnieniem należy do zlewki
wstawić
niezbyt
duży
termometr.
Rys. 3.165
Pokaz wrzenia wody po zmniejszonym
ciśnieniem
Rys. 3.164
Zagotujemy wodę w kolbie. Niech woda gotuje
się 1-2 minuty. Następnie odstawiamy kolbę i
natychmiast zakorkujemy. Woda przestała
wrzeć. Umocujmy kolbę na statywie ( jest
gorąca) i umieśćmy nad zlewem lub miseczką.
Teraz skierujmy na nią strumień zimnej
wody.(rys.3.164). Mimo, że temperatura wody
była niższa niż 1000C, to w całej objętości
pojawiły się pęcherzyki pary - woda wrzała. W
zakorkowanej kolbie nad powierzchnią wody
panowało
ciśnienie
mniejsze
od
atmosferycznego, dlatego że w wyniku
ochłodzenia szkła z zewnątrz część pary się
skropliła. Ta część, która pozostała,
i powietrze wywierały na powierzchnię wody w
kolbie ciśnienie mniejsze od atmosferycznego
Wyznaczanie ciepła właściwego ciała stałego
•
Wyznaczamy masę kolorymetru wraz z mieszadełkiem,
a następnie nalewamy do niego około
2
3
wysokości wody
wyznaczając jej masę m1 i temperaturę początkową t1.
•
W zlewce z wodą ogrzewamy w temperaturze wrzenia przez
kilka minut bryły metalowe zawieszone na nici. Masa m2
badanego ciała powinna być znana ( należy zauważyć, że jeżeli
masa badanego ciała będzie mała to w niedostatecznym stopniu
ogrzeje wodę w kalorymetrze przez co wynik pomiaru ciepła
właściwego będzie obarczony dużym błędem).
•
Wrzucamy badane ciało do kalorymetru i wyznaczamy
temperaturę końcową. Dla jej dokładnego uchwycenia
notujemy w tabelce wyniki obserwacji temperatury
w kalorymetrze po wrzuceniu do wody ciała.
Czas t, min
Temperatura
T,0C
•
Temperatura przechodzi przez maximum, po czym zaczyna się
obniżać.
•
Dane wpisujemy do tabelki
Masa wody w Temperatura
kalorymetrze
wody t1, 0C
m1, kg
Masa ciała Temperatura
Temperatura
stałego m2, początkowa
końcowa t, 0C
kg
ciała
stałego
t 0, 0C
100
Ciepło
właściwe ciała
stałego
c,
J
kg ⋅ 0 C
•
Obliczamy ilość ciepła, którą woda z kalorymetru pobrała
ogrzewając się od temperatury t1 do t,
•
Obliczamy ilość ciepłą oddanego przez ciało przy ochładzaniu
się od t0 do t,
•
Wyprowadzamy wzór na obliczanie ciepła właściwego przy
uwzględnianiu pojemności cieplnej kalorymetru i obliczamy w
tym przypadku wartość ciepła właściwego badanego ciała
stałego,
•
Określamy błąd względny pomiaru i notujemy ostateczną
wartość wyznaczonego ciepła właściwego.
•
Wszystkie części kalorymetru są wykonane z aluminium,
którego ciepło właściwe wynosi 849
•
J
kg ⋅ 0 C
W celu otrzymania dokładniejszego pomiaru należy uwzględnić
ciepło pobrane przez część termometru zanurzoną w
kalorymetrze. Można obliczyć, że do ogrzania 1cm3 szkła lub
rtęci o 10C potrzeba średnio 1,93 J. Ciepło pobrane przez
termometr wynosi
Qt = V ⋅ r (t p − t )
gdzie: V-objętość
części
w kalorymetrze
tp - temperatura otoczenia
r = 1,93
J
cm ⋅ C
3 o
termometru
zanurzonej
Przyrząd do demonstracji punktu krytycznego
eteru /przystawka do diaskopu/
Rys. l Przystawka do diaskopu
1. -próbka z eterem
2. - termometr
3. - spirala grzejna
4. - obudowa
1. Przystawkę założyć do rzutnika typu „Biofiz" lub „Profil".
Umieszczamy ją tak samo jak maletkę z uchwytem do przeźroczy.
2. Włączyć oświetlenie i ustawić ostrość obrazu na ekranie, odległość
ekranu od aparatu projekcyjnego około 5 m.
3. W uchwyt wstawić termometr o zakresie od 0° do 300"C tak, aby jego
zbiornik z rtęcią znajdował się na poziomie cieczy w próbce.
4. Grzejnik przystawki zasilić napięciem zmiennym /około 15V7, które
można czerpać z uzwojenia wtórnego transformatora rozbieralnego,
zasilacza uniwersalnego, zasilacza regulowanego itp. Można włączyć do
obwodu amperomierz i ustalić natężenie prądu w granicach 3 do 3,5A
5. Ogrzewać próbkę do około 190"C, w pobliżu temperatury krytycznej
można wyłączyć zasilanie. Zjawisko przejścia substancji w stan krytyczny
można demonstrować kilkakrotnie, w tym celu ogrzewamy próbkę i następnie
oziębiamy /poprzez wyłączenie napięcia/.
Uwaga:
ZE WZGLĘDU NA BEZPIECZEŃSTWO NIE PODGRZEWAĆ PRÓBKI
POWYŻEJ TEMPERATURY 210°C !
Przyrząd opracowany przez J.Morawca i S.Viscardiego został zatwierdzony
jako pomoc szkolna przez Ministerstwo Oświaty i Szkolnictwa Wyższego
pismem z dnia 11 czerwca 1970 r. Znak rozpoznawczy: PS 4572-F-660/70