Fizyka atomowa
Ćwiczenia
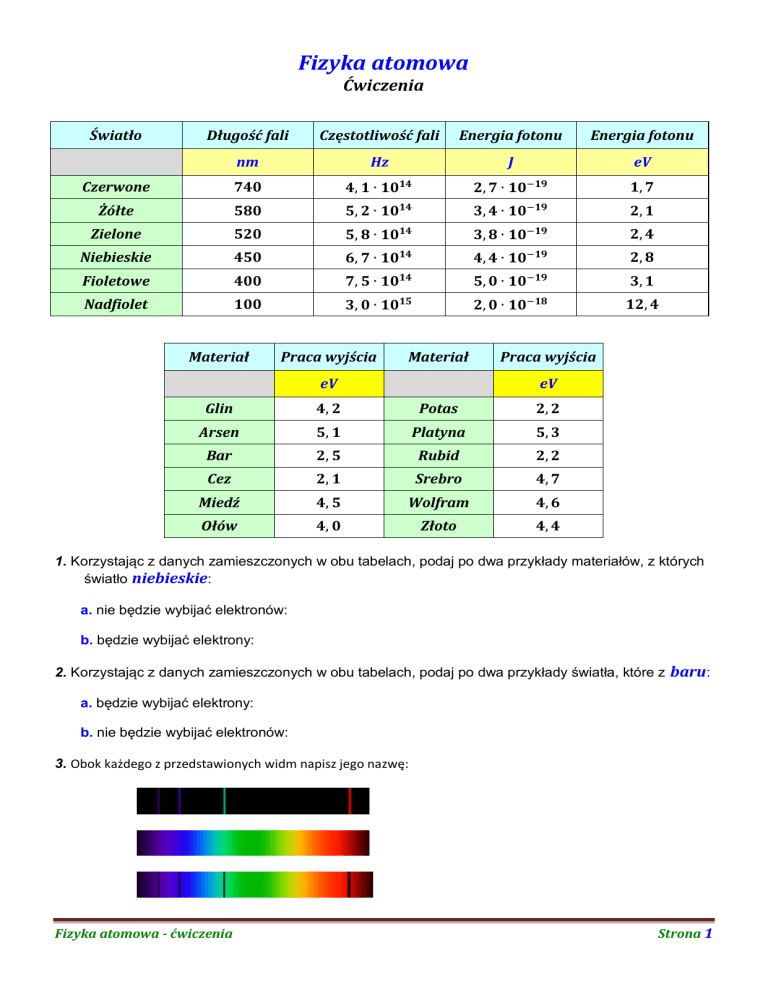
Światło
Długość fali
Częstotliwość fali
Energia fotonu
Energia fotonu
nm
Hz
J
eV
Czerwone
Żółte
Zielone
Niebieskie
Fioletowe
Nadfiolet
Materiał
Praca wyjścia
Materiał
eV
Praca wyjścia
eV
Glin
Potas
Arsen
Platyna
Bar
Rubid
Cez
Srebro
Miedź
Wolfram
Ołów
Złoto
1. Korzystając z danych zamieszczonych w obu tabelach, podaj po dwa przykłady materiałów, z których
światło niebieskie:
a. nie będzie wybijać elektronów:
b. będzie wybijać elektrony:
2. Korzystając z danych zamieszczonych w obu tabelach, podaj po dwa przykłady światła, które z baru:
a. będzie wybijać elektrony:
b. nie będzie wybijać elektronów:
3. Obok każdego z przedstawionych widm napisz jego nazwę:
Fizyka atomowa - ćwiczenia
Strona 1
4. Promień orbity elektronu w modelu Bohra wyraża zależność:
. Pierwsza orbita w atomie
wodoru (
) ma promień
. Czy elektron w atomie wodoru może
się znajdować na orbicie o promieniu:
a.
c.
Tak
Nie
Tak
Nie
b.
d.
Tak
Nie
Tak
Nie
5. Energię elektronu na n - tej tzw. orbicie dozwolonej wyraża zależność:
. Czy elektron
w atomie wodoru może mieć podaną poniżej energię?
a.
Tak
Nie
b.
Tak
Nie
c.
Tak
Nie
d.
Tak
Nie
6. Na poniższych rysunkach został pokazany (bez zachowania proporcji) atom wodoru. Podpisz każdy z
rysunków, używając określeń "emisja fotonu" lub "absorpcja fotonu". Jeżeli któryś z rysunków
dotyczył emisji, to dodatkowo napisz nazwę serii widmowej, w której ten przypadek się zawierał.
- elektron
Fizyka atomowa - ćwiczenia
- proton
Strona 2
7. Ponumerowanym polom przypisz (na oddzielnej kartce) brakujący tekst (słowo, zdanie, liczbę itp.).
Znane są następujące zakresy fal elektromagnetycznych (podaj przynajmniej cztery) [1]. Fale
elektromagnetyczne widzialne dla człowieka (światło) zawierają fale o długościach z zakresu (ilu
nanometrów) [2]. Fale nieco dłuższe od widzialnych noszą nazwę (jaką?) [3], natomiast fale nieco
krótsze od światła nazywa się (jak?) [4].
Na gruncie falowej teorii światła można było wyjaśnić takie zjawiska, jak (podaj przynajmniej dwa)
[5], natomiast wyjaśnienie zjawiska fotoelektrycznego zewnętrznego wymagało przyjęcia, że światło jest
[6]. Zjawisko to polega na [7]. Wyjaśnienie zjawiska fotoelektrycznego zostało podane przez (kogo?) [8]
w roku [9]. Zjawisko fotoelektryczne zajdzie, jeżeli długość fali padających fotonów będzie (mniejsza,
większa, taka sama?) [10], jak pewna długość graniczna zależna tylko od (czego?) [11]. Gdyby energia
padających fotonów wynosiła 5 elektronowoltów, a praca wyjścia 3 elektronowolty, to energia kinetyczna
wybijanych elektronów miałaby wartość (ile elektronowoltów?) [12].
Wszystkie
ciała
o
temperaturze
powyżej
zera
kelwinów
emitują
promieniowanie
elektromagnetyczne zwane (jak?) [13]. Jeżeli dane ciało emituje promieniowanie zawierające fale o
długościach z całego zakresu widzialnego dla człowieka (tzw. widmo światła białego), to mówimy o tzw.
widmie [14]. Jeśli natomiast widmo promieniowania zawiera tylko pewne długości fal z tego zakresu, to
jest to tzw. widmo [15]. Widmo ciągłe światła białego mają (jakie substancje?) [16]. Z kolei widmo
liniowe dają [17].
Energia fotonu jest wprost proporcjonalna do [18] i odwrotnie proporcjonalna do [19]. Jeżeli
częstotliwość fali związanej z fotonem wzrośnie dwa razy, to wartość jego energii (jak się zmieni?) [20],
jeżeli natomiast długość fali związanej z fotonem zmaleje trzy razy, to wartość jego energii (jak się
zmieni?) [21]. Gdyby energia fotonu wynosiła
dżula, to wyrażona w elektronowoltach
miałaby wartość [22]. Fotony światła o barwie zielonej mają (taką samą, większą, mniejszą?) [23]
energię, jak fotony światła o barwie fioletowej.
Model promieniowania atomu wodoru podany (przez kogo?) [24] miał wyjaśnić (co?) [25]. Jego
podstawą są (ile?) [26] postulaty kwantowe. Na orbicie pierwszej energia elektronu jest (największa,
najmniejsza?) [27]. Ze wzrostem numeru orbity energia elektronu (wzrasta, maleje, nie zmienia się?)
[28]. Jeżeli elektron przeskoczył z orbity trzeciej na drugą, to nastąpiła (emisja, absorpcja?) [29] energii
w postaci fotonu. Jeżeli promień pewnej orbity wynosi
, to orbitą tą jest orbita o numerze (jakim?)
[30]. Wartość energii elektronu na tej orbicie wynosi (ile elektronowoltów?) [31]. Linie widmowe tworzą
tzw. serie dla których wspólną cechą jest numer orbity końcowej elektronu (przeskok na orbitę o takim
samym promieniu). Jeżeli orbitą końcową jest orbita pierwsza, to jest to seria (kogo?) [32], w przypadku
orbity drugiej seria (kogo?) [33], natomiast dla trzeciej seria (kogo?) [34].
Fizyka atomowa - ćwiczenia
Strona 3