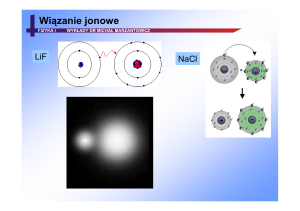
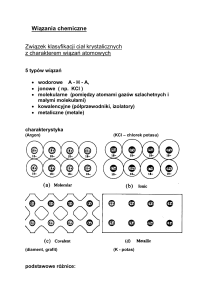
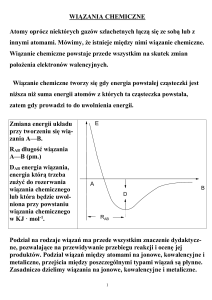
Wiązania chemiczne
- Elektronowa teoria wiązań chemicznych ,
- Orbitale molekularne (cząsteczkowe),
wiązanie sigma (σ) i wiązanie pi (π),
- Klasyfikacja wiązań chemicznych
Elektronowa teoria wiązań
Lewisa - Kossela
• Wiązanie chemiczne – to wzajemne oddziaływanie
elektronów walencyjnych atomów pierwiastka
(pierwiastków) łączących się w cząsteczki (molekuły)
homoatomowe (np. O2, S8) lub heteroatomowe (np. CO2)
• Atomy łącząc się w cząsteczki dążą do osiągnięcia
konfiguracji elektronowej na zewnętrznej powłoce
(powłoce walencyjnej) zapewniającej im minimum
energetyczne a tym samym bierność chemiczną,
jaką posiadają pierwiastki grupy 18 – helowce.
• Atomy łącząc się w cząsteczki dążą do uzupełnienia
lub zredukowania walencyjnej powłoki elektronowej
do powłoki walencyjnej najbliższego helowca,
czyli osiągnięcia dubletu elektronowego helu (1s2)
lub oktetu elektronowego ns2np6 pozostałych helowców.
Orbitale molekularne –
cząsteczkowe (wiązanie σ i π)
• Orbital molekularny: s – s; wiązanie σ
• Powstaje w wyniku czołowego zbliżenia
i nałożenia się orbitali atomowych s i s
obsadzonych niesparowanymi elektronami
o przeciwnej orientacji spinu:
s
s
s–s
Orbitale molekularne –
cząsteczkowe (wiązanie σ i π)
• Orbital molekularny: s – p; wiązanie σ
• Powstaje w wyniku czołowego zbliżenia
i nałożenia się orbitali atomowych s i p
obsadzonych niesparowanymi elektronami
o przeciwnej orientacji spinu:
•
s
p
s–p
Orbitale molekularne –
cząsteczkowe (wiązanie σ i π)
• Orbital molekularny: px – px; wiązanie σ
• Powstaje w wyniku czołowego zbliżenia
i nałożenia się orbitali atomowych px i px
obsadzonych niesparowanymi elektronami
o przeciwnej orientacji spinu:
• px
px
px – px
Orbitale molekularne –
cząsteczkowe (wiązanie σ i π)
• Orbital molekularny: py – py; wiązanie π
• Powstaje w wyniku bocznego zbliżenia i nałożenia się
orbitali atomowych py i py obsadzonych niesparowanymi
elektronami o przeciwnej orientacji spinu:
•
py
py
py – py
Orbitale molekularne –
cząsteczkowe (wiązanie σ i π)
• Orbital molekularny: pz– pz; wiązanie π
• Powstaje w wyniku bocznego zbliżenia i nałożenia się
orbitali atomowych pz i pzobsadzonych niesparowanymi
elektronami o przeciwnej orientacji spinu:
•
pz
pz
pz – pz
Klasyfikacja wiązań ze względu
na różnicę elektroujemności ∆E
• Wiązanie atomowe (kowalencyjne): ∆E< 0,4
• Wiązanie atomowe (kowalencyjne) spolaryzowane:
0,4 ≤ ∆E ≤ 1,7
• Wiązanie jonowe: ∆E > 1,7
• W praktyce, nie związku chemiczne o 100% udziale
wiązań tego samego typu, dla określenie typu
wiązań w związku przyjmuje się umownie zasadę
udziału określonych wiązań przekraczających 50%.
• Udział wiązań jonowych w związku chemicznym:
dla ∆E = 1,7 wynosi 51%, ∆E = 0,4 wynosi 4%,
∆E = 1,6 wynosi 46%.
Trójkąt wiązań
•
Wiązanie metaliczne Cs
Wiązanie atomowe 100%
F2
Większy udział wiązania
kowalencyjnego –
wiązanie kowalencyjne
spolaryzowane
50%
CsF
wiązanie jonowe 100%
Większy udział wiązania
jonowego – wiązanie jonowe
Pozostałe typy wiązań
• Wiązania metaliczne – występują
w kryształach matali i ich stopów,
• Wiązania koordynacyjne – wiązanie
donorowo-akceptorowe,
• Wiązanie wodorowe – szczególny przypadek
wiązania koordynacyjnego,
• Oddziaływania van der Waalsa
– siły van der Waalsa (oddziaływania
miedzycząsteczkowe)