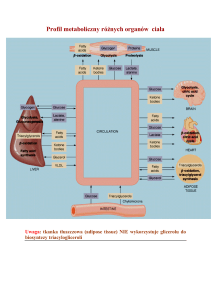
Węglowodany
12/11/2011
1
TRAWIENIE
Hydrolityczny rozkład węglowodanów
-amylaza ślinowa i trzustkowa rozkładają
wiązania glikozydowe 1,4
-1,6-glukozydazy rozkładają wiązania
glikozydowe 1,6
U przeżuwaczy trawienie wspomagają enzymy
wytwarzane przez bakterie
12/11/2011
2
WCHŁANIANIE
Transport wtórnie aktywny
Glukoza i galaktoza wchłaniają się szybko, wbrew
gradientowi stężeń, wymagają zużycia energii i obecności
jonu sodowego
Dyfuzja ułatwiona (przez nośnik)
Fruktoza, mannoza, pentozy są wchłaniane zgodnie z
gradientem stężeń. Transport odbywa się w wyniku
tworzenia przejściowego połączenia nośnik-substrat,
które ulegając rozpadowi uwalnia substrat do wnętrza
komórki
12/11/2011
3
LOSY WCHŁONIĘTYCH WĘGLOWODANÓW
Transport glukozy przez błonę komórkową:
transporter mózgowo-erytrocytarny (kierunek
dokomórkowy)
transporter wątrobowy (kierunek zmienny)
transporter mięśniowy insulinozależny (mięśnie
szkieletowe, serce,
tkanka tłuszczowa) – kierunek dokomórkowy
Fosforylacja glukozy
Metabolizm glukozy – synteza i rozkład glikogenu
- synteza glukozy
- katabolizm glukozy -glikoliza, cykl
12/11/2011
pentozowy
4
Glikogen
łatwo uruchamiana zapasowa forma glukozy
rozgałęziony polimer o dużej masie cząsteczkowej
zbudowany z reszt glukozy połączonych wiązaniami
1,4 i 1,6 glikozydowymi
magazynowany głównie w wątrobie i mięśniach
szkieletowych
występuje w cytoplazmie komórek w postaci ziaren, które
zawierają też białka regulatorowe oraz enzymy
katalizujące syntezę i degradację glikogenu
12/11/2011
5
Metabolizm glikogenu
regulacja stężenia glukozy we krwi
magazyn glukozy dla pracy mięśni
różne szlaki metaboliczne
hormonalna regulacja (adrenalina, glukagon,
insulina, cAMP, fosforylacja)
dziedziczne wady enzymatyczne
12/11/2011
6
Rozpad glikogenu
Fosforylaza glikogenowa rozszczepia wiązania 1,4.
Powstaje glukozo-1-fosforan – nie „ucieka” z
komórek.
Fosforoliza – rozszczepienie wiązania wywołane przez
ortofosforan (w przeciwieństwie do hydrolizy,które
odnosi się do rozkładu wywołanego przez cząsteczkę
wody).
Fosforolityczne rozszczepienie glikogenu jest korzystne
energetycznie ponieważ uwolniony cukier jest
ufosforylowany i nie może dyfundować z komórek
(wolna glukoza może)
12/11/2011
7
WĄTROBA
utrzymuje stałe stężenie glukozy we krwi
uwalnia do krwi glukozę potrzebną do pracy mózgu
i mięśni szkieletowych dzięki obecności glukozo-6fosfatazy – hydrolityczny rozpad (brak w mięśniach i
mózgu)
Glukozo-6-fosforan + H2O glukoza + Pi
12/11/2011
8
ROZPAD GLIKOGENU
Fosforylaza glikogenowa - wiązania 1,4.
Transferaza i -1,6-glukozydaza przekształcają
rozgałęzioną cząsteczkę w łańcuchową
Fosfoglukomutaza przekształca glukozo-1-fosforan
w glukozo-6-fosforan i umożliwia dalsze przemiany
Glukozo-6-fosfataza odszczepia fosfor. Glukoza
może „uciec” z komórki. Enzym jest w wątrobie,
jelitach i nerkach, BRAK go w mięśniach
12/11/2011
9
Fosforylaza glikogenowa
Glikogenn + Pi Glukozo-1-fosforan + Glikogenn-1
Rozszczepieniu ulegają wiązania pomiędzy C1 końcowej
reszty a C4 reszty następnej
Fosfoglukomutaza
Glukozo-1-fosforan Glukozo-6-fosforan
12/11/2011
10
DEGRADACJA
Glikogenn + Pi fosforylaza glikogenn-1 + glukozo-1-fosforan
SYNTEZA
Glikogenn + UDP-glukoza syntaza glikogenn+1 + UDP
12/11/2011
11
SYNTEZA GLIKOGENU
Donorem reszt glukozy jest UDP-glukoza –
syntetyzowana z glukozo-1-fosforanu i UTP przy udziale
pirofosforylazy UDP-glukozy
Syntaza glikogenowa przenosi zaktywowane jednostki
glukozylowe na grupy hydroksylowe przy C4 końcowych
reszt glikogenu tworząc wiązania -1,4. Funkcję inicjatora
pełni glikogenina
Enzym rozgałęziający tworzy rozgałęzienia potrzebne do
lepszej rozpuszczalności i dużej ilości nieredukujących
reszt będących miejscem działania fosforylazy i syntazy
glikogenowej
12/11/2011
12
Aktywacja glukozy
Pirofosforylaza UDP-glukozy
Glukozo-1-fosforan + UTP UDP-glukoza + PPi
12/11/2011
13
KONTROLA METABOLIZMU GLIKOGENU
Fosforylaza glikogenowa
regulacja poprzez allosteryczne efektory
regulacja poprzez odwracalną fosforylację
reagującą na
hormony
współpracuje z fosforanem pirydoksalu
12/11/2011
14
FOSFORYLAZA W MIĘŚNIACH
Jest dimerem lub tetramerem
Występuje w formie aktywnej (a) i nieaktywnej (b)
a przekształca się w b poprzez hydrolizę fosfoserynowej
reszty przy udziale fosfatazy-1 białek
a jest aktywna niezależnie od poziomu ATP czy AMP
b ulega przekształceniu w a poprzez fosforylację reszty
seryny przy udziale kinazy fosforylazowej
b wykazuje aktywność w obecności dużych stężeń AMP,
hamuje ją ATP i glukozo-6-fosforan (w spoczynku –
nieaktywna, podczas pracy mięśni - aktywna)
12/11/2011
15
FOSFORYLAZA W MIĘŚNIACH
Aktywacja mięśniowej fosforylazy b przez
AMP prowadzi do szybkiego uruchamiania
glikogenu
Brak glukozo-6-fosfatazy w mięśniach
umożliwia pozostawanie powstałego z
rozkładu glikogenu glukozo-6-fosforanu
wewnątrz komórek w celu wytwarzania energii
12/11/2011
16
FOSFORYLAZA W WĄTROBIE
Fosforylaza a ulega inaktywacji poprzez
wiązanie glukozy (wątroba produkuje glukozę dla
mięśni)
Fosforylaza b nie jest aktywowana przez AMP
Celem degradacji glikogenu w wątrobie jest
tworzenie glukozy wysyłanej do innych tkanek
gdy jej stężenie we krwi jest małe
12/11/2011
17
SYNTAZA GLIKOGENOWA
Katalizuje przeniesienie glukozy z UDP-glukozy
do rosnącego łańcucha polisacharydowego
12/11/2011
18
SYNTAZA GLIKOGENOWA
fosforylacja – defosforylacja (modyfikacja kowalencyjna)
regulacja hormonalna
Fosforylacja aktywnej formy a powoduje przekształcenie w
zazwyczaj nieaktywną formę b (pojawia się przy dużych
stężeniach glukozo-6-fosforanu)
Zdefosforylowana forma a jest aktywna niezależnie od
glukozo-6-fosforanu
Fosforylacja wpływa na aktywność syntazy odwrotnie
niż na aktywność fosforylazy
12/11/2011
19
Kinaza fosforylazowa
Jest aktywowana przez fosforylację – kinaza A
białek (zależna od cyklicznego AMP) oraz jony
wapniowe (ważne podczas skurczu mięśni)
12/11/2011
20
REGULACJA HORMONALNA
Glukagon
wydzielany w odpowiedzi na niskie stężenie glukozy we
krwi
działa poprzez cAMP
wyzwala rozkład glikogenu głównie w wątrobie
hamuje syntezę glikogenu (poprzez hamowanie syntazy)
hamuje syntezę kwasów tłuszczowych
hamuje glikolizę
stymuluje glukoneogenezę
EFEKT – wzrost uwalniania glukozy przez
wątrobę
12/11/2011
21
REGULACJA HORMONALNA
Adrenalina
wydzielana w odpowiedzi na niskie stężenie glukozy we krwi
wyzwala rozkład glikogenu głównie w mięśniach
hamuje syntezę glikogenu poprzez wzrost poziomu cAMP
hamuje pobieranie glukozy przez mięśnie, jako materiał
energetyczny zużywane są wtedy kwasy tłuszczowe
stymuluje wydzielanie glukagonu, hamuje insuliny
EFEKT – zwiększenie ilości glukozy uwalnianej do krwi
przez wątrobę, a zmniejszenie wykorzystania jej przez
mięśnie
12/11/2011
22
REGULACJA HORMONALNA
Insulina
indukuje syntezę glikogenu w mięśniach i wątrobie poprzez
pobudzenie szlaku defosforylacji i aktywację syntazy glikogenowej
oraz hamuje degradację glikogenu (defosforylacja kinazy
fosforylazowej i fosforylazy a)
hamuje glukoneogenezę w wątrobie
przyspiesza glikolizę w wątrobie, co zwiększa syntezę kwasów
tłuszczowych
ułatwia wnikanie glukozy do komórek mięśni i tkanki tłuszczowej
wpływa stymulująco na syntezę białek
12/11/2011
23
GLUKONEOGENEZA
Synteza glukozy z prekursorów niecukrowych w
wątrobie.
Prekursory niecukrowe: mleczan, aminokwasy,
glicerol. Wchodzą w glukoneogenezę jako pirogronian,
szczawiooctan lub dihydroksyaceton.
U zwierząt nie zachodzi przekształcanie kwasów
tłuszczowych w glukozę – nie ma możliwości
przekształcania acetyloCoA w pirogronian
12/11/2011
24
Glukoneogeneza nie jest dokładnym odwróceniem
glikolizy
Reakcje nieodwracalne glikolizy:
glukoza + ATP glukozo-6-fosforan + ADP
(heksokinaza)
12/11/2011
25
+ ATP fruktozo-1,6bis-fosforan + ADP (fosfofruktokinaza)
fruktozo-6-fosforan
12/11/2011
26
+ ADP pirogronian
+ ATP (kinaza pirogronianowa)
fosfoenolopirogronian
12/11/2011
27
Glikoliza
To łańcuch reakcji przekształcających glukozę w
pirogronian z jednoczesnym wytwarzaniem energii. W
organizmach tlenowych jest wstępnym etapem cyklu
Krebsa i łańcucha oddechowego uwalniających większość
energii zawartej w glukozie.
Odbywa się w cytoplazmie.
Cel:
Wytwarzanie ATP
Dostarczanie składników budulcowych do różnych
reakcji
Pirogronian dostarcza metabolitów pośrednich
przemian aminokwasów, lipidów i innych
12/11/2011
28
Etapy glikolizy
Pierwszy etap: Synteza fruktozo-1,6-bis-fosforanu
Fosforylacja glukozy
Izomeryzacja pierścienia piranozowego w furanozowy czyli aldozy
w heksozę
Druga fosforylacja
Drugi etap:
Rozszczepienie 6 węglowego związku na dwa trójwęglowe
Izomeryzacja związków trójwęglowych
Przekształcenie aldehydu-3-fosfoglicerynowego w 1,3bisfosfoglicerynian
Przekształcenie 1,3-bisfosfoglicerynianu w 3-fosfoglicerynian –
redukcja NAD do NADH i tworzenie ATP
12/11/2011
29
Etapy glikolizy
Trzeci etap:
Przegrupowanie wewnątrzcząsteczkowe 3fosfoglicerynianu w 2-fosfoglicerynian
Dehydratacja 2-fosfoglicerynianu w fosfoenolopirogronian
Tworzenie pirogronianu i drugiej cząsteczki ATP
12/11/2011
30
Fruktoza może wchodzić do glikolizy poprzez:
Fosforylację fruktozy przy C1 i następnie
rozszczepienie na dwie triozy
Fosforylację przy C6 głównie w tkance
tłuszczowej
Galaktoza przekształca się w glukozę poprzez
fosforylację przy C1, połączenie z UDP-glukozą i
epimeryzację. Reakcja jest odwracalna i niezbędna
do syntezy cukrów złożonych
12/11/2011
31
Kontrola glikolizy
Fosfofruktokinaza
Jest hamowana przez wysoki poziom ATP, cytrynian i
obniżenie pH. Proces sprzężony z hamowaniem
heksokinazy.
Jest aktywowana przez AMP oraz fruktozo-2,6bisfosforan
Glukokinaza obecna w wątrobie i aktywna przy dużych
stężeniach glukozy kieruje ją do syntezy glikogenu lub
cyklu pentozowego i produkcji NADPH
12/11/2011
32
Kontrola glikolizy
Kinaza pirogronianowa
Kontroluje wypływ intermediatów z cyklu.
Jest hamowana przez ATP i alaninę (dającą sygnał
obfitości składników budulcowych)
Jest aktywowana przez fruktozo-1,6-bisfosforan
Adrenalina
Stymuluje glikolizę w mięśniach a hamuje w wątrobie
12/11/2011
33
Zaburzenia gospodarki węglowodanowej
wynikające z nieprawidłowego bilansu
energetycznego
- otyłość (bilans nadmiernie dodatni)
- niedożywienie (bilans ujemny)
genetyczne – wady enzymatyczne (zespoły złego
wchłaniania, zaburzenia przemiany galaktozy
i glikogenu)
wynikające z nieprawidłowej regulacji hormonalnej
- cukrzyca
12/11/2011
34
Otyłość
Dodatni bilans energetyczny prowadzi do
gromadzenia triglicerydów w tkance tłuszczowej
podskórnej.
W celu utrzymania prawidłowej gospodarki
węglowodanowo-lipidowej zwiększa się wydzielanie
i stężenie insuliny we krwi. Insulina hamuje
aktywność lipazy wewnątrzkomórkowej.
Konsekwencje – stłuszczenie wątroby, nadciśnienie,
choroba wieńcowa, cukrzyca
12/11/2011
35
Niedożywienie
Stan głodu charakteryzuje się zużywaniem przez
organizm własnych zapasów energetycznych. Po 3
dniach głodzenia ustala się nowa równowaga –
zmniejsza się stężenie insuliny a zwiększa glukagonu
przemiany kataboliczne – zwiększona lipoliza i
stężenie kwasów tłuszczowych. Powstają ciała
ketonowe i nasilona jest glukoneogeneza z
aminokwasów (białka mięśni). Azot w postaci
mocznika jest usuwany z moczem – ujemny bilans
azotowy.
Konsekwencje – ketoza, kwasica metaboliczna
12/11/2011
36
Zespoły złego wchłaniania i enzymopatie
dotyczy enzymów rozkładających disacharydy
galaktozemia – wada na poziomie transurydylazy prowadzi do
zablokowania przemian galaktozy i gromadzenia się tego
cukru. Prowadzi do poważnych zmian w układzie nerwowym,
nerkach, wątrobie. Wczesne wykrycie i usunięcie z diety
galaktozy pozwalają na uratowanie pacjenta.
glikogenozy (choroby spichrzeniowe) – zaburzenia przemian
glikogenu prowadzą do kumulacji tego cukru w wątrobie
(osłabienie sprawności narządu oraz marskość) i mięśniach
(mechaniczne uszkodzenie włókien).
12/11/2011
37
Hipoglikemia
To stan “niedocukrzenia”, pojawiający się gdy poziom cukru we
krwi spada poniżej 2-5 mmol/l.
Do najczęściej występujących objawów niedocukrzenia należą:
głód, kołatanie serca, drżenie, potliwość, mrowienie wokół ust i
języka, niekiedy ból głowy.
Konsekwencją braku podjęcia właściwych działań, mogą być
zaburzenia funkcji mózgu, upośledzenie funkcji poznawczych,
narastająca dezorientacja, różnorodne zaburzenia neurologiczne
i zachowania, a ostatecznie - utrata przytomności z
towarzyszącymi drgawkami. Długotrwałe i często występujące
hipoglikemie mogą prowadzić do nieodwracalnego uszkodzenia
mózgu, a nawet śmierci.
12/11/2011
38
HIPOGLIKEMIA
na czczo – nadmierne zużycie, zaburzenie
magazynowania glukozy, upośledzenie
glikogenolizy, guz wysp Langerhansa
po posiłku – hipersekrecja insuliny, uszkodzenie
wątroby (upośledzony metabolizm insuliny), niedobór
glikokortykosterydów (niedoczynność nadnerczy lub
przysadki), polekowa (salicylany, leki hipoglikemizujące)
12/11/2011
39
Hiperglikemia
To stan, w którym stężenie glukozy we krwi
przekracza 15 mmol/l. Nie jest poważnym stanem,
jeżeli trwa krótko.
Przedłużone
okresy
nawet
umiarkowanie
podwyższonego poziomu cukru we krwi, jeżeli nie
są rozpoznane i prawidłowo leczone, mogą być
przyczyną stanu zagrożenia życia i prowadzić do
poważnych powikłań cukrzycy.
12/11/2011
40
HIPERGLIKEMIA
cukrzyca (niedobór insuliny, insulinooporność)
choroba Cushinga (nadmiar ACTH lub glikokortykoidów)
akromegalia (nadmiar hormonu wzrostu)
urazy mózgu (wzrost amin katecholowych, kortyzolu)
wstrząs (wzrost amin katecholowych, kortyzolu
12/11/2011
41
CUKRZYCA
typ I – insulinozależna
(zwana również cukrzycą młodzieńczą) jest spowodowana
bezwzględnym brakiem insuliny i występuje u osób
młodych, szczupłych. W leczeniu stosuje się dietę i
insulinę. Może mieć bardziej chwiejny przebieg ze
skłonnością do niedocukrzeń i śpiączki.
typ II – insulinoniezależna
(zwana również cukrzycą dorosłych) występuje u osób po
35.-40. roku życia, najczęściej otyłych. Obserwuje się
częstsze występowanie rodzinne. Przyczyną tej choroby
jest oporność tkanek obwodowych (mięśni, tkanki
tłuszczowej i wątroby) na insulinę lub upośledzenie jej
wydzielania. Leczenie polega na stosowaniu odpowiedniej
diety, leków doustnych i/lub insuliny.
12/11/2011
42
Zaburzenia metabolizmu w cukrzycy
hiperglikemia (zwiększona dodatkowo nasiloną syntezą
glukozy z aminokwasów i kwasów tłuszczowych)
glukozuria
odwodnienie tkanek (zwiększona osmolarność osocza)
poliuria
polidypsja
głównym źródłem energii są tłuszcze (kwasy tłuszczowe
ketonemia i ketonuria) i białka
hyperlipidemia
kwasica ketonowa ( śpiączka)
12/11/2011
43
Powikłania ostre w cukrzycy
nieketonowa śpiączka hiperosmolarna
(znaczna hiperglikemia ze znacznym
odwodnieniem tkanek)
kwasica mleczanowa (wynika z nadmiernej
produkcji kwasu mlekowego i braku
możliwości jego transformacji do glukozy w
wyniku upośledzenia glukoneogenezy w
mięśniach)
12/11/2011
44
Powikłania późne w cukrzycy
Uszkodzenia funkcji śródbłonka naczyń
retinopatia cukrzycowa (proliferacja naczyń
siatkówki, zaćma)
nefropatia ( białkomocz)
nadciśnienie (czynnik proliferacyjny – IGF-1)
miażdżyca (modyfikacja lipoprotein)
12/11/2011
45
Diagnostyka laboratoryjna zaburzeń gospodarki
węglowodanowej
badanie stężenia glukozy we krwi
badanie stężenia glukozy w moczu
dobowe wydalanie glukozy z moczem
związki ketonowe w moczu
próby tolerancji glukozy
badanie stężenia insuliny we krwi
12/11/2011
46
Glikowana hemoglobina
Hemoglobina glikowana - HbA1c - HbA z przyłączoną
nieenzymatycznie, trwale cząsteczką glukozy (na skutek
zwiększonego poziomu glukozy we krwi) do N-końcowych
aminokwasów łańcuchów globiny.
Zawartość HbA1c wyraża się jako odsetek zmienionej
hemoglobiny do jej całkowitego stężenia, służy on do oceny
wyrównania metabolicznego cukrzycy.
Glikacja jest to proces łączenia glukozy z białkami (m.in.
hemoglobiną). Proces przebiega powoli i jest prawie
nieodwracalny. Trwa przez cały okres życia krwinki czerwonej,
wynoszący przeciętnie 120 dni, dlatego jest on wskaźnikiem
glikemii w czasie ostatnich 3 miesięcy. Krwinki czerwone
zdrowych dorosłych osobników zawierają 4–6 procent
hemoglobiny
glikowanej
(HbA1c).
12/11/2011
47
Fruktozamina (izoglukozamina)
To glikowane białko osocza krwi (głównie albumina).
Stężenie fruktozaminy koreluje z stopniem wyrównania
glikemii w przebiegu cukrzycy ale nie koreluje z ryzykiem
rozwoju powikłań cukrzycowych.
W związku z okresem półtrwania albumin wynoszącym 1420 dni, jej poziom świadczy o wyrównaniu cukrzycy w
przebiegu ostatnich 2 tygodni od oznaczenia.
W przypadku hipoalbuminemii wartość diagnostyczna
oznaczenia fruktozaminy traci na znaczeniu.
12/11/2011
48
Ketoza u krów wysokomlecznych,
zatrucie ciążowe u owiec
Intensywne pobieranie glukozy z krwi podczas
laktacji (także ciąży) prowadzi do krańcowej
hipoglikemii często przy jednoczesnej małej
ilości glikogenu w wątrobie. Zmniejsza się
wydzielanie insuliny przez co zmniejsza się
zużywanie glukozy a także wzmaga się lipoliza w
tkance tłuszczowej. Prowadzi to do wzrostu
stężenia kwasów tłuszczowych i następnie ciał
ketonowych. Pojawia się stłuszczenie wątroby a
także kwasica metaboliczna.
12/11/2011
49
12/11/2011
50