Hipotermia – fragment pracy P.Sosnowskiego,
1.2. Przyczyny wywołujące hipotermię
Hipotermią przyjęto określać obniżenie temperatury ciała poniżej 35C. Podczas obniżania
temperatury ciała bilans cieplny ustroju staje się ujemny. Utrata ciepła jest większa niż jego
wytwarzanie i akumulacja. Hipotermia może powstać nawet przy całkowicie sprawnych
mechaniz-mach termoregulacji, gdy ustrój narażony na zimno pozostaje w warunkach
uniemożliwiających świadomą obronę. Obniżenie temperatury ciała może też nastąpić z
przyczyn wewnątrzustrojowych, jako skutek niewydolności mechanizmów biorących udział
w termoregulacji (gentilelo 94, Schaler 90, Brodersen 96).
Ze względu na sposób wywołania hipotermii, a także charakter odpowiedzi metabolicznych
mówimy o hipotermii przypadkowej lub indukowanej.
Z przypadkową hipotermią mamy do czynienia kiedy dochodzi do obniżania temperatury
ciała na skutek oddziaływania czynników fizycznych np. podczas przebywania w zimnej
wodzie, w czasie mroźnych zamieci śnieżnych, przy jednoczesnym braku ciepłego lub
wodoszczelnego ubrania ( Hesselberg 95 ).
Indukowaną hipotermię wywołują środki krążeniowe rozszerzające naczynia i obniżające
ciśnienie krwi, leki przeciwgorączkowe i neuroleptyczne oraz narkotyki ( Strutton 96,
Bernard 98, Forstot 95, Matuszek 86 ). Leki mogą modyfikować temperaturę ciała
specyficznie - działając na ośrodki termoregulacji lub niespecyficznie - działając na inne
ośrodki lub drogi nerwowe (Chen 96, Sharif 96 ).
Hipotermia często jest konsekwencją anestezji. Leki anestetyczne powodują poszerzenie
zakresu temperatur w jakich pojawiają się reakcje termoregulacyjne z 0,2oC do blisko 4oC (
Lopez 94, Sessler 94 ).
W tym przypadku hipotermia ma charakter kombinowany tj. spowodowany jednoczesnym
działaniem leków anestetycznych oraz środowiska. Hipotermia występuje jako efekt uboczny
podczas długotrwałych zabiegów operacyjnych, zwłaszcza na otwartej jamie brzusznej (
Frank 94, Suchorzewska 97, Echerbam 90, Joachimson PP ), a także jako skutek masywnych
transfuzji (Ferrara 90 ).
Często hipotermia towarzyszy takim chorobom jak śpiączka cukrzycowa, hipoglikemia
( Passias 96 ), niedoczynność tarczycy ( Schaller 90 ), masywne krwotoki (Smith 98, Burch
92 ) czy ciężkie oparzenia ( Gueugniaud PY 1996 ).
Obniżanie temperatury ciała obserwuje się w takich stanach jak jadłowstręt psychiczny lub
oty-łość ( Hartman 1995, Severien 92 ). Wolno postępujące obniżanie się temperatury ciała
nawet w temperaturze pokojowej można obserwować u ludzi starych, niedożywionych, z
urazami centralnego układu nerwowego, dysfunkcją autonomicznego lub motorycznego
układu nerwowego ( Hazama 92, Mouton 96 Collins 86, White 96 ). Hipotermia w przebiegu
niektórych chorób zakaźnych ( cholera, błonica, ospa) jest skutkiem toksycznego uszkodzenia
narządów biorących udział w termoregulacji ( Alcami A 1996, Basilico 1997,Shukla 1995 ).
1.3. Klasyfikacja hipotermii
Jak dotychczas nie zostały przyjęte jednolite standardy klasyfikowania hipotermii. Wg
Okamury obniżenie temperatury ciała do 30C to hipotermia płytka, od 30C do 25C
średnia, 25C - 20C głęboka a 20C do 10C graniczna ( Malec 92) . Delorme zaproponował
podział, gdzie 35C - 30C to hipotermia lekka, 30C - 20C średnia a poniżej 20C głęboka,
( Delorme 75).
W ośrodkach klinicznych przyjmuje się jeszcze inne przedziały temperatur uwzględniając
objawy kliniczne ( Antretter 95 ). Uwzględniane jest tu pojęcie tzw. „ zera biologicznego
tkanek ”, będące graniczną dla danej tkanki temperaturą, poniżej której ustają czynności
fizjologiczne przy zachowanej zdolności tkanki do powrotu do stanu prawidłowego (
Dogliotti 1953). Najwyższą wartość - 31C zero biologiczne przyjmuje dla kory mózgu, dla
pnia mózgu 27C - 28C ( 166 Juvenalle 1954) a dla rdzenia kręgowego wynosi 24C (
Majstrach 1950, Marsala 97 ).
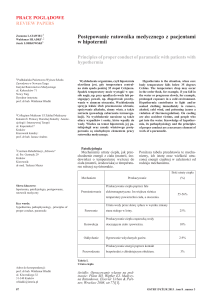
Głębokość hipotermii
łagodna 32-35C
umiarkowana 28-35C
amnezja, apatia, zanik
działań racjonalnych
zaburzenia EEG, halucynacje,
utrata świadomości
obwodowe zwężenie naczyń,
bradykardia
wzrost częstości pracy serca,
migo-
głęboka < 28C
śpiączka, obniżenie aktywności elektrycznej mózgu
spadek tętna i rzutu serca, arytmie
spadek RR, tętna,
przedłużony skurcz serca,
brak tętna na obwodzie,
tanie komór lub asystolia
dreszcze
hiporefleksja, sztywność, zanik
dreszczy
bezdech, brak odruchów
Ryc. 1. Głębokość hipotermii uwzględniająca kryteria kliniczne (wg Antrettera)
1.4. Reakcje ustroju na zimno
Podczas działania zimna na organizm dochodzi do uruchomienia szeregu reakcji
adaptacyjnych. Pojawiają się one gdy temperatura wewnętrzna ciała obniży się poniżej
36,5C. Ogólnie można podzielić je na behawioralne i autonomiczne. Reakcje narządowe i
metaboliczne są wypadkową: 1) czasu ekspozycji i intensywności z jaką zimno działa na
organizm, 2) odpowiedzi nerwowej i humoralnej na stres, 3) szybkości wyczerpywania się
rezerw energetycznych oraz 4) tego czy świadomość ustroju jest zachowana czy też nie.
1.5. Termoregulacja na poziomie OUN
Odczuwanie zimna związane jest z pobudzeniem termoreceptorów znajdujących się
zarówno w tkankach powierzchniowych jak i głębokich: w mózgu, rdzeniu kręgowym, w
górnych drogach oddechowych, przewodzie pokarmowym, mięśniach i naczyniach żylnych,
skórze i podskórnej tkance tłuszczowej. Impulsacja z tych receptorów przekazywana jest do
podwzgórza w którym zlokalizowany jest ośrodek termoregulacji. Składa się on z dwóch
części, w podwzgórzu przednim znajduje się ośrodek ” utraty ciepła ” zawiadujący reakcjami
zwiększającymi eliminację ciepła. Natomiast w podwzgórzu tylnym położony jest ośrodek ”
zachowania ciepła ”, kierujący rekcjami powodującymi zmniejszanie utraty ciepła przez
organizm i zwiększaniem produkcji ciepła. Neurony zlokalizowane w przednim podwzgórzu
mają charakter termodetektorów i głównie reagują na wzrost temperatury uruchamiając
wydzielanie potu oraz wywołując rozszerzenie naczyń skóry i tkanki podskórnej. Neurony
wrażliwe na zimno występują nielicznie w podwzgórzu przednim. Natomiast neurony
znajdujące się w podwzgórzu tylnym nie mają charakteru termodedektorów stanowiąc stację
przełącznikową dla impulsacji z termoreceptorów obwodowych. Ich pobudzenie wyzwala
reakcje termogenezy chemicznej. Bardzo wąski, 0,20C zakres temperatury, w którym reaguje
ośrodek termoregulacji sugeruje istnienie jednego punktu wrażliwości centralnego termostatu
( Lopez 94)
Centralny układ nerwowy
Wzgórze
nadnercza
ZIMNO
Skutki:
termoreceptory
SKÓRA
zwężenie naczyń
utrata
Podwzgórze
układ adrenergiczny
mięśnie
rozszerzenie
naczyń, drżenie
serce +
serce -
termogeneza
termogeneza
tarczyca
termogeneza
ciepła
Reakcja:
wczesna
wczesna
późna
Ryc. 2. Reakcje ustrojowe uruchamiane podczas ekspozycji organizmu na zimno (wg
Schaler)
1.6. Zmiany czynnościowe
W przebiegu szybkiego obniżania temperatury organizmu obserwuje się trzy fazy - faza
pierwsza to pobudzenie, trwa ona do obniżenia się temperatury ciała poniżej 34C.
Mechanizmy adaptacyjne, z jednej strony nasilają procesy wytwarzania ciepła, z drugiej
hamują jego utratę. Pobudzenie termoreceptorów obwodowych uruchamia reakcję stresową.
W efekcie następuje pobudzenie układu adrenergicznego, a także wzrost wydzielania
hormonów rdzenia nadnerczy. Katecholaminy pobudzają ośrodek oddechowy i ośrodek
krążenia w rdzeniu przedłużonym ( Kusuoka H 91 ). Zintensyfikowanej pracy serca i układu
oddechowego towarzyszy zwiększona produkcja ciepła. Jednocześnie ośrodek termoregulacji
poprzez pobudzenie motoneuronów , doprowadza do zwiększenia napięcia mięśni
szkieletowych co zwiększa produkcję ciepła o około 50% ( Moss 86 Seiyama 96 ). Jeśli ilość
ciepła dostarczanego tą drogą jest niewystarczająca uruchomiona zostaje termogeneza
drżeniowa. Hydroliza ATP uwalnia ciepło, a uruchomione jednocześnie reakcje
komórkowego łańcucha oddechowego wytwarzają dodatkowe jego ilości. Efektem jest wzrost
przemiany materii i produkcji ciepła nawet o 500% ( Zwischenberger 87, Macintyre 87 ).
W miarę oziębiania organizmu obserwuje się wzrost wydzielania zarówno TSH jak i
hormonów tarczycy, czego efektem jest wzrost przemiany materii ( termogeneza
bezdrżeniowa ) i produkcji ciepła co określa się jako efekt kalorygenny ( Fregly 89, Niida
1991, Dubuc 89). Jednakże uważa się, że termogeneza bezdrżeniowa nie jest najważniejszym
źródłem produkcji ciepła u osób dorosłych ( Hynson 93 ). Okuda ( 1986 ) stwierdził u
szczurów w warunkach umiarkowanej hipotermii ( ok. 350C ) wzrost wydzielania TSH i
hormonów tarczycy, natomiast w głębokiej hipotermii ( poniżej 240C ) zmiany te nie były
statystycznie znamienne. Sugeruje on, że wzrost wydzielania TSH wywołany jest
zwiększonym wydzielaniem TRH przez podwzgórze. Po przecięciu dróg aferentnych do
podwzgórza stwierdzano brak wydzielania TSH oraz hormonów tarczycy ( Herbute 1984 ).
Sugerowałoby to uruchomienie odpowiedzi na oziębienie na drodze nerwowej. Wzrost
poziomów hormonów tarczycy obserwowano już po 40 minutach ekspozycji na zimno, który
utrzymywał się zależnie od czasu przebywania w tych warunkach ( Sawhney 95, Vybiral 84
).
Zwiększeniu wytwarzania ciepła towarzyszy zmniejszenie jego utraty, co następuje
poprzez zwężenie naczyń krwionośnych skóry i tkanki podskórnej ( centralizacja przepływu
krwi ) oraz zniesienie czynności gruczołów potowych ( Granberg 91, Kurz 95, De Witte 98 ).
W fazie tej obserwuje się charakterystyczny fazowy przepływ krwi przez naczynia
krwionośne obwodowych części ciała – tzw. fale Lewisa. Jeśli ochłodzenie jest znacznego
stopnia to pojawiają się okresowe rozszerzenia naczyń i zwiększenie przepływu krwi.
Mechanizm ten ma na celu chronienie tych części ciała przed odmrożeniem( Swenson 96,
Meusen 86). Jeżeli temperatura tych obszarów obniża się bardziej, przepływ krwi przez
zagrożone obszary ustaje całkowicie ( Johnson 86, Major 81, Savard 85, Vising 91 ).
Po fazie pobudzenia następuje faza druga - zmniejszonej reaktywności ośrodków rdzenia
przedłużonego. Kiedy temperatura ciała obniży się poniżej 34C, obserwuje się postępujące
zwolnienie akcji serca. Tłumaczone jest ono oddziaływaniem schłodzonej krwi na układ
bodźco-przewodzący serca. Przy temperaturze poniżej 28C pojawiają się bloki serca, a w
przypadku narkozy i zabiegów chirurgicznych może wystąpić migotanie komór ( Moss 86 ).
Podczas oziębiania komórek rozrusznikowych serca królika stwierdzono obniżenie
przewodności błony komórkowej dla jonów Na+, K+, Ca++ a także obniżenie aktywności
pomp Na+-K+ oraz Ca++ ( Hagiwara 1992, Willis 87 ). Przepływ wieńcowy krwi podczas
głębokiej hipotermii jest znacznie zmniejszony ( do 40% wyjściowego ) jednak
proporcjonalnie większy niż w innych tkankach i narządach, gdzie osiąga wartości niższe niż
20% wyjściowych ( Anzai 1978, Tveita 94 ). Jest to spowodowane redystrybucją krwi oraz
autoregulacją przepływu wieńcowego, w efekcie jest on proporcjonalny do zużycia tlenu
przez serce ( Su 80, London 88 ).
W miarę obniżania temperatury ciała również czynność układu oddechowego ulega
redukcji. Zimno hamuje czynność ośrodka oddechowego. Zwiększa się martwa przestrzeń
zarówno anatomiczna jak i fizjologiczna oraz zaleganie krwi w płucach ( Gautier 86, Sladen
85 Joahimsson PO 87). Charakterystyczny dla hipotermii jest wzrost powinowactwa
hemoglobiny do tlenu ( przesunięcie krzywej dysocjacji w lewo ). Jednocześnie na skutek
lepszego rozpuszczania się CO2 w osoczu zmniejsza się wartość współczynnika oddechowego
RQ ( Giesbrecht 97, Bacher 97, Frappell 98 ).
W nerkach obserwuje się proporcjonalne do obniżania się temperatury zmniejszenie
resorbcji zwrotnej w kanalikach nerkowych. Szczególnie istotne jest zmniejszenie resorbcji
jonów sodu. Zwiększona utrata jonów sodu, mimo zmniejszonej filtracji powoduje, że ilość
wydalanego moczu zwiększa się - przy temperaturze 32C dwukrotnie, a przy 30C nawet
trzykrotnie ( Broman 95 ).
Utrata wody z organizmu jest powodem zwiększenia lepkości krwi. Podwyższenie
wartości hematokrytu dodatkowo potęguje przechodzenie elementów morfotycznych krwi z
puli śledzionowej do krążenia obwodowego. W osoczu wzrasta poziom -globulin przy
jednoczesnym obniżeniu - i -globulin. Obserwuje się zaburzenia produkcji tromboksanu A2
przez płytki krwi, a przy obniżeniu temperatury ciała poniżej 33C wydłużenie czasów protrombinowego i tromboplastynowego ( valeri 92, valeri 87, Reed 92, Johnston 89 ).
Obniżeniu ulega stężenie jonów K+ na skutek przesunięcia ich do przestrzeni
wewnątrzkomórkowej. Natomiast wzrost stężenia potasu w płynie zewnątrzkomórkowym
świadczy o głębokiej kwasicy, lizie komórek i obumieraniu tkanek ( Schaller 90, Mair 94
Locher 91). Narasta kwasica na skutek zwiększonej retencji CO2 spowodowanej
niewydolnością mikrokrążenia ( Hauge 95, Blayo 80 ). Na skutek wzrostu lepkości krwi
rośnie ciśnienie tętnicze. Dopiero obniżenie temperatury ustroju poniżej 32C wywołuje
spadek ciśnienia tętniczego, głównie na skutek nasilającej się niewydolności serca. Przy
temperaturze 25C ciśnienie skurczowe lewej komory obniża się nawet o ponad 50% (
Larcan 83, Tveita 94) .
Obniżaniu się temperatury ciała towarzyszy zmniejszanie się przepływu mózgowego o 67% na każdy 1C. ( Michenfelder 91, Todd 92, Cheng 95 ). Jednocześnie zanika pobudliwość
ośrodków korowych. U ludzi, już przy temperaturze ciała 35C obserwuje się niebezpieczne
dla życia objawy psychiczne polegające głównie na braku chęci do walki o przetrwanie,
zaburzenia świadomości, niezdolność do artykulacji mowy. Przy temperaturze 30C dochodzi
do utraty świadomości i niemożności wykonywania ruchów dowolnych ( Smith 96,
Christensen 90, Braun 96 ).
W przewodzie pokarmowym obserwowane jest zmniejszenie perystaltyki jelit. Już przy
obniżeniu temperatury do 34C może nastąpić niedrożność jelit ( Udassin 97, Simic 97 ).
Przepływ krwi przez wątrobę zmniejsza się, jakkolwiek spadek ten jest mniejszy niż w
innych narządach. Zwiększa się natomiast zastój krwi i przechodzenie płynu do przestrzeni
zewnątrzkomórkowej. Czynność odtruwająca wątroby zmniejsza się, maleje wydzielanie
żółci ( Mathie 93). Hamowana jest również czynność zewnątrzwydzielnicza trzustki ( Panzig
86, Edwards 86) .
Poniżej 26C - 27C faza druga przechodzi w fazę trzecią - odpowiadającą letargowi.
Stwierdza się objawy zbliżone do objawów śmierci klinicznej, oziębienie ciała i bladość
powłok, brak tętna na obwodzie, brak odruchów neurologicznych i sztywność mięśni.
Czynność układu krążenia i oddychania jest prawie nieuchwytna ( Braun 96,Antretter 95, 97,
Lloyd 96). W głębokiej hipotermii obserwuje się obniżenie neurosekrecji w obrębie osi
podwzgórze-przysadka, a także zmniejszone wydzielanie hormonów tarczycy ( Okuda
86,Ririe 98, Naumenko 96). Obniżona jest sekrecja katecholamin, która w temperaturze
poniżej 20C ustaje całkowicie, znoszone jest także obwodowe działanie adrenaliny ( Patchev
91, Hirvonen 95 ). W fazie tej, czynności termoregulacyjne są jeszcze zachowane czego
wyrazem są dreszcze i wzmożone zużycie tlenu podczas ogrzewania ustroju ( Lenhard 97).
Jeżeli działanie zimna na ustrój jest długotrwałe, zmiany mają podobny przebieg, jednak po
kilku godzinach następuje śmierć w wyniku wyczerpania rezerw energetycznych ustroju (
Shepard 91, Bittel 92 ).
1.7. Zmiany metaboliczne
Podczas hipotermii obserwuje się hiperglikemię i hipoinsulinemię. Zaburzenia
metabolizmu glukozy są głębsze aniżeli wynikałoby to z samego obniżenia temperatury ciała
i wywołanego tym zmniejszenia intensywności reakcji enzymatycznych oraz mniejszego
zapotrzebowaniem energetycznego tkanek. Uważa się, że przyczyną hiperglikemii jest
wzmożone wydzielanie katecholamin ( Motamed 98, Tsvietovskaia 96, Sun 97).
W efekcie nasilona zostaje glikogenoliza wątrobowa przy jednoczesnym zintensyfikowaniu
lipolizy i zużycia WKT przez tkanki ( Kubota 98, Tveita 94, Kuntschen 86, ). Tezę tę
potwierdza obniżenie poziomu glukozy obserwowane podczas eksperymentów z
wywoływaniem hipotermii u zwierząt po adrenalektomii lub po zastosowaniu preparatów
blokujących receptory -adrenergiczne ( Kimura 90, Smythe 89, Bray 91 ). W trakcie badań
przeprowadzonych u ludzi podczas hipotermii również stwierdzono obniżenie poziomu
insuliny skojarzone z jednoczesnym wzrostem stężenia katecholamin i glukozy w surowicy
krwi ( Hoo-Paris 91, Tsvetovskaia 94, Kuroshima 83 ). Dodatkowy wpływ potęgujący
hipoinsulinemię ma bezpośrednie działanie niskiej temperatury. W badaniach na izolowanej
trzustce stwierdzono przy temperaturze 16C zahamowanie wydzielania insuliny. Natomiast
w zakresie temperatur 26C - 38C obserwowano wprost proporcjonalną zależność, pomiędzy
temperaturą, a ilością insuliny uwalnianej ze stymulowanej glukozą trzustki ( Escolar 90,
Buchanan 91 ). Oczywiście oba te mechanizmy: bezpośrednie działanie niskiej temperatury
jak i hamujący wpływ katecholamin mogą się wzajemnie uzupełniać ( Shepard 93 ). Ponadto
w trakcie hipotermii dochodzi do zaburzenia stosunku insulina/ glukagon. Wg Ungera
decyduje on o intensywności metabolizmu ( Unger 76 ). Obniżenie tego stosunku dodatkowo
nasila stymulowaną przez katecholaminy glikogenolizę wątrobową i lipolizę w tkance
tłuszczowej. W konsekwencji w surowicy krwi rośnie stężenie wolnych kwasów
tłuszczowych i glicerolu ( Lehot 92 ).
1.8. Zaburzenia homeostazy energetycznej podczas hipotermii
Zmiany metaboliczne obserwowane podczas hipotermii są konsekwencją zaburzeń w
gospodarce energetycznej ustroju. Przy istniejącym ujemnym bilansie energetycznym
polegają na, zmniejszeniu zużycia jak i wytwarzania energii ( Vallerand 93,Jansson 87 ).
Podstawową rolę w gospodarce energetycznej ustroju pełnią nukleotydy adenylowe. Są to
związki stanowiące połączenie kwasu ortofosforowego i nukleozydów. Di- i trifosforany
nukleozydów mają jedno lub dwa wiązania fosforanowe bogate w energię. Są to związki
makroergiczne, potocznie nazywane związkami wysokoenergetycznymi. Magazynowanie
energii w tych związkach zachodzi głównie w warunkach tlenowych drogą fosforylacji
oksydacyjnej, oraz w mniejszym stopniu, w warunkach beztlenowych, podczas fosforylacji
substratowej. Przy rozpadzie wiązań wysokoenergetycznych tych związków uwalniana jest
wolna energia - przy rozpadzie ATP do ADP ok. 32kJ/mol, odpowiednio ADP do AMP
27kJ/mol. Nukleotydy purynowe w postaci ATP stanowią główne źródło zmagazynowanej
energii. Dominacja ATP wśród nukleotydów wydaje się sugerować specjalną rolę tego
nukleotydu w metabolizmie ustrojów żywych ( Singer 90 ).
W miarę obniżania temperatury ciała następuje zmniejszanie się aktywności enzymów
odpowiedzialnych za rozkład związków wysokoenergetycznych, a także zmniejszone zużycie
ATP przez tkanki ( Krauss 89-91, Van der Veen 90, ). Badania prowadzone w naszej
Katedrze potwierdziły, że w hipotermii zmniejsza się zawartość ATP w tkankach i we krwi.
Dla procesów energetycznych zachodzących w ustroju istotny jest nie tylko poziom
nukleotydów adenylowych ale ich wzajemny stosunek znany jako ładunek energetyczny
adenylanów ( AEC ), a opisany w równaniu - [ ATP + 0,5 ADP ]/ [ ATP + ADP + AMP ]
przez Atkinsona ( Atk 77 ). Badania nasze prowadzone na szczurach poddanych
krótkotrwałej hipotermii ( 26C ) potwierdziły, że wartość ładunku energetycznego
adenylanów świadczy o oszczędzaniu energii w tych warunkach ( Krauss 87, Koźlik 1987 ).
Należy podkreślić, że charakter i głębokość zmian metabolicznych w przebiegu hipotermii
indukowanej zależy w dużym stopniu od stopnia wyłączenia czynności ośrodkowego układu
nerwowego, co wynika ze sposobu i głębokości uśpienia. Przy stosunkowo płytkim
znieczuleniu ogólnym zmiany metaboliczne są takie jakie obserwuje się podczas reakcji
stresowej i polegają na wzroście stężeń WKT, glukozy i glicerolu w surowicy krwi. Przy
uśpieniu głębokim nie obserwuje się zmian w poziomach tych metabolitów, a przy bardzo
głębokim procesy metaboliczne przebiegają w sposób obserwowany u zwierząt zapadających
w sen zimowy ( Yager 96, Cherel 95 )
1.9. Zastosowanie hipotermii
Zgodnie z prawem Van’t Hoffa Arheniusa, wraz z obniżaniem temperatury zachodzi
zmniejszanie szybkości reakcji chemicznych. W granicach pomiędzy 40C a 5C szybkość
reakcji zmniejsza się o połowę na każde 10C obniżenia temperatury ciała.
Spowolnienie reakcji biochemicznych wywołuje zwolnienie metabolizmu tkankowego co w
efekcie zmniejsza zapotrzebowanie na tlen. Konsekwencją obniżenia temperatury ciała jest
zwiększenie tolerancji ustroju na niedotlenienie. Czas w którym narządy mogą funkcjonować
przy zmniejszonej podaży tlenu bez wystąpienia nieodwracalnych zmian wydłuża się.
Dotyczy to szczególnie tkanek o intensywnym metaboliźmie takich jak centralny układ
nerwowy lub mięsień serca ( Michenfelder 91, Swain 91, Sano 92 ).
Pierwsze doniesienia o zastosowaniu hipotermii jako potencjalnej metody zmniejszenia
wtórnych uszkodzeń mózgu pochodzą już z lat czterdziestych ( Fay44 i 45). W 1950 roku po
serii eksperymentów z ochładzaniem powierzchniowym kanadyjski badacz Biegelow
sugerował możliwość klinicznego zastosowania hipotermii. Pod koniec tego roku wykazał, że
można bezpiecznie zatrzymać na 15 minut krążenie krwi u psów schłodzonych do
temperatury 20C ( Biegelow 50 x2 ). Stwierdzono, że hipotermia taka zmniejsza zużycie
energii i zapotrzebowanie na tlen ( Rosomoff 59, Bellamy 66).
Ochronne działanie hipotermii wyraża się zahamowaniem obniżania poziomu ATP, co
zapobiega powstawaniu nieodwracalnych zmian w komórce ( Kaijser 85, Masuda 92, Locked
95, Portman 94 ). W latach pięćdziesiątych potwierdzono także celowość stosowania
indukowanej hipotermii jako czynnika chroniącego centralny układ nerwowy przed
niedotlenieniem zwłaszcza podczas operacji z zatrzymaniem krążenia ( Bigelow 1950,
Rosomoff 59).
W 1960 roku do praktyki klinicznej wprowadzono hipotermię głęboką połączoną z
zatrzymaniem krążenia (Belamy 96, Marion 96). Hipotermia stała się wkrótce metodą
powszechnie stosowaną szczególnie podczas zabiegów kardiochirurgicznych prowadzonych z
zastosowaniem krążenia pozaustrojowego. Okazało się jednak, zwłaszcza w przebiegu
hipotermii głębokiej ( około 15C ), że występują powikłania neurologiczne np. choreoatetoza
( DeLeon 98 ). Natomiast następstwem zaburzeń w gospodarce tłuszczowej i
węglowodanowej bywało obserwowane już w latach pięćdziesiątych przez Knockera, a
później przez Browna, tak znaczne nasilenie infiltracji narządów wewnętrznych przez lipidy,
że prowadziło to do śmierci ustroju ( Knocker 1955, Brown 1962 ). Jak się okazało w trakcie
badań eksperymentalnych najbardziej narażone na infiltrację są narządy aktywnie
wychwytujące lipidy - serce, wątroba, nerki i nadnercza. Wykazano, że zmiany te pojawiały
się nawet po stosunkowo krótkiej hipotermii ( 2,5 godziny w temperaturze 25 - 27C ).
Powikłania będące skutkiem schładzania organizmu spowodowały, że po początkowym
okresie entuzjazmu, w latach późniejszych zainteresowanie hipotermią jako metodą leczniczą
zmniejszyło się ( Marion 96 ).
Ponowny wzrost zainteresowania hipotermią jest obserwowany od lat 80-tych. Wiąże się on
głównie z rozwojem transplantologii. Szereg ośrodków prowadziło wówczas badania nad
możliwościami przechowywania narządów pobranych celem dokonania przeszczepu
(Palombo 88, Shragge 81 ). W tym czasie prowadziliśmy w naszej Katedrze badania nad
zmianami w poziomie substratów energetycznych ze szczególnym uwzględnieniem zmian w
zawartości nukleotydów adenylowych w sercu poddanemu hipotermii i następczej reperfuzji (
Dyszkiewicz 88, Krauss 88-91 IIIx,).