ROZDZIAŁ 7
Farmakoterapia (I) – leki wziewne
Graeme P. Currie1, Brian J. Lipworth2
Aberdeen Royal Infirmary, Aberdeen, Wielka Brytania
Asthma and Allergy Research Group, Ninewells Hospital and Medical School, Dundee,
Wielka Brytania
1
2
NAJWAŻNIEJSZE INFORMACJE
• Wszyscy chorzy na przewlekłą obturacyjną chorobę płuc
•
•
•
•
(POChP) powinni w celu zmniejszenia nasilenia objawów stosować krótko działające leki rozszerzające oskrzela (krótko działające agonisty β2 lub krótko działające leki antycholinergiczne).
Terapię długo działającymi lekami rozszerzającymi oskrzela
(długo działającymi lekami antycholinergicznymi lub długo
działającymi agonistami β2) należy rozpocząć u tych chorych
z utrzymującymi się objawami i zaostrzeniami, u których FEV1
wynosi ≥50% wartości należnej.
Kortykosteroidy wziewnie nie powinny być stosowane w monoterapii POChP.
U chorych z utrzymującymi się objawami i zaostrzeniami,
u których FEV1 wynosi <50% wartości należnej, trzeba rozważyć zastosowanie długo działających agonistów β2 wraz
z wziewnymi kortykosteroidami lub długo działającymi lekami
antycholinergicznymi.
Długo działające leki antycholinergiczne, długo działające
agonisty β2 i kortykosteroidy podawane wziewnie powinny
być stosowane u chorych z zaawansowaną postacią choroby,
u których utrzymują się objawy i zaostrzenia.
Przewlekła obturacyjna choroba płuc (POChP) jest schorzeniem niejednorodnym i przypadek każdego pacjenta
należy rozpatrywać indywidualnie. Dotyczy to nie tylko
postaci, przebiegu naturalnego, objawów, niepełnosprawności czy częstotliwości zaostrzeń, ale również odpowiedzi
na leczenie. Stopniowe ustalanie leczenia farmakologicznego POChP opiera się zwykle na:
• zaawansowaniu ograniczenia przepływu powietrza;
• ciężkości objawów (zwykle duszności);
• ograniczeniach czynnościowych;
• występowaniu i częstotliwości zaostrzeń.
Wpływ fizjologiczny leków
rozszerzających oskrzela stosowanych
wziewnie
Wydaje się coraz bardziej oczywiste, że wziewne leki rozszerzające oskrzela zapewniają istotne korzyści kliniczne
wynikające nie tylko ze zwiększenia natężonej objętości
wydechowej pierwszosekundowej (FEV1). Oparcie się jedynie na samych pomiarach czynnościowych płuc w celu
34
Całkowita
pojemność
płuc
Wentylacja
objętością
oddechową
Zdrowe
płuco
W spoczynku Podczas wysiłku Podczas wysiłku
bez leku
z lekiem
rozszerzającego rozszerzającym
oskrzela
oskrzela
Pacjenci z POChP
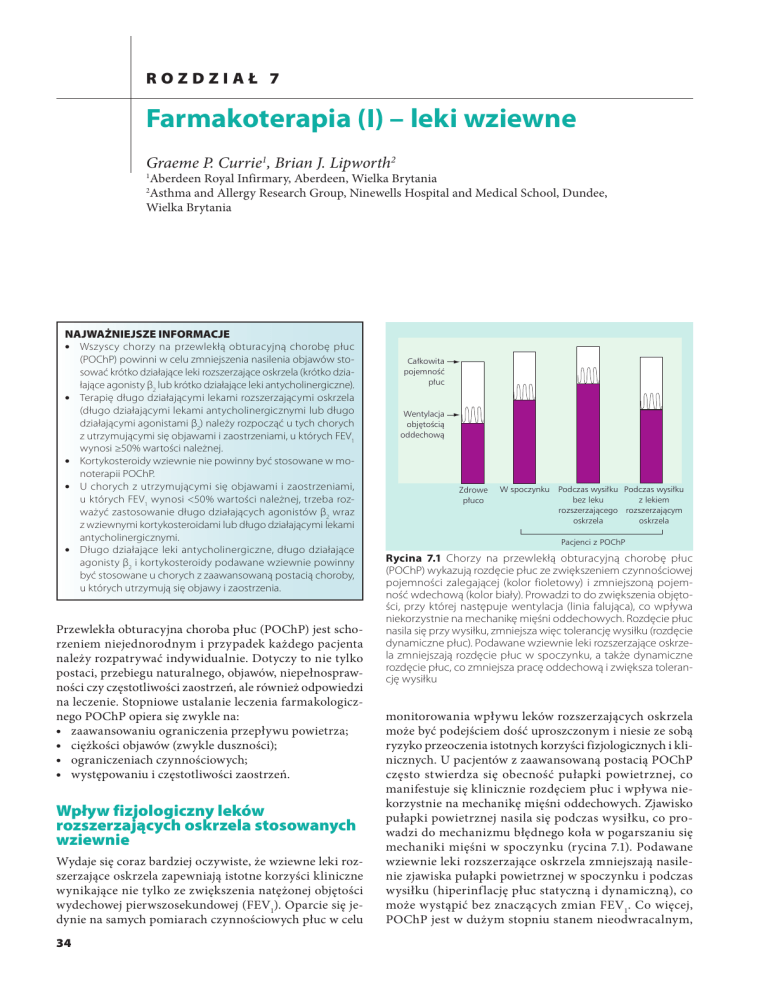
Rycina 7.1 Chorzy na przewlekłą obturacyjną chorobę płuc
(POChP) wykazują rozdęcie płuc ze zwiększeniem czynnościowej
pojemności zalegającej (kolor fioletowy) i zmniejszoną pojemność wdechową (kolor biały). Prowadzi to do zwiększenia objętości, przy której następuje wentylacja (linia falująca), co wpływa
niekorzystnie na mechanikę mięśni oddechowych. Rozdęcie płuc
nasila się przy wysiłku, zmniejsza więc tolerancję wysiłku (rozdęcie
dynamiczne płuc). Podawane wziewnie leki rozszerzające oskrzela zmniejszają rozdęcie płuc w spoczynku, a także dynamiczne
rozdęcie płuc, co zmniejsza pracę oddechową i zwiększa tolerancję wysiłku
monitorowania wpływu leków rozszerzających oskrzela
może być podejściem dość uproszczonym i niesie ze sobą
ryzyko przeoczenia istotnych korzyści fizjologicznych i klinicznych. U pacjentów z zaawansowaną postacią POChP
często stwierdza się obecność pułapki powietrznej, co
manifestuje się klinicznie rozdęciem płuc i wpływa niekorzystnie na mechanikę mięśni oddechowych. Zjawisko
pułapki powietrznej nasila się podczas wysiłku, co prowadzi do mechanizmu błędnego koła w pogarszaniu się
mechaniki mięśni w spoczynku (rycina 7.1). Podawane
wziewnie leki rozszerzające oskrzela zmniejszają nasilenie zjawiska pułapki powietrznej w spoczynku i podczas
wysiłku (hiperinflację płuc statyczną i dynamiczną), co
może wystąpić bez znaczących zmian FEV1. Co więcej,
POChP jest w dużym stopniu stanem nieodwracalnym,
Farmakoterapia (I) – leki wziewne
a opieranie się jedynie na wynikach pomiarów czynności
płuc może prowadzić do pominięcia istotnego korzystnego
wpływu na takie parametry jak statyczne objętości płuc,
jakość życia oraz częstotliwość zaostrzeń.
Krótko działające leki rozszerzające
oskrzela
Krótko działające agonisty receptorów β2, jak na przykład
salbutamol i terbutalina, działają bezpośrednio na mięśniówkę gładką oskrzeli, powodując rozszerzenie światła
dróg oddechowych (tabela 7.1). Ta grupa leków zmniejsza
duszność, poprawia czynność płuc i jest skuteczna przy
stosowaniu „na żądanie”.
Krótko działające leki antycholinergiczne, takie jak ipratropium, równoważą wzmożone, zależne od nerwu błędnego,
napięcie mięśniówki oskrzeli i również rozszerzają oskrzela.
W niektórych badaniach wykazano, że leki te zmniejszają
duszność, poprawiają czynność płuc i jakość życia pacjentów oraz redukują konieczność stosowania leków w trybie
nagłym.
Wszystkim chorym na POChP należy więc przepisywać
krótko działające leki rozszerzające oskrzela (agonisty β2
lub leki antycholinergiczne) podawane wziewnie w razie
wystąpienia dolegliwości. Pacjentom przyjmującym tiotropium – długo działający lek antycholinergiczny – nie
powinno się przepisywać krótko działających leków antycholinergicznych, należy raczej zalecić stosowanie w razie
potrzeby krótko działających agonistów receptorów β2.
Tabela 7.1 Właściwości farmakologiczne podstawowych leków
rozszerzających oskrzela stosowanych w POChP
Grupa
Lek
Czas rozpoczęcia
działania
(minuty)
Szczyt
działania
(minuty)
Czas
działania
(godziny)
Krótko
działający
agonista
receptora β2
Salbutamol
Terbutalina
5
5
60–90
60–90
4–6
4–6
Długo
działający
agonista
receptora β2
Formoterol
Salmeterol
5
45–60
60–90
120–240
12
12
Krótko działający lek
antycholinergiczny
Ipratropium
5–15
60–120
4–6
Długo działający lek
antycholinergiczny
Tiotropium
(Spiriva)
15
60–240
36
Długo działające leki rozszerzające
oskrzela
W POChP można stosować dwie grupy długo działających
leków rozszerzających oskrzela: długo działające leki an-
35
tycholinergiczne (tiotropium) oraz długo działające agonisty receptora β2 (formoterol i salmeterol). Wiele badań
oceniało skuteczność tych leków w POChP, a wytyczne
zalecają, aby długo działający lek rozszerzający oskrzela
stosować w monoterapii u pacjentów z objawami i FEV1
≥50% wartości należnej. Jeśli nadal utrzymują się objawy,
można zalecić równoczesną terapię długo działającym
lekiem rozszerzającym oskrzela z drugiej grupy stosowanym poprzez osobne urządzenie do podawania wziewnego.
Długo działające leki antycholinergiczne i długo działające
agonisty receptora β2 są zwykle dobrze tolerowane, chociaż
u niektórych pacjentów mogą występować działania niepożądane (ramka 7.1).
Ramka 7.1 Działania niepożądane długo działających
leków rozszerzających oskrzela
• Długo działające agonisty receptora β2
–– Tachykardia
–– Drżenie drobnofaliste
–– Ból głowy
–– Skurcze mięśniowe
–– Wydłużenie odstępu QT
–– Hipokaliemia
–– Uczucie niepokoju
• Długo działające leki antycholinergiczne
–– Suchość w jamie ustnej
–– Nudności
–– Zaparcie
–– Ból głowy
–– Tachykardia
–– Jaskra z wąskim kątem przesączania
–– Zaburzenia odpływu moczu
Długo działające leki antycholinergiczne
Ograniczenie przepływu powietrza w POChP ma etiologię
wieloczynnikową i częściowo zależną od potencjalnie odwracalnego dużego napięcia cholinergicznego. Co więcej,
mechanizmy, w których uczestniczy nerw błędny, przejawiają się zwiększonym wydzielaniem gruczołów podśluzówkowych u chorych na POChP. Wiedza ta doprowadziła
do stworzenia długo działających leków antycholinergicznych podawanych raz dziennie (tiotropium).
Istnieją trzy główne podtypy receptorów muskarynowych (M1, M 2 i M3). Pobudzenie zarówno receptorów
M1, jak i M3 prowadzi do skurczu oskrzeli, receptor M 2
zaś przeciwdziała temu mechanizmowi. W przeciwieństwie do ipratropium, tiotropium szybko odłącza się od
receptora M2 (minimalizuje więc utratę jakichkolwiek domniemanych korzyści) i wolno odłącza się od receptora
M3. To zaś powoduje zmniejszenie początkowego napięcia
mięśniówki oskrzeli, rozluźnienie mięśni gładkich i rozszerzenie oskrzeli przez dłuższy okres. Jest to jedyny dopuszczony długo działający lek antycholinergiczny; może
być podawany przez inhalator suchego proszku aktywowany oddechem (Handihaler) lub inhalator miękkiej mgły
(Respimat).
Wiele badań u chorych na POChP wykazało, że tiotropium jest skuteczniejsze niż placebo lub ipratropium
pod względem wpływu na czynność płuc, objawy, jakość
życia i zaostrzenia. W metaanalizie dziewięciu badań tio-
ABC POChP
FEV1 (l)
36
1,80
Tiotropium
Grupa kontrolna
*
*
*
*
1,60
*
*
*
1,40
*
*
*
*
*
*
*
*
*
*
*
1,20
FEV1 po podaniu
leku
rozszerzającego
oskrzela
FEV1 przed
podaniem
leku
rozszerzającego
oskrzela
0
FVC (l)
(a)
3,50
*
*
3,25
*
*
*
*
3,00
*
*
*
FVC po podaniu
leku
rozszerzającego
oskrzela
*
*
FVC przed
podaniem
leku
rozszerzającego
oskrzela
2,75
0
01
6
12
18
24
30
36
48
Miesiąc
30. dzień
(b)
tropium było związane z redukcją zaostrzeń i częstości
przyjęć do szpitala w porównaniu z placebo i ipratropium.
W tej samej analizie wykazano, że tiotropium było znacząco lepsze w poprawie czynności płuc w porównaniu
z długo działającymi agonistami β2. W badaniu przeprowadzonym przez Tashkina i wsp. (2008) zbadano w okresie 4 lat wpływ dodawania tiotropium do innych leków
u prawie 6000 pacjentów z FEV1 <70% wartości należnej.
Tiotropium w porównaniu z placebo powodowało poprawę czynności płuc i jakości życia zależnej od zdrowia,
zmniejszenie śmiertelności i częstości zaostrzeń, chociaż
nie zmniejszało ogólnej szybkości spadku FEV1. W badaniu podgrup wykazano jednak, że u chorych z mniej
zaawansowaną postacią choroby (średnia FEV1 wynosiła
59% wartości należnej) tiotropium zmniejszało szybkość
pogarszania się czynności płuc (rycina 7.2). Mechanizm,
dzięki któremu tiotropium zmniejsza częstość zaostrzeń,
nie jest jasny, może być jednak związany z utrzymującym
się rozszerzeniem oskrzeli, zapobiegającym pogorszeniu
się czynności płuc w okresach infekcji.
Długo działające agonisty β2
42
Długo działające agonisty β2 wpływają bezpośrednio na
receptory adrenergiczne β2, wywołując zmniejszenie napięcia mięśni gładkich i rozszerzenie oskrzeli. Dwa najczęściej stosowane leki – formoterol i salmeterol – podaje się 2
razy dziennie. W przeciwieństwie do krótko działających
Rycina 7.2 Wpływ dodania tiotropium na średnią natężoną objętość
wydechową pierwszosekundową
(FEV1) (a) oraz natężoną pojemność
życiową (FVC) (b) przed podaniem leku rozszerzającego oskrzela i po jego
podaniu u pacjentów z mniej zaawansowaną postacią przewlekłej obturacyjnej choroby płuc (POChP). Przedruk za zgodą z: Decramer M, Celli B,
Kesten S, Lystig T, Mehra S, Tashkin DP.
Effect of tiotropium on outcomes in
patients with moderate chronic obstructive pulmonary disease (UPLIFT):
a prespecified subgroup analysis of
a randomised controlled trial. Lancet
2009; 374: 1171–1178
agonistów β2, zarówno salmeterol, jak i formoterol mają
względnie lipofilowy charakter (są rozpuszczalne w tłuszczach) i przez dłuższy czas pozostają związane z receptorem. Te czynniki mogą częściowo tłumaczyć dłuższy czas
ich działania. Badania in vitro wykazały, że formoterol
w większym stopniu niż salmeterol obniża napięcie mięśni gładkich.
Systematyczny przegląd piśmiennictwa Cochrane’a wykazał na podstawie 23 badań oceniających wpływ długo
działających agonistów β2, że salmeterol prowadzi do niewielkiej poprawy czynności płuc i wyraźnego zmniejszenia
częstości zaostrzeń, chociaż obserwowano różny wpływ na
inne wyniki końcowe, takie jak zależna od zdrowia jakość
życia lub ustępowanie dolegliwości.
Połączenia długo działającego leku
antycholinergicznego oraz długo działającego
agonisty β2
Kilka badań oceniło wpływ łącznego stosowania długo
działającego leku antycholinergicznego oraz długo działającego agonisty β2 (formoterolu i salmeterolu). W jednym
z nich stosowanie tiotropium wraz z formoterolem prowadziło do większej poprawy czynności płuc niż w przypadku stosowania tych leków pojedynczo. W innym badaniu
dodanie tiotropium do salmeterolu nie poprawiało czynności płuc, częstości zaostrzeń i hospitalizacji.
Kortykosteroidy
podawane wziewnie
Do powszechnie przepisywanych kortykosteroidów podawanych wziewnie można zaliczyć dipropionian beklometazonu, budezonid oraz propionian flutykazonu. Należy
zwrócić uwagę, że w przeszłości u wielu chorych na POChP
– nawet tych, którzy mieli minimalne objawy oraz łagodne ograniczenie przepływu powietrza – stosowano wziewne kortykosteroidy w monoterapii. Działo się tak mimo
względnego braku działania kortykosteroidów na neutrofilowe mechanizmy zapalenia oraz szczupłości dowodów
wykazujących istotne korzyści krótko- i długoterminowe.
W przeszłości lekarze praktycy nieprawidłowo rozciągali
korzystne działanie leczenia przeciwzapalnego w astmie na
POChP, problemem był także brak alternatywnych strategii leczenia farmakologicznego. Rzeczywiście, dokładna
rola kortykosteroidów podawanych wziewnie w leczeniu
POChP była kwestią sporną w ostatnich dekadach, a wiele
dużych badań wieloośrodkowych oraz metaanaliz próbowało wyjaśnić wątpliwości.
Z dość dużą pewnością ustalono, że kortykosteroidy podawane wziewnie w monoterapii nie wywierają istotnego
wpływu na zmniejszenie szybkości spadku FEV1 (rycina 7.3) ani na śmiertelność. W dużym badaniu Burge i wsp.
(2000) wykazali, że podawanie 1000 μg/dobę flutykazonu
prowadziło do zmniejszania zaostrzeń o 25%, a największe
korzyści obserwowano w grupie pacjentów, u których średnia wartość FEV1 wynosiła <50% wartości należnej. W innych badaniach nie wykazano jednoznacznego wpływu na
wtórne punkty końcowe leczenia, a poprawa jakości życia
i zmniejszenie nasilenia objawów były niewielkie lub nie
występowały w ogóle. W metaanalizie Cochrane’a z 2007 r.,
oceniającej ponad 13 000 pacjentów, długotrwała terapia
kortykosteroidami podawanymi wziewnie nie zmniejszała spadku FEV1 i nie wywierała żadnego korzystnego
wpływu na zmniejszenie śmiertelności. Leczenie tymi
środkami było jednak związane ze zmniejszeniem średniej liczby zaostrzeń w roku oraz szybkości pogarszania
się jakości życia. Dawkowanie kortykosteroidów wziewnych konieczne do osiągnięcia maksymalnie korzystnego
działania przy minimalnych działaniach niepożądanych
(optymalny indeks terapeutyczny) nie zostało ustalone
w sposób jednoznaczny. Obecnie posiadane dowody sugerują, że kortykosteroidy podawane wziewnie powinny
być przepisywane chorym z FEV1 <50% wartości należnej,
u których występują częste (>2 rocznie) zaostrzenia.
Średnia zmiana wartości wyjściowej FEV1 (l)
Farmakoterapia (I) – leki wziewne
37
0
–0,05
–0,10
–0,15
–0,20
Budezonid
Placebo
–0,25
0
3
6
9
12
15 19
21
24 27 30 33 36
Czas (miesiące)
Rycina 7.3 Nie wykazano, aby kortykosteroidy podawane wziewnie wpływały na szybkość pogarszania się czynności płuc u pacjentów z przewlekłą obturacyjną chorobą płuc (POChP). W badaniu tym podczas 36-miesięcznej obserwacji nie wykazano różnic
w średniej zmianie wartości wyjściowej natężonej objętości wydechowej pierwszosekundowej (FEV1) w grupie placebo i grupie
leczonej budezonidem. Przedruk za zgodą z: Vestbo et al. Lancet
1999; 353: 1819–1823
Rycina 7.4 Kandydoza jamy ustnej i gardła u pacjenta z przewlekłą obturacyjną chorobą płuc (POChP) stosującego duże dawki
kortykosteroidów wziewnie
Działania niepożądane kortykosteroidów
podawanych wziewnie
Kortykosteroidy podawane wziewnie wywołują działania
niepożądane zarówno miejscowe, jak i ogólnoustrojowe.
Typowe miejscowe działania niepożądane to kandydoza
jamy ustnej i gardła (rycina 7.4) oraz dysfonia. W poprzednich badaniach wykazano, że u pacjentów stosujących
kortykosteroidy wziewnie częściej występują podbiegnięcia krwawe (rycina 7.5), obserwowano także zmniejszenie
stopnia zmineralizowania kości oraz hamowanie osi podwzgórze–przysadka–nadercza. Co więcej, badanie TORCH
Rycina 7.5 Rozległe podbiegnięcia krwawe u pacjenta otrzymującego kortykosteroidy wziewnie
prowadzone przez Calverleya i wsp. (2007) wykazało, że
u pacjentów stosujących kortykosteroidy wziewnie, zarówno w monoterapii, jak i w połączeniu z długo działającymi agonistami β2, występuje zwiększone ryzyko zapalenia
płuc.
ABC POChP
Łączne stosowanie kortykosteroidów
podawanych wziewnie i długo
działających agonistów β2
Większość badań oceniających długo działające agonisty β2
oraz kortykosteroidy podawane wziewnie wykazała wyższość łącznego podawania obu leków w porównaniu ze stosowaniem jednego z nich. Dla przykładu w największym
badaniu oceniającym flutykazon i salmeterol (TORCH) ich
łączne podawanie okazało się w okresie 3 lat obserwacji
lepsze niż stosowanie tych leków w monoterapii w zakresie
przeżywalności, FEV1, częstotliwości zaostrzeń oraz jakości życia. W badaniach oceniających łączne podawanie budezonidu i formoterolu redukcja częstotliwości zaostrzeń
(25%) w porównaniu z placebo była podobna jak w badaniu
TORCH. W większości badań oceniających łączne stosowanie długo działających agonistów β2 i kortykosteroidów
podawanych wziewnie średnia FEV1wynosiła <50% wartości należnej. W badaniu przeprowadzonym przez Wedzichę
i wsp. (2008) łączne stosowanie flutykazonu i salmeterolu
zostało porównane z tiotropium. Częstotliwość występowania zaostrzeń w obu grupach była podobna, jakkolwiek
w grupie, w której stosowano dwa leki, częstość zapalenia
płuc była większa, a śmiertelność – mniejsza. W Wielkiej
Brytanii dopuszczone jest łączne podawanie kortykosteroidów oraz długo działających agonistów β2 przy użyciu
inhalatora u chorych z FEV1 <60% wartości należnej i przy
liczbie zaostrzeń >2 rocznie.
Terapia potrójna
Wielu pacjentom z zaawansowaną POChP przepisywane
są łącznie długo działający lek antycholinergiczny, długo działający agonista β2 oraz kortykosteroid podawane
wziewne. Nie dokonano pełnej oceny takiego potrójnego
połączenia leków. W badaniach przeprowadzonych przez
Tashkina i wsp. (2008) oraz Welte i wsp. (2009) dodanie
tiotropium do flutykazonu i salmeterolu w jednym z badań
zmniejszało zaostrzenia, w drugim zaś nie. Jednak w kolejnym badaniu dodanie tiotropium do formoterolu oraz
budezonidu w porównaniu ze stosowaniem samego tiotropium zapewniło większą poprawę czynności płuc i stanu
ogólnego zdrowia oraz zmniejszenie nasilenia objawów
i ciężkości zaostrzeń. Wydaje się uzasadnione, aby te trzy
Zaostrzenia/pacjenta
38
0,4
P<0,001
0,3
0,2
0,1
0,0
0
15
30
45
60
75
90
Dni od randomizacji
Rycina 7.6 Średnia liczba ciężkich zaostrzeń przypadających na
jednego pacjenta w zależności od czasu u chorych leczonych tiotropium oraz placebo (liliowe kwadraty) w porównaniu z grupą
leczoną tiotropium w połączeniu z budezonidem/formoterolem
(niebieskie kółka). Przedruk za zgodą z: Welte T, Miravitlles M, Hernandez P et al. Efficacy and tolerability of budesonide/formoterol
added to tiotropium in COPD patients. American Journal of Respiratory and Critical Care in Medicine 2009; 180: 741–750 (autorzy
dziękują firmie AstraZeneca za pokrycie kosztów praw autorskich
umożliwiających reprodukcję tej ryciny)
Algorytm stosowania terapii wziewnej
Duszność lub
ograniczenie
wysiłku
Krótko działający agonista receptorów β lub krótko działający antagonista receptorów muskarynowych, o ile to wskazane*
Natężona objętość wydechowa
pierwszosekundowa (FEV1) ≥50%
Zaostrzenia lub
utrzymująca się
duszność
Długo działający agonista
receptorów β
Utrzymujące się
zaostrzenia
lub duszność
Natężona objętość wydechowa
pierwszosekundowa (FEV1) <50%
Długo działający antagonista
receptorów muskarynowych
Odstawić SAMA
Długo działający agonista
receptorów β wraz z kortykosteroidem
podawane wziewnie przez inhalator
Długo działający antagonista
receptorów muskarynowych
Odstawić SAMA
Zaproponować LAMA zamiast
regularnego stosowania
SAMA 4 razy dziennie
Rozważyć LABA wraz z
LAMA, jeśli skuteczność ICS
zmniejszyła się lub jest źle tolerowany
Zaproponować LAMA
zamiast regularnego stosowania
SAMA 4 razy dziennie
Długo działający agonista receptorów β oraz
kortykosteroid podawane wziewnie w inhalatorze
Rozważyć LABA plus LAMA, jeśli skuteczność ICS
zmniejszyła się lub lek ten jest źle tolerowany
Długo działający antagonista receptorów muskarynowych
wraz z długo działającym agonistą receptorów β oraz
kortykosteroidem podawane wziewnie przez jeden inhalator
Skróty: SAMA = krótko działający antagonista receptorów muskarynowych, LAMA = długo działający antagonista receptorów muskarynowych, LABA = długo działający agonista receptorów β
ICS = kortykosteroid podawany wziewnie
Zaproponować terapię (silne dowody skuteczności)
Rozważyć terapię (dowody skuteczności słabsze)
Rycina 7.7 Diagram przedstawiający algorytm farmakoterapii lekami podawanymi wziewnie u pacjentów z przewlekłą obturacyjną
chorobą płuc (POChP). FEV1, natężona objętość wydechowa pierwszosekundowa. Przedruk za zgodą z: O’Reilly J, Jones MM, Parnham J,
Lovibond K, Rudolf M. Management of stable chronic obstructive pulmonary disease in primary and secondary care: summary of updated NICE guidance. BMJ 2010; 340:c3134
Farmakoterapia (I) – leki wziewne
grupy leków stosować u tych pacjentów z zaawansowaną
obturacją oskrzeli, u których występują nawracające zaostrzenia i utrzymują się objawy. Może też jednak występować „efekt sufitowy” w zakresie zaostrzeń, a działanie
addytywne poszczególnych leków może być mniejsze niż
oczekiwane.
Podsumowanie leczenia wziewnego
Ponieważ ograniczenie przepływu powietrza jest uniwersalną cechą klinicznie istotnej POChP, leki rozszerzające
oskrzela odgrywają integralną rolę na wszystkich etapach
choroby. U wszystkich pacjentów z objawową postacią
POChP należy stosować wziewnie krótko działające leki
rozszerzające oskrzela na żądanie.
U pacjentów z utrzymującymi się objawami i zaostrzeniami uaktualnione wytyczne NICE sugerują, że należy
regularnie podawać leki stosowane wziewnie (same lub
w połączeniach), zależnie od odsetka wartości należnej
FEV1 (rycina 7.7).
Jeśli FEV1 wynosi ≥50% wartości należnej, możliwe jest
podawanie raz dziennie długo działającego leku antycholinergicznego lub 2 razy dziennie długo działającego agonisty β2. Jeśli objawy i zaostrzenia się utrzymują, możliwe
jest stosowanie zarówno długo działającego leku antycholinergicznego wraz z długo działającym agonistą β2, jak
i długo działającego agonisty β2 wraz z kortykosteroidem
podawanym wziewnie. Dowody na to drugie podejście są
słabe, a przepisanie inhalatorów zawierających oba leki
(długo działającego agonistę β2 i kortykosteroid) musi być
zgodne z obowiązującymi zasadami rejestracji.
Jeśli FEV1 wynosi <50% wartości należnej, w leczeniu
można stosować lek antycholinergiczny w monoterapii
raz dziennie lub długo działającego agonistę β2 plus kortykosteroid wziewnie (oba leki podawane w jednym inhalatorze). Jeśli objawy i zaostrzenia się utrzymują, należy
rozważyć wszystkie trzy grupy leków. Na wszystkich etapach choroby przy stosowaniu kortykosteroidów wziewnie
pacjenci powinni mieć świadomość potencjalnego ryzyka
rozwoju działań niepożądanych (włącznie z zapaleniem
płuc).
Zalecane piśmiennictwo
Aaron SD, Vandemheen KL, Fergusson D et al. Tiotropium in combination with placebo, salmeterol, or fluticasone–salmeterol for treatment
of chronic obstructive pulmonary disease: a randomized trial. Annals of
Internal Medicine 2007; 146: 545–555.
Appleton S, Poole P, Smith B, Veale A, Lasserson TJ, Chan MM.
Long-acting β2-agonists for chronic obstructive pulmonary disease patients with poorly reversible airflow limitation. The Cochrane Database
of Systematic Reviews 2006 July 19; 3: CD001104.
Barr RG, Bourbeau J, Camargo CA, Ram FS. Tiotropium for stable
chronic obstructive pulmonary disease: a meta-analysis. Thorax 2006;
61: 854–862.
Calverley PM, Boonsawat W, Cseke Z, Zhong N, Peterson S, Olsson
H. Maintenance therapy with budesonide and formoterol in chronic
obstructive pulmonary disease. European Respiratory Journal 2003; 22:
912–919.
Celli B, Decramer M, Kesten S, Liu D, Mehra S, Tashkin DP. Mortality in the 4 year trial of tiotropium (UPLIFT) in patients with COPD.
39
American Journal of Respiratory and Critical Care Medicine 2009; 180:
948–955.
Decramer M, Celli B, Kesten S, Lystig T, Mehra S, Tashkin DP. Effect
of tiotropium on outcomes in patients with moderate chronic obstructive pulmonary disease (UPLIFT): a prespecified subgroup analysis of
a randomised controlled trial. Lancet 2009; 374: 1171–1178.
Sin DD, Tashkin D, Zhang X et al. Budesonide and the risk of pneumonia: a meta-analysis of individual patient data. Lancet 2009; 374:
712–719.
Szafranski W, Cukier A, Ramirez A et al. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary
disease. European Respiratory Journal 2003; 21: 74–81.
van Noord JA, Aumann JL, Janssens E et al. Comparison of tiotropium once daily, formoterol twice daily and both combined once daily
in patients with COPD. European Respiratory Journal 2005; 26: 214–222.
Yang IA, Fong KM, Sim EH, Black PN, Lasserson TJ. Inhaled corticosteroids for stable chronic obstructive pulmonary disease. The Cochrane
Database of Systematic Reviews 2007 April 19; (2): CD002991.
Piśmiennictwo
Burge PS, Calverley PMA, Jones PW, Spencer S, Anderson JA, Maslem TK. Randomised, double blind, placebo controlled study of fluticasone propionate in patients with moderate to severe chronic obstructive
pulmonary disease: the ISOLDE trial. BMJ 2000; 320: 1297–1303.
Calverley PMA, Anderson JA, Celli B et al. and the TORCH investigators. Salmeterol and fluticasone propionate and survival in chronic
obstructive pulmonary disease. New England Journal of Medicine 2007;
356: 775–789.
Tashkin DP, Celli B, Senn S et al. A 4-year trial of tiotropium in
chronic obstructive pulmonary disease. New England Journal of Medicine 2008; 359: 1543–1554.
Wędzicha JW, Calverley PMA, Seemungal TA, Hagan G, Ansari Z,
Stockley RA for the INSPIRE investigators. The prevention of chronic
obstructive pulmonary disease exacerbations by salmeterol/fluticasone
propionate or tiotropium bromide. American Journal of Respiratory and
Critical Care Medicine 2008; 177: 19–26.
Welte T, Miravitlles M, Hernandez P et al. Efficacy and tolerability of
budesonide/formoterol added to tiotropium in COPD patients. American
Journal of Respiratory and Critical Care Medicine 2009; 180: 741–750.









