1
•Elektron na najniższej orbicie w atomie wodoru posiada
energię -13.6eV.
•Kolejnym orbitom przypisane są główne liczby kwantowe n.
•Orbitalna liczba kwantowa l opisuje kształt orbity.
•Magnetyczna liczba kwantowa m opisuje orientację
przestrzenną orbity.
•Wewnętrzny moment pędu (ruch wirowy) elektronu opisuje
liczba spinowa s.
•Liczby l, m i s przyczyniają się do rozszczepienia poziomów
energetycznych określonych przez główną liczbę kwantową
(każdemu zestawowi liczb n, l, m i s odpowiada inna
energia).
2
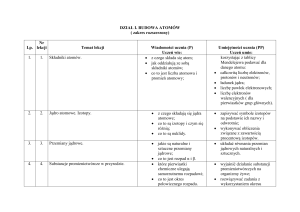
Stan elektronu w atomie jest określony przez cztery
liczby kwantowe: główną (n), orbitalną (l),
magnetyczną (m) oraz spinową (s).
Zakaz Pauliego (zasada Pauliego): W atomie nie
mogą istnieć dwa elektrony o identycznych
wszystkich liczbach kwantowych (tylko jeden
elektron może przebywać w danym stanie
kwantowym).
Wolfgang Pauli (1900-1958)
Nagroda Nobla z fizyki 1945
Ogólna postać zakazu Pauliego: Dwa fermiony (cząstki o spinie
połówkowym: 1/2,3/2, itd.) nie mogą przebywać w jednym stanie
kwantowym.
3
Powłoka
Podpowłoka
Ilość elektronów
na wypełnionej
podpowłoce
Ilość elektronów
na wypełnionej
powłoce
Elektrony wypełniają podpowłoki zaczynając od tych o
najniższej energii.
4
konfiguracja energia jonizacji [eV]
konfiguracja energia jonizacji [eV]
5
6
Fermiony – cząstki o spinie połówkowym. Przykłady fermionów:
elektron, proton, neutron. Podlegają zakazowi Pauliego (tylko
jeden fermion na jednym poziomie energetycznym).
Bozony – cząstki o spinie całkowitym. Przykłady bozonów:
foton, mezon. Nie podlegają zakazowi Pauliego (wiele bozonów
może przebywać na tym samym poziomie energetycznym).
7
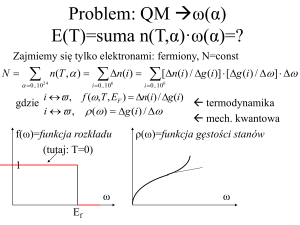
f
Rozkład Fermiego Diraca
określa prawdopodobieństwo
obsadzenia poziomów
energetycznych przez elektrony
(fermiony).
Ef – energia Fermiego:
maksymalna energia elektronów
w temperaturze 0K (zera
bezwzględnego).
E-Ef
E Ef
f exp
k BT
8
Energia
Fermiego
Fermiony
Bozony
9
Widmo promieniowania molibdenu
K, K - promieniowanie charakterystyczne
Promieniowanie charakterystyczne
powstaje w wyniku wybicia elektronu z
głębokich poziomów energetycznych, a
następnie powrotu elektronu na poziom
niższy.
Przejście LK linia K
Przejście MK linia K
Promieniowanie charakterystyczne X
(rentgenowskie) – promieniowanie
elektromagnetyczne o długości fali 10pm10nm. Występuje w przypadku ciężkich
pierwiastków (np. Cu, Mo).
10
11
Atom w stanie
podstawowym
Atom w stanie
wzbudzonym
Absorpcja fotonu
Atom w stanie
wzbudzonym
Atom w stanie
podstawowym
Emisja spontaniczna
12
Atom w stanie
wzbudzonym
Atom w stanie
podstawowym
stan metastabilny
energia
wyjściowa
Emisja wymuszona
Foton o energii E zwiększa
prawdopodobieństwo powrotu
wzbudzonego atomu do stanu
podstawowego.
Foton emitowany ma taką samą fazę jak
foton padający – powstaje wiązaka
światła spójnego.
energia
wejściowa
Inwersja obsadzeń – więcej elektronów
jest w stanie wzbudz.onym niż w stanie
podstawowym
13
Emisja wymuszona- laser
Emisja spontaniczna fotonów
w różnych kierunkach
światło
spójne
zwierciadło
Fotony
powstałe w
trakcie emisji
wymuszonej
Zwierciadło
półprzepuszczalne
energia
wejściowa
14
Lama wyładowcza – lampa która świeci dzięki wyładowaniu elektrycznemu
przechodzącemu przez zjonizowany gaz (najczęściej gaz szlachetny).
Lampa wyładowcza emituje fotony powstające przy przejścia elektronów ze
stanów o wyższych energiach do stanów o energiach niższych.
lampa wodorowa
lampa kryptonowa
15