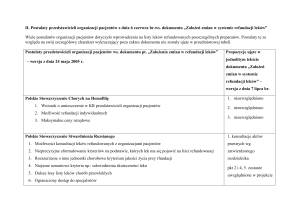
Postulaty Organizacji Branżowych (zwanych dalej OB), zgłaszane podczas konsultacji
projektu założeń do projektu ustawy o zmianie ustawy „O refundacji leków […]”
w zestawieniu ze zmianami wprowadzonymi do projektu nowelizacji ww. ustawy z dnia 18
września 2013 r.
POSTULATY ZGŁASZANE PODCZAS KONSULTACJI PROJEKTU ZAŁOŻEŃ ORAZ
ZAŁOŻEŃ DO PROJEKTU NOWELIZACJI USTAWY O ZMIANIE USTAWY O
REFUNDACJI - UWZGLĘDNIONE:
1. Umożliwienie uczestnictwa w konsultacjach na etapie opiniowania projektu
nowelizacji.
2. Uznanie maksymalnego charakteru cen dla leków szpitalnych.
3. Przyjęcie zasady odrębnego określenia warunków refundacji dla poszczególnych
leków w programie lekowym.
4. Rezygnacja z wprowadzenia planowanej w założeniach zasady gwarancji liniowości
cen różnych mocy tego samego leku.
POSTULATY, ZGŁASZANE PODCZAS KONSULTACJI PROJEKTU ZAŁOŻEŃ ORAZ
ZAŁOŻEŃ DO PROJEKTU NOWELIZACJI USTAWY O ZMIANIE USTAWY
O REFUNDACJI – CZĘŚCIOWO UWZGLĘDNIONE:
1. Wprowadzono procedurę zmiany decyzji refundacyjnej.
Nie uwzględniono:
- postulatu OB wyłączenia z trybu zmiany decyzji wprowadzania dodatkowych
wskazań dla leku już refundowanego (szczególnie dla leków szpitalnych).
2. Przepisy regulujące eksport leków.
Nie uwzględniono:
– wprowadzenia nakazu sprzedaży na terenie Polski leku, w stosunku do którego GIF
wydał zakaz wywozu;
- braku przepisów „dyscyplinujących” apteki;
- niewłaściwego sformułowania obowiązku dostaw w ilościach zaspakajających
potrzeby pacjentów
3. Jednoznacznie wskazano obowiązek pisemnego sporządzania przez Komisję
Ekonomiczną stanowisk wraz z uzasadnieniem.
Nie uwzględniono:
- postulatu w zakresie wyeliminowania możliwości zmiany przez całą Komisję
postanowień przyjętych przez Komisję w pięcioosobowym składzie, w jakim
podpisany został wynik negocjacji.
POSTULATY, ZGŁASZANE PODCZAS KONSULTACJI PROJEKTU ZAŁOŻEŃ ORAZ
ZAŁOŻEŃ DO PROJEKTU NOWELIZACJI USTAWY O ZMIANIE UWTSAWY O
REFUNDACJI – NIEUWZGLĘDNIONE:
1. Art. 2 pkt 6 - Nie uwzględniono przepisów o stosowaniu ceny zbytu przez
wnioskodawcę
Przepis ten – popierany przez OB - znajdował się w założeniach ale nie znalazł się w
samym projekcie nowelizacji. Nie usunięto także wątpliwości co do tego, do jakich
transakcji stosuje sie przepisy o obligatoryjnych marżach hurtowych, a w
szczególności nie potwierdzono, że ograniczenia marżowe nie mają zastosowania do
transakcji wewnątrz grupy kapitałowej.
2. Art. 2 pkt 27 - Nie poszerzono definicji "wnioskodawcy" tak, aby podmiot obracający
lekiem w ramach grupy kapitałowej nie będący ani podmiotem odpowiedzialnym, ani
jego przedstawicielem, mógł mieć status wnioskodawcy.
3. Art. 15 - Nie uwzględniono przepisów o metodologii obliczania limitu z
uwzględnieniem danych rynkowych i poziomu sprzed trzech miesięcy.
Przepisy te – popierane przez OB - znajdowały się w założeniach ale nie znalazły się
w samym projekcie nowelizacji.
4. Mimo uznania maksymalnego charakteru cen leków szpitalnych nie wprowadzono
konsekwentnej zmiany w art. 15 - wyłączenia z grupowania terapeutycznego i
określania limitu leków stosowanych w programach lekowych i chemioterapii .
5. Zachowano krytykowaną przez OB zmianę definicji odpowiednika, polegającą na
usunięciu z dotychczasowej definicji przesłanki tożsamości wskazań. Nie wyłączono
też z zakresu pojęcia odpowiednika, leków biopodobnych. Ponadto Negatywnie
należy ocenić wykreślenie z art. 44 o substytucji aptecznej, obowiązku uwzględniania
przez osobę wydającą lek, tożsamości wskazań rejestracyjnych leku z recepty i
zamiennika. To oznacza, że w świetle ustawy refundacyjnej odpowiednikami będą
produkty, które zgodnie z zarejestrowanymi wskazaniami, nie powinny być stosowane
zamiennie. Dodatkowe zmiany jak brak możliwości zamiany leku tańszego na droższy
oraz substytucja na leki dostępne ze 100 % odpłatnością powoduje, iż wnioskujemy o
ponowna analizę art. 44 z uwzględnieniem uwag przedstawionych w ramach
uzgodnień społecznych do projektu nowelizacji
6. Art. 31 a i 31 b – zachowano krytykowane przez OB powoływanie zespołów
koordynacyjnych do programów lekowych.
7. Art. 15 - Nie uwzględniono postulowanego przez OB kryterium „tożsamość wskazań
lub przeznaczeń” kwalifikacji leków do grupy limitowej – przeciwnie - wprowadzono
kryterium „podobieństwa wskazań lub przeznaczeń”
8. Nie wprowadzono rozwiązania pozwalającego na zastosowanie trybu zbliżonego do
aktualnie działającej chemioterapii niestandardowej dla leków zarejestrowanych
po 1 stycznia 2012 r.
9. Nie zmieniono obowiązku Prezesa NFZ (opisanego w art. 102 ust. 5 Ustawy o
świadczeniach opieki zdrowotnej finansowanych ze środków publicznych) co do
publikacji danych o wielkości kwoty refundacji i liczbie zrefundowanych opakowań.
Wprowadzono natomiast dodatkowy obowiązek publikacji danych z uwzględnieniem
liczby pacjentów.
2
10. Nie wprowadzono proponowanego przez OB rozwiązania, którego celem jest
ponowne wprowadzenie do systemu refundacji środków uzyskanych przez NFZ od
Wnioskodawców w związku z realizacją instrumentów dzielenia ryzyka.
11. Nie wprowadzono szczegółowych regulacji dotyczących wysokości progu kosztu
uzyskania QALY dla terapii onkologicznych i stosowanych w chorobach rzadkich.
12. Nie doprecyzowano przepisów dotyczących wzajemnej relacji cenowej tego samego
leku przed i po wygaśnięciu tzw. wyłączności rynkowej.
13. Nie uwzględniono postulatów Izby Gospodarczej „FARMACJA POLSKA” w
zakresie utrzymania marży hurtowej na poziomie obowiązującym w 2013 r.
14. Nie zrealizowano zapowiadanego w projekcie założeń i postulowanego przez Izbę
Gospodarczą „FARMACJA POLSKA” zdefiniowania reklamy działalności aptek
NOWE ZAPISY PROJEKTU, KTÓRE NIE ZNALAZŁY SIĘ W ZAŁOŻENIACH, A
KTÓRE MAJĄ NEGATYWNY WPŁYW NA BRANŻĘ
1. Ograniczenie możliwości negocjacji z Komisją Ekonomiczną.
Art. 19 reguluje zasady negocjacji z Komisją Ekonomiczną. Projekt wprowadza
podział na część negocjacji z Zespołem i ustalenia Komisji w pełnym składzie. Mimo
zgodności protokołu z negocjacji z Zespołem, Komisja może zarządzić ponowne
negocjacje (tylko jednokrotnie). Takie ograniczenie wpływa negatywnie na
przewidywalność rozstrzygnięć refundacyjno-cenowych (wynik negocjacji z
Zespołem nie jest dla całej Komisji wiążący), ponadto wnioskodawca wyłączony jest z
etapu procesu, toczącego się przed Komisją. Za sprzeczny z KPA należy uznać brak
możliwości negocjacji w przypadku złożenia wniosku o ponowne rozpatrzenie
sprawy, o którym mowa w projektowanym artykule 19 ust. 9.
Postulujemy - przy założeniu dwuetapowości systemu negocjacji (zespół oraz
Komisja) nieograniczanie ilości rund negocjacyjnych. Proponujemy także
dopuszczenie możliwości negocjowania warunków refundacji w przypadku złożenia
wniosku o ponowne rozpatrzenie sprawy, o którym mowa w projektowanym artykule
19 ust. 9.
2. Ryzyko naruszenia poufności instrumentów dzielenia ryzyka.
Art. 102 ust. 5 pkt 31 i 31a Ustawy o świadczeniach opieki zdrowotnej finansowanych
ze środków publicznych dotyczy sposobu publikacji informacji o wysokości kwoty
refundacji i ilości zrefundowanych opakowań wg kodów EAN. Z regulacji nie
usunięto pkt. 31 (aktualny sposób publikacji pozostaje obowiązujący, a co za tym idzie
naruszona jest tajemnica RSS), a jedynie dodano nowy obowiązek publikacji przez
Prezesa NFZ informacji o wielkości refundacji i liczbie pacjentów (wg EAN).
Proponowane brzmienie nie zapewnia więc realizacji postulatu o zachowaniu
tajemnicy handlowej.
Postulujemy deklarowane na etapie projektu założeń doprecyzowanie przepisów w
sposób pozwalający na zachowanie zasad tajemnicy handlowej.
3
3. Wprowadzenie obowiązku opłat w postępowaniach wszczynanych w odpowiedzi na
wezwanie Ministra Zdrowia.
Nowelizowana ustawa przewiduje możliwość wezwania wnioskodawcy przez
Ministra do złożenia wniosku refundacyjnego. Postulujemy zwolnienie wnioskodawcy
z opłat w przypadku wszystkich tych wniosków, które inicjowane są przez stronę
publiczną (np. art. 35a ust 1, czy art. 36a).
Postulujemy zniesienie co do zasady obowiązku opłat za czynności inicjowane przez
instytucje publiczne.
4. Okres obowiązywania decyzji refundacyjnych - doprecyzowania wymagają
rozwiązania art. 11 a, które pozwolą na ujednolicenie okresu obowiązywania różnych
decyzji o refundacji tego samego produktu w różnych wskazaniach.
Materiał przygotowany przez Izbę Gospodarczą „FARMACJA POLSKA” i Związek
Pracodawców Innowacyjnych Firm Farmaceutycznych Infarma przekazany w dniu 4
listopada 2013 r. ministrowi S. Neumannowi.
4