Choroba Glässera
Jak zrozumieć i kontrolować
ten złożony problem?
Dan Tucker PhD MRCVS
Choroba Glässera:
Jak zrozumieć i kontrolować ten złożony problem?
Spis treści
Czym jest choroba Glässera?
1
Jakie są najlepsze sposoby monitorowania
choroby Glässera?
2
Monitorowanie na fermie
2
Postępowanie diagnostyczne
2
Badanie poubojowe: jakie zmiany anatomopatologiczne towarzyszą
chorobie Glässera?
3
Interpretacja skali nasilenia zapalenia błon surowiczych
w badaniu poubojowym 4
Jakie są koszty?
7
Co mogę zrobić?
8
Ograniczanie wpływu choroby poprzez odpowiednie
procedury zarządzania 7
Leczenie
9
Zwalczanie
9
Szczepienia
10
Czy powinienem szczepić?
10
Kiedy szczepienie staje się ekonomicznie opłacalne?
10
Kiedy należy szczepić?
12
Co może zmniejszać skuteczność szczepień?
12
Czynniki zależne od szczepionek
13
Czynniki zależne od zwierząt
13
Podsumowanie 13
n Czym jest choroba Glässera?
Pojawieniu się choroby Glässera (ChG)
towarzyszy nagły wzrost śmiertelności,
sięgający nawet 50% w ciężkich przypadkach. U chorych zwierząt, zwykle
warchlaków i tuczników, będą pojawiać się objawy w postaci podwyższonej ciepłoty wewnętrznej, osowiałości
i niechęci do poruszania aż po skrajne
wyniszczenie oraz drgawki. Choroba
powoduje znaczne straty ekonomiczne
nie tylko na skutek zwiększonej śmiertelności, lecz również z powodu spowolnionych przyrostów u przewlekle
chorych zwierząt.
Choroba Glässera ma postać
posocznicy, powodowanej bakteriami z gatunku Haemophilus parasuis
(HPS). Te mikroorganizmy, zasiedlające
fizjologicznie jamę nosową, w sytuacjach stresowych i/lub upośledzenia
odporności przedostają się do krwiobiegu i ostatecznie powodują zmiany
chorobowe na błonach surowiczych
(wyściełających jamę klatki piersiowej,
jamę brzuszną, opony mózgowe, worek osierdziowy oraz torebki stawowe)
prowadzące do ich silnego i rozległego
uszkodzenia. Mimo iż HPS jest często
jednym z patogenów wywołujących
zapalenie płuc, to ChG powoduje
najwyższą śmiertelność. Wyróżnia się
cztery typowe obrazy choroby:
n
n
systemach odchowu warchlaków
W
choroba może pojawiać się wówczas, gdy prosięta odsadzone
pochodzą z więcej niż jednego
sektora rozrodowego, a każde jest
źródłem zakażenia odmiennymi
szczepami HPS.
n
horoba o ciężkim przebiegu może
C
wystąpić u nowo zakupionych zwierząt hodowlanych o wysokim statusie zdrowotnym wprowadzanych do
obiektów produkcyjnych o niższym
statusie zdrowotnym.
n
większona częstotliwość wystęZ
powania chorób upośledzających
odporność, takich jak PRRS (zespół
rozrodczo-oddechowy świń) oraz
PMWS (poodsadzeniowy wielonarządowy zespół wyniszczający) może
wpływać na wzrost zachorowalności
na ChG, obserwowany w ostatnich
latach przez lekarzy weterynarii –
specjalistów chorób trzody chlewnej.
Naukowcy sugerują ponadto, że HPS
jest nie tylko głównym czynnikiem
etiologicznym ChG, lecz również
ybuchy choroby o najcięższym
W
przebiegu pojawiają się w stadach
o wysokim statusie zdrowotnym,
niemających wcześniej kontaktu
z mikroorganizmem, w których zakażenie pojawia się po raz pierwszy.
1
przyczynia się do rozwoju chorób
układu oddechowego wraz z innymi
drobnoustrojami powodującymi zapalenie płuc, takimi jak Mycoplasma
hyopneumoniae.
n Jakie są najlepsze sposoby
monitorowania choroby
Glässera?
Monitorowanie ChG opiera się zasadniczo na obserwacji objawów klinicznych.
Niemniej jednak powstanie Brytyjskiego
Systemu Nadzoru nad Zdrowiem Trzody
Chlewnej (BPHS, ang. British Pig Health
Scheme) pozwala producentom oraz
lekarzom weterynarii wykrywać trudniej
dostrzegalne objawy choroby już w rzeźniach, przyczyniając się do ujawnienia
chorobotwórczego wpływu zakażeń HPS,
które nie są jeszcze widoczne na fermie
na poziomie klinicznym, lecz już zmniejszają zyskowność produkcji.
Monitorowanie na fermie
Wyróżnia się następujące objawy
kliniczne choroby:
n
n
wielu osobników obserwuje się
U
osowiałość, wzrost ciepłoty wewnętrznej, brak łaknienia oraz
objawy bólowe.
n
zrost śmiertelności. Chore osobniki
W
są w bardzo ciężkim stanie i bez
leczenia szybko padają.
n
2
iek: choroba może rozwijać się
W
u zwierząt w każdym wieku, lecz
zwykle pojawia się po odsadzeniu.
ulawizna powodowana zapaleniem
K
stawów.
n
P rzebarwienia skóry takie jak:
wysypka, zaczerwienienie czy
fioletowe zabarwienie obwodowych
części ciała.
n
bjawy neurologiczne od drgawek
O
mięśniowych po ataki drgawek
poprzedzające zgon.
n
P ostać przewlekła może przejawiać
się słabymi przyrostami oraz kaszlem
obserwowanymi w grupach zwierząt.
Postępowanie diagnostyczne
Rozpoznanie zwykle opiera się na
przeprowadzeniu sekcji padłych osobników oraz laboratoryjnych badań hodowlanych.
W badaniu sekcyjnym obserwuje się
zmiany typowe dla zapalenia błon surowiczych, tj. obecność gęstego, lepkiego
lub ziarnistego kremowego nalotu,
obejmujące jedną lub kilka z poniższych
struktur anatomicznych:
n
płucna: zmiany zapalne błony suroO
wiczej wyściełającej jamę klatki piersiowej powodujące przyleganie płuc
do jej ścian.
n
trzewna: stan zapalny w obrębie
O
jamy brzusznej prowadzący do przywarcia jelit do jej ścian. Anatomiczne
połączenie tej jamy ciała z workiem
mosznowym sprawia, że u knurów
może dochodzić do powiększenia
moszny.
n
Stawy: zmiany zapalne.
n
sierdzie: zmiany zapalnie obejmująO
ce zewnętrzną powierzchnię mięśnia
sercowego oraz worek osierdziowy
n
pony mózgowe: zapalenie opon
O
mózgowych
Jedyną metodą pozwalającą potwierdzić
podejrzenie wybuchu ChG jest wyizolowanie HPS z jednego bądź kilku opisanych
powyżej miejsc objętych zmianami chorobowymi. Szczególnie istotna jest izolacja
bakterii ze struktur innych niż drogi oddechowe, ponieważ wiele niechorobotwórczych szczepów zasiedla jamę nosową zarówno u zdrowych, jak i chorych zwierząt.
Badanie poubojowe: jakie zmiany
anatomopatologiczne towarzyszą
chorobie Glässera?
Badanie poubojowe pozwala uzyskać
niewielkim nakładem finansowym cenne informacje dotyczące występowania
wielu chorób obniżających efektywność produkcji. Wartość tych informacji
dodatkowo podkreśla zakres danych
możliwych do uzyskania tą drogą, obrazujący procesy chorobowe na przestrzeni
czasowej i wskazujący na konieczność
przeprowadzenia dodatkowych bardziej
swoistych badań na fermie. Takie informacje są obecnie gromadzone przez BPHS
i obejmują dane z przeszło 80% objętych
monitoringiem ferm w Anglii oraz Walii
(system Farm Assured) oraz w Szkocji za
pośrednictwem systemu Wholesome Pigs.
W najbliższych latach nowe europejskie
regulacje w zakresie bezpieczeństwa
i higieny żywności stworzą konieczność
wprowadzenia systemu informacji o łańcuchu pokarmowych (ang. Food Chain
Information) umożliwiającego przekazywanie wyników badań poubojowych
z powrotem do producentów.
wskazuje na ChG, natomiast w przypadku
zmian zlokalizowanych na wielu narządach (na przykład zapalenie opłucnej
z towarzyszącym zapaleniem osierdzia)
istnieje już większe prawdopodobieństwo,
że ChG jest pierwotnym procesem chorobowym. Lekarze weterynarii powinni zwracać uwagę na występowanie w badaniu
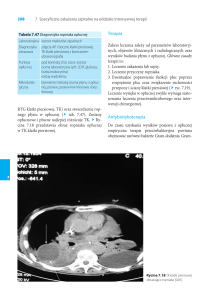
poubojowym następujących zmian anatomopatologicznych (patrz Rycina 1):
n
apalenie opłucnej. Należy mieć
Z
na uwadze fakt, że zapalenie opłucnej przy braku zmian na innych błonach surowiczych może rozwijać się
w przebiegu chorób powodowanych
przez inne patogeny, takie jak Pasteurella, Actinobacillus, Streptococcus,
Bordetella oraz Mycoplasma.
n
Zapalenie osierdzia.
n
Zapalenie otrzewnej.
n
apalenie stawów (nie jest monitoroZ
wane w ramach systemu BPHS).
Rycina 1. F
ragment
żebra
z widocznym zapaleniem
błon surowiczych.
Zapalenie
opłucnej
Zapalenie
osierdzia
Zapalenie błon surowiczych obejmujące
jedną strukturę anatomiczną (przykładowo
wyłącznie zapalenie opłucnej) nie zawsze
3
Rycina 2. Zmiany w postaci: zapalenia opłucnej, osierdzia i otrzewnej
występujące w grupach produkcyjnych świń skierowanych na ubój.
(Dane zgromadzone przez BPHS dla 9445 grup zwierząt pomiędzy lipcem 2005 a czerwcem 2007)
90
Odsetek grup zwierząt
80
zapalenie osierdzia
70
zapalenie opłucnej
60
zapalenie otrzewnej
50
40
30
20
10
0
zero
>0 - 2
>2 - 5
>5 - 10
>10 - 20
>20
Częstotliwość występowania zmian w grupie zwierząt (%)
Występowanie więcej niż jednego z wymienionych powyżej procesów patologicznych określa się jako zapalenie błon
surowiczych, będące złożonym procesem
chorobowych wskazującym na ChG.
Interpretacja skali nasilenia zapalenia błon surowiczych w badaniu
poubojowym
Pojawienie się zapalenia błon surowiczych w grupie produkcyjnej zwierząt powinno skłaniać do wysunięcia
podejrzenia ChG. W ramach BPHS nie
rejestruje się obecnie wszystkich przypadków zapalenia błon surowiczych, lecz
istnieją wyraźne dowody wskazujące, że
w badaniach poubojowych świń w Wielkiej Brytanii zapalenie błon surowiczych
obserwuje się coraz częściej.
Na rycinie 2 przedstawiono łączne dane
zgromadzone przez BPHS obejmujące
4
wszystkie skierowane na ubój zwierzęta
w okresie pierwszych dwóch lat istnienia
programu (lipiec 2005 – czerwiec 2007).
Wykres przedstawia ogólną częstotliwość występowania zapalenia opłucnej,
osierdzia i otrzewnej, natomiast nie
wskazuje, czy wszystkie powyższe zmiany anatomopatologiczne obserwowano
u jednego zwierzęcia. Niemniej jednak
zgromadzone dane wyraźnie sygnalizują
częstotliwość występowania zapalenia
błon surowiczych w populacji trzody
chlewnej w Wielkiej Brytanii. Uwagę
zwraca fakt, że tylko u 18% i 41% partii
nie stwierdzano zmian w postaci zapalenia opłucnej czy zapalenia osierdzia. Co
więcej, w 25% zaobserwowano zapalenie osierdzia przy wskaźniku chorobowości >5% w obrębie grupy. Zapalenie
otrzewnej występowało w 15% grup
przy częstotliwości równej bądź przekra-
Rycina 3. Rozkład sektorów produkcyjnych z uwzględnieniem częstotliwości
jednoczesnego występowania zapalenia opłucnej i osierdzia.
(Dane BPHS50zgromadzone od 1 kwietnia do 30 czerwca 2007)
Odsetek sektorów produkcyjnych
45
40
35
30
25
20
15
10
5
0
zero
>0-2
>2-4
>4-6
>6-8
>8-10 >10-12 >12-14 >14-16 >16-18 >18-20
>20
Częstotliwość występowania zapalenia opłucnej i osierdzia w obrębie sektora produkcyjnego (%)
czającej 2% w obrębie grupy. Raporty
BPHS należy więc analizować pod kątem
zwiększonej częstotliwości występowania
zmian w więcej niż jednej z następujących kategorii: zapalenie opłucnej,
zapalenie osierdzia oraz zapalenie
otrzewnej. W raportach BPHS zapalenie
błon surowiczych oznacza jednoczesne
występowanie zapalenia opłucnej i zapalenia osierdzia, które może również,
poza innymi schorzeniami, wskazywać
na ChG.
Szczegółowa analiza danych pozyskanych z bazy BPHS obejmujących 700
sektorów produkcyjnych, z których
w okresie od 1 kwietnia do 30 czerwca
2007 pochodziło 47 359 świń, lepiej
uwidacznia częstotliwość występowania
zapalenia opłucnej i osierdzia w brytyjskiej populacji trzody chlewnej (patrz:
Rycina 3). Podczas trzymiesięcznego
okresu obserwacji jedynie w 10% sektorów nie stwierdzono żadnych zmian zapalnych na błonach surowiczych, natomiast pojedyncze osobniki z zapaleniem
opłucnej i osierdzia były obecne w 53%
badanych sektorów. W 14% sektorów
częstotliwość występowania zapalenia
opłucnej i osierdzia wynosiła >5%, natomiast w 4% wszystkich sektorów takie
zmiany stwierdzano u co najmniej 10%
zwierząt. Dane przedstawione na rycinie
3 wskazują, że na większości sektorów
produkcyjnych częstotliwość występowania jednocześnie zapalenia opłucnej
i osierdzia nie przekraczała 2%. Na tej
podstawie można więc wnioskować, że
w przypadku częstotliwości pojawiania
się zapalenia opłucnej i osierdzia w obrębie grupy produkcyjnej przekraczającej
2% jej zmniejszenie może pozytywnie
wpłynąć na wyniki produkcyjne. Przy
5
Rycina 4. Rozkład grup produkcyjnych zwierząt skierowanych na ubój
z uwzględnieniem częstotliwości występowania ciężkiego zapalenia opłucnej.
35
(Dane zgromadzone
przez BPHS dla 9445 grup zwierząt pomiędzy lipcem 2005 a czerwcem 2007)
Odsetek grup zwierząt
30
25
20
15
10
5
0
zero
>0-2
>2-5
>5-10
>10-20
>20
Częstotliwość występowania zmian w grupie zwierząt (%)
podejrzeniu ChG producent powinien
wspólnie z lekarzem weterynarii nadzorującym fermę poddać analizie indywidualne dane przekazywane co kwartał
do systemu BPHS po kątem innych oznak
zapalenia błon surowiczych, jako uzupełnienie postępowania diagnostycznego
prowadzonego na fermie.
Prostszą, lecz zarazem mniej dokładną
metodą pozwalającą stwierdzić, czy
przypadki ChG pojawiają się na fermie,
jest oznaczenie częstotliwości występowania na poziomie grupy produkcyjnej
ciężkiego zapalenia opłucnej. Należy
mieć jednak na uwadze, że samo zapalenie opłucnej nie zawsze rozwija się
tylko w przebiegu ChG. Zmiany w postaci zapleniana opłucnej trzeba więc
analizować w połączeniu z zapaleniem
osierdzia i/lub zapaleniem otrzewnej
oraz uzupełnić poprzez prowadzone
6
na fermie obserwacje w kierunku oznak
klinicznej bądź podklinicznej postaci
choroby. Na rycinie 4 przedstawiono
częstotliwość występowania ciężkiego
zapalenia opłucnej w 9445 grupach
produkcyjnych (dane BPHS zebrane pomiędzy lipcem 2005 a czerwcem 2007).
Zaledwie w 32% grup nie stwierdzono przypadków ciężkiego zapalenia
opłucnej. W 43% badanych grup częstotliwość występowania takich zmian
anatomopatologicznych przekraczała
5% w obrębie grupy, a w 11% grup
wynosiła ponad 20%. Rozkład danych
na wykresie wskazuje, że częstotliwość
występowania ciężkiego zapalenia
opłucnej przekraczająca 5% może
zmniejszać efektywność produkcji i konkurencyjność producentów, w stosunku
do pozostałych badanych grup, gdzie
wartość ta była mniejsza niż 5%.
Acute Glässer’s Disease. M White. NADIS Pig Health. Dec 2006. See www.nadis.org.uk
1 Jakie są koszty?
Koszty związane z ChG trudno jest dokładnie określić. Raport NADIS1 (National Animal Disease Information Service)
podaje, że śmiertelność poodsadzeniowa w ostrych wybuchach ChG sięga
8 % i utrzymuje się nawet 4 tygodnie,
a spowolnienie przyrostów w perspektywie długoterminowej wynosi 50g/dzień
u przewlekle chorych zwierząt, u których
w badaniu poubojowym stwierdza się
zapalenie opłucnej. W analizach danych
produkcyjnych (Pig World, September
2006) przyjęto, że zmiana poziomu
śmiertelności o1% ma wartość 50
pensów w przeliczeniu na skierowane
na ubój zwierzę, a spowolnienie przyrostów równe 50g/dzień osiąga przy
uboju wartość 1,05 £. Przy założeniu,
że „normalny” poziom śmiertelności
Rycina 5. Ciężkie
zapalenie opłucnej
wynoszący 2% wzrośnie do 8%, koszt
choroby wyniesie 3 £ na 1 ubite zwierzę. Ponadto, jak wskazuje wykres 2,
częstotliwość występowania zapalenia
opłucnej może sięgać 20% w obrębie
grupy produkcyjnej – wówczas koszt,
przyjmując 1,05 £ za 50g obniżonych
przyrostów masy ciała na dzień, dla grupy 100 zwierząt osiąga wartość 21,00
£ (21 pensów na zwierzę). Koszty związane ze śmiertelnością i spowolnieniem
przyrostów wynoszą więc w przybliżeniu
3,21 £ w przeliczeniu na zwierzę. Do tej
kwoty należy jednak dodać koszty obniżenia wskaźnika wykorzystania paszy
(zmiana tego wskaźnika o 0,1 kosztuje
1,40 £ za świnię, przyjmując koszt paszy w wysokości 140 £ za tonę) oraz
leków i dodatkowych nakładów pracy
związanych z leczeniem i hospitalizacją.
Choroba Glässera może więc kosztować
producenta nawet 5,00 £ w przeliczeniu
na 1 zwierzę.
Koszt schorzeń układu oddechowego
powodowanych prze HPS jest jeszcze
trudniej oszacować, gdyż drobnoustrój
ten jest zazwyczaj jednym z kilku czynników etiologicznych powodujących zapalenie płuc, takich jak mykoplazmy. David
Burch (Pig World, February 2007) oszacował, że w skali oceny nasilenia zmian
w płucach wartość równa 10 (około 10
% objętości płuc jest zniszczonych procesem chorobowym) kosztuje w przeliczeniu na zwierzę 2,15 £ (z uwzględnieniem obniżonych średnich dziennych
przyrostów, zmniejszenia efektywności
wykorzystania paszy oraz podwyższonej
śmiertelności). Jednakże korygując te pa-
Zdjęcie dzięki uprzejmości BPEX
7
rametry o obecnie przyjęte koszty BPEX
(Pig World, February 2007), całkowity
koszt wyniesie 2,59 £.
Choroba Glässera jest zatem bardzo
kosztowna.
n Co mogę zrobić?
Niezwykle trudno jest wyeliminować
HPS z sektorów produkcyjnych, a w opinii wielu osób podjecie takich działań
niosłoby pewne ryzyko, gdyż wybuchy
ChG o najcięższym przebiegu występują
w stadach, które wcześniej nie miały
kontaktu z tym drobnoustrojem. Większość producentów decyduje się więc
„żyć razem z HPS”, przyjmując strategię
działania zapewniającą niską częstotliwość występowania ChG bądź brak
choroby, co z kolei jest warunkowane
wysokim poziomem odporności zwierząt. Cel ten można osiągnąć poprzez
odpowiednie praktyki zarządzania,
leczenie oraz szczepienia.
Ograniczanie wpływu choroby
poprzez odpowiednie procedury
zarządzania
Choroba Glässera pojawia się najczęściej
w systemach produkcji, gdzie jakość
8
siary jest niska bądź jej pobór niewielki.
W tradycyjnych systemach produkcji od
oproszenia do tuczu lochy posiadające
odporność na HPS wytwarzają siarę,
która będzie zabezpieczać miot przed
tymi samymi szczepami tego mikroorganizmu. Wraz z powolnym zanikaniem
odporności siarowej organizmy prosiąt
są zasiedlane przez bakterie i jednocześnie wytwarzają własną odporność czynną przeciwko tej chorobie. Drobnoustrój
i ChG pozostają więc „pod kontrolą”
z wyjątkiem sporadycznych przypadków,
kiedy pojedyncze prosięta nie pobrały
odpowiedniej ilości siary bądź aktywność ich układu immunologicznego była
stłumiona z innych powodów. Wśród
kluczowych elementów strategii zarządzania należy wymienić następujące:
n
S iara: należy zoptymalizować pobór
przez prosięta dobrej jakości siary
w okresie po urodzeniu utrzymując
w stadzie odpowiednią liczbę loch
wieloródek, aby wyrównać niską
jakość siary loszek. Dobrej jakości
żywienie i ograniczenie stresu wpływa na przebieg laktacji
n
graniczanie źródeł pozyskiwania
O
prosiąt w systemach produkcji
warchlaków i tuczników: łączenie
prosiąt odsadzonych pochodzących
z wielu ferm hodowlanych wymaga
starannego planowania. Należy,
gdy tylko możliwe, unikać takich
praktyk, a w innych przypadkach
postępować zgodnie ze schematem
piramid, aby zyskać pewność, że
u dostawców warchlaków występują podobne szczepy HPS.
n
klimatyzacja: w przypadku wproA
wadzania zwierząt zarodowych
należy mieć opracowany program
aklimatyzacji, szczególnie dla zwierząt pochodzących ze stad o wyższym statusie zdrowotnym niż sektor docelowy. Należy wprowadzić
szczepienia (patrz kolejna strona)
i unikać bezpośredniego kontaktu
z populacją rezydującą przez 3-4
tygodnie, po czym stopniowo łączyć
ze sobą zwierzęta.
n
Immunosupresja: należy kontrolować inne choroby o potencjale immunosupresyjnym, takie jak PMWS
oraz PRRS. Należy podawać zbilansowaną paszę i unikać niedoborów
witaminowo – mineralnych, które
będą upośledzać sprawność układu
odpornościowego i w efekcie predysponować do rozwoju ChG.
nione, gdyż efekty zmian w zarządzaniu
pojawiają się powoli, nie są w 100 %
skuteczne i na poziomie lokalnym mogą
być trudne w realizacji.
Leczenie
HPS jest bardzo wrażliwy na działanie
antybiotyków. W kontroli wybuchów
ChG stosowano z powodzeniem wiele
metod podawania leków z paszą oraz
wodą do picia. W niedawnym badaniu
stwierdzono zadowalającą wrażliwość
izolowanych w Wielkiej Brytanii bakterii
na penicylinę, ceftiofur, erytromycynę,
tylmikozynę, enrofloksacynę oraz florfenikol2. W tym samym badaniu zaobserwowano jednak znaczącą oporność na
te same substancje czynne izolatów HPS
pochodzących z Hiszpanii, co zdaniem
autorów może być związane z częstszym i powszechniejszym stosowaniem
leków przeciwbakteryjnych w produkcji
trzody chlewnej w tym kraju. W perspektywie długoterminowej stosowanie
samej tylko farmakoterapii może jednak
okazać się nierealne.
Zwalczanie
Zakażenia HPS jest bardzo trudno
wyeliminować, a większość lekarzy
weterynarii zgadza się, że takie działania nie wpłyną korzystnie na status
zdrowotny stad, gdyż brak kontaktu
Powyższe ważne praktyki zarządzania
z zasady uzupełnia się leczeniem i szczepieniem. W przypadku bardzo wysokiej
śmiertelności i dużych strat produkcyjnych takie postępowanie jest uzasadde la Fuente AJ, Tucker AW, Navas J, Blanco M, Morris SJ, Butierrez-Martin CB. Antimicrobial susceptibility patterns of
Haemophilus parasuis from pigs in the United Kingdom and Spain. Vet Microbiol. 2007. Feb 25; 120 (1-2): 184-91.
2
9
z tym mikroorganizmem sprawia, że
stają się one podatne na wybuchy ChG
o ciężkim przebiegu. Jako że HPS jest
zwykle przekazywany prosiętom przez
lochy w ciągu kilku pierwszych dni życia, nawet najwcześniejsze odsadzanie
bądź wprowadzenie leczenia może nie
pozwolić na całkowita eliminację mikroorganizmu. Jedynym bezpiecznym sposobem eliminacji HPS jest cesarskie cięcie
i sztuczny odchów (będący sam w sobie
ogromnym wyzwaniem z uwagi na
inne oportunistyczne patogeny). Należy
jednak raz jeszcze podkreślić, że stada
niemające kontaktu z drobnoustrojem
są niezwykle podatne na wybuchy ChG
o bardzo ciężkim przebiegu.
Szczepienia
Dostępność szczepionek pozwoliła
na wprowadzenie znaczących zmian
w strategiach kontroli chorób związanych z zakażeniami HPS. Jednym z problemów, którym należy sprostać, jest
fakt, że ChG mogą wywoływać różne
szczepy HPS. Istnieją jednak wyraźne
n
Czy powinienem szczepić?
Jest to decyzja warunkowana ekonomicznie. Podejmując ją należy uwzględnić
wiek zwierząt, w którym będą szczepione, oraz okres prowadzenia szczepień.
Kiedy szczepienie staje się ekonomicznie opłacalne?
Przeprowadzenie końcowej kalkulacji
wymaga oszacowania kosztów choroby
i szczepionek łącznie z nakładami pracy
związanymi z ich podawaniem oraz
określenia skuteczności i przydatności
szczepienia w kontroli choroby (patrz
dalej). Jeśli szczepionka cechuje się właściwościami zabezpieczającymi przeciwko więcej niż jednej chorobie, tak jak
Suvaxyn® M. hyo – Parasuis zapewniający ochronę przed ChG oraz mykoplazmowym zapaleniem płuc (powodowanym przez Mycoplasma hyopneumo-
Rapp-Gabrielsen VJ, Gabrielsen DA. 1992. Prevalence of H. parasuis serovars among isolates from swine.
Am J Vet Res. 53(5), 136.
Kielstein, P & Rapp-Gabrielson V. 1992. Designation of 15 serovars of Haemophilus parasuis on the basis of immunodiffusion
using heat-stable antigen extracts. Journal of Clinical Microbiology Vol. 30: p. 862-865
5
Rapp-Gabrielson et al., 1996. Proceedings of the 14th IPVS Congress, Italy, p. 300.
6
Rapp-Gabrielson, V., et al. Haemophilus parasuis: Immunity in Swine after Vaccination.
Veterinary Medicine. Jan. 1997. p. 83-89
7
Angen et al. 2004. Serological characterization of Danish Haemophilus parasuis isolates.
Veterinary Microbiology 103 (2004) 255-258
3
4
10
dowody wskazujące, że szczepy zawarte
szczepionkach zapewniają znacznego
stopnia odporność krzyżową. Dane
pochodzące ze Stanów Zjednoczonych3
(powtórzone w Niemczech4) potwierdzają, że serotypy 4 oraz 5 są najczęściej
powiązane z rozwojem ChG. Serotypy
te stanowią zasadniczy komponent preparatu Suvaxyn® M. hyo – Parasuis. Zabezpieczenie oferowane przez tę szczepionkę zapewnia odporność krzyżową
przeciw innym serotypom HPS5,6, obejmującą przeszło 50% znanych szczepów
chorobotwórczych7.
niae), należy wziąć pod uwagę korzyści
płynące z obniżenia kosztów związanych z występowaniem obu jednostek
chorobowych. Wprowadzenie szczepień, przyjmując oszacowany koszt ChG
(patrz powyżej) i skuteczność szczepień
na poziomie 67%*, pozwoli zaoszczędzić co najmniej 2,15 £ w przeliczeniu
na zwierzę w efekcie ograniczenia liczby
przypadków ChG (bez uwzględnienia
oszczędności wynikających z lepszego
wykorzystania paszy oraz zmniejszenia
ilości podawanych leków). Analiza powinna jednak zawsze uzależniona od
specyficznych warunków panujących
na danej fermie. Jeśli występuje tam
mykoplazmowe zapalenie płuc dające
w obrazie anatomopatologicznym zmiany oceniane w skali na 10, zastosowanie
preparatu Suvaxyn® M. hyo – Parasuis
mogłoby przynieść dodatkowe oszczędności rzędu 1,74£ na zwierzę wynikające ze zmniejszenia częstotliwości występowania tej choroby (przy skuteczności
szczepień równej 67%). W opisywanych
przykładzie całkowita korzyść finansowa
wyniosłaby zatem 3,91£, co stanowi
znaczącą kwotę nawet po odjęciu kosztów szczepionek i ich podawania.
Wśród typowych sytuacji, pomijając
powyższe kalkulacje, w których wprowadzenie szczepień z zastosowaniem
preparatu Suvaxyn® M. hyo – Parasuis
byłoby uzasadnione należy wymienić
następujące:
n
T rwała czynna postać ChG z lub bez
towarzyszącego mykoplazmowego
zapalenia płuc: jednym z przykładów mogą być kierowane na tucz
warchlaki pochodzące od różnych
hodowców i będące nosicielami
odmiennych szczepów HPS. Drugi
przykład to ferma, na której występuje PMWS upośledzające odporność zwierząt.
n
awracająca czynna postać ChG
N
z towarzyszącym mykoplazmowym
zapaleniem płuc. Przykład: sektor
produkcyjny o dość wysokim statusie zdrowotnym przy zmiennym
poziomie odporności matczynej.
*Skuteczność szczepień jest zależna od występowania w populacji świń różnych serotypów HPS.
11
n
J ako środek profilaktyczny przy
wprowadzaniu zwierząt zarodowych o dość wysokim statusie zdrowotnym do stad o niższym statusie.
n
ależy szczepić prosięta odsadzoN
ne co najmniej trzy i pól tygodnia
przed przewidywanym kontaktem
z mikroorganizmem sugerując się
typowym wiekiem, kiedy w sektorze
obserwuje się przypadki ChG. Jeśli
zakłada się, że poziom przeciwciał siarowych jest niski, wówczas
szczepienia można rozpocząć już
od 1 tygodnia życia, natomiast przy
wysokim poziomie odporności matczynej wskazane jest zaczekać do 3
tygodnia życia.
n
prowadzanym do stada zakuW
pionym zwierzętom hodowlanym
o wysokim statusie zdrowotnym
drugą dawkę szczepionki należy podawać co najmniej 3 tygodnie przed
przewiezieniem na fermę.
Kiedy należy szczepić?
W tym przypadku należy uwzględnić
dwa czynniki: po pierwsze okres czasu
upływający pomiędzy szczepieniem
a wytworzeniem zabezpieczającej odporności i po drugie utrudnienia związane ze szczepieniem młodych prosiąt
przy współistnieniu silnej odporności
siarowej.
Szczepienie z zastosowaniem preparatu
Suvaxyn® M. hyo – Parasuis polega na
podaniu dwóch dawek w odstępie
2-3 tygodni w celu uzyskania działania
zabezpieczającego przed HPS pojawiającego się trzy i pół tygodnia po drugiej
dawce. Istnieją pewne dowody wskazujące, że większość szczepionek cechuje się do pewnego stopnia mniejszą
skutecznością przy podawaniu młodym
prosiętom posiadającym silną odporność
siarową. Na podstawie tych informacji
można sformułować kilka praktycznych
wskazówek:
12
n
Co może zmniejszać
skuteczność szczepień?
Choć szczepienia okazały się niezwykle
opłacalnym ekonomicznie narzędziem
w kontroli chorób zakaźnych, ich działanie pozostaje wciąż procesem biologicznym, co wymaga w celu osiągnięcia jak
najlepszych rezultatów przestrzegania
określonych praktyk oraz zaleceń. Przyczyny leżące u podłoża niepowodzeń przy
stosowaniu szczepień, mogą być związane z samą szczepionką bądź organizmem
zwierzęcia, zostały szczegółowo omówione w poprzedniej publikacji.
Czynniki zależne od szczepionek
Zawsze należy zapoznać się z treścią ulotki
informacyjnej dołączonej do preparatu
i zachować ją oraz postępować zgodnie z zamieszczonymi tam wytycznymi.
Najczęstsze przyczyny nieskuteczności
szczepień związane są niewłaściwym
przechowywaniem, przygotowywaniem
oraz podawaniem preparatów. Większość
szczepionek wymaga przechowywania
w warunkach chłodniczych w temperaturze od +2°C do +8°C. Ważne jest również
wymieszanie zawiesiny przed wykonywaniem iniekcji, jak również właściwe
dawkowanie oraz unikanie wprowadzania
zanieczyszczeń.
Czynniki zależne od zwierząt
Szereg czynników zależnych od organizmu zwierzęcia lub związanych z zarządzaniem może przyczyniać się do uzyskiwania gorszych, niż zakładane, wyników
szczepień. Tego rodzaju problemy można
zazwyczaj wyeliminować poprzez konsultacje z lekarzem weterynarii. Nieodpowiednie szczepienie bądź brak możliwości
jego przeprowadzenia przed kontaktem
z mikroorganizmem lub też styczność
ze szczepem dającym jedynie częściową
odporność krzyżową ze szczepem szczepionkowym to niepomyślne, lecz realne
sytuacje. W niektórych przypadkach może
rozwijać się słabsza i niekiedy niegwarantująca zabezpieczenia odpowiedź
immunologiczna na szczepienie. Takie
działanie immunosupresyjne wywierać
może wiele czynników, jak niedojrzałość
zwierząt (poniżej 1 tygodnia życia), stres,
inne choroby (przykładowo PNWS), niektóre leki (np. glikokortykoidy), niedobory
żywieniowe oraz mikotoksyny. Ponadto,
jak wspomniano powyżej, wysoki poziom
odporności siarowej może zaburzać odpowiedź organizmu na szczepienia i stąd
należy odpowiednio dostosować czas ich
wykonywania.
n Podsumowanie
Choroba Glässera to schorzenie o ciężkim
przebiegu wywierające duży wpływ na
zyskowność produkcji nawet na fermach
o wysokim statusie zdrowotnym. Czynnik etiologiczny H. parasuis przyczynia
się ponadto do rozwoju chorób układu
oddechowego powodujących dodatkowe
koszty poza tymi, związanymi z ChG.
W rozpoznawaniu choroby przydatne są
takie narzędzia diagnostyczne jak oznaczanie poziomu śmiertelności, opisywanie
obrazu klinicznego oraz badania poubojowe. Dodatkowa analiza efektywności
wykorzystania paszy pozwala precyzyjnie
określić ekonomiczne następstwa choroby
w danym sektorze produkcyjnym. Z uwagi na ostry i niekiedy nieprzewidywalny
przebieg choroby oraz jej duży wpływ na
zyskowność produkcji, strategie kontroli
zazwyczaj łączą zmianę praktyk zarządzania, leczenie oraz szczepienia, które
stanowią wysoce efektywny element
każdego programu kontroli, jeśli tylko
postępuje się zgodnie z zaleceniami producentów szczepionek.
13
Podwójny problem?
Na mykoplazmowe
zapalenie płuc i chorobę Glässera
jest już jedno rozwiązanie!
Suvaxyn® M. hyo – Parasuis to jedyna szczepionka zabezpieczająca równocześnie przed
mykoplazmowym zapaleniem płuc (powodowanym przez Mycoplasma hyopneumoniae)
oraz chorobą Glässera (powodowanej przez
Haemophilus parasuis).
Ponadto Suvaxyn® M. hyo – Parasuis jest jedyną
zarejestrowaną szczepionką przeciwko zakażeniom H. parasuis zawierającą serotypy 5 oraz 4.
chorób powodujących ogromne straty
ekonomiczne.
Dzięki udowodnionej skuteczności, długo
utrzymującej się odporności oraz wodnemu
adiuwantowi Suvaxyn® M. hyo – Parasuis
jest szczepionką z wyboru w zwalczaniu
choroby Glässera.
Biorąc pod uwagę powyższe waściwości
Suvaxyn M. hyo - Parasuis jest unikalnym
produktem ograniczającym wpływ dwóch
Zoetis Polska Sp. z o.o., ul. Postępu 17b, 02-676 Warszawa, tel. +48 22 335 61 01 (do 03), www.zoetis.com