Wymagania edukacyjne z chemii dla klas trzecich gimnazjum niezbędne do uzyskania poszczególnych śródrocznych ocen klasyfikacyjnych
Klasy IIIA, III B, III E, III F
Rok szkolny 2015/2016
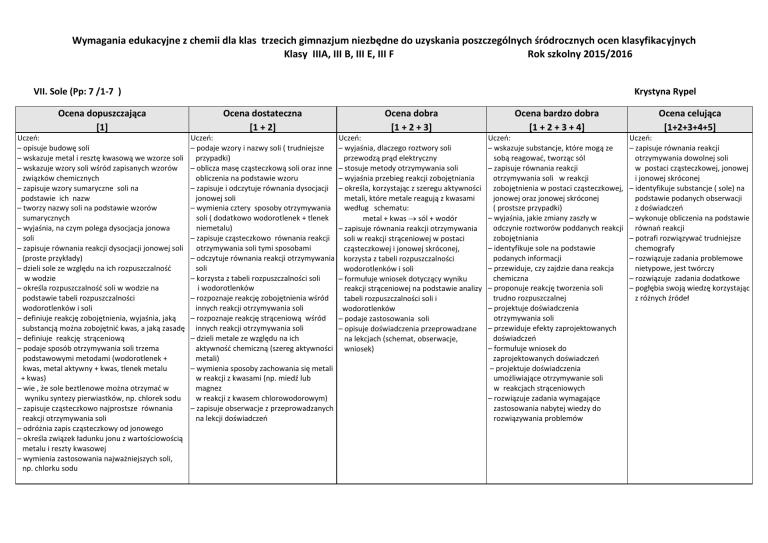
VII. Sole (Pp: 7 /1-7 )
Krystyna Rypel
Ocena dopuszczająca
[1]
Ocena dostateczna
[1 + 2]
Ocena dobra
[1 + 2 + 3]
Ocena bardzo dobra
[1 + 2 + 3 + 4]
Ocena celująca
[1+2+3+4+5]
Uczeń:
– opisuje budowę soli
– wskazuje metal i resztę kwasową we wzorze soli
– wskazuje wzory soli wśród zapisanych wzorów
związków chemicznych
– zapisuje wzory sumaryczne soli na
podstawie ich nazw
– tworzy nazwy soli na podstawie wzorów
sumarycznych
– wyjaśnia, na czym polega dysocjacja jonowa
soli
– zapisuje równania reakcji dysocjacji jonowej soli
(proste przykłady)
– dzieli sole ze względu na ich rozpuszczalność
w wodzie
– określa rozpuszczalność soli w wodzie na
podstawie tabeli rozpuszczalności
wodorotlenków i soli
– definiuje reakcję zobojętnienia, wyjaśnia, jaką
substancją można zobojętnić kwas, a jaką zasadę
– definiuje reakcję strąceniową
– podaje sposób otrzymywania soli trzema
podstawowymi metodami (wodorotlenek +
kwas, metal aktywny + kwas, tlenek metalu
+ kwas)
– wie , że sole beztlenowe można otrzymać w
wyniku syntezy pierwiastków, np. chlorek sodu
– zapisuje cząsteczkowo najprostsze równania
reakcji otrzymywania soli
– odróżnia zapis cząsteczkowy od jonowego
– określa związek ładunku jonu z wartościowością
metalu i reszty kwasowej
– wymienia zastosowania najważniejszych soli,
np. chlorku sodu
Uczeń:
– podaje wzory i nazwy soli ( trudniejsze
przypadki)
– oblicza masę cząsteczkową soli oraz inne
obliczenia na podstawie wzoru
– zapisuje i odczytuje równania dysocjacji
jonowej soli
– wymienia cztery sposoby otrzymywania
soli ( dodatkowo wodorotlenek + tlenek
niemetalu)
– zapisuje cząsteczkowo równania reakcji
otrzymywania soli tymi sposobami
– odczytuje równania reakcji otrzymywania
soli
– korzysta z tabeli rozpuszczalności soli
i wodorotlenków
– rozpoznaje reakcję zobojętnienia wśród
innych reakcji otrzymywania soli
– rozpoznaje reakcję strąceniową wśród
innych reakcji otrzymywania soli
– dzieli metale ze względu na ich
aktywność chemiczną (szereg aktywności
metali)
– wymienia sposoby zachowania się metali
w reakcji z kwasami (np. miedź lub
magnez
w reakcji z kwasem chlorowodorowym)
– zapisuje obserwacje z przeprowadzanych
na lekcji doświadczeń
Uczeń:
– wyjaśnia, dlaczego roztwory soli
przewodzą prąd elektryczny
– stosuje metody otrzymywania soli
– wyjaśnia przebieg reakcji zobojętniania
– określa, korzystając z szeregu aktywności
metali, które metale reagują z kwasami
według schematu:
metal + kwas sól + wodór
– zapisuje równania reakcji otrzymywania
soli w reakcji strąceniowej w postaci
cząsteczkowej i jonowej skróconej,
korzysta z tabeli rozpuszczalności
wodorotlenków i soli
– formułuje wniosek dotyczący wyniku
reakcji strąceniowej na podstawie analizy
tabeli rozpuszczalności soli i
wodorotlenków
– podaje zastosowania soli
– opisuje doświadczenia przeprowadzane
na lekcjach (schemat, obserwacje,
wniosek)
Uczeń:
– wskazuje substancje, które mogą ze
sobą reagować, tworząc sól
– zapisuje równania reakcji
otrzymywania soli w reakcji
zobojętnienia w postaci cząsteczkowej,
jonowej oraz jonowej skróconej
( prostsze przypadki)
– wyjaśnia, jakie zmiany zaszły w
odczynie roztworów poddanych reakcji
zobojętniania
– identyfikuje sole na podstawie
podanych informacji
– przewiduje, czy zajdzie dana reakcja
chemiczna
– proponuje reakcję tworzenia soli
trudno rozpuszczalnej
– projektuje doświadczenia
otrzymywania soli
– przewiduje efekty zaprojektowanych
doświadczeń
– formułuje wniosek do
zaprojektowanych doświadczeń
– projektuje doświadczenia
umożliwiające otrzymywanie soli
w reakcjach strąceniowych
– rozwiązuje zadania wymagające
zastosowania nabytej wiedzy do
rozwiązywania problemów
Uczeń:
– zapisuje równania reakcji
otrzymywania dowolnej soli
w postaci cząsteczkowej, jonowej
i jonowej skróconej
– identyfikuje substancje ( sole) na
podstawie podanych obserwacji
z doświadczeń
– wykonuje obliczenia na podstawie
równań reakcji
– potrafi rozwiązywać trudniejsze
chemografy
– rozwiązuje zadania problemowe
nietypowe, jest twórczy
– rozwiązuje zadania dodatkowe
– pogłębia swoją wiedzę korzystając
z różnych źródeł
VIII. Węgiel i jego związki z wodorem (Pp: 8/ 1-9)
Ocena dopuszczająca
[1]
Ocena dostateczna
[1 + 2]
Ocena dobra
[1 + 2 + 3]
Ocena bardzo dobra
[1 + 2 + 3 + 4]
Ocena celująca
[1+2+3+4+5]
Uczeń:
– określa, czym zajmuje się chemia organiczna
– definiuje pojęcie węglowodory
– wymienia naturalne źródła węglowodorów
– stosuje zasady BHP w pracy z gazem ziemnym
oraz produktami przeróbki ropy naftowej
– opisuje budowę i występowanie metan
– opisuje właściwości metanu, etenu i etynu
– zna nazwy potoczne etenu i etynu
– opisuje, na czym polegają spalanie całkowite
i niecałkowite, zna produkty spalania
całkowitego i niecałkowitego
– uzgadnia równania reakcji spalania (proste
przypadki)
– definiuje pojęcie szereg homologiczny
– definiuje pojęcia: węglowodory nasycone
i węglowodory nienasycone
– klasyfikuje alkany do węglowodorów
nasyconych, a alkeny i alkiny do nienasyconych
– określa wpływ węglowodorów nasyconych
i nienasyconych na wodę bromową (lub
rozcieńczony roztwór manganianu (VII) potasu)
– podaje wzory ogólne szeregów
homologicznych alkanów, alkenów i alkinów
– podaje zasady tworzenia nazw alkenów
i alkinów na podstawie nazw alkanów
– przyporządkowuje dany węglowodór do
odpowiedniego szeregu homologicznego
– odróżnia wzór sumaryczny od wzorów
strukturalnego i półstrukturalnego
– zapisuje wzory sumaryczne i nazwy alkanu,
alkenu i alkinu (do pięciu atomów węgla )
– zapisuje wzory strukturalne i półstrukturalne
węglowodorów (proste przykłady)
– oblicza masy cząsteczkowe węglowodorów
Uczeń:
– wyjaśnia pojęcie szereg homologiczny
– buduje model cząsteczki metanu, etanu,
etenu i etynu
– zapisuje wzory sumaryczne, strukturalne
i półstrukturalne oraz podaje nazwy
alkanów, alkenów i alkinów do 10 atomów
węgla w cząsteczce
– opisuje najważniejsze zastosowania etenu
i etynu
– wyjaśnia różnicę między spalaniem
całkowitym a niecałkowitym
– zapisuje równania reakcji spalania metanu,
etanu, etenu, etynu
– porównuje budowę etanu, etenu i etynu
– wyjaśnia, na czym polegają reakcje addycji
(przyłączania) i polimeryzacji
– definiuje pojęcia: polimeryzacja, monomer
i polimer
– opisuje właściwości chemiczne metanu,
etenu i etynu (aktywność chemiczna,
reakcje przyłączania)
– określa, od czego zależą właściwości
fizyczne węglowodorów
– określa stan skupienia i łatwość spalania
węglowodorów w zależności od liczby
atomów węgla w cząsteczce na przykładzie
alkanów
– wykonuje proste obliczenia dotyczące
węglowodorów
Uczeń:
– proponuje, jak doświadczalnie wykryć
produkty spalania węglowodorów
– zapisuje równania reakcji spalania
całkowitego i niecałkowitego węglowodorów
– odczytuje podane równania reakcji
chemicznej
– wyjaśnia zależność między długością
łańcucha węglowego a właściwościami
(np. stanem skupienia, lotnością, palnością)
alkanów
– opisuje właściwości i zastosowania
polietylenu
– wyjaśnia dlaczego eten i etyn ulegają
reakcji addycji i polimeryzacji, a metan nie
ulega
– zapisuje równania reakcji przyłącznia
do etenu , etyn i propenu (z użyciem
wzorów sumarycznych)
– podaje sposoby otrzymywania etenu
i etynu
– opisuje i porównuje właściwości alkanów,
alkenów i alkinów
– wyjaśnia, co jest przyczyną większej
reaktywności chemicznej węglowodorów
nienasyconych w porównaniu
z węglowodorami nasyconymi
– wyjaśnia, jak doświadczalnie odróżnić
węglowodory nasycone od nienasyconych
– opisuje przeprowadzane doświadczenia
chemiczne
– wykonuje obliczenia stechiometryczne
Uczeń:
– dokonuje analizy właściwości
węglowodorów
– potrafi wykryć obecność węgla
i wodoru w związkach organicznych
– wyjaśnia, dlaczego węglowodory są
nierozpuszczalne w wodzie,
a rozpuszczają się w benzynie
– wyjaśnia wpływ wiązania
wielokrotnego w cząsteczce
węglowodoru na jego reaktywność
chemiczną
– zapisuje równania reakcji przyłączania
do węglowodorów zawierających
wiązanie wielokrotne (wzory
strukturalne)
– zapisuje równania reakcji
polimeryzacji etenu
– zapisuje równania reakcji
otrzymywania etenu z polietylenu
– zapisuje równania reakcji
otrzymywania etynu z karbidu
– projektuje doświadczenia chemiczne
umożliwiające odróżnienie
węglowodorów nasyconych od
nienasyconych
– rozwiązuje zadania wymagające
zastosowania nabytej wiedzy do
rozwiązywania problemów
Uczeń:
– podaje nazwy
halogenowodorów
– zapisuje równanie reakcji
polimeryzacji propenu,
chloroetenu
– określa produkty polimeryzacji
propenu
– na przykładzie butanu
i butenu wyjaśnia zjawisko
izomerii
– rozwiązuje chemografy
o większym stopniu trudności
– dokonuje obliczeń na
podstawie równania reakcji
chemicznej
– stosuje zdobytą wiedzę
w złożonych zadaniach,
nietypowych, jest twórczy
– rozwiązuje zadania dodatkowe
– pogłębia swoją wiedzę
korzystając z różnych źródeł
IX. Pochodne węglowodorów (Pp: I/9, II/9, III/9 pkt. 1-9 oraz pkt. 11 i 12)
Ocena dopuszczająca
[1]
Ocena dostateczna
[1 + 2]
Ocena dobra
[1 + 2 + 3]
Ocena bardzo dobra
[1 + 2 + 3 + 4]
Uczeń:
– dowodzi, że alkohole, kwasy karboksylowe,
estry, aminy, aminokwasy są pochodnymi
węglowodorów
– opisuje budowę pochodnych węglowodorów
(grupa węglowodorowa + grupa funkcyjna)
– wymienia pierwiastki chemiczne wchodzące w
skład pochodnych węglowodorów
– klasyfikuje daną substancję organiczną do
odpowiedniej grupy związków chemicznych
– określa, co to jest grupa funkcyjna
– zapisuje nazwy i wzory grup funkcyjnych ( dla
kwasów i alkoholi)
– zaznacza grupy funkcyjne w alkoholach, kwasach
karboksylowych, estrach, aminach i
aminokwasach i podaje ich nazwy
– zapisuje wzory ogólne alkoholi, kwasów
karboksylowych i estrów
– zapisuje wzory sumaryczne i strukturalne prostych
alkoholi monohydroksylowych i kwasów
karboksylowych (do 2 atomów węgla w cząsteczce)
oraz tworzy ich nazwy
– zaznacza we wzorze kwasu karboksylowego
resztę kwasową oraz podaje jej wartościowość
– określa, co to są nazwy zwyczajowe
i systematyczne
– wymienia reguły tworzenia nazw
systematycznych związków organicznych
– podaje nazwy zwyczajowe omawianych kwasów
karboksylowych (mrówkowy, octowy)
– opisuje najważniejsze właściwości metanolu,
etanolu, glicerolu oraz kwasów etanowego
i metanowego
– opisuje podstawowe zastosowania etanolu i
kwasu etanowego
– dokonuje podziału alkoholi na mono i
polihydroksylowe oraz kwasów karboksylowych
na nasycone i nienasycone
– wymienia nazwy poznanych kwasów
tłuszczowych
– opisuje właściwości długołańcuchowych
Uczeń:
– zapisuje nazwy i wzory omawianych grup
funkcyjnych
– zapisuje wzory i wymienia nazwy alkoholi
– zapisuje wzory sumaryczny i strukturalny
glicerolu
– uzasadnia stwierdzenie, że alkohole
i kwasy karboksylowe tworzą szeregi
homologiczne
– podaje odczyn roztworu alkoholu
– bada odczyn roztworu, zna barwy
wskaźników w roztworach o
odpowiednim odczynie
– podaje przykłady kwasów organicznych
występujących w przyrodzie i wymienia
ich zastosowania
– tworzy nazwy prostych kwasów
karboksylowych (do 5 atomów węgla
w cząsteczce) oraz zapisuje ich wzory
sumaryczne i strukturalne
– podaje właściwości kwasów metanowego
(mrówkowego) i etanowego (octowego)
– omawia dysocjację jonową kwasów
karboksylowych
– zapisuje równania dysocjacji jonowej
kwasu mrówkowego i octowego
– podaje odczyn kwasu mrówkowego
i octowego
– planuje doświadczenie pozwalające
zobojętnić kwas mrówkowy lub octowy
– zapisuje równania kwasu mrówkowego
i octowego z: metalami, tlenkami metali
i zasadami
– podaje nazwy soli pochodzących od
kwasów metanowego i etanowego
– zapisuje wzory sumaryczne kwasów
palmitynowego, stearynowego i
oleinowego
– porównuje kwasy nasycone i nienasycone
– opisuje, jak doświadczalnie udowodnić,
że dany kwas karboksylowy jest kwasem
Uczeń:
– wyjaśnia, dlaczego alkohol etylowy
wykazuje odczyn obojętny
– wyjaśnia, w jaki sposób tworzy się nazwę
systematyczną glicerolu
– zapisuje równania reakcji spalania
alkoholi
– podaje nazwy zwyczajowe i
systematyczne kwasów karboksylowych
– wyjaśnia, dlaczego wyższe kwasy
karboksylowe nazywa się kwasami
tłuszczowymi
– porównuje właściwości kwasów
organicznych i nieorganicznych
– porównuje właściwości kwasów
karboksylowych
– opisuje fermentację alkoholową i octową
– opisuje równania reakcji chemicznych
dla kwasów karboksylowych
– podaje nazwy soli kwasów organicznych
– określa miejsce występowania wiązania
podwójnego w cząsteczce kwasu
oleinowego
– projektuje doświadczenie chemiczne
umożliwiające odróżnienie kwasów
oleinowego od palmitynowego lub
stearynowego
–zapisuje wzory mydeł: sodowego i
potasowego
– opisuje rolę katalizatora w reakcji
chemicznej
– zapisuje równania reakcji otrzymywania
podanych estrów
– tworzy wzory estrów na podstawie
podanych nazw kwasów i alkoholi
– zapisuje wzory poznanej aminy i
aminokwasu
– opisuje budowę i właściwości amin na
przykładzie metyloaminy
– opisuje budowę, właściwości fizyczne
i chemiczne aminokwasów na
Uczeń:
– zapisuje wzory dowolnych alkoholi
i kwasów karboksylowych
– zapisuje równania reakcji
chemicznych dla alkoholi, kwasów
karboksylowych o wyższym stopniu
trudności (np. więcej niż 5 atomów
węgla w cząsteczce)
– podaje metodę otrzymywania kwasu
octowego
– wyjaśnia zależność między długością
łańcucha węglowego a stanem
skupienia i reaktywnością chemiczną
alkoholi oraz kwasów karboksylowych
– zapisuje równania reakcji
otrzymywania estru o podanej nazwie
lub podanym wzorze
– projektuje doświadczenie chemiczne
umożliwiające otrzymanie mydła
– projektuje doświadczenie chemiczne
umożliwiające otrzymanie estru
o podanej nazwie
– opisuje właściwości estrów w
kontekście ich zastosowań
– analizuje konsekwencje istnienia
dwóch grup funkcyjnych w cząsteczce
aminokwasu
– zapisuje równanie reakcji tworzenia
dipeptydu
– wyjaśnia mechanizm powstawania
wiązania peptydowego
– formułuje wnioski z doświadczeń
chemicznych
– wykonuje obliczenia
stechoiometryczne
Ocena celująca
[1+2+3+4+5]
Uczeń:
– zapisuje równania reakcji
chemicznych zachodzących w
twardej wodzie po dodaniu mydła
sodowego
– zapisuje równania reakcji
chemicznych w postaci
cząsteczkowej, jonowej oraz
skróconej jonowej
– omawia różnicę między reakcją
estryfikacji a reakcją zobojętniania
– wyjaśnia, co to jest hydroliza
estru
– zapisuje równania reakcji
hydrolizy estru o podanej nazwie
lub wzorze
– rozwiązuje zadania o większym
stopniu trudności dotyczące
stężeń procentowych i obliczeń
stechiometrycznych
– dokonuje obliczeń na
podstawie równania reakcji
chemicznej
– potrafi wykorzystać swoją wiedzę
do rozwiązywania złożonych zadań,
nietypowych, jest twórczy
– rozwiązuje zadania dodatkowe
– pogłębia swoją wiedzę
korzystając z różnych źródeł
kwasów karboksylowych (kwasów tłuszczowych:
stearynowego i oleinowego)
– definiuje pojęcie mydła
– wymienia związki chemiczne, będące
substratami reakcji estryfikacji
– definiuje pojęcie estry
– wymienia przykłady występowania estrów
w przyrodzie
– opisuje zagrożenia związane z alkoholami
(metanol, etanol)
– zna toksyczne właściwości poznanych substancji
– określa, co to są aminy i aminokwasy
– podaje przykłady występowania amin i
aminokwasów
nienasyconym
przykładzie glicyny
– zapisuje wzory estrów ( do czterech
– opisuje przeprowadzone doświadczenia
atomów węgla)
chemiczne, zapisuje obserwacje i wnioski
– tworzy nazwy estrów pochodzących
od podanych nazw kwasów i alkoholi
– wyjaśnia, na czym polega reakcja
estryfikacji
– określa sposób otrzymywania wskazanego
estru, np. octanu etylu
– wymienia właściwości fizyczne octanu
etylu
– opisuje budowę i właściwości amin na
przykładzie metyloaminy
– zapisuje wzór najprostszej aminy
– opisuje negatywne skutki działania
etanolu na organizm ludzki
Sposoby sprawdzania osiągnięć edukacyjnych uczniów:
1. Bieżące sprawdzanie osiągnięć edukacyjnych ucznia, będące podstawą ustalania ocen bieżących w skali, o której mowa w § 52 Statutu Gimnazjum
w Niepołomicach, odbywa się w następujących formach:
1) wypowiedzi ustne obejmujące materiał nauczania jednej, dwóch lub trzech ostatnich lekcji;
2) wypowiedzi ustne obejmujące materiał nauczania jednego lub więcej działów programowych, zapowiadane według zasad ustalonych dla sprawdzianów
pisemnych;
3) kartkówki – krótkie pisemne sprawdziany trwające nie dłużej niż 15 minut i obejmujące materiał nauczania z jednej, dwóch lub trzech ostatnich lekcji;
4) kartkówki – krótkie pisemne sprawdziany trwające nie dłużej niż 15 minut i obejmujące wskazany, ściśle określony przez nauczyciela materiał nauczania nie
większy niż jeden dział programowy;
5) sprawdziany pisemne obejmujące materiał nauczania jednego lub więcej działów programowych;
6) ćwiczenia i zadania praktyczne;
7) ćwiczenia i zadania wykonane na lekcji;
8) ćwiczenia i zadania wykonane w domu;
2. Sprawdzian pisemny, o którym mowa w pkt 5, nauczyciel wpisuje do dziennika lekcyjnego oraz informuje uczniów o jego zakresie, formie i terminie z co najmniej
tygodniowym wyprzedzeniem. Każdy sprawdzian pisemny powinien być poprzedzony powtórzeniem wiadomości i podaniem wymagań jakim uczeń będzie musiał sprostać.
3. Kartkówki, o których mowa w pkt 3, nie wymagają zapowiadania.
5. O kartkówkach, o których mowa w pkt 4, nauczyciel informuje uczniów z tygodniowym wyprzedzeniem.
6. Sprawdziany pisemne i kartkówki mogą mieć formę testu.
7. W ciągu tygodnia mogą być przeprowadzone najwyżej trzy pisemne sprawdziany i nie więcej niż jeden w danym dniu.