FIZYKA ATOMOWA (c.d.)
Układ okresowy pierwiastków
Zasady obsadzania poziomów
Konfiguracje elektronowe
Energia jonizacji
Promieniowanie rentgenowskie
Widmo ciągłe i charakterystyczne
Prawo Moseleya
Przejścia atomowe. Lasery.
UKŁAD OKRESOWY PIERWIASTKÓW
W układzie okresowym pierwiastki są uporządkowane według rosnącej liczby
atomowej Z (czyli rosnącej liczby elektronów).
Elektrony w atomie dążą do zajęcia jak najniższych poziomów energetycznych, z
uwzględnieniem zakazu Pauliego.
Elektrony o tej samej wartości głównej liczby kwantowej n tworzą powłokę.
[2(2l+1)]
K (n=1)
L (n=2)
M (n=3)
Dana powłoka dzieli się na podpowłoki, utworzone z elektronów odpowiadających
różnym wartościom orbitalnej liczby kwantowej l.
Elektrony wypełniają powłoki i podpowłoki zaczynając od tych najniżej
położonych (o najniższej energii).
Energia
1 elektron
2 elektrony
stan
podstawowy
5p i 6s o niższej
energii niż 4f
Energia
ZASADY OBSADZANIA
POZIOMÓW
5s o niższej
energii niż 4d
4s o niższej
energii niż 3d
KONFIGURACJE ELEKTRONOWE
Ilość
możliwych
do
obsadzenia stanów dla danej
powłoki określa wartość
głównej liczby kwantowej n.
[2(2l+1)]
[2n2]
K2
2
L8
2
6
M18
2
6
10
N32
2
6
10
14
O50
2
6
10
14
18
2
6
10
14
18
22
2
6
10
14
18
22
P72
Q98
26
Max. liczba elektronów w
podpowłoce o danej wartości
l jest równa wartości lb.
kwantowej m pomnożonej
przez ilość ustawień spinu .
UKŁAD OKRESOWY PIERWIASTKÓW
UKŁAD OKRESOWY PIERWIASTKÓW
Własności chemiczne pierwiastków są ściśle związane z konfiguracją elektronów.
ENERGIA JONIZACJI
Energia jonizacji [eV]
Energia jonizacji [ kJ/mol ]
Uzyskane na podstawie spektroskopii atomowej energie jonizacji (energia
potrzebna do oderwania elektronu z atomu) wskazują na istnienie daleko
posuniętej korelacji pomiędzy pomierzonymi przy pomocy zderzeń atomowych
potencjałami jonizacyjnymi a położeniem pierwiastka w tablicy Mendelejewa
(wewnątrz atomu musi istnieć perfekcyjny porządek, ład i harmonia).
Liczba atomowa Z
ENERGIA JONIZACJI
Energia jonizacji [ kJ/mol ]
Z rozkładu elektronów walencyjnych w atomach widać między innymi, na czym
polega tworzenie okresów w układzie okresowym pierwiastków, gdzie w tym
układzie jest właściwe miejsce wodoru i dlaczego takie a nie inne miejsce zajmują
w nim metale przejściowe, lantanowce, czy aktynowce.
grupy główne
1 - 2 (blok s)
grupy główne
13 - 18 (blok p)
pierwiastki
przejściowe
(blok d)
lantanowce
(blok f)
Liczba atomowa Z
PROMIENIOWANIE RENTGENOWSKIE
Promienie Röntgena (lub inaczej promienie X) promieniowanie elektromagnetyczne o wysokiej
częstotliwości (małej długości fali) powstające w
wyniku przejść elektronowych na najbardziej
wewnętrzne
orbity
atomowe
(podczas
wyhamowywania elektronów o dużej prędkości).
Długość fali promieni rentgenowskich
(RTG) jest rzędu 10-9-10-12 [m], w związku z
czym mają one dużą zdolność przenikania
ciał, jonizują ośrodki przez które przechodzą
i nie są odchylane w polu magnetycznym.
PROMIENIOWANIE RENTGENOWSKIE
Do rejestracji promieniowania rentgenowskiego używa się
fotograficznych, komór jonizacyjnych i liczników Geigera-Müllera.
klisz
Natężenie wiązki promieni rentgenowskich maleje wykładniczo wraz ze
wzrostem grubości absorbenta.
I I 0e
x
I0 - natężenie wiązki padającej
μ - współczynnik absorpcji (w. osłabienia)
x - grubość warstwy
Absorpcja promieni rentgenowskich zależy od rodzaju ciała absorbującego
(pierwiastki ciężkie pochłaniają promienie RTG silniej niż pierwiastki lekkie).
Taka własność promieni RTG umożliwia ich
zastosowanie do diagnostyki medycznej,
defektoskopii rentgenowskiej, itp.…
Należy jednak pamiętać, że długotrwałe
działanie promieni rentgenowskich na
organizm ludzki zwłaszcza o dużym
natężeniu jest szkodliwe.
WIDMO CIĄGŁE I CHARAKTERYSYCZNE
Złożony charakter widma promieniowania rentgenowskiego jest rezultatem
nakładania się dwóch efektów:
• emisji promieniowania hamowania elektronów na anodzie lampy → widmo
hamowania (widmo ciągłe), które rozciąga się od pewnej granicznej długości
fali (λgr) do dowolnie dużych długości fal.
• emisji promieniowania charakterystycznego fotonów o dyskretnych energiach
→ widmo charakterystyczne (widmo liniowe) przyjmujące formę ostrych,
wąskich linii występujących na tle widma hamowania.
widmo ciągłe
λgr
widmo
charakterystyczne
widmo hamowania wolframu
(wraz ze wzrostem napięcia
przyspieszającego elektrony λgr
przesuwa się w stronę fal krótkich)
widmo charakterystyczne (linie serii
K) na tle widma ciągłego molibdenu
WIDMO CIĄGŁE I CHARAKTERYSYCZNE
Istnienie krótkofalowej granicy widma (λgr), wynika z zasady zachowania energii:
E f max Eke
hνgr eU
c
hc
λ
gr
νgr
eU
Kształt widma hamowania i wartość λgr nie zależą od materiału anody.
Widmo charakterystyczne jest widmem liniowym (przejścia elektronów odbywają
się między poziomami energetycznymi o ściśle określonej energii) i zależy od
materiału anody.
PRAWO MOSELEYA
Opisując teoretycznie widmo charakterystyczne można posłużyć wzorem na
długości linii widma optycznego wodoru:
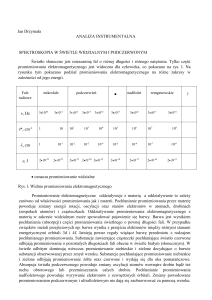
1 ν
1
2 1
RH Z 2 2
λ c
n2 n1
RH - stała Rydberga
Z - liczba atomowa
n12, n22 - niższy i wyższy stan (poziom) energetyczny elektronu
W przypadku promieniowania rentgenowskiego należy jednak uwzględnić fakt,
że na dany elektron oddziałuje nie tylko jądro (o ładunku +Ze), ale i też
osłabiające pole elektryczne jądra inne elektrony (ekranowanie jądra):
1
1
,
2
2
n1
n2
RH cZ - a 2
gdzie a jest stałą ekranowania
PRAWO MOSELEYA
Pierwiastek kwadratowy z częstotliwości danej linii rentgenowskiego
widma charakterystycznego jest liniowo zależny od liczby atomowej .
PRZEJŚCIA ATOMOWE
Konsekwencją oddziaływania promieniowania elektromagnetycznego z materią
jest pochłaniane lub emitowanie energii przez atomy lub cząsteczki materii w
pewnych dyskretnych i skończonych porcjach (kwantach energii).
Kwant energii promieniowania elektromagnetycznego może być przez atom
(cząstkę) pochłonięty lub wypromieniowany w procesie absorpcji lub emisji, co
zawsze prowadzi do zmiany ich energii.
Zgodnie z postulatami Bohra i Plancka oraz złożeniami Einsteina w zjawisku
absorpcji i emisji można wyróżnić trzy procesy:
hν
E2
hν
E
E1
ABSORPCJA
E2
E2
hν
2hν
E
E
E1
EMISJA
SPONTANICZNA
wzbudzanie cząstki przez
pochłonięty kwant energii zachodząca samorzutnie
(foton) przy spełnionym (bez wpływu czynników
warunku Bohra:
zewn.) emisja fotonów
ΔE1,2 = hν = E2 - E1
przez wzbudzone atomy
E1
EMISJA
WYMUSZONA
emisja zgodnych w fazie
(spójnych) fotonów przez
wzbudzony atom w skutek
zderzenia z fotonem o νrez
RÓWNOWAGA TERMICZNA
Jeżeli ciało (zbiór jednakowych atomów) ma stałą temperaturę, to ustala się
równowaga dynamiczna zachodzących jednocześnie trzech procesów (absorpcji
promieniowania, emisji spontanicznej i wymuszonej).
Równowaga ta polega na tym, że liczba fotonów absorbowanych w jednostce
czasu jest równa liczbie fotonów emitowanych w jednostce czasu.
Średnia liczba atomów w stanie wzbudzonym pozostaje również stała w czasie i
podlega rozkładowi Boltzmanna:
N2 N1e
E 2 E1
kT
gdzie:
N1 - liczba w stanie podstawowym o energii E1,
N2 - liczba w wzbudzonym o energii E2,
T - temperatura ciała,
k - stała Boltzmanna.
Z rozkładu Boltzmanna wynika, że obsadzenie poziomów N2 << N1 i w takiej
sytuacji padające na układ promieniowanie jest silnie absorbowane, a emisja
wymuszona odgrywa niewielką rolę.
LASERY
Kluczową sprawą w działaniu lasera jest to, aby przez jakiś czas (chociaż bardzo
krótki) liczba atomów w stanie wzbudzonym była większa niż w stanie
podstawowym (czyli odwrotnie niż normalnie N1 << N2).
Równowagę termiczną między liczbą atomów N1 i N2 można zakłócić w dwojaki
sposób:
• przez rozdzielenie atomów wzbudzonych od atomów niewzbudzonych,
• przez wykorzystanie tzw. metastabilnych stanów atomów (stanów wzbudzonych
o stosunkowo długim czasie życia).
W obu tych przypadkach dla uzyskania
przewagi liczby atomów w stanie
wzbudzonym
należy
doprowadzić
energię z zewnątrz.
Padające na taki układ światło będąc
słabo absorbowanym (mała ilość
atomów w stanie E1) indukuje
jednocześnie przejścia ze stanu E2 do E1
(zapoczątkowana emisja wymuszona
wzmaga natężenie światła co z kolei
wywołuje dalszą emisję wymuszoną).
stan metastabilny
energia
wyjściowa
energia
wejściowa
LASERY
Laser (Light Amplification by Stimulated Emission of Radiation ≡ „ wzmocnienie
światła przez wymuszoną emisję promieniowania”) - urządzenie wytwarzające
spójną (koherentną) i monochromatyczną wiązkę światła (wiązka fotonów o tej
samej częstotliwości, fazie i kierunku drgań) o wąskim przedziale długości i
niezwykle silnym natężeniu.
Podstawą działania laserów (akcji laserowej lub wzmocnienia kwantowego) są
procesy kwantowe, zwane inwersją obsadzenia i pompowaniem optycznym :
• inwersja obsadzenia - przy wzbudzaniu atomów silnym błyskiem świetlnym
krótkotrwała sytuacja, podczas której więcej elektronów znajduje się na
poziomach wzbudzonych niż na poziomie podstawowym;
• pompowanie optyczne - wytworzenie inwersji obsadzenia drogą absorpcji
światła.
emisja spontaniczna fotonów
o różnych kierunkach
zwierciadło
spójne
światło
lasera
zwierciadło
półprzepuszczalne
emisja wymuszona
fotonów
energia wejściowa
TYPY I ZASTOSOWANIE LASERÓW
Najpopularniejsze typy laserów :
• lasery krystaliczne o działaniu impulsowym (np. rubinowy Al2O3 z domieszką
chromu );
• lasery gazowe (atomowe (He-Ne), jonowe (Ar) i molekularne (CO2));
• lasery szklane (materiałem laserowym są tu szkła optyczne aktywowane np.
Nd3+, Yb3+, Er3+, Mo3+ i in.);
• lasery cieczowe (materiałem aktywnym jest wodny lub alkoholowy roztwór
niektórych barwników organicznych);
• lasery półprzewodnikowe i impulsowe z parami metali (np.: Cd, Ge, As, Se, Sn,
Te, Pb, Mg, Ca, Cu czy Zn).
Zastosowania laserów:
• medycyna (w chirurgii i okulistyce - operacje siatkówki oka),
• zapis i przenoszenie sygnałów optycznych (w przestrzeń przez atmosferę np.
Ziemia-Księżyc lub w telekomunikacji - światłowody),
• w handlu (do odczytu kodów paskowych),
• wykrywanie i badanie zanieczyszczeń atmosfery (np. szkodliwych składników
gazów spalinowych),
• w radiolokacji laserowej (pod warunkiem czystości atmosfery);
• w technologii precyzyjnego ciecia i spawania.