UNIWERSYTET PRZYRODNICZY WE WROCŁAWIU
mgr inż. Justyna Sołtysiak
Właściwości biologiczne i ekologiczne inwazyjnych chwastów z rodzaju
rdestowiec (Fallopia spp.) w warunkach miejskich
na przykładzie Wrocławia
Praca doktorska wykonana
w Katedrze Botaniki i Ekologii Roślin
pod kierunkiem
dr hab. inż. Teresy Brej, prof. nadzw.
Wrocław 2012
Składam gorące podziękowania
Pani dr hab. Teresie Brej, prof. nadzw.
za przekazaną wiedzę
oraz zaangażowanie i pomoc
w realizacji niniejszej pracy doktorskiej
SPIS TREŚCI
SPIS TREŚCI ---------------------------------------------------------------------------------------------------------- 3
1.
WSTĘP----------------------------------------------------------------------------------------------------------- 4
2.
CEL I ZAKRES PRACY -------------------------------------------------------------------------------------- 7
3.
INWAZJE BIOLOGICZNE – WYMIAR GLOBALNY ZJAWISKA--------------------------------- 8
4.
GATUNKI Z RODZAJU RDESTOWIEC, FALLOPIA – JAKO OBIEKTY BADAŃ --------- 12
4.1. POZYCJA TAKSONOMICZNA BADANYCH RDESTOWCÓW --------------------------------4.2. NATURALNE I ANTROPOGENICZNE ROZMIESZCZENIE GEOGRAFICZNE
TAKSONÓW Z RODZAJU FALLOPIA --------------------------------------------------------------4.3. PRZYKŁADY INWAZJI RDESTOWCÓW POZA NATURALNYM ZASIĘGIEM
WYSTĘPOWANIA---------------------------------------------------------------------------------------4.4. WYBRANE WŁAŚCIWOŚCI MORFOLOGICZNE RDESTOWCÓW ---------------------------
12
14
18
21
5.
WROCŁAW JAKO TEREN PROWADZONYCH BADAŃ----------------------------------------- 26
6.
METODYKA BADAŃ -------------------------------------------------------------------------------------- 29
6.1. BADANIA TERENOWE -------------------------------------------------------------------------------6.2. DOŚWIADCZENIA WAZONOWE ------------------------------------------------------------------6.3. PRACE LABORATORYJNE ---------------------------------------------------------------------------6.3.1.
ANALIZY CHEMICZNE------------------------------------------------------------------------6.3.2.
OKREŚLENIE PLOIDALNOŚCI RDESTOWCÓW ----------------------------------------6.3.3.
STATYSTYCZNA ANALIZA DANYCH ------------------------------------------------------
7.
29
37
39
39
40
40
WYNIKI BADAŃ -------------------------------------------------------------------------------------------- 41
7.1. BADANIA TERENOWE W OBSZARZE WROCŁAWIA ----------------------------------------- 41
7.1.1.
ROZMIESZCZENIE SKUPISK RDESTOWCÓW ------------------------------------------- 41
7.1.2.
WŁAŚCIWOŚCI CHEMICZNE GLEB --------------------------------------------------------- 61
7.1.3.
CHARAKTERYSTYKA WYBRANYCH KLONÓW RDESTOWCÓW ------------------- 66
7.1.4.
DYNAMIKA WZROSTU ORAZ PRZEBIEG FAZ ROZWOJOWYCH RDESTOWCÓW
W WARUNKACH MIEJSKICH ----------------------------------------------------------------- 72
7.2. WYNIKI DOŚWIADCZEŃ WAZONOWYCH------------------------------------------------------ 85
7.2.1.
WPŁYW METALI CIĘŻKICH NA PRZEBIEG WZROSTU I ROZWOJU
RDESTOWCÓW ----------------------------------------------------------------------------------- 85
7.2.2.
AKUMULACJA METALI CIĘŻKICH W NADZIEMNYCH I PODZIEMNYCH
CZĘŚCIACH RDESTOWCÓW ------------------------------------------------------------------ 96
8.
DYSKUSJA WYNIKÓW ----------------------------------------------------------------------------------- 101
9.
PODSUMOWANIE WYNIKÓW BADAŃ I WNIOSKI -------------------------------------------- 114
10.
LITERATURA ---------------------------------------------------------------------------------------------- 118
11.
ZAŁĄCZNIKI ----------------------------------------------------------------------------------------------- 131
3
1. WSTĘP
Szata roślinna poszczególnych rejonów Ziemi ukształtowała się na przestrzeni
miliardów lat. Pod wpływem czynników klimatycznych oraz procesów geologicznych
zachodziły
w
biosferze
naturalne
zmiany,
mające
swe
odzwierciedlenie
w rozmieszczeniu i składzie gatunkowym współczesnych zbiorowisk roślinnych.
W miarę upływu czasu istotnym elementem determinującym przeobrażenia
świata ożywionego stał się człowiek, który spowodował globalną migrację gatunków.
Początkiem przemieszczania się elementów flory były wędrówki ludów pierwotnych,
z którymi „wędrowały” owoce i nasiona roślin. Za szczególnie ważny dla flory
centralnej Europy, uważa się okres neolitu, w którym rozwój rolnictwa przyczynił się
do synantropizacji szaty roślinnej [Kornaś 1990]. W zbiorowiskach towarzyszących
człowiekowi obok reprezentantów flory rodzimej (apofitów) coraz częściej pojawiali się
obcy przybysze (antropofity), zawlekani celowo lub przypadkowo do nowej ojczyzny
z różnych zakątków świata. Istotnym punktem w historii wędrówek roślinnych był rok
1492 – odkrycie przez Krzysztofa Kolumba Ameryki. Umożliwiło to swobodne
przemieszczanie się roślin pomiędzy starym a nowym kontynentem, poza naturalnymi
barierami środowiska takimi, jak pasma górskie czy oceany.
Czas przybycia nowych gatunków roślin na kontynent europejski był podstawą
do wyodrębnienia wśród nich dwóch grup: archeofitów – przybyłych przed końcem XV
wieku oraz kenofitów (neofitów1) – zawleczonych i osiedlonych w Europie po roku
1492 [Kornaś 1972].
Współcześnie udział antropofitów we florach poszczególnych rejonów świata
wykazuje duże zróżnicowanie. Największą liczbę zadomowionych roślin obcego
pochodzenia (ponad 2000 gatunków) odnotowano w Stanach Zjednoczonych Ameryki
oraz w Australii [Vitousek i in. 1997]. Szacuje się, że na wyspach oceanicznych gatunki
obce mogą stanowić nawet ponad 50% miejscowej roślinności [Sharma i in. 2005].
1
W literaturze zagranicznej gatunki zasiedlające Europę po XV wieku określane są wyłącznie mianem neofitów
[Wittig 2004].
4
Lista roślin przybyłych do Polski przed końcem XV wieku zawiera 140
gatunków [Zając i Zając 1975 cyt. za: Tokarska-Guzik 2003]. Pierwsze zestawienie
dotyczące trwale zadomowionych na terenie kraju kenofitów pochodzi z roku 1968
i obejmuje 117 gatunków [Kornaś 1968 cyt. za: Tokarska-Guzik 2003]. Trzy dekady
później ich liczbę oszacowano już na 251 gatunków [Zając i in. 1998]. Obecnie
w Polsce występuje 1017 obcych gatunków roślin, 460 z nich to gatunki zadomowione,
które reprezentowane są przez 160 archeofitów i 300 kenofitów [Tokarska-Guzik 2005].
Wśród gatunków obcych najpoważniejsze zagrożenie dla różnorodności biologicznej
stanowią kenofity (neofity). Niektóre z nich, określane mianem „inwajderów” (z ang.
invider – najeźdźca), wywołują poważne straty w środowisku przyrodniczym drogą
intensywnej ekspansji.
Naukowcy główną winą za narastające zjawiska inwazji biologicznych
obarczają człowieka [Vitousek i in. 1997; McKinney 2006]. Do najważniejszych
czynników odpowiedzialnych za ten stan rzeczy zaliczane jest wprowadzanie do
uprawy nowych, obcych gatunków, otwieranie dodatkowych dróg migracji oraz
udostępnianie do kolonizacji nowych siedlisk [Faliński 2004].
O podatności ekosystemów na ekspansje gatunków obcych decydują ich
właściwości ekologiczne. Do szczególnie narażonych na masowe inwazje biologiczne
należą ekosystemy miejskie [Żołnierz i Antczak 2005], których rozwój jest procesem
niekontrolowanym pod względem presji człowieka na środowisko naturalne
[Szymanowski 2004]. Flora miast w środkowej części Europy charakteryzuje się dużą
liczbą gatunków nierodzimych, zwłaszcza neofitów [Witting 2004]. Według Pyška
[1998] udział gatunków obcych w europejskich miastach wynosi średnio 40%, z czego
15% przypada na archeofity, a 25% na neofity.
Poszerzanie zasięgu szlaków migracyjnych (drogi, autostrady, linie tramwajowe
i kolejowe) czy rozbudowa potencjalnych ośrodków rozprzestrzeniania się gatunków
(parki, ogrody miejskie i ogródki działkowe) to tylko niektóre elementy działalności
ludzkiej, sprzyjające domestyfikacji roślin obcych [Wittig 2004; Vilá i in. 2007].
Istotnym wykładnikiem antropopresji w miastach, wpływającym na stan lokalnej flory
są modyfikacje warunków środowiska.
Zjawiskiem występującym powszechnie w dużych aglomeracjach jest tak zwana
miejska wyspa ciepła [McDonnell i in. 1997; Crutzen 2004], która propaguje rozwój
termofilnych gatunków obcego pochodzenia [Wittig 2004]. Inną cechą obszarów
zurbanizowanych jest zmiana bilansu wodnego, wskutek czego miasta odznaczają się
5
większą suchością powietrza, niż tereny do nich przyległe. Ponadto, w środowiskach
miejskich występują wysokie koncentracje polutantów pyłowych i gazowych. Gleby
miejskie są często zasolone i zanieczyszczone metalami ciężkimi. Środowisko miejskie
stwarza więc trudne warunki dla bytujących w nim organizmów roślinnych.
Tymczasem szeroka skala tolerancji oraz możliwość szybkiego dostosowania się do
zmieniających właściwości środowiska to główne cechy roślin inwazyjnych [Kornaś
1990; Bradley i in. 2010].
Wśród przykładów inwazyjnych gatunków roślin występujących w naszym
kraju na szczególną uwagę zasługują azjatyckie chwasty z rodzaju Fallopia
(rdestowiec): Fallopia japonica var. japonica (rdestowiec japoński), Fallopia
sachalinensis
(rdestowiec
sachaliński)
oraz
ich
mieszaniec
–
Fallopia
× bohemica (rdestowiec pośredni). Wymienione gatunki preferują silnie przekształcone
siedliska antropogeniczne [Child i Waal 1997; Mandák i in. 2004]. W miastach, gdzie
szybko zwiększają swój areał opanowują tereny ruderalne np. przydroża, wysypiska,
gruzowiska, nasypy kolejowe, a także podmiejskie łąki i tereny nadrzeczne. Spotkać je
można w parkach i ogrodach, do których zazwyczaj zostały wprowadzone jako rośliny
ozdobne. Rdestowce zasiedlają również obszary o wysokich koncentracjach metali
ciężkich w glebie (np. tereny poprzemysłowe, pobocza autostrad). To zagadnienie nie
było jednak jeszcze szczegółowo badane.
Specyficzne właściwości miast, o których wspomniano wcześniej mogą
protegować rozprzestrzenianie się gatunków z rodzaju Fallopia. Na tym tle pojawiają
się pytania i problemy związane z biologią i ekologią rdestowców, pozwalającą im
odnosić niezwykły sukces kolonizacyjny w ekosystemach miejskich.
6
2. CEL I ZAKRES PRACY
Praca dotyczy zagadnień biologicznych, związanych ze zjawiskiem postępującej
na terenie Wrocławia inwazji azjatyckich gatunków roślin z rodzaju rdestowiec,
Fallopia. Celem pracy było określenie wpływu ekosystemu miejskiego (na przykładzie
Wrocławia) na wybrane właściwości biologiczne i ekologiczne trzech gatunków
rdestowców: Fallopia japonica var. japonica (Houtt.) Ronse Decraense, Fallopia
× bohemica (Chrtek et Chrtková) J.P. Bailey i Fallopia sachalinensis (F.W. Schmidt
ex Maxim.) Nakai. W trakcie czteroletnich badań podjęto realizację następujących
zadań:
•
Przedstawienie wzorców rozmieszczenia skupisk poszczególnych taksonów
rdestowców w powiązaniu z warunkami ekologicznymi miasta (topografia
zabudowy miejskiej, czynniki klimatyczne i edaficzne).
•
Bliższe określenie badanych gatunków z rodzaju Fallopia – zwłaszcza ich pozycji
taksonomicznej, głównych cech morfologicznych i przyczyn inwazji.
•
Określenie dynamiki wzrostu i rozwoju rdestowców – w oparciu o przebieg faz
rozwojowych, z uwzględnieniem specyfiki warunków miejskich.
•
Poznanie reakcji badanych gatunków z rodzaju Fallopia na nadmiar metali ciężkich
(cynk, ołów, miedź, chrom i kadm) – znamiennych dla środowiska dużych miast.
Wyżej sformułowany zakres pracy oparto na badaniach terenowych, które rozszerzono
o doświadczenia szklarniowe. Uzyskano w ten sposób pełniejszy obraz reakcji
badanych gatunków roślin na ekologiczne warunki miasta.
7
3. INWAZJE BIOLOGICZNE – WYMIAR GLOBALNY
ZJAWISKA
Pojęcie inwazji biologicznej odnosi się do wszystkich grup organizmów żywych
[Di Castri 1990]. Według Global Invasive Species Programme [2011] organizmy
inwazyjne (IAS) (ang. invasive alien species) to gatunki nierodzime, które wywierają
szkodliwe efekty na środowisko i ekonomię, są niebezpieczne dla zdrowia człowieka,
a ich introdukcja i (lub) rozprzestrzenianie zagraża różnorodności biologicznej.
Podobną definicję znaleźć można w krajowej literaturze. Tokarska-Guzik [2002]
podaje,
że
gatunki
inwazyjne
to
nierodzime
organizmy
wywołujące
lub
charakteryzujące się potencjalnymi możliwościami wywołania szkód w środowisku,
strat ekonomicznych lub stwarzające zagrożenie dla zdrowia ludzi. Według Di Castri
[1990] za inwazyjny uznawany jest ten gatunek, który został przetransportowany
przypadkowo lub celowo przez człowieka i rozprzestrzenia się masowo poza swoim
naturalnym zasięgiem występowania.
Wiadomo, że nie każdy sprowadzony gatunek wykazuje właściwości inwazyjne.
Zgodnie z regułą zaproponowaną przez Williamsona [1993] jeden na dziesięć
sprowadzonych obcych gatunków udaje się introdukować introdukcji, natomiast jedna
na dziesięć introdukcji kończy się zadomowieniem w nowej ojczyźnie, a tylko jeden na
dziesięć zadomowionych obcych gatunków zdolny jest do inwazji biologicznej.
Faliński [2004] definiuje inwazję biologiczną jako: “jedną z form ekspansji
gatunku, czyli wypróbowanych przez przyrodę sposobów powiększania i umacniania
swego stanu posiadania”. Ten sam autor powołując się na Eltona [1958] wyjaśnia, że
inwazja biologiczna wyraża się gwałtownym i masowym wkraczaniem gatunku na
nowe, niezdobyte dotąd stanowiska i terytoria, dzięki możliwości przekraczania barier
geograficznych.
Proces inwazji biologicznej przebiega w trzech etapach [Di Castri 1990].
Pierwszym z nich jest introdukcja, czyli wprowadzenie gatunku do nowego środowiska
[Di Castri 1990; Heger i Trepl 2003; Sharma 2005]. Zjawisko to, jak już wcześniej
wspomniano, może mieć charakter świadomy (sprowadzanie w celach użytkowych) lub
przypadkowy [Sharma 2005]. Obecnie szacuje się, że w różnych rejonach świata
zadomowionych jest aż 30 000 gatunków roślin egzotycznych, sprowadzonych na nowe
tereny w celach uprawnych [Pimentel i in. 2007]. Jednak za główne źródła nowych
inwazji uważa się niezamierzone introdukcje [Solarz 2007].
8
Kluczowym etapem pomyślnie zakończonej introdukcji jest weryfikacja
przybyłych propagul pod względem ich zdolności do rozwoju i tworzenia nowych
pokoleń [Fabiszewski i Brej 2005]. Po zakończonej introdukcji werbunek osobników
potomnych uzależniony jest od dostępności siedlisk dla nowych kolonizatorów oraz od
tempa przeżywalności przybywających propagul [Fabiszewski i Brej 2005]. Spośród
ogromnej ich liczby duża część ginie, głównie w wyniku niekorzystnych warunków
środowiska [Williamson 1996], a czynnikiem dokonującym silnej selekcji jest klimat.
Największe szanse mają rośliny, które na nowym obszarze natrafiły na warunki
klimatyczne podobne do regionów, z których pochodzą.
Kolejny etap inwazji – kolonizacja następuje, gdy rośliny w trwałej już populacji
rozmnażają się, a populacja staje się samowystarczalna [Fabiszewski i Brej 2005].
Trwała kolonizacja prowadzi do ostatniego stadium inwazji biologicznej, którym jest
naturalizacja populacji w nowym środowisku [Faliński 2004; Sharma 2005]. Gatunek,
który uległ naturalizacji (zadomowieniu) włącza się do miejscowej flory. Ze względu na
zdolność do skutecznego rozmnażania i rozprzestrzeniania, stanowi poważne
zagrożenie dla lokalnej przyrody [Richardson i in. 2000].
Pomimo licznych badań nad zjawiskiem inwazji biologicznych badacze wciąż
stawiają fundamentalne pytania: (1) jakie cechy czynią dany gatunek inwazyjnym oraz
(2) dlaczego jedne ekosystemy są bardziej podatne na inwazje niż inne? [Rejmánek
1995].
Rośliny inwazyjne to grupa bardzo zróżnicowana, a ich fenomen wyjaśniany jest
na poziomie genetycznym, morfologicznym, fizjologicznym i ekologicznym. Zdolności
do inwazji wykazują gatunki charakteryzujące się między innymi: dużą liczbą
produkowanych nasion, szybkim i skutecznym transportem materiału biologicznego,
efektywnym rozmnażaniem, szybkim wzrostem biomasy, krótkim okresem stadium
juwenilnego, dużymi rozmiarami, a także zmiennością fenotypową czy zdolnością do
tworzenia mieszańców z gatunkami pokrewnymi na drodze hybrydyzacji [Jackowiak
1999; Faliński 2004; Sharma i in. 2005; Ellstrand 2009]. To ostatnie zagadnienie jest
ostatnimi czasy szczególnie badane.
We współczesnej literaturze zwraca się także uwagę na potencjalne zdolności
roślin inwazyjnych do oddziaływania allelopatycznego [Hierro i Callaway 2003;
Gniazdowiska 2005; Vichotová i Šerá 2008].
9
Davis i in. [2000] wskazuje trzy czynniki, mające największy wpływ na przebieg
procesu inwazji biologicznej. Oprócz liczby propagul napływających do środowiska
(tzw. presji propagul) i specyficznych właściwości gatunków inwazyjnych, znacząca
jest podatność środowisk na inwazje biologiczne. Poszczególne ekosystemy wykazują
różny stopień wrażliwości na inwazje biologiczne. Gatunki wchodzące w skład
biocenozy
powiązane
są
ze
sobą
wzajemnymi
zależnościami.
Im
większa
bioróżnorodność tym silniejsze oddziaływania międzygatunkowe i mniejsza liczba
otwartych na nowo przybyłe gatunki nisz. Na tej podstawie powstała hipoteza
“bogactwa gatunkowego”. Zgodnie z nią, w wielu przypadkach silne interakcje
pomiędzy gatunkami mogą ograniczać lub całkowicie uniemożliwić ekspansję roślin
obcych. Inną, równie często przywoływaną przez badaczy hipotezą jest zaproponowana
przez Darwina w 1859 roku hipoteza “wrogów naturalnych” [Hierro i Callaway 2003].
Mówi ona, że brak wyspecjalizowanych wrogów naturalnych (roślinożerców
i patogenów), kontrolujących liczebność przybyłych gatunków przyczynia się do ich
sukcesu w nowych ekosystemach [Sharma i in. 2005]. Niestety, żadna z licznych,
funkcjonujących w literaturze hipotez nie wyjaśnia do końca istoty procesu
współczesnych inwazji biologicznych.
Ekologiczne skutki biologicznych inwazji dotyczą wszystkich poziomów
organizacji życia: poszczególnych osobników, gatunków, populacji, zbiorowisk oraz
całych ekosystemów [Van der Velde i in. 2006]. Gatunki inwazyjne mogą wywoływać
redukcję wzrostu i rozwoju u gatunków rodzimych. W wyniku skutecznej konkurencji
gatunki lokalne szybko wypierane są ze środowiska, dlatego obecność w ekosystemach
gatunków inwazyjnych uważana jest powszechnie za poważne zagrożenie dla
bioróżnorodności [Vitousek i in. 1997; Scalera 2010]. Gatunki inwazyjne wpływają na
pulę genową lokalnych populacji poprzez spontaniczne krzyżowanie się z osobnikami
pokrewnymi i tworzenie form mieszańcowych. Badania pokazują, że nowo powstałe
hybrydy mają często większe predyspozycje do inwazji, niż rodzicielskie formy [Lee
2002]. Obecność gatunków inwazyjnych działała także destrukcyjnie na zależności
troficzne w ekosystemach i modyfikuje właściwości siedliska [Sharma i in. 2005].
Rośliny inwazyjne powodują także wymierne skutki ekonomiczne, gdyż walka
z nimi wymaga wielu wysiłków i poważnych nakładów finansowych. Pimentel i in.
[2007] podaje, że światowe coroczne, ogólne koszty związane z inwazjami
biologicznymi szacowane są w setkach milionów lub nawet miliardach dolarów.
10
Na przykład roczne koszty związane z walką na terenie Ameryki Północnej z inwazyjną
krwawnicą pospolitą (Lythrum salicaria) wynoszą 45 milionów dolarów [Van der
Velde i in. 2006]. Według Macka i in. [2000], inwazje biologiczne powodują
w gospodarce światowej rocznie straty w wysokości 1,4 miliardów dolarów. Na
przykład, w Indiach każdego roku straty w rolnictwie spowodowane przez
zadomowione chwasty obcego pochodzenia dochodzą do 30% wartości produkcji
[Pimentel i in. 2007]. W ciągu ostatnich 15 lat z budżetu Unii Europejskiej
sfinansowano
niemal
300
projektów
badawczych,
poświeconych
problemom
wywołanym przez gatunki inwazyjne, o wartości przekraczającej 132 milionów euro
[Scalera 2010].
Znany jest także wpływ gatunków inwazyjnych na zdrowie i życie człowieka.
Introdukowane organizmy mogą być powodem niebezpiecznych dla człowieka
i zwierząt chorób. Niektóre z nich, np. obce gatunki z rodzaju Heracleum ze względu na
obecność fotodynamicznych związków powodują poparzenia skóry [Pyšek i in. 2010],
inne, jak Ambrosia artemisiifolia tworzą pyłek wywołujący u człowieka poważne
alergie [Wayne i in. 2002].
Obecnie, wiele organizacji międzynarodowych, między innnymi Global Invasive
Species Programme (GISP), Invasive Species Specialist Group (ISSG) czy Cooperative
Islands Initiative (CII) pracuje nad zasadami działania, które mogą pomóc w usuwaniu
niechcianych przybyszów.
W Polsce gatunkom obcym i inwazyjnym poświęca się wciąż za mało uwagi.
Brak jest np. jednoznacznych przepisów prawnych dotyczących kwestii zwalczania
gatunków obcych [Radecki 2009], ważnej z punktu widzenia ochrony rodzimej fauny
i flory. Najbardziej aktualne dane, dotyczące gatunków obcych, występujących na
terenie naszego kraju można znaleźć w bazie Instytutu Ochrony Przyrody PAN
w Krakowie „Gatunki obce w Polsce”. Obecnie, baza ta obejmuje wykaz 1202 obcych
gatunków roślin, zwierząt oraz grzybów.
11
4. GATUNKI Z RODZAJU RDESTOWIEC, FALLOPIA –
JAKO OBIEKTY BADAŃ
4.1. POZYCJA TAKSONOMICZNA BADANYCH RDESTOWCÓW
W warunkach miejskich Wrocławia badaniami objęto trzy wysoce inwazyjne
gatunki roślin:
•
Fallopia japonica var. japonica (Houtt.) Ronse Decraene var. japonica, [syn.:
Polygonum cuspidatum Sieb. et Zucc., Reynoutria japonica Houtt.], rdestowiec
ostrokończysty = rdestowiec japoński
•
Fallopia sachalinensis (F.W. Schmidt ex Maxim.) Nakai [syn.: Polygonum
sachalinense F. Schmidt, Reynoutria sachalinensis (F. Schmidt) Nakai], rdestowiec
sachaliński
•
Fallopia × bohemica (Chrtek et Chrtková) J.P. Bailey [syn.: Polygonum
× bohemicum (Chrtek et Chrtková) P.F. Zika et A.L. Jacobson, Reynoutria
× bohemica Chrtek et Chrtková], rdestowiec pośredni
Pomimo licznych badań nad rdestowcami, nadal istnieje sporo niejasności
w kwestii ich nazewnictwa i przynależności taksonomicznej. W literaturze spotkać
można trzy sposoby klasyfikacji rdestowców. Mandák i in. [2003] podaje, że niektórzy
badacze zaliczają wymienione gatunki do rodzaju Reynoutria. Inni, za Zicą
i Jacobsonem [2003] rozpatrują rodzaj Fallopia wraz z rodzajem Reynoutria jako
taksonomiczny synonim rodzaju Polygonum [Mandák i in. 2005]. Takie ujęcie
systematyczne preferują między innymi Zhou i in. [2003], Jacob [2006] czy Barney i in.
[2006].
Natomiast
Ronse
Decraene
i
Akeroyd
[1998]
oraz
Bailey
i Stace [1992] zaliczają wymienione gatunki do rodzaju Fallopia, wydzielając w jego
obrębie sekcję Reynoutria. Bailey i Stace [1992] podkreślają, że badania cytologiczne
wyraźnie uzasadniają konieczność wyłączenia rdestowców z rodzaju Polygonum. Ten
typ klasyfikacji spotykamy także w publikacjach Beerlinga i in. [1994; 1995]
Hollingswortha i in. [1998; 1999; 2000] oraz Marigo i Pautou [1998].
Niedostatecznie wyjaśniona jest taksonomia rdestowców także w krajach ich
naturalnego występowania. Szczególnym przedmiotem rozważań jest rdestowiec
japoński. W Japonii opisano następujące odmiany tego gatunku: Fallopia japonica
(Houtt.) Ronse Decraene var. japonica, Fallopia japonica var. compacta (Hooker fil.)
12
J.P.
Bailey,
Fallopia
japonica
var.
uzenensis
(Honda)
K.Yonekura
& Ohashi oraz Fallopia japonica var. terminalis (comb. nova).
W Chinach rdestowiec japoński pierwotnie został zaklasyfikowany jako Fallopia
forbesii (Hance) Yonekura et O. Ohashi oraz Reynoutria elliptica (Koisz.) Migo
ex Naki (syn.) [Bailey 2003], jednak w najnowszej florze Chin – opracowanej przez
Zhengy`ego i Ravela [2003] wymienione wyżej taksowy nazwane zostały Fallopia
forbesii i Reynoutria japonica i uznawane są za chińską i japońską odmianę tego
samego gatunku [Bailey i Wisskirchen 2006]. Natomiast we florze Korei występują:
Fallopia forbesii i Fallopia japonica var. japonica [Kim i Park 2000].
Nieścisłości taksonomiczne dotyczą także międzygatunkowego mieszańca
opisanego po raz pierwszy na terenie Europy jako Fallopia × bohemica (Chrtek
et Chrtková) J.P. Bailey. W obrębie naturalnego zasięgu występowania gatunków
rodzicielskich, mieszaniec ten został rozpoznany jedynie w Japonii i oznaczony jako
Reynoutria × mizushimae Yokouchi ex T. Shimizu [Bailey 2003].
Ze względu na problemy taksonomiczne w obrębie rodzaju, wszystkie gatunki
i ich mieszańce określane są często w literaturze zagranicznej w szerokim znaczeniu
jako Japanese Knotweed s.l. [Bailey 2003; Bailey i Wisskirchen 2006; Bailey i in. 2007;
Bailey i in. 2008].
W niniejszej pracy przyjęto klasyfikację i nazewnictwo za Ronse Decraene
i Akeroyd [1998] oraz Bailey i Stace [1992], posługując się nazwą rodzajową Fallopia.
Nazwa „Fallopia” jest też stosowana w publikacjach wszystkich autorów anglosaskich.
W literaturze krajowej natomiast preferowana jest nazwa rodzajowa „Reynoutria” –
według Mirka i in. [1995].
13
4.2. NATURALNE I ANTROPOGENICZNE ROZMIESZCZENIE
GEOGRAFICZNE TAKSONÓW Z RODZAJU FALLOPIA
Pierwotny zasięg geograficzny rdestowców pokazano w tab. 1. Przedstawiciele
z rodzaju Fallopia to gatunki wschodnioazjatyckie, a najszerszy zasięg występowania
ma Fallopia japonica. Obejmuje on Japonię, Chiny, Północną i Południową Koreę oraz
Tajwan [Sukopp i Sukopp 1988; Beerling i in. 1994; Beerling i in. 1995; Bailey 2003;
Bailey i in. 2007]. W Japonii jest rośliną dziko rosnącą i rozprzestrzenia się wzdłuż
dróg i autostrad, zyskując miano jednego z najbardziej uciążliwych chwastów [Sukopp i
Sukopp 1988]. Rośnie także na znacznych wysokościach (2400–3800 m.n.p.m)
[Beerling i in. 1994]. W krajach azjatyckich, górska odmiana rdestowca
ostrokończystego (Fallopia japonica var. compacta) jest ważnym składnikiem
pionierskich stadiów sukcesyjnych na glebach wulkanicznych, występuje między
innymi na górze Fidżi [Maruta 1994; Adachi i in. 1996; Zhou i in. 2003]. Wśród
azjatyckich odmian rdestowca japońskiego są też endemity, jak np. Fallopia japonica
var. terminali, który spotykany jest wyłącznie na wyspach Izu [Bailey 2003].
Rdestowiec sachaliński w naturze występuje w Japonii, Korei, Sachalinie oraz
na izolowanej wyspie Ullung-do [Sukoppn i Starfinger 1995; Bailey 2003; Bailey i in.
2008]. Gatunek ten preferuje tereny niżej położone, rośnie w dolinach górskich rzek.
Porasta także wybrzeża klifowe [Bailey i in. 2008]. Sporadycznie znajdowany jest na
wysokościach od 900 do 1000 m.n.p.m. [Sukopp i Starfinger 1995].
Fallopia japonica (var. japonica) i Fallopia sachalinensis rozprzestrzeniły się
daleko poza granicami naturalnego zasięgu (rys. 1 i 2). Obecnie spotykane są
w większości krajów europejskich – od Półwyspu Skandynawskiego (Norwegia,
Finlandia), poprzez centrum kontynentu – aż w Bułgarii i Portugalii [Beerling i in.
1994]. Nieliczne stanowiska rdestowców odnotowano również w rejonie Morza
Śródziemnego; brak jest danych dotyczących ich występowania we Włoszech, Albanii,
a także w europejskiej części Turcji i Rosji [Bailey 2003; Alberternst i Bőhmer 2006;
Bailey i in. 2007]. Poza Europą, wtórny zasięg rdestowców japońskiego i
sachalińskiego obejmuje Amerykę Północną [Seiger 1997; Barney i in. 2006] oraz
Australię i Nową Zelandię [Berling i in. 1994; Alberternst i Bőhmer 2006; Bailey i in.
2007; Bailey i in. 2008]. Fallopia japonica występuje na znacznej części terytorium
Kanady – od Ontario i Quebec'u, przez Nową Fundlandię – po Wyspę Księcia Edwarda.
W Stanach Zjednoczonych (część północno–wschodnia) rdestowiec japoński jest
14
spotykany w obszarze stanowiącym 71% powierzchni całego kraju. Występuje w
okolicach rzeki Mississippi oraz na półpustynnych terenach stanów Colorado i Utah
[Seiger 1997; Barney i in. 2006]. Izolowane populacje tego gatunku odnotowano także
na Alasce [Barney i in. 2006].
Zasięg geograficzny Fallopia × bohemica (z niewielkimi wyjątkami) pokrywa
się z obszarem występowania jego osobników rodzicielskich (rys. 3). Rdestowiec
pośredni szybko rozprzestrzenia się w północnej i centralnej części Europy [Bailey
i Stace 1992; Mandák i in. 2004; Bailey i Wisskirchen 2006; Bailey i in. 2007]. Jego
obecność potwierdzono między innymi w: Czechach, Polsce, Francji, Niemczech
i Wielkiej Brytanii [Bailey i in. 1996; Fojcik i Tokarska-Guzik 2000; Mandák i in.
2004; Bailey i Wisskirchen 2006]. Poza kontynentem europejskim, klony Fallopia
× bohemica zostały zidentyfikowane w Ameryce Północnej, Nowej Zelandii i Australii
[Bailey 2003; Zika i Jacobson 2003; Gammon i Kesseli 2010]. Potwierdzono także
obecność rdestowca pośredniego w krajach azjatyckich, na obszarze naturalnego
występowania Fallopia japonica i Fallopia sachalinensis. Klony mieszańca
zidentyfikowane przez Yokouchi jako Reynoutria × mizushimae [Bailey 2003; Mandák
i in. 2004] odnaleziono także na japońskiej wyspie Honshu [Bailey 2003].
Tab. 1 Pierwotny zasięg przedstawicieli z rodzaju Fallopia (według Baileya, 2003)
Takson
Fallopia japonica var. japonica
Pierwotny zasięg geograficzny
Japonia
Fallopia japonica var. compacta
Wyspy: Honshu, Kyushu i Shikoku
Szczyty gór i wulkanów
Wyspa Honshu i południe kraju
Fallopia japonica var. uzenensis
Obszary nad Morzem Japońskim i północno–
wschodnia część Honshu
Fallopia japonica var. terminalis
Wyspy Izu
Fallopia japonica
Fallopia forbseii (Fallopia elliptica)
Fallopia sachalinensis
Fallopia × bohemica
(F. japonica × F. sachalinensis)
Wyspy Amami- Oshima, Tokumo-shima
Chiny
Korea
Szeroko rozprzestrzeniony w obu krajach
Japonia
Hokkaido i północno–zachodnia Honshu
USSR
Wyspa Sakhalin
Korea
Wyspa Ullung
Japonia
Północno–zachodnia część wyspy Honshu
15
Rys. 1. Pierwotny i wtórny zasięg rdestowca japońskiego (według Jegra, 1995)
Rys. 2. Pierwotny i wtórny zasięg rdestowca sachalińskiego (według Jegra, 1995)
Pierwotny zasięg
Wtórny zasięg
16
Rys. 3. Rozmieczenie rdestowca pośredniego na terenie Europy
(według Baileya i Wisskirchena, 2006)
17
4.3. PRZYKŁADY INWAZJI RDESTOWCÓW POZA NATURALNYM
ZASIĘGIEM WYSTĘPOWANIA
Europejska historia migracji gatunków z rodzaju Fallopia rozpoczęła się w XIX
wieku. Pierwsze okazy Fallopia japonica zostały sprowadzone z Chin w 1825 roku
[Conolly 1977] i posadzone w jednym z okręgów Londynu – Chiswick, gdzie nie
przetrwały [Bailey i Conolly 2000]. Nowy klon rdestowca japońskiego sprowadził w
1840 roku Philippe von Siebold, rozpoczynając jego hodowlę w założonej przez siebie
szkółce w Leiden (zachodnia Holandia). W roku 1847 gatunek ten został nagrodzony
złotym medalem przez Towarzystwo Rolnicze i Ogrodnicze (Society of Agriculture
i Horticulture) w Utrechcie – jako najbardziej interesująca roślina ozdobna, a od roku
1848 dostępny był w sprzedaży [Bailey i Conolly 2000]. Rdestowiec japoński,
zachwalany w fachowych czasopismach, szybko zyskał popularność. Podkreślano nie
tylko jego walory dekoracyjne, ale i przydatność do celów medycznych [Bailey
i Conolly 2000]. W Europie Środkowej rdestowiec ostrokończysty wykorzystywany był
jako roślina paszowa, a podczas II Wojny Światowej jego liści używano do wyrobu
papierosów [Beerling i in. 1994].
Do Ameryki Północnej rdestowiec japoński został sprowadzony w 1902 roku
[Higgins 1977 cyt. za: Beerling i in. 1994], a do Nowej Zelandii trafił w roku 1935
[Webb i in. 1988 cyt. za: Beerling i in. 1994], gdzie używany był często do umacniania
skarp, wydm i hałd pokopalnianych [Child i Wade 2000]. W Europie najwcześniejsze
doniesienia o ucieczkach tego gatunku z hodowli pochodzą z Niemiec (Rhur) i Wielkiej
Brytanii (Walia) [Conolly 1977]. Pierwsze wzmianki o pojawieniu się dzikich
stanowisk rdestowca japońskiego na ziemiach polskich sięgają drugiej połowy XIX. W
roku 1882 rdestowiec ostrokończysty notowany był na terenie Gniezna, a w 1893 we
Wrocławiu, rok później na Pobrzeżu Bałtyku, a następnie na Górnym Śląsku [TokarskaGuzik 2005].
Drugi z rdestowców – Fallopia sachalinensis był kilkukrotnie sprowadzany do
Europy [Mandák i in. 2004]. Najważniejszą rolę w rozprzestrzenieniu się tego gatunku
odegrały ogrody botaniczne, zwłaszcza Ogród Botaniczny w Petersburgu i londyński
„Kew Garden” [Sukopp i Starfniger 1995; Bailey i Conolly 2000]. Fallopia
sachalinensis chętnie sadzony był w parkach i ogrodach [Mandák i in. 2004]. Polecano
go na paszę dla bydła [Andre 1893 cyt. za: Bailey i Conolly 2000] oraz na cele opałowe
[Marigo i Pautou 1998]. Używany był też do produkcji środka przeciwko chorobom
18
grzybowym roślin [Sukopp i Starfniger 1995; Bailey i Conolly 2000], a pokaźnych
rozmiarów liście służyły do ochrony owoców sprzedawanych na targowiskach w
krajach klimatu gorącego [Marigo i Pautou 1998]. Pierwsze wzmianki o zdziczałych
stanowiskach rdestowca sachalińskiego pochodzą z roku 1869 z terenu Niemiec, Czech
i Wielkiej Brytanii [Pashley i in. 2007]. W Polsce omawiany gatunek odnotowano po
raz pierwszy na początku XX – w zachodniej i północnej części kraju, natomiast
masowa ekspansja Fallopia sachalinensis rozpoczęła się w 1980 roku [Tokarska-Guzik
2003].
Informacje o obecności na terenie Europy nowego taksonu z rodzaju Fallopia –
międzygatunkowego mieszańca gatunków Fallopia japonica i Fallopia sachalinensis
pojawiły się stosunkowo niedawno. Rdestowiec pośredni (Fallopia × bohemica)
pierwszy raz został opisany w roku 1983 na terenie Czech [Mandák i in. 2004; Sukopp
i Starfinger 1995]. Jednak Bailey i Conolly [2000] podają, że Fallopia × bohemica rósł
w angielskich ogrodach już od roku 1872. Natomiast według Mandáka i in. [2004],
rdestowiec pośredni uprawiany był w Ogrodzie Botanicznym Uniwersytetu Karola w
Pradze, a pierwsze okazy zielnikowe tego gatunku pochodzą z 1905 roku.
19
Fot. 1. Rdestowce na obszarze naturalnego występowania – na górze Fidżi [Kurose i in. 2006]
Fot. 2. Rdestowce na obszarze wtórnego występowania – na jednym z wrocławskich osiedli
20
4.4. WYBRANE WŁAŚCIWOŚCI MORFOLOGICZNE RDESTOWCÓW
Najważniejsze cechy morfologiczne rdestowców zestawiono w tabeli numer 2.
Podstawowymi cechami umożliwiającymi identyfikację poszczególnych taksonów są
kształt i wielkość liści [Bailey i Wisskirsen 2006; Bailey i in. 2008]. W przypadku
wątpliwości, jako dodatkową cechę przyjmuje się sposób owłosienia spodniej strony
blaszki liściowej [Bailey i in. 2008]. Liście rdestowca japońskiego są wyraźnie ucięte
u nasady i ostro zakończone (rys. 4), a włoski na spodzie liścia są prawie niewidoczne,
zredukowane do krótkich papili [Fojcik i Tokarska-Guzik 2000]. Rdestowiec
sachaliński jest najłatwiej rozpoznawalnym gatunkiem ze względu na pokaźne liście
z sercowatą nasadą i dużą ilość gęstych włosków [Bailey i Stace 1992; Tiébré i in.
2007a]. Fallopia × bohemica (podobnie jak większość form mieszańcowych) wykazuje
pośrednie cechy pomiędzy gatunkami rodzicielskimi [Fojcik i Tokarska-Guzik 2000].
Wszystkie rdestowce są klonalnymi, polikarpicznymi geofitami, o pokaźnych
rozmiarach części nadziemnych i podziemnych [Bailey i in. 2007]. Brock [1994]
oszacował, że biomasa nadziemnej części rdestowców z 1 ha porośniętego przez nie
obszaru, na głębokości 25 cm, wynosi 14 000 kg. W systemie podziemnych kłączy
rdestowców magazynowane są składniki pokarmowe, co zapewnia roślinie żywotność
w okresie ich niedoboru. Podejrzewa się, iż zawarte w kłączach związki fenolowe mogą
redukować
liczebność
lokalnych
gatunków
roślin
–
poprzez
oddziaływanie
allelopatyczne [Simens i Blossey 2007].
Znamienną cechą rdestowców jest ich duża zdolność do regeneracji – przede
wszystkim z części podziemnych [Bimová i in. 2003]. Udowodniono eksperymentalnie,
że nowa roślina może powstać z fragmentu kłącza o masie zaledwie 0,7g [Brock i in.
1995]. Możliwa jest także regeneracja z części łodygowych [Bimová i in. 2003]. Siła
reprodukcji wegetatywnej pędów nadziemnych rdestowców potwierdzona została przez
Fabiszewskiego i Brej [2005]. Pędy rdestowca japońskiego umieszczone na różnej
głębokości w glebie wykazywały po 3 miesiącach średni przyrost segmentów
wynoszący 13,2 cm.
W granicach wtórnego zasięgu występowania gatunki z rodzaju Fallopia
rozmnażają się głównie drogą wegetatywną. Ze względu na małą różnorodność
genetyczną możliwości generatywnej propagacji rdestowców są ograniczone. Dotyczy
to zwłaszcza Fallopia japonica, który na terenie całej Europy występuje
prawdopodobnie w postaci jednolitego pod względem genetycznym, oktoploidalnego
21
klonu żeńskiego [Hollingsworth i in. 1990; Hollingsworth i Bailey 2000; Mandák i in.
2005; Pashley i in. 2007]. Nieco większe zróżnicowanie genetyczne wykazuje
rdestowiec sachaliński. Na obszarze kontynentu europejskiego zanotowano tetra
i heksaploidalne okazy [Hollingsworth i in. 1998; Hollingsworth i Bailey 2000].
Najczęściej spotykane są hermafrodytyczne tetraploidalne klony Fallopia sachalinensis
[Bailey i in. 2007].
Rdestowce wykazują zdolności do międzygatunkowego krzyżowania się.
Hybrydyzacja w obrębie rodzaju Fallopia odgrywa prawdopodobnie znaczącą rolę
w ewoluowaniu omawianych gatunków. Mandák i in. [2004] podają, że mieszańce
wykazują w porównani z osobnikami rodzicielskimi wyższą zdolność do inwazji i są
trudniejsze do zwalczania. Ponadto, powstałe hybrydy mogą krzyżować się
z osobnikami rodzicielskimi [Bailey i in. 2008], a nowe formy mieszańców zwiększają
różnorodność genetyczną w obrębie rodzaju Fallopia i tym samym – szanse na
poszerzenie zasięgu geograficznego [Bailey i in. 2007].
Przedstawiciele rodzaju Fallopia należą do roślin stwarzających poważne
problemy ekologiczne i ekonomiczne. Przede wszystkim redukują różnorodność
biologiczną [Bimová i in. 2004]. W europejskiej i światowej bazie danych na temat
gatunków inwazyjnych rdestowiec japoński zaliczany jest do 100 najgroźniejszych
inwazyjnych gatunków obcych [Delivering alien invasive species in Europe 2011; The
global invasive species database 2011]. Stanowiska rdestowców tworzą zwarte
fitocenozy, zacieniające teren i uniemożliwiające wzrost innym gatunkom [Sukopp i
Sukopp 1988; Bauer 1994]. Ponadto, rozwój gatunków sąsiednich ogranicza gruba
warstwa słabo rozkładającej się ściółki [Bauer 1994]. Aczkolwiek, istnieje niewielka
grupa gatunków współtowarzyszących zwartym kępom rdestowców, należą do nich
wczesnowiosenne geofity np. Ficaria bulbifera, a także gatunki ruderalne, jak Urtica
dioica czy Geranium robertianum [Bimová i in. 2004]
Rdestowce, a zwłaszcza Fallopia × bohemica zmieniają właściwości fizyczne
i chemiczne siedliska [Simens i Blossey 2007]. Modyfikują lokalne układy
hydrologiczne i powodują erozję gleby [Alberternst i Böhmer 2006].
W celu usunięcia rdestowców stosuje się metody kombinowane (usuwanie
mechaniczne i zwalczanie na drodze chemicznej), a likwidacja zarośli tych uciążliwych
chwastów
nawet
przy
regularnym
ich
zwalczaniu
zajmuje
kilka
lat.
Ze wszystkich gatunków, najbardziej odporny na likwidację jest rdestowiec pośredni
[Bailey i in. 2008].
22
Obecnie badane są możliwości wykorzystania metod biologicznych do
zwalczania tych uciążliwych chwastów, z wykorzystaniem owadów, np. Aphalaria
itadori oraz patogenów grzybowych [Kurose i in. 2006; Bailey 2010].
23
A.
B.
5 cm
C.
C.
B.
A.
Rys. 4. Kształt i wielkość liści rdestowców oraz typy owłosienia blaszek liściowych: A. Fallopia
japonica (var. japonica), B. Fallopia sachalinensis, C. Fallopia × bohemica (według Fojcik
i Tokarskej-Guzik, 2000 oraz Baileya i in. , 2008)
24
Tab. 2. Charakterystyczne cechy morfologiczne i genetyczne trzech gatunków z rodzaju Fallopia
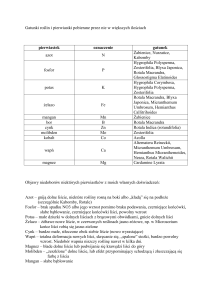
(według Fojcik i Tokarskiej-Guzik, 2000 oraz Bailey, 2003)
Fallopia japonica
łodyga
liście
kwiatostany
kwiaty
owoce
liczba
chromosomów
Fallopia x bohemica
Fallopia sachalinensis
2–3 m wysokości
2,5 – 4 m wysokości
dochodząca do 4 m
wysokości
Kształt liści:
szeroko – jajowato
trójkątne
szczyt zwężony w długi
kończyk
nasada ucięta lub tępo–
klinowato zwężona
Kształt liści:
szeroko – jajowate
szczyt zaostrzony lub
wybiegający w długi, ostry
kończyk
nasada tępo klinowata
(górne liście) lub lekko
sercowata (dolne liście)
Kształt liści:
szeroko – podłużnie
jajowate
szczyt tępo zaostrzony
nasada sercowata
Wymiary:
5–15 (–18) cm długie
4–10 (–13) cm szerokie
Wymiary:
10–23 (–27) cm długie
9–20 (–22) cm szerokie
Wymiary:
15–35 (–43) cm długie
10–20 (–27) cm szerokie
Współczynnik długości do
szerokości: 1–1,5
Współczynnik długości do
szerokości: 1–1,6
Współczynnik długości do
szerokości: 1,5–1,7
Owłosienie:
włoski na spodniej stronie
liścia niewidoczne i
zredukowane do krótkich
jednokomórkowych papli
o silnie nabrzmiałej
postawie
Owłosienie:
włoski na spodzie, blaszki
wyraźnie widoczne,
krótkie 1–4 komórkowe, o
silnie zgrubiałej podstawie
Owłosienie:
Spód liścia wyraźnie długo
owłosiony, włoski 4–12
komórkowe, o nie
zgrubiałej podstawie
wiecha 4–12 cm długa
najdalsze gałązki
kwiatostanu sięgają ¾
blaszki (o 5–7 cm dłuższe
od ogonka liściowego)
wiecha 5–10 cm długa
najdalsze gałązki
kwiatostanu sięgają ½–
¼ blaszki (o 2–4 cm
dłuższe od ogonka
liściowego
wiecha 8–9 cm długa
najdalsze gałązki
kwiatostanu sięgają ¼
blaszki (o 1–2 cm dłuższe
od ogonka liściowego
pęczki 2–4 kwiatowe,
pręciki nie wystają z
okwiatu
skrzydełka okwiatu w
nasadzie nagie, nie
zbiegają po szypułce
kwiatowej,
3–4 mm szerokie
pęczki 3–5 (–6) kwiatowe,
pręciki wystają z okwiatu
skrzydełka zbiegające po
szypułce kwiatowej,
2–3 mm szerokie
pęczki 4–7 kwiatowe,
pręciki wystają z okwiatu
skrzydełka okwiatu
stopniowo zwężające się,
wyraźnie zbiegają po
szypułce kwiatowej,
1,5–2 mm szerokie
orzeszek czarny,
błyszczący
orzeszek brązowy,
błyszczący
orzeszek
ciemnopurpurowy,
błyszczący
2n=88
2n = 44
2n = 66
2n = 44
2n = 66
2n = 88
25
5. WROCŁAW JAKO TEREN PROWADZONYCH BADAŃ
Wrocław,
podobnie
jak
inne
aglomeracje
jest
miejscem
bytowania
i rozprzestrzeniania gatunków inwazyjnych z rodzaju Fallopia.
Miasto leży w południowo–zachodniej Polsce w województwie dolnośląskim.
Jest czwartym pod względem liczby ludności miastem w Polsce i piątym pod względem
powierzchni – 293 km2. Wrocław usytuowany jest w obrębie makroregionu Nizina
Śląska, w rozciągającej się Pradolinie Wrocławsko-Magdeburskiej. Główną oś
hydrauliczną miasta stanowi Odra, której długość wraz z kanałami i odnogami wynosi
54,4 km. Kolejne 53 km stanowią jej cztery dopływy: Widawa, Oława, Ślęza
i Bystrzyca [Szymanowski 2004].
Wrocław położony jest w strefie umiarkowanych szerokości geograficznych, w
typie klimatu przejściowego, z przewagą wpływów oceanicznych. Ze względu na swoje
usytuowanie (przedpole Sudetów) miasto uważane jest za „wrocławsko-opolski obszar
ciepła”. Docierające w ten rejon masy powietrza ulegają dynamicznemu ogrzewaniu
osiadając
po
zewnętrznej
stronie
masywów
górskich
[Szymanowski
2004].
Konsekwencją położenia miasta w Dolinie Odry jest jego słabsze przewietrzanie oraz
wzrost udziału mgieł i zamgleń [Drzeniecka-Osiadacz i in. 2010]. Dodatkowymi
elementami modyfikującymi klimat miasta są charakter pokrycia i sposób użytkowania
terenu. Zmiany te są szczególnie widoczne w obrębie silnie zurbanizowanych rejonów
miasta. Najcieplejszymi jego częściami są obszary o zwartej i luźnej zabudowie, tereny
komunikacyjne, przemysłowe i handlowe, najchłodniejszymi zaś lasy, obszary
nadrzeczne oraz pastwiska i łąki [Drzeniecka-Osiadacz i in. 2010].
We Wrocławiu najczęściej w roku (przez 250 dni) występuje tzw. pogoda ciepła,
podczas której przeważają dni ze średnią temperaturą dobową w zakresie od 5,1 do
15˚C. Sporadycznie pojawia się typ pogody gorącej, gdy średnia dobowa temperatura
przekracza 25˚C. Pogoda chłodna (o średniej temperaturze dobowej w przedziale 1,0–
5,0˚C) występuje przez około 32 dni w roku, natomiast tak zwana pogoda
przymrozkowa z temperaturą od 0,1 do 0,5˚C (średnia dobowa) ma miejsce w ciągu 86
dni w roku [Dubicki i in. 2002]. Przymrozki pojawiają się późną wiosną i wczesną
jesienią. W ostatnich latach przymrozki wiosenne zdarzają się w maju, a pierwsze
przymrozki jesienne przypadają już na II dekadę września [Dubicki i in. 2002].
26
Średnia
roczna
temperatura
powietrza
we
Wrocławiu
wynosi
9,0˚C.
Najzimniejszym miesiącem jest styczeń z temperaturą –0,4˚C (średnia miesięczna),
najcieplejszym zaś lipiec, w czasie którego średnia temperatura wynosi 18,8˚C [Dubicki
i in. 2002]. Miarą stopnia kontynentalizmu klimatu jest amplituda roczna temperatury.
We Wrocławiu wynosi ona 19,2˚C, co stawia miasto wśród obszarów nizinnej części
Polski, odznaczających się najniższymi wielkościami tego wskaźnika [Dubicki i in.
2002]. W ostatnich latach zaobserwowano wzrost średniej rocznej temperatury. Bardzo
ciepłe były dwie ostatnie dekady XX wieku oraz początek XXI [Drzeniecka-Osiadacz i
in. 2010]. Zmniejszyła się też liczba dni o niskiej temperaturze, zwłaszcza w
przejściowych porach roku [Drzeniecka-Osiadacz i in. 2010].
Wrocław należy do miast o niskiej sumie opadów atmosferycznych (około 589
mm), które występują zazwyczaj w ciągu 167 dni w roku [Dubicki i in. 2002].
Maksimum opadów (66% ich sumy rocznej) przypada na okres letni. W ostatnich latach
XX wieku wzrosła liczba dni bez opadów, co znalazło swe odbicie w malejącym
trendzie opadów atmosferycznych na obszarze miasta. Zmienił się także charakter
opadów – obecnie w rejonie Wrocławia występują często burze i opady ulewne, będące
przyczyną lokalnych podtopień i powodzi [Dubicki i in. 2002].
Roczna amplituda ciśnienia atmosferycznego w mieście wynosi około 4,0 hPa,
co świadczy również o przejściowym charakterze klimatu – pomiędzy morskim,
a kontynentalnym [Drzeniecka-Osiadacz i in. 2010 cyt. za: Dębicka 1994].
We Wrocławiu dominują wiatry zachodnie. Średnia roczna prędkości wiatru z
przekracza 3,0 m·s-1. Maksymalne prędkości wiatru (4,2 m·s-1) występują w okresie
zimowym [Drzeniecka-Osiadacz i in. 2010].
Jednym ze skutków uprzemysłowienia miasta jest zanieczyszczenie środowiska.
Wrocław jest przykładem aglomeracji, gdzie na stosunkowo niedużej powierzchni
zlokalizowana jest duża liczba obiektów przemysłowych. Szymanowski [2004] za
Bernhardem [1990] podaje, że w latach 80 i na początku lat 90 XX wieku na terenie
Wrocławia
funkcjonowało
aż
7000
zakładów,
z
których
121
emitowało
zanieczyszczenia gazowe i pyłowe. Współcześnie, pod względem wielkości emisji
zanieczyszczeń
gazowych
i
pyłowych
Wrocław
zajmuje
czołowe
miejsce
w województwie dolnośląskim – po powiecie zgorzeleckim [Kwiatkowska-Szykulska
i in. 2002]. Zakładem mającym największy udział w emisji zanieczyszczeń jest
Elektrociepłownia Wrocław [Kwiatkowska-Szykulska i in. 2002].
27
Znaczny udział w zanieczyszczeniu powietrza atmosferycznego w mieście ma
transport drogowy, który wpływa na stężenie tlenków azotu, lotnych związków
organicznych i pyłów [Raport o stanie środowiska województwa dolnośląskiego 2010].
Wrocław położony jest na przecięciu ważnych szlaków komunikacyjnych, przez miasto
przebiegają drogi międzynarodowe oraz europejskie korytarze transportowe. Ponadto,
na terenie miasta zlokalizowane są dwa dworce kolejowe i międzynarodowy port
lotniczy. Mogą to być potencjalne szlaki migracji obcych gatunków roślin
Głównymi zanieczyszczeniami powietrza, których pomiary prowadzone są
w ramach monitoringu jakości powietrza są: dwutlenek siarki, dwutlenek azotu, tlenki
węgla, pył zawieszony PM10, benzen i ołów. Jak wynika z porównań z innymi
aglomeracjami miejskimi, Wrocław jest miastem o lepszej jakości powietrza,
z wyjątkiem stwierdzonych dość dużych stężeń dwutlenku azotu, co lokuje miasto na
wysokim
miejscu
w
kraju
pod
względem
zanieczyszczeń
atmosferycznych
Zanieczyszczenia powietrza migrują do wód i gleb. Stan jakości wód w mieście uległ
ostatnio poprawie, pomimo to wśród wód podziemnych nadal przeważają wody
zaliczane do III i V klasy czystości [Pieroński i in. 2010].
Według danych Wojewódzkiego Inspektoratu Ochrony Środowiska [2010], na
niektórych
obszarach
Wrocławia
stwierdzono
przekroczenia
dopuszczalnych
standardów co do jakości gleb. Dotyczy to przede wszystkim metali ciężkich, między
innymi Zn, Cd, Cu i Pb [Korabiewski i in. 2010]. Na terenach wodonośnych został
także przekroczony dopuszczalny poziom zawartości Cr [Raport o stanie środowiska
województwa dolnośląskiego 2010]. Oceniając stopień zanieczyszczenia gleb metalami
ciężkimi w sześciostopniowej skali IUNG nie stwierdzono w obszarze Wrocławia
występowania gleb silnie zanieczyszczonych i bardzo silnie zanieczyszczonych [Raport
o stanie środowiska województwa dolnośląskiego 2010].
28
6. METODYKA BADAŃ
6.1. BADANIA TERENOWE
Badania
terenowe
prowadzono
w
latach
2009–2011
w
granicach
administracyjnych Wrocławia. Pierwszym etapem prac była analiza rozmieszczenia
trzech gatunków rdestowców (Fallopia japonica, Fallopia sachalinensis, Fallopia
× bohemica) na terenie miasta oraz charakterystyka zajmowanych przez te gatunki
siedlisk.
Przedstawicieli z rodzaju Fallopia na terenie Wrocławia zinwentaryzowano na
siedliskach półnaturalnych i antropogenicznych. Identyfikacji gatunku dokonywano
w oparciu o cechy morfologiczne liści (głównie kształt i rozmiary), które pobierano
z środkowej części pędu. Ze względu na ścisłe powiązania klonalne rdestowców, jako
odrębne skupiska przyjęto kępy oddalone od siebie o co najmniej 2 metry. Lokalizację
skupisk określono odbiornikiem globalnego systemu pozycjonowania (GPS), a ich
powierzchnie zmierzono za pomocą taśm mierniczych. W przypadku zarośli
o znacznych powierzchniach pomiaru dokonano za pomocą odbiornika GPS.
W badaniach dotyczących rozmieszczenia rdestowców na terenie Wrocławia
wykorzystano
metodę
kartowania.
Na
podkłady
mapowe
naniesiono
siatkę
o podstawowym polu badawczym w wymiarach 1000 m x 1000 m. W każdym
z kwadratów obliczono oddzielnie liczbę skupień Fallopia japonica, Fallopia
sachalinensis i Fallopia × bohemica. W związku z tym wyznaczono cztery klasy
zagęszczenia (liczba skupisk /1 km2): I – 1 skupisko, II – 4 skupiska, III – 10 skupisk
oraz IV – powyżej 10 skupisk. Ponadto w poszczególnych kwadratach określono
powierzchnię skupisk rdestowców. W tym celu wyróżniono następujące przedziały:
I – 1–10 m2, II – 10–40 m2, III – 40–200 m2 oraz IV – powyżej 200 m2.
Określono
również
zależność
pomiędzy
rozmieszczeniem
stanowisk
rdestowców, a wybranymi warunkami ekologicznymi Wrocławia (termika miasta
i topografia zabudowy miejskiej). W tym celu stanowiska rdestowców naniesiono na
mapy ilustrujące rozkład miejskiej wyspy ciepła oraz stopień zabudowy miasta.
Ze względu na sposób użytkowania terenu, siedliska gatunków z rodzaju
Fallopia sklasyfikowano według następujących typów:
I – obszary o zabudowie mieszkaniowej jedno lub wielokondygnacyjnej
II – tereny zieleni miejskiej – trawniki, parki, zieleńce i skwery miejskie
29
III – obszary niezagospodarowane – zaliczono tu także dzikie wyspiska śmieci,
zwałowiska i guzowiska
IV – tereny usługowe i przemysłowe – w tym obiekty użyteczności publicznej
(np. cmentarze) wraz z parkingami
V – pobocza dróg i torów kolejowych
VI – tereny nadwodne – położone w bezpośrednim sąsiedztwie rzek, stawów
oraz rowów melioracyjnych
W każdym z wyróżnionych typów obliczono procentowy udział klonalnych kęp
rdestowców oraz zajmowaną przez nie powierzchnię.
Do dalszych badań wybrano po 10 stanowisk rdestowca japońskiego
i pośredniego. Przy wyborze stanowisk badawczych kierowano się przede wszystkim
topografią zabudowy i sposobem użytkowania terenu oraz odległością obiektu od sieci
szlaków komunikacyjnych. Ponadto, stanowiska ulokowane były w centralnej i
południowej części Wrocławia, ze względu na częste występowanie rdestowców, a
zwłaszcza rdestowca pośredniego w tym rejonie miasta (rys.5). Badania dotyczące
rdestowca sachalińskiego ograniczono do 3 obiektów ze względu na rzadkie
występowanie tego gatunku na terenie miasta. Początkowo prowadzono je na jednym
stanowisku (przy ul. Tatarakowej). W drugim roku badań odnaleziono dwa kolejne
stanowiska Fallopia sachalinensis (przy ul. Karmelkowej i Żernickiej), które
uwzględniono w dalszej części badań.
Charakterystykę badanych obiektów zamieszczono poniżej. Przypisana im
numeracja stosowana jest w dalszej części pracy.
30
▲23
●8 ■11
●4 ■16
●3
■17
●5
●2
▲21
●6 ●10
■15■19
■18
●7
■20■12
■14
●9
●1
■13 ●1
▲22
Rys. 5. Rozmieszczenie stanowisk badawczych na terenie Wrocławia
● – stanowiska Fallopia japonica
■ – stanowiska Fallopia × bohemica
▲– stanowiska Fallopia sachalinensis
Charakterystyka stanowisk badawczych
Stanowiska Fallopia japonica
Stanowisko 1. (51°04.588' N 17°02.997' E) – znajduje się w południowej części miasta,
przy ul. Morwowej. Kępy rdestowca japońskiego porastają niezabudowany teren,
tworząc skupienie o powierzchni 83,0 m2. Potencjalnymi ośrodkami rozprzestrzeniania
się Fallopia japonica są znajdujące się w pobliżu ogródki działkowe oraz ruchliwa
droga.
Stanowisko 2. (51°06.945' N 17°06.787' E) – położone jest w południowo–wschodniej
części Wrocławia, na skrzyżowaniu ul. Mydlanej z ul. Swojczycką, niedaleko Odry.
Zarośla
rdestowców
ciągną
się
wzdłuż
drogi,
tworząc
zwarte
skupisko
o powierzchni 40,4 m2.
Stanowisko 3. (51°07.460' N 17°03.043' E) – zlokalizowane w centrum miasta w
jednym z ogródków, przy bloku wielokondygnacyjnym (ul. Elizy Orzeszkowej).
31
Rdestowiec japoński nasadzony tu jako roślina ozdobna ma doskonałe warunki do
rozwoju. Fallopia japonica zajmuje powierzchnię 32,0 m2.
Stanowisko 4. (51°06.734' N 16°59.862' E) – położone w przemysłowej części
Wrocławia, przy ul. Robotniczej, na niezagospodarowanym terenie przy ruchliwej
drodze i nasypie kolejowym. Kępy rdestowca japońskiego rosną w cieniu, pod
wiaduktem kolejowym, tworzą skupienie o powierzchni 17,2 m2.
Stanowisko 5. (51°07.404' N 17°04.146' E) – usytuowane we wschodniej części terenu
badań, nad Starą Odrą. Do obserwacji wybrano jedno z wielu występujących tu zarośli
Fallopia japonica. Pędy rdestowca japońskiego rosły w pełnym słońcu, na powierzchni
54,0 m2.
Stanowisko 6. (51°06.168' N 17°04.311' E) – punkt badawczy znajduje się na wale
przeciwpowodziowym Odry. Występujące tu okazy rdestowca japońskiego tworzą kępy
o powierzchni 12,9 m2.
Stanowisko 7. (51°05.568' N 17°01.992' E) – zlokalizowane na południu Wrocławia, na
skwerze miejskim przy ulicy Sieradzkiej, niedaleko ruchliwej drogi i parkingu.
Stanowisko jest dobrze nasłonecznione, rdestowiec japoński porasta powierzchnię 15,7
m2.
Stanowisko 8. (51°06.853' N 16°58.274' E) – znajduje się na ulicy Strzegomskiej, tuż
przy nasypie kolejowym i ruchliwej drodze. Rośliny wystawione są na intensywne
oddziaływanie promieni słonecznych. Stanowisko zajmuje powierzchnię1,3 m2.
Stanowisko 9. (51°05.075' N 17°01.443' E) – położone jest przy alei Wiśniowej na
niezagospodarowanym terenie, przylegającym bezpośrednio do ogródków działkowych.
W pobliżu skupień rdestowców znajduje się droga i linia tramwajowa. Zauważono, że
opisywane stanowisko było miejscem składowania resztek organicznych pochodzących
z ogródków działkowych, które mogły wzbogacać glebę w składniki odżywcze.
Stanowisko 10. (51°06.233' N 17°04.957' E) –obiekt badawczy usytuowany przy ul.
Zygmunta Wróblewskiego, na niezagospodarowanym obszarze. Kępy rdestowca
japońskiego są tu rozproszone. Łącznie zajmują powierzchnię 25,2 m2. W pobliżu
stanowiska znajduje się betonowe ogrodzenie, zacieniające część terenu. Zwrócono
także uwagę na obecność studzienki kanalizacyjnej, z której korzenie roślin mogły być
dodatkowo zasilane prez makro i mikroelementy.
32
Stanowiska Fallopia × bohemica
Stanowisko 11. (51°07.304' N 17°00.455' E) – zlokalizowane w północno–zachodniej
części miasta, przy ul. Gnieźnieńskiej. Fallopia × bohemica rośnie w towarzystwie
zwartych kęp rdestowca japońskiego. Oba gatunki tworzą zarośla ciągnące się wzdłuż
nasypu kolejowego. Na uwagę zasługuje fakt bliskiego sąsiedztwa ogródków
działkowych oraz ruchliwej drogi. Do badań wybrano skupienie rdestowca pośredniego
o powierzchni 24,1 m2.
Stanowisko 12. (51°05.153' N 17°02.681' E) – niewielkie skupisko rdestowca
pośredniego (6,9 m2), zlokalizowane tuż przy ogródku, przy bloku na ul. Kamiennej.
Niedaleko znajduje się droga i duży parking. Obserwowane kępy rosły w cieniu
budynku na piaszczystym podłożu.
Stanowisko 13. (51°04.671' N 17°02.390' E) – największe ze wszystkich odnalezionych
skupień Fallopia × bohemica, o łącznej powierzchni 1223,0 m2. Rośliny porastały tu
niezagospodarowany fragment terenu, znajdujący się w centrum wysokiej zabudowy
mieszkaniowej, przy ulicy Orzechowej. W roku 2010 w wyniku budowy lini
tramwajowej część płatów została zlikwidowana. Rok później rośliny odrosły znacznie
zwiększając zajmowaną powierzchnię.
Stanowisko 14. (51°05.383' N 17°02.932' E) – znajduje się przy ulicy Paczkowskiej.
Obserwowane skupisko zajmowało 3,0 m2. Kępy rosły na kamienistej glebie, pokrytej
warstwą składowanych w tym miejscu popiołów, powstałych prawdopodobnie po
spalaniu węgla.
Stanowisko 15. (51°05.739' N 17°01.295' E) – rozległe stanowisko ulokowane na
niezagospodarowanym terenie, w centrum miasta przy ruchliwej ulicy Powstańców
Śląskich, niedaleko lini tramwajowej. Do badań spośród 7 odnotowanych tam skupisk
rdestowca pośredniego wybrano kępy zajmujące powierzchnie 40 m2.
Stanowisko 16. (51°06.710' N 16°59.999' E) – położone przy ul. Robotniczej, na
parkingu tuż przy budynkach gospodarczych. Fallopia × bohemica porastała tu wąski
niewybetonowany pas o powierzchni 8,1 m 2. Niedaleko obiektu znajduje się ruchliwa
droga i linia tramwajowa.
Stanowisko 17. (51°06.035' N 17°04.643' E) – zlokalizowane przy samym brzegu
koryta Odry. Badania prowadzono na skupisku o powierzchni 38,0 m2.
Stanowisko 18. (51°05.666' N 17°01.746' E) – znajduje się w środkowej części miasta,
na nieużytkowanym terenie, tuż przy centrum handlowym na skrzyżowaniu ulicy
Sanockiej i Ślężnej. Rdestowiec pośredni tworzy tu kilka rozległych płatów. W wyniku
33
zabiegów pielęgnacyjnych kępy rdestowców są wycinane i wypalane. Prace te nie
przynoszą oczekiwanych efektów; co roku na stanowisku pojawiają się nowe pędy
Fallopia × bohemica. Do badań wybrano skupisko o powierzchni 125,8 m2 rosnące w
pełnym słońcu.
Stanowisko 19. (51°05.911' N 17°01.840' E) – zlokalizowane na terenie parkingu przy
ul. Swobodnej. Mieszaniec zajmuje tu powierzchnię 37,5 m2. Występuje na silnie
przekształconym podłożu, zajmując wolne, niezabetonowane przestrzenie. W pobliżu
stanowiska znajduje się droga i linia tramwajowa.
Stanowisko 20. (51°05.080' N 17°02.378' E) – położone jest na parkingu, pomiędzy
blokami przy ul. Ślicznej. Kępy rdestowca pośredniego zajmują tu niewielką
powierzchnię – 0,8 m2. Podczas prowadzenia badań stanowisko było kilkukrotnie
koszone.
Stanowiska Fallopia sachalinensis
Stanowisko 21. (51°06.190' N 17°08.635' E) – znajduje się w południowo – wschodniej
części miasta przy ul. Tatarakowej, w bliskim sąsiedztwie Odry. Rdestowiec sachaliński
rośnie tu w półcieniu, który tworzy korona Ulmus dioica. Zajmuje powierzchnię 108,2
m2.
Satnowisko 22. (51°04.617' N 16°57.792' E) – położone przy ruchliwym skrzyżowaniu
ulicy Wiejskiej z ulicą Karmelkową. Kępy Fallopia sachalinensis tworzą tu płat
o powierzchni 42,0 m2. Stanowisko jest regularnie koszone, a pędy rdestowca
sachalińskiego wypalane.
Stanowisko 23. (51°07.342' N i 16°56.085' E) – usytułowane przy ul. Żernickiej,
niedaleko ogródków działkowych i zabudowy mieszkaniowej. Stanowisko zajmuje
powierzchnię 97,5 m2. Na stanowisku panują dogodne dla wzrostu i rozwoju roślin
warunki, kłącza rdestowca są zasilane w wodę z pobliskiego rowu melioracyjnego.
W okresie prowadzenia badań stanowisko było często wypalane.
34
Z każdego stanowiska w bezpośrednim sąsiedztwie sytemu części podziemnych
roślin pobrano materiał glebowy (z głębokości 0–15 cm), który poddano analizom
chemicznym określając: kwasowość czynną, kwasowość wymienną, zawartość Corg i
Nog, zawartość przyswajalnych form potasu, fosforu i magnezu oraz koncentracje
wybranych metali ciężkich (Cd, Cr, Cu, Pb, Zn).
Następnie przeprowadzono analizę morfologiczną liści i kwiatów rdestowców.
W analizie liści wykorzystano metodę opisaną przez Tiébré i in. [2007a]
Badaniami objęto sześć cech morfologicznych liści (rys. 6). Ze środkowej części pędów
pobrano losowo po 10 liści, które wysuszono i zmierzono przy pomocy kalki
milimetrowej, z dokładnością do 1,0 mm.
Rys. 6. Schemat pomiaru sześciu cech morfologicznych liści rdestowców (według Tiébré i in.,
2007a)
1. szerokość podstawy liścia [cm]
2. szerokość środkowej części liścia [cm]
3. długość liścia [cm]
4. wcięcie blaszki liściowej [cm]
5. długość wierzchołka liścia [cm],
6. szerokość wierzchołka liścia [cm]
35
Badania kwiatów rdestowców dotyczyły ich płci. Przeprowadzono je na 10
okazach Fallopia japonica występujących na opisanych wcześniej stanowiskach (od 1
do 10), 20 klonach Fallopia × bohemica oraz jednym okazie Fallopia sachalinensis.
Liczbę analizowanych prób rdestowca pośredniego zwiększono ze względu na duże
zróżnicowanie morfologiczne tego gatunku. Materiał do badań pobrano ze stanowisk od
11 do 20 oraz dodatkowo z obiektów zlokalizowanych przy ul. Grunwaldzkiej,
Nasypowej i pl. Św. Macieja. W przypadku rdestowca sachalińskiego analizy
ograniczono do jednej próby, bowiem w okresie badań stanowiska tego gatunku były
kilkukrotnie niszczone, między innymi poprzez regularne wypalanie jego kęp.
Na 10 stanowiskach rdestowca japońskiego i pośredniego oraz jedym
stanowisku rdestowca sachalińskiego (nr 21) przeprowadzono także obserwacje
przebiegu
faz
rozwojowych.
Badania
wykonano
podczas
dwóch
sezonów
wegetacyjnych, w latach 2009–2010. Obejmowały on okres od pojawienia się na
powierzchni gleby pierwszych pąków pędowych (marzec/kwiecień) – do opadania liści
rdestowców (listopad/grudzień). Ponadto, na każdym ze stanowisk w okresie od
kwietnia do maja określono średni przyrost pędów rdestowców [cm]. Pomiary
prowadzono na 10 losowo wybranych pędach, które zostały odpowiednio oznakowane,
aby zawsze dokonać pomiaru tych samych łodyg. Wykonano je w regularnych
cotygodniowych odstępach.
36
6.2. DOŚWIADCZENIA WAZONOWE
Doświadczenia wazonowe wykonano w hali wegetacyjnej Rolniczego Zakładu
Doświadczalnego w Pawłowicach. Eksperymenty przeprowadzono w trakcie dwóch
sezonów wegetacyjnych, (1) w okresie od lipca do października 2009 roku oraz (2) od
czewca do września 2010 roku. Pierwszy etap badań dotyczył rdestowca japońskiego –
najczęstszego reprezentanta rodzaju Fallopia na terenie Wrocławia. Testowano jego
reakcje na toksyczne działanie Cd, Cr, Cu, Pb oraz Zn. Uzyskane wyniki badań
pozwoliły na zaprojektowanie drugiej serii doświadczeń, w których obserwowano
wpływ metali na wzrost i rozwój trzech gatunków rdestowców (Fallopia japonica,
Fallopia × bohemica i Fallopia sachalinensis). Spośród pięciu testowanych wcześniej
metali do dalszych badań wybrano Cd – metal, który akumulowany był przez Fallopia
japonica w największych ilościach oraz Cr – pierwiastek, którego nawet duży dodatek
do gleby nie ograniczał rozwoju rdestowca japońskiego. Przy wyborze metali ciężkich
kierowano się także wcześniejszymi badaniami, których wyniki sugerowały zdolność
rdestowców do kumulacji niektórych metali ciężkich (zwłaszcza chromu) [Sołtysiak i
in. 2011].
W doświadczeniach wykorzystano glebę średnią o znanych właściwościach
chemicznych (tab.3), do której zaaplikowano w postaci roztworów odpowiednie dawki
metali ciężkich. Zastosowane dawki metali ciężkich zamieszczono w tab. 4 i 5. Wazony
z glebą bez dodatku metali stanowiły próbę kontrolną. Każdy wariant testowano w
czterech powtórzeniach. Ze względu na ograniczone możliwości propagacji rdestowców
drogą generatywną (na terenie Europy występują wyłącznie żeńskie okazy rdestowca
japońskiego) materiałem użytym do doświadczenia były części podziemne. Do
doświadczeń zastosowano fragmenty kłączy wraz z nielicznymi i bardzo drobnymi
korzeniami. Oczyszczone uprzednio z gleby kłącza o takiej samej liczbie pączków oraz
zbliżonej masie – 14,5 g w przypadku rdestowca japońskiego i pośredniego oraz 20,5 g
w przypadku rdestowca sachalińskiego umieszczono w wazonach. Materiał roślinny do
pierwszego doświadczenia pobrano ze stanowiska nr 8 przy ul. Strzegomskiej. W
drugiej cześci badań wykorzystano kłącza pochodzące ze stanowiska położonego nad
rzeką Odra (Fallopia japonica – stanowisko nr 5 i Fallopia × bohemica – stanowisko nr
17) oraz przy ul. Tatarakowej (Fallopia sachalinensis – stanowisko nr 21). Kłącza
umieszczono na głębokości 5 cm i przysypano 1,5 cm warstwą piasku. Zgodnie z
metodyką stosowaną w tego rodzaju eksperymentach [Żurbicki 1974] w pierwszych
37
tygodniach rośliny podlewano 300 ml wody destylowanej, a w późniejszym okresie (po
wytworzeniu przez roślinę pędów nadziemnych) ilość wody dostosowywano do ciężaru
wazonu. Raz w tygodniu przestawiano wazony według ustalonego schematu, aby
zapewnić roślinom jednakowe warunki. Obserwacje wzrostu i rozwoju rdestowców
wykonywano cotygodniowo przez okres 14 tygodni. Określono zdolność roślin do
regeneracji w poszczególnych wariantach doświadczalnych, prześledzono ich dynamikę
wzrostu prowadząc regularne pomiary przyrostu pędów [cm]. Zwracano także uwagę na
ogólny rozwój roślin i ewentualne uszkodzenia morfologiczne pędów.
Doświadczenie trwało trzy miesiące. Uzyskany materiał roślinny poddano
dalszym analizom i pomiarom biometrycznym. Określono następujące parametry:
świeżą masę pędów nadziemnych [g], suchą masę pędów nadziemnych [g], długość
pędów [cm], liczbę liści na pędzie [szt.] oraz długość i szerokość blaszki liściowej [cm].
W podziemnych i nadziemnych częściach rdestowców zbadano zawartość metali
ciężkich [mg·kg-1].
Tab. 3. Właściwości chemiczne gleby użytej w doświadczeniach wazonowych
Gleba
I
doświadczenie
II
doświadczenie
pH
N og
C org
%
%
KCl
H2O
5,9
6,3
0,092
5,3
5,9
0,112
Zawartość form
przyswajalnych
[mg·100g-1]
Zawartość
metali ciężkich
[mg·kg-1]
K2O
P2O5
Mg
Cd
Cr
Cu
Pb
Zn
1,4
32,6
13,5
4,7
0,1
6,7
8,4
10,2
27,1
1,2
26,7
11,6
4,0
0,2
7,2
8,4
11,0
40,0
Tab. 4. Zastosowane dawki wybranych metali ciężkich w I doświadczeniu wazonowym z udziałem
Fallopia japonica
Metal
Dawka [mg·kg-1]
Cd – zaaplikowano w postaci roztworu CdCl2
20, 100, 200
Cr – zaaplikowano w postaci roztworu CrO3
10, 20, 100
Cu – zaaplikowano w postaci roztworu CuSO4 x 5H2O
100, 200, 300
Pb – zaaplikowano w postaci roztworu Pb(NO3)2
50, 100, 200
Zn – zaaplikowano w postaci roztworu ZnSO4 x 7H2O
100, 200, 300
Gatunek
Fallopia japonica
Tab. 5. Zastosowane dawki wybranych metali ciężkich w I doświadczeniu wazonowym z udziałem
trzech gatunków rdestowców
Metal
Dawka [mg·kg-1]
Cd – zaaplikowano w postaci roztworu CdCl2
200
Cr – zaaplikowano w postaci roztworu CrO3
100
Gatunek
Fallopia japonica,
Fallopia sachalinensis
Fallopia × bohemica
38
6.3. PRACE LABORATORYJNE
6.3.1.
ANALIZY CHEMICZNE
Próbki gleby pobrane ze stanowisk, na których wystepują rdestowce wysuszono
w temperaturze pokojowej w warunkach zapewniających ochronę przed ich
zanieczyszczeniem. Następnie materiał glebowy utarto w moździerzach, przesiano
przez sita o średnicy oczek 2 mm i zmielono w młynku agatowym. Analizy chemiczne
gleb wykonano zgodnie z metodyką stosowaną w laboratoriach Stacji Chemiczno–
Rolniczych:
•
Kwasowość czynną (pH w H2O) i wymienną (pH w KCl) określono metodą
potencjometryczną.
•
Zawartość węgla organicznego [%] oznaczono metodą Tiurina.
•
Udział azotu ogólnego [%] określono metodą Kjeldahla.
•
Zawartość przyswajalnego fosforu oznaczono metodą potencjometryczną.
•
Zawartość przyswajalnego potasu oznaczono metodą fotometrii płomieniowej.
•
Zawartość magnezu określono metodą spektrometrii absorpcyjnej.
•
Zawartość w materiale glebowym wybranych metali ciężkich: kadmu, chromu,
miedzi, ołowiu i cynku [mg·kg-1] oznaczono za pomocą spektrometru absorpcji
atomowej (AAS – wersja płomieniowa). Mineralizację przeprowadzono w bloku
elektrycznym z użyciem mieszaniny stężonego HCl i HNO3 w stosunku
objętościowym 3:1.
W materiale roślinnym pochodzącym z doświadczenia wazonowego określono
zawartość następującyh metali ciężkich: Cd, Cr, Cu, Zn i Pb. Analizie poddano części
nadziemne roślin (liście). Kłącza i korzenie analizowano wspólnie – jako podziemne
części rdestowców z uwagi na znikomy udział korzeni. Części podziemne oczyszczono
z gleby poprzez trzykrotne płukanie w wodzie wodociągowej oraz sześciokrotnie w
wodzie dejonizowanej. Liście płukano dwukrotnie w wodzie wodociągowej i
dejonizowanej. Tak przygotowany materiał wysuszono w suszarce z wymuszonym
obiegiem powietrza w temperaturze 85˚C. Następnie materiał roślinny zmielono w
młynku elektrycznym. Próbki zmineralizowano na mokro w mieszaninie stężonego HCl
i HNO3 w stosunku 3:1. Zawartość metali ciężkich oznaczono przy użyciu spektrometru
plazmowego (ICP– AES).
39
6.3.2. OKREŚLENIE PLOIDALNOŚCI RDESTOWCÓW
Badania dotyczące liczby chromosomów przeprowadzono na 20 okazach
rdestowca pośredniego i jednym okazie rdestowca sachalińskiego. W analizie
ploidalności nie uwzględniono klonów rdestowca japońskiego, gdyż porównując
uzyskane wynik dotyczące morfologii liści oraz kwiatów wrocławskich klonów
Fallopia japonica z danymi literaturowymi [Bailey i Stace 1992; Kim i Park 2000;
Tiébré i in. 2007a; Zica i Jacobson 2003; Bailey i in. 2008] przyjęto założenie, iż
odpowiadają one klonowi o oktoploidalnej liczbie chromosomów.
Badania liczby chromosomów wykonano w trakcie pobytu na stażu w
laboratorium na Uniwersytecie w Leicester. Posłużono się tu metodyką Baileya [1989].
Materiał badawczy stanowiły młode korzenie rdestowców pobrane, z roślin
wyhodowanych w warunkach szklarniowych. Materiał roślinny umieszczono w 0,002
molowym roztworze 8–hydroksychinoliny na 24 godziny. Następnie zalano go
roztworem alkoholu etylowego i kwasu octowego w stosunku objętościowym 3:1. Po
upływie 30 minut korzenie zalano 5 – molowym HCl, a na końcu 70% alkoholem
etylowym. Następnie sporządzono preparaty, które po utrwaleniu analizowano pod
mikroskopem. Wykonano także dokumentację fotograficzną.
6.3.3. STATYSTYCZNA ANALIZA DANYCH
Analizy statystyczne uzyskanych danych przeprowadzono za pomocą pakietu
Statistica v. 9.1 (StatSoft Inc. 2010). W celu stwierdzenia istotnych statystycznie
zależności pomiędzy zastosowanymi dawkami metali ciężkich, a ich kumulacją w
nadziemnych i podziemnych częściach roślin wyznaczono współczynniki korelacji.
Zgodność danych z rozkładem normalnym analizowano testem W Shapiro-Wilka. Dla
danych o rozkładzie normalnym stosowano współczynnik korelacji liniowej Pearsona
(r). Dane o rozkładzie odbiegającym od normalnego badano metodą nieparametryczną
wyznaczając współczynnik korelacji Spearmana (Rs). W analizie cech morfologicznych
rdestowców występujących na danych stanowiskach zastosowano jednoczynnikową
analizę wariancji ANOVA. Grupy jednorodne wyznaczono testem HSD Tukeya. Tą
samą metodą posłużono się w odniesieniu do zawartości metali ciężkich w
nadziemnych i podziemnych częściach roślin hodowanych w doświadczeniach
wazonowych. Wykresy do pracy sporządzono w programie Statistica oraz Excel.
40
7. WYNIKI BADAŃ
7.1. BADANIA TERENOWE W OBSZARZE WROCŁAWIA
7.1.1.
ROZMIESZCZENIE SKUPISK RDESTOWCÓW
Na obszarze Wrocławia w latach 2009–2011 zlokalizowano 310 skupisk
rdestowców o łącznej powierzchni 1,1343 ha. Na rys. 7 przedstawiono procentowy
udział poszczególnych gatunków rdestowców w ogólnej liczbie odnalezionych skupień.
Najczęściej notowanym we Wrocławiu taksonem był rdestowiec japoński (Fallopia
japonica), który stanowił 73,2% ogólnej liczby skupisk. Drugi z rdestowców –
rdestowiec sachaliński (Fallopia sachalinensis) występował sporadycznie, uzyskując
zaledwie 5,2% ogółu. Udział rdestowca pośredniego (Fallopia × bohemica)
w całkowitej liczbie skupisk wyniósł 21,6%.
Rys. 8 ilustruje procentowy udział poszczególnych gatunków rdestowców pod
względem zajmowanej przez nie powierzchni. Kępy rdestowca japońskiego porastały
54,8% całkowitej powierzchni, podczas gdy rdestowiec sachaliński zajmował zaledwie
4,6% ogółu. Na szczególną uwagę zasługuje stosunkowo duży udział powierzchni
zajmowanej przez Fallopia × bohemica. Liczba stanowisk rdestowca pośredniego była
ponad trzykrotnie niższa od dominującego na terenie Wrocławia rdestowca
japońskiego, pomimo to kępy Fallopia × bohemica stanowiły aż 40,6% powierzchni
wszystkich zlokalizowanych skupisk.
41
21,6%
Fallopia japonica
5,2%
Fallopia x bohemica
Fallopia sachalinensis
73,2%
Rys. 7. Udział trzech gatunków rdestowców w ogólnej liczbie odnotowanych skupisk
4,6%
Fallopia japonica
40,6%
Fallopia x b ohemica
54,8%
Fallopia sachalinensis
Rys. 8. Udział trzech gatunków rdestowców pod względem zajmowanej powierzchni
42
Rozmieszczenie gatunków z rodzaju Fallopia w granicach administracyjnych
Wrocławia przedstawiono na rys. 9–11. Jak wspomniano wcześniej, posłużono się tu
metodą kartogramu, przyjmując za podstawowe pole badawcze kwadrat o boku 1000 m.
Na obszarze badań wyznaczono łącznie 340 kwadratów. Obecność przedstawicieli
z rodzaju Fallopia stwierdzono w 79 polach badawczych, które stanowią ponad 23%
powierzchni miasta.
Fallopia japonica zlokalizowany został w 53 kwadratach, czyli na około 15,6%
powierzchni badanego terenu. Skupiska tego gatunku rozproszone były niemal we
wszystkich częściach Wrocławia, z wyjątkiem północnych i skrajnie zachodnich
terenów. Fallopia sachalinensis występował w trzech z 340 kwadratów, czyli na
niespełna 1% powierzchni miasta. Omawiany takson odnotowany został w południowej,
zachodniej oraz wschodniej części terenu badań. Kępy Fallopia × bohemica
występowały natomiast w 23 polach badawczych, czyli na około 6,8% powierzchni
miasta. Gatunek ten najczęściej spotykany był w centralnej i zachodniej części
Wrocławia, gdzie często towarzyszył agregacjom rdestowca japońskiego.
Analizując liczbę skupisk poszczególnych gatunków rdestowców w każdym
z kwadratów, wydzielono cztery klasy zagęszczenia (liczba skupisk poszczególnych
gatunków rdestowców/1 km2– pole badawcze): I – 1 skupisko; II – 4 skupiska; III – 10
skupisk; IV – powyżej 10 skupisk.
Rys. 12–14 przedstawiają zagęszczenie skupień Fallopia japonica, Fallopia ×
bohemica i Fallopia sachalinensis i na terenie Wrocławia.
W 53 kwadratach zajmowanych przez rdestowca japońskiego dominowały
skupiska o zagęszczeniu w zakresie od 2 do 4. Omawiana klasa zagęszczenia
obejmowała 24 pola badawcze. Pojedyncze kępy Fallopia japonica (I klasa
zagęszczenia) odnotowano w 13 kwadratach. Skupiska z najwyższej klasy (ponad 10
skupień/1 km2) wystąpiły w zaledwie 3 polach badawczych.
W przypadku Fallopia sachalinensis, obecność skupisk stwierdzono w dwóch
klasach: od 2 do 4 (2 polach badawcze) oraz od 5 do 10 ( 1 pole badawcze).
Kępy
rdestowca
pośredniego
podobnie,
jak
japońskiego
występowały
najczęściej w zagęszczeniu od 2 do 4 na 1 km2. Odnotowano je w ponad połowie
kwadratów, w których stwierdzono obecność Fallopia × bohemica. W siedmiu polach
występowały pojedyncze skupiska tego gatunku, natomiast największe zagęszczenie
kęp rdestowca pośredniego (10 skupisk/ 1 km2) wystąpiło w jednym polu badawczym.
43
Na rys. 15–17 zilustrowano powierzchnie skupisk rdestowców w podstawowym
polu badawczym (1 km2). W tym celu wyróżniono następujące grupy: I – 1–10 m2, II –
10–40 m2, III – 40–200 m2, IV – powyżej 200 m2.
W przypadku rdestowca japońskiego dominowały skupiska w przedziale 10–40
2
m , które zajmowały prawie połowę pól badawczych (23 kwadraty z 53). Najmniejsze
pod względem powierzchniowym kępy (1–10 m2) mieściły się w 12 kwadratach, zaś
skupiska w grupie 40–200 występowały w 11 polach badawczych. Kępy Fallopia
japonica przekraczające 200 m2 występowały w 7 kwadratach. Odnotowano je przede
wszystkim na obrzeżach centrum i zachodniej części Wrocławia.
W dwóch kwadratach, w zachodniej i południowej części miasta występowały
skupiska rdestowca sachalińskiego, których powierzchnia mieściła się w przedziale 40–
200 m2. We wschodniej części Wrocławia (w jednym polu badawczym) znaleziono zaś
skupiska o powierzchni przekraczającej 200 m2.
Skupiska Fallopia × bohemica wykazywały niewielkie zróżnicowanie pod
względem udziału w poszczególnych klasach powierzchni. Najwięcej – 7 pól
badawczych zajmowały najmniejsze płaty, których powierzchnia nie przekraczyła 10
m2. Skupiska w grupie 10–40 m2 oraz 40–200 m2 odnotowano w 5 polach badawczych.
Największe kępy, te o powierzchni powyżej 200 m2 wystąpiły w 6 kwadratach.
Zlokalizowano je w zachodniej, centralnej i południowej części Wrocławia.
44
Rys. 9. Rozmieszczenie Fallopia japonica na obszarze Wrocławia, na tle sieci kwadratów o powierzchni 1 km 2
45
Rys. 10. Rozmieszczenie Fallopia × bohemica na obszarze Wrocławia, na tle sieci kwadratów o powierzchni 1 km 2
46
Rys. 11. Rozmieszczenia Fallopia sachalinensis na terenie Wrocławia, na tle sieci kwadratów o powierzchni 1 km 2
47
Rys. 12. Zagęszczenie skupisk Fallopia japonica na terenie Wrocławia (liczba skupisk/1 km2)
48
Rys. 13. Zagęszczenie skupisk Fallopia × bohemica na terenie Wrocławia (liczba skupisk/1 km2)
49
Rys. 14. Zagęszczenie skupisk Fallopia sachalinensis na terenie Wrocławia (liczba skupisk/1 km2)
50
Rys. 15. Powierzchnia skupisk Fallopia japonica na terenie Wrocławia z podziałem na grupy wielkości (m2/1 km2)
51
Rys. 16. Powierzchnia skupisk Fallopia × bohemica na terenie Wrocławia z podziałem na grupy wielkości (m2/1 km2)
52
Rys. 17. Powierzchnia skupisk Fallopia sachalinensis na terenie Wrocławia z podziałem na grupy wielkości (m2/1 km2)
53
Uzyskane dane pozwoliły na przeanalizowanie wpływu lokalnych
warunków klimatycznych – w postaci zjawiska tzw. miejskiej wyspy ciepła na
rozmieszczenie rdestowców w granicach administracyjnych Wrocławia (rys. 18).
Miejska wyspa ciepła we Wrocławiu odznacza się skomplikowaną
strukturą [Szymanowski 2004]. Strefy o podwyższonej temperaturze (tzn. 6 do
10) obejmują głównie obszary o zwartej zabudowie np. osiedla: Szczepin,
Popowice i Pilczyce (w północno–zachodniej część miasta), Krzyki, Partnice i
Ołtaszyn (na południu), czy Biskupin, Sępolno i Bartoszowice (we wschodniej
części Wrocławia). Najwyższe temperatury (10 strefa) odnotowuje się w
centralnej części miasta, między innymi w dzielnicy Śródmieście [Szymanowski
2004]. Dzielnice peryferyjne, takie jak Psary, Oporów, Maślice Wielkie czy
Wojnów tworzą własne „ogniska ciepła”. Występujące tam lokalne spadki
temperatury, które generują tereny rekreacyjno–parkowe (strefa nr 3).
Najchłodniejszymi częściami Wrocławia (strefy nr 1 i 2) są pola irygacyjne i
tereny wodonośne, obszary lotniska Starachowice, tereny rolnicze pomiędzy
Ołtaszynem a Jagodnem oraz obszary położone na północny zachód od Psiego
Pola i Leśnicy [Szymanowski 2004].
Interpretując otrzymane wyniki można stwierdzić, że w ekosystemie
miejskim czynnik termiczny może oddziaływać na rozprzestrzenianie się
gatunków z rodzaju Fallopia. We Wrocławiu najwięcej stanowisk rdestowca
japońskiego i pośredniego odnotowano w strefach o podwyższonej temperaturze
(strefa 6, 7, 8), a także w najcieplejszych częściach miasta (strefa 9 i 10).
Rdestowiec sachaliński występował w nieco chłodniejszych rejonach miasta –
(strefa 3 i 4). W najchłodniejszych częściach Wrocławia (strefy nr 1 i 2) skupiska
rdestowców występowały bardzo rzadko. W drugiej strefie ciepła zlokalizowano
jedno skupienie rdestowca pośredniego (zachodnia część miasta) oraz dwa
stanowiska rdestowca japońskiego (południe Wrocławia). Najchłodniejszą częścią
miasta (na granicy 1 i 2 strefy), w obrębie którego potwierdzono obecność
rdestowców były okolice lotniska Starachowice. Odnaleziono tam dwa niewielkie
skupiska Fallopia × bohemica.
Struktura miejskiej wyspa ciepła, jak wspomniano wcześniej, nawiązuje
ściśle do układu urbanistycznego miasta. O przebiegu miejskiej wyspy ciepła na
danym obszarze decyduje m.in. ocieplający wpływ zabudowy, obecność
dodatkowych źródeł emitujących ciepło [Studnik-Wójcikowska 2002], gęstość
54
zaludnienia oraz natężenie ruchu komunikacyjnego [Szymanowski 2004]. Na
przykład, najcieplejsze rejony Wrocławia (10 strefa) w wyniku braku zwartej
zabudowy wzdłuż południowego koryta Odry dzielą się na dwa obszary ciepła.
Nie wykazano natomiast istotnego wpływu ochładzającego rzeki w terenie
zabudowanym [Szymanowski 2004].
Rys. 19 pokazuje rozmieszczenie gatunków z rodzaju Fallopia we
Wrocławiu z uwzględnieniem stopnia jego zabudowy. Widać tu tendencje
rdestowców, zwłaszcza japońskiego i pośredniego do rozprzestrzeniania w się
w
centralnych,
zabudowanych
częściach
miasta.
Obszary
zabudowane
zaznaczono na mapie kolorami od czerwonego do szarego. Współcześnie zajmują
one 31,4% powierzchni miasta. Pozostałe 68,8% stanowią tereny niezabudowane,
do których należą tereny zielone (np. parki i ogrody działkowe) oraz zbiorniki
wodne. Wśród nich najliczniej przez rdestowce zasiedlane są tereny nadwodne.
Na pozostałych terenach niezabudowanych występują pojedyncze stanowiska
rdestowców.
55
1,2 – Strefa zimna
3,4,5 – Strefa umiarkowana
6,7,8 – Strefa ciepła
9,10 – Strefa najcieplejsza
Fallopia japonica
Fallopia sachalinensis
Fallopia x bohemica
Rys. 18. Rozmieszczenie trzech gatunków rdestowców na tle miejskiej wyspy ciepła we Wrocławiu (na podstawie mapy Szymanowskiego, 2004)
56
Tereny zabudowane
Tereny przemysłowe
Tereny zieleni miejskiej i ogródki dzialkowe
Zbiorniki wodne
Fallopia japonica
Fallopia sachalinensis
Fallopia x bohemica
Rys. 19. Rozmieszczenie trzech gatunków rdestowców we Wrocławiu z uwzględnieniem zabudowy terenu (na podstawie mapy Szymanowskiego, 2004)
57
Ze względu na sposób użytkowania terenu we Wrocławiu wyróżniono cztery
typy siedlisk rdestowców: I – obszary zabudowy mieszkaniowej jedno lub
wielokondygnacyjnej, II – tereny zieleni miejskiej (trawniki, parki, ogródki działkowe,
zieleńce i skwery miejskie), III – obszary niezagospodarowane (w tym dzikie
śmietniska, zwałowiska i gruzowiska), IV – tereny usługowe i przemysłowe (w tym
obiekty użyteczności publicznej wraz z parkingami), V – pobocza dróg i torów
kolejowych, VI – tereny nadwodne (brzegi rzek, stawów i rowów melioracyjnych).
Procentowy udział rdestowców w poszczególnych typach siedlisk przedstawiono
na rys. 20 i 21, na których uwzględniono liczbę skupień oraz ich powierzchnię.
Najwięcej kęp rdestowca japońskiego odnotowano na obszarach zabudowy
mieszkaniowej (26,0% ogółu) i na terenach niezagospodarowanych (20,7% ogółu). Na
obszarach zabudowy mieszkaniowej występowały niewielkie i silnie rozproszone
skupiska, których łączna powierzchnia stanowiła 3,1% całkowitej powierzchni tego
gatunku. Natomiast na terenach niezagospodarowanych kępy rdestowca japońskiego
zajmowały 22,6% powierzchni ogólnej. Prawie 20% zarośli Fallopia japonica
zlokalizowano na terenach nadwodnych, głównie wzdłuż Odry. Rdestowiec japoński
tworzył tam duże zwarte skupiska, których powierzchnia stanowiła 51,4% ogółu.
Najmniej skupisk Fallopia japonica zlokalizowano na obszarach zieleni miejskiej.
Wśród siedlisk najczęściej zajmowanych przez rdestowca pośredniego
dominowały tereny niezagospodarowane (41,8% ogółu). Występujące tutaj kępy
stanowiły 46,7% ogólnej powierzchni tego gatunku. Na terenach nadwodnych Fallopia
× bohemica spotykany był rzadziej, a skupiska rdestowca pośredniego tworzyły tam
duże płaty, stanowiąc tym samym 45,4% powierzchni ogólnej. Najmniej stanowisk
Fallopia × bohemica odnotowano na terenach zieleni miejskiej.
Obecność rdestowca sachalińskiego stwierdzono na zaledwie trzech z sześciu
wyróżnionych typów siedlisk: na terenach niezagospodarowanych (75%), na poboczach
dróg i torów kolejowych (18,8%) oraz na terenach nadwodnych (6,2%). Największą
powierzchnię,
stanowiącą
43,6%
powierzchni
wszystkich
skupisk
Fallopia
sachalinensis, zajmowały kępy występujące na poboczach dróg i torów kolejowych.
Najmniejsze pod względem powierzchniowym stanowiska (zajmujące 17,5% ogółu)
zlokalizowano na obszarach zabudowy mieszkaniowej.
58
I – obszary zabudowy mieszkaniowej jedno lub wielokondygnacyjnej
II – tereny zieleni miejskiej
III –obszary niezagospodarowane
IV – tereny usługowe i przemysłowe
V – pobocza dróg i torów kolejowych
VI – tereny nadwodne
Rys. 20. Procentowy udział kęp rdestowców (a – Fallopia japonica, b – Fallopia × bohemica,
c – Fallopia sachalinensis) w poszczególnych typach siedlisk z uwzględnieniem liczby skupień
59
I – obszary zabudowy mieszkaniowej jedno lub wielokondygnacyjnej
II – tereny zieleni miejskiej
III –obszary niezagospodarowane
IV – tereny usługowe i przemysłowe
V – pobocza dróg i torów kolejowych
VI – tereny nadwodne
Rys. 21. Procentowy udział kęp rdestowców (a – Fallopia japonica, b – Fallopia × bohemica,
c – Fallopia sachalinensis) w poszczególnych typach siedlisk z uwzględnieniem powierzchni skupień
60
7.1.2.
WŁAŚCIWOŚCI CHEMICZNE GLEB
Niektóre właściwości chemiczne gleb pobranych z 23 stanowisk rdestowców
przedstawiono w tab. 6 i 7.
Rdestowiec japoński występował na glebach, których pH mierzone w KCl
mieściło się w zakresie od 6,1 do 7,3, zaś w H2O w przedziale od 6,7 do 7,5. Wśród
nich dominowały gleby o odczynie obojętnym, czyli takie, których pH w KCl mieściło
się w zakresie od 6,6 do 7,2, zaś w H2O w przedziale od 6,9 do 7,4. Rdestowiec
pośredni zajmował gleby o nieco szerszym zakresie pH, tzn. od 5,4 do 7,9
– pH w KCl, a w H2O od 6,0 do 8,0. Natomiast Fallopia sachalinensis porastał gleby
obojętne, których pH mierzone w KCl wyniosło od 7,0, a w H2O – 7,3 i 7,4 i gleby
słabo zasadowe – pH w KCl 7,7, a w H2O 7,8.
Większość analizowanych prób glebowych odznaczała się bardzo wysoką
zawartością przyswajalnych form P, K i Mg. Za takie gleby uznaje się te, w których
zawartość przekracza 20 mg P2O5/100 g gleby, 25 mg K2O/100g gleby oraz 7,0 mg
Mg/100g gleby (mg·100g-1) [Karczewska i Kabała 2008]. Najwyższe zawartości P2O5
(129,5 mg·100g-1) i K2O (127,0 mg·100g-1) miała gleba ze stanowiska Fallopia
japonica (nr 3) zlokalizowanego w ogrodzie przydomowym przy ul. Elizy
Orzeszkowej. Najmniej fosforu (poniżej 13,0 mg·100g-1) zawierał materiał ze stanowisk
Fallopia × bohemica przy ul. Paczkowskiej (nr 14) oraz Swobodnej (nr 19).
Najmniejsze zawartości potasu (11,5 mg·100g-1) stwierdzono w glebie ze stanowiska nr
6 (Fallopia japonica – Odra). W próbie pochodzącej ze stanowiska nr. 14 stwierdzono
wysokie zawartości magnezu (35,0 mg·100g-1), natomiast najmniej Mg (zaledwie 3,60
mg·100g-1) zawierał materiał glebowy ze stanowiska nr 20. Gleby pobrane ze stanowisk
Fallopia japonica zawierały od 2,10% (stanowisko 2) do 11,32% C organicznego
(stanowisko 6) oraz od 0,15% (stanowisko 8) do 0,40% N ogólnego (stanowisko 6).
Zawartość Corg i Nog w glebach pokrytych przez Fallopia × bohemica zawierała się w
szerokich przedziałach. W przypadku węgla od 1,20% (stanowisko 19) aż do 14,48%
(stanowisko 14), a w przypadku N od 0,03% (stanowisko 12) do 0,42% (stanowisko
16). Fallopia sachalinensis występował na glebach, w których zawartości
C organicznego kształtowała się w zakresie od 3,23% do 1,15 %, a N ogólnego
w przedziale od 0,23% do 0,05%.
Znamienną cechą środowiska miejskiego jest zanieczyszczenie gleb metalami
ciężkimi. Pierwiastkami śladowymi, których poziom w warunkach miejskich często
61
przekracza progowe normy są Cd, Cr, Cu, Zn oraz Pb. Zawartości dopuszczalnych
stężeń metali ciężkich w glebach Polski określone zostały w Rozporządzeniu Ministra
Środowiska dnia 9 września 2002 r. w sprawie w standardów jakości gleby oraz
standardów
jakości
ziemi
(Dz.U.02.165.1359).
Analizując
uzyskane
wyniki
stwierdzono, że w wybranych próbach glebowych poziom metali ciężkich przekraczał
zawartości naturalne. Natomiast dopuszczalny poziom metali ciężkich został
przekroczony w przypadku Zn i Pb.
Zawartość Cd w materiale glebowym pochodzącym ze stanowisk rdestowców
kształtowała się w granicach od 0,21 do 1,91 mg·Pkg-1 – stanowiska Fallopia japonica,
od 0,04–2,99 mg·Pkg-1 – stanowiska Fallopia × bohemica oraz od 0,01 do 0,97 mg
·kg-1 – stanowiska Fallopia sachalinensis. Naturalna zawartość kadmu w glebach mieści
się w przedziale od 0,03 do 0,3 µg·g-1 (mg·kg-1) [Allen 1989]. Wartość ta została
przekroczona w próbach pochodzących ze stanowisk nr 3 (1,91 mg·kg-1) oraz nr 14
(2,21 mg·kg-1). Zgodnie z Rozporządzeniem Ministra Środowiska [2002] dopuszczalna
zawartość Cd w gruntach zabudowanych i zurbanizowanych (z wyjątkiem terenów
komunikacyjnych i przemysłowych) wynosi 4,0 mg·Pkg-1. W żadnej z badanych prób
nie stwierdzono przekroczenia tej wartości.
Chrom w glebach, na których rosły kępy rdestowca japońskiego występował
w granicach od 14,60 do 61,50 mg·kg-1 (w przypadku rdestowca pośredniego od 7,90
do 47,30 mg·kg-1, a rdestowca sachalińskiego od 10,10 do 18,0 mg·kg-1). Jak podaje
Allen [1989], naturalna zawartość Cr w glebach waha się w zakresie od 10 do 200 µg
·g-1 (mg·kg-1), a dopuszczalna zawartość tego pierwiastka w glebach wynosi 150
mg·kg-1 [Rozporządzenie Ministra Środowiska 2002]. W analizowanych glebach
naturalna zawartość Cr został przekroczona w próbie pochodzącej ze stanowiska nr 6
(61,50 mg·kg-1), natomiast jego dopuszczalne zawartości nie zostało przekroczone.
Gleby pochodzące ze stanowisk badawczych zawierały znaczne ilości miedzi,
tzn. od 15,0 do 171,7 mg·kg-1 w przypadku Fallopia japonica, od 11,6 do 116,0 mg·kg-1
– Fallopia × bohemica oraz 7,20 – 39,60 mg·kg-1 – Fallopia sachalinensis. We
wszystkich próbach została przekroczona naturalna zawartość Cu, która według Allena
[1989] waha się w granicach od 0,1 do 1,0 µg·g-1 (mg·kg-1). Zgodnie
z rozporządzeniem, dopuszczalna zawartość miedzi w glebach to 150,0 mg·kg-1, a więc
wartość ta w analizowanym materiale glebowym nie została przekroczona.
We wszystkich badanych glebach stwierdzono wysokie zawartości Zn. Allen
[1989] podaje, że normalna zawartość tego pierwiastka w glebach wynosi od 20–300
62
µg·g-1 (mg·kg-1), natomiast według Knoxa i in. [1999] wynosi ona od 40 do 70 mg·kg-1.
Zgodnie z rozporządzeniem, dopuszczalna zawartość cynku w glebie nie może
przekraczać 300 mg Zn ·kg-1 sm gleby. W 13 z 23 analizowanych prób glebowych
zanotowano przekroczenie wskazanych w rozporządzeniu norm. Najwyższą zawartość
Zn (1721,0 mg·kg-1) miała gleba ze stanowiska nr 14 (Fallopia × bohemica
– ul.Paczkowska).
Materiał glebowy zawierał od 2,6 mg·kg-1 (stanowisko rdestowca japońskiego)
do 1135,0 mg·kg-1 (rdestowiec pośredni) ołowiu. Naturalna zawartość tego pierwiastka
w glebach wynosi od 2 do 29 µg·g-1 (mg·kg-1) [Allen 1989], natomiast według Gorlacha
i Gambusia
[2000] kształtuje się w zakresie od 1 do 25 mg·kg-1. Dopuszczalna
zawartość Pb zgodnie z rozporządzeniem wynosi 100 mg·kg-1. Została ona
przekroczona w siedmiu z 23 analizowanych prób glebowych.
63
Tab. 6. Właściwości chemiczne gleb na terenie Wrocławia (stanowiska Fallopia japonica, Fallopia
× bohemica i Fallopia sachalinensis)
pH
Stanowisko
N ogólny
C organiczny
Formy przyswajalne
[mg·100g -1]
K2O
P2O5
Mg
KCl
H2O
%
%
1
2
3
4
5
7,2
7,3
7,1
6,7
6,6
7,4
7,5
7,1
6,9
6,9
0,17
0,21
0,20
0,31
0,21
5,19
3,24
3,55
2,10
3,50
38,5
36,3
127,0
42,4
21,7
47,0
26,6
129,5
64,0
30,9
6,2
9,1
16,6
15,5
19,2
6
7
8
9
10
6,1
7,2
7,3
6,9
7,2
6,7
7,4
7,5
7,2
7,4
0,40
0,34
0,15
0,25
0,18
11,32
3,76
2,50
3,49
5,06
11,5
54,8
28,9
58,0
20,5
22,1
72,5
24,7
65,5
29,7
17,5
8,2
8,0
12,2
6,2
Średnia
Minimum
Maksimum
Odchylenie stand.
Współczynnik
zmienności [%]
6,9
6,1
7,3
0,4
7,2
6,9
7,5
0,4
0,2
0,1
0,4
0,1
4,4
2,1
11,3
2,6
44,0
11,5
127,0
32,7
51,3
22,1
129,5
33,3
11,9
6,2
19,2
5,0
5,6
4,0
33,9
60,0
74,4
65,0
41,8
6,6
7,9
7,4
7,6
7,1
6,9
6,0
6,8
8,0
7,5
7,6
7,3
7,1
6,5
0,33
0,03
0,14
0,27
0,29
0,42
0,40
4,06
1,20
1,50
14,48
5,97
7,09
8,61
47,7
21,4
23,4
24,4
34,0
59,7
37,8
48,5
17,7
32,7
12,4
58,5
49,5
22,5
19,3
6,5
11,1
35,0
5,4
10,2
4,1
5,4
7,5
7,1
6,9
6,0
7,6
7,3
7,1
0,10
0,04
0,12
0,16
1,80
1,10
2,40
4,80
27,8
38,8
30,5
34,5
34,9
12,8
44,0
33,4
18,4
16,5
3,6
13,0
5,4
7,9
0,8
6,0
8,0
0,6
0,03
0,42
0,1
1,10
14,48
4,3
21,4
59,7
12,0
12,4
58,5
16,5
3,6
35,0
9,7
11,0
8,3
68,0
89,5
34,7
49,6
74,4
7,7
7,0
7,0
7,2
7,0
7,7
0,4
7,8
7,3
7,4
7,5
7,3
7,8
0,3
0,05
0,24
0,22
0,14
0,05
0,24
0,10
1,15
3,23
3,23
2,5
1,2
3,2
1,2
32,6
57,7
35,0
41,8
32,6
57,7
13,9
15,7
39,5
22,9
26,0
15,7
39,5
12,2
5,3
14,1
12,3
10,6
5,3
14,1
4,6
5,6
3,5
63,3
47,3
33,2
46,9
44,0
Fallopia japonica
Fallopia × bohemica
11
12
13
14
15
16
17
18
19
20
Średnia
Minimum
Maksimum
Odchylenie stand.
Współczynnik
zmienności [%]
Fallopia sachalinensis
21
22
23
Średnia
Minimum
Maksimum
Odchylenie stan.
Współczynnik
zmienności [%]
64
Tab. 7. Zawartość metali ciężkich [mgּkg-1] w materiale glebowym pobranym ze stanowisk Fallopia
japonica, Fallopia × bohemica i Fallopia sachalinensis
Zawartość metali ciężkich (mgּkg-1)
Numer
stanowiska
Cd
Cr
Cu
Pb
Zn
Fallopia japonica
1
2
0,80
0,21
14,6
16,1
117,7
42,2
321,9
84,6
406,4
174,8
3
4
5
6
7
8
9
10
1,91
0,57
0,79
3,28
0,31
0,65
0,60
0,23
16,3
21,0
16,9
61,5
16,8
30,9
13,8
13,1
101,5
106,7
15,0
81,3
27,9
171,7
31,8
30,8
151,2
151,5
20,6
83,9
48,1
99,8
55,9
41,6
1007,0
368,3
302,7
900,6
173,7
345,8
317,6
139,7
Średnia
Minimum
Maksimum
Odchylenie stand.
0,93
0,23
3,28
1,0
22,1
13,1
61,5
14,8
72,2
15,0
171,7
51,2
105,9
20,6
321,9
87,6
413,7
139,7
1007,0
299,5
Współczynnik
zmienności [%]
102,3
66,8
70,4
82,7
72,4
Fallopia × bohemica
11
12
0,37
0,11
21,1
7,9
40,9
12,0
62,1
34,1
216,7
112,6
13
14
15
16
17
18
19
20
0,28
2,21
0,75
0,70
2,99
0,26
0,04
0,97
11,7
21,3
14,0
28,9
47,3
8,6
14,3
25,0
51,9
116,0
105,9
59,2
70,9
17,9
11,6
29,6
38,2
1336,0
110,0
364,1
107,1
32,7
11,5
67,1
183,6
1721,0
622,5
544,4
862,0
137,1
65,0
223,3
Średnia
Minimum
Maksimum
Odchylenie stand.
0,86
0,04
2,99
0,98
20,0
7,9
47,3
11,9
51,6
11,6
116,0
37,2
216,3
11,5
1336,0
406,3
448,8
65,0
1721,0
511,8
Współczynnik
zmienności [%]
112,5
59,3
72,0
187,8
109,2
Fallopia sachalinensis
21
22
23
0,01
0,62
0,53
10,1
17,7
18,0
7,2
35,0
39,6
10,6
62,6
62,1
55,6
500,0
157,4
0,38
0,01
0,62
0,3
15,3
10,1
18,0
4,5
27,3
7,2
39,6
17,5
45,1
10,6
62,6
29,9
237,7
55,6
500,0
232,8
86,5
29,3
64,3
66,3
98,0
Średnia
Minimum
Maksimum
Odchylenie stand.
Współczynnik
zmienności [%]
65
7.1.3.
CHARAKTERYSTYKA WYBRANYCH KLONÓW RDESTOWCÓW
W celu prawidłowego określenia gatunków z rodzaju Fallopia występujących na
terenie Wrocławia przeprowadzono analizę morfologiczną liści i kwiatów. Ponadto,
u rdestowca sachalińskiego i pośredniego wykonano badania cytologiczne określając
ich liczbę chromosomów. Umożliwiło to prawidłową identyfikację oraz porównanie
występujących we Wrocławiu przedstawicieli rodzaju Fallopia z rdestowcami z innych
obszarów – w dyskusji wyników.
I – Charakterystyka liści rdestowców
Pierwsze analizowane cechy dotyczyły liści rdestowców. Jak podkreślają Bailey
i Wisskirchen [2006], Bailey i in. [2007] oraz Tiébré i in. [2007a] morfologia liści,
a w szczególności kształt i wielkość blaszek liściowych – to podstawowe elementy
ułatwiające identyfikcję i charakterystykę poszczególnych taksonów. Analizę
morfologiczną liści przeprowadzono w oparciu o metodykę Tiébré i in. [2007a].
Uwzględniono tu następujące cechy: I– szerokość podstawy liścia [cm], II – szerokość
środkowej części liścia [cm], III– długość liścia [cm], IV– wcięcie blaszki liściowej
[mm], V– długość wierzchołka liścia [cm] oraz VI– szerokość wierzchołka liścia [cm].
Pomiary przeprowadzono na 10 klonach Fallopia japonica (stanowiska badawcze od 1
do 10) i Fallopia x bohemica (stanowiska od 11 do 20) oraz trzech klonach Fallopia
sachalinensis (stanowiska od 21 do 23). Charakterystykę liści rdestowców
przedstawiono w tab. 8.
W przypadku rdestowca japońskiego dla I i VI cechy liści (szerokość podstawy
liścia i szerokość wierzchołka liścia) wyznaczono 5 grup jednorodnych. Najmniejszą
średnią szerokość podstawy miały liście pobrane ze stanowiska nr 1 (6,4 cm),
najwyższe średnie wartości badanej cechy wykazał materiał ze stanowiska nr 3 (8,4 cm)
i 10 (8,5 cm). Największą szerokość miały wierzchołki roślin występujących na
stanowisku nr 6 (1,1 cm), najmniejszą zaś na stanowisku nr 3 (1,5 cm). Wśród średnich
wartości II i III cechy (szerokość środkowej części liścia i długość liścia) wyróżniono 4
grupy jednorodne. Najmniejsze średnie wartości II cechy miały liście ze stanowisk nr 1
i 4 (9,6 cm) oraz 9 (9,8 cm), najwyższe ze stanowiska nr 3 (11,5 cm). Liście Fallopia
japonica na stanowiskach nr 4 i 9 były najkrótsze (1,8 cm i 12,4 cm), najdłuższe liście
miały pędy na stanowisku nr 3 (14,6 cm), 7 (14,0 cm) oraz 10 (14,3 cm). Dla cech V
(długość wierzchołka liścia) wyznaczono 3 grupy jednorodne. Średnia długość
wierzchołka liści kształtowała się w granicach 1,2 cm (stanowisko 7) do 1,6 cm
66
(stanowisko 4 i 8). Wszystkie liście Fallopia japonica charakteryzowały się „uciętą”
nasadą i niepowcinaną blaszką liściową.
Pobrane z trzech stanowisk liście Fallopia sachalinensis wykazały niewielki
stopień zróżnicowania. Dla I cechy wyznaczono 3 grupy jednorodne. Średnia szerokość
podstawy liści rdestowca sachalińskiego wahała się w przedziale od 18,4 cm do 20,2
cm. Cechy II, III, IV i V zaliczono do tej samej grupy. Szerokość środkowej części
liścia (II cecha) kształtowała się w zakresie od 19,4 cm do 20,2 cm. Najdłuższe liście
(25,4 cm) miały rośliny ze stanowiska nr 21, najkrótsze zaś (23,8 cm) ze stanowiska nr
23. Wcięcie blaszki liściowej kształtowało się od 27 mm do 34 mm. Dla VI cechy –
szerokość wierzchołka liścia (VI cecha) wyznaczono 2 grupy jednorodne. Średnia
szerokości
wierzchołka
liściki
rdestowca
sachalińskiego
zawierała
się
w przedziale od 0,9 cm do 1,4 cm.
Liście Fallopia × bohemica ze względu na pośredni charakter pomiędzy
osobnikami rodzicielskimi wykazywały wyższe – w porównaniu z gatunkami
rodzicielskimi – zróżnicowanie badanych cech. W przypadku IV cechy liści rdestowca
pośredniego wyznaczono sześć grup jednorodnych, dla I i V siedem grup jednorodnych,
zaś dla cechy II dziewięć grup. Najmniejszym wcięciem blaszki liściowej (wartość
średnia) charakteryzowały się liście pochodzące ze stanowisk nr 12 i 14 (4,0 mm i 3,0
mm), natomiast największym ze stanowiska 16 (22 mm). Największą średnią szerokość
podstawy oraz środkowej części liścia miał materiał pobrany ze stanowiska nr 16 (14,3
cm – I cecha i 16,0 cm – II cecha), najmniejszą zaś liście pochodzące ze stanowiska nr
18 (7,4cm – I cecha i 9,9 cm – II cecha). Średnia długość wierzchołka liści ze
stanowisk 16 i 18 była najmniejsza (1,2 cm), najdłuższa zaś u liści ze stanowiska 14
(2,0 cm). W przypadku III i IV cech wyróżniono sześć grup jednorodnych. Analiza
wykazała, że najdłuższe liście Fallopia × bohemica pochodziły ze stanowisk 14 i 19
(18,5 cm – wartości średnie), a najkrótsze ze stanowiska 18 (13,3 cm). Ostatnią badaną
cechą była szerokość wierzchołka liściowego, tu wyznaczono 5 grup jednorodnych. Do
grupy o największej średniej szerokości wierzchołka zaliczono liście ze stanowisk 11
(1,5 cm), 14 (1,7 cm) oraz 17 i 18 (1,6 cm), najmniejsza średnią szerokość posiadały
wierzchołki liści ze stanowiska 19 (0,9 cm).
Przedstawione wyniki pomiarów sześciu cech liści rdestowców występujących
we Wrocławiu okazów rdestowców są zbieżne z danymi literaturowymi. Podobne cechy
morfologiczne liści wykazują okazy notowane na terenie Europy [Bailey i Wisskirchen
67
2006; Tiébré i in. 2007a; Bailey i in. 2008] i Ameryki Północnej [Zica i Jacobson 2003;
Barney i in. 2006].
Tab. 8. Średnie wartości badanych cech liści trzech gatunków rdestowców z poszczególnych
stanowisk. Grupy jednorodne wyznaczone za pomocą testu HSD Tukeya po jednoczynnikowej
analizie wariancji
Liczby oznaczone tą samą literą nie różnią się istotnie przy poziomie p≤ 0,05
Szerokość
podstawy
liścia [cm]
(I)
Szerokość
środkowej
części liścia
[cm]
(II)
Długość
liścia [cm]
(III)
Wcięcie
blaszki
[mm]
(IV)
Długość
wierzchołka
[cm]
(V)
Szerokość
wierzchołka
[cm]
(VI)
1
6,4 a
9,6 a
12,8 ab
brak
1,3 ab
1,2 ab
2
7,1 ab
10,4 ab
12,7 ab
brak
1,3 ab
1,2 ab
3
8,4 c
11,5 c
14,6 c
brak
1,5 ab
1,5 c
4
7,1 ab
9,5 a
11,8 a
brak
1,6 ab
1,4 abc
5
7,1 ab
10,3 ab
12,8 ab
brak
1,5 ab
1,3 abc
6
7,4 abc
10,4 ab
12,7 ab
brak
1,3 ab
1,1 a
7
7,7 bc
10,4 ab
14,0 c
brak
1,2 a
1,3 abc
8
7,1 ab
10,4 ab
13,6 bc
brak
1,6 c
1,3 abc
9
7,4 abc
9,8 a
12,4 a
brak
1,4 ab
1,4 bc
10
8,5 c
11,0 bc
14,3 c
brak
1,5 ab
1,3 abc
11
9,3 bc
12,8 de
18,3 ab
9,0 abc
1,6 abcd
1,5 a
12
8,0 ab
12,5 bcd
17,2 ab
4,0 c
1,9 cd
1,4 ab
13
7,8 a
10,9 abc
16,6 bc
7,0 bc
1,8 bcd
1,0 bc
14
7,8 ab
10,8 ab
18,5 a
3,0 c
2,0 d
1,7 a
15
10,6 cd
12,7 cde
17,3 ab
11,0 ab
1,7 bcd
1,1 bc
16
14,3 f
16,0 f
17,5 ab
22,0 d
1,2 a
1,4 ab
17
12,7 ef
14,5 ef
18,3 ab
13,0 a
1,4 abc
1,6 a
18
7,4 a
9,9 a
13,3 d
14,0 a
1,2 a
1,6 a
19
12,0 de
15,4 f
18,5 a
12,0 ab
1,3 ab
0,90 c
20
8,4 ab
11,5 abcd
15,2 c
12,0 ab
1,6 abc
1,1 bc
Numer
stanowiska
Fallopia japonica
Fallopia × bohemica
Fallopia sachalinensis
21
18,4 a
19,9 a
25,4 a
34,0 a
1,0 a
0,9 b
22
19,2 ab
19,4 a
24,2 a
28,0 a
0,8 a
1,4 a
23
20,2 b
20,2 a
23,8 a
27,0 a
0,9 a
1,1 a
68
II – Charakterystyka kwiatów rdestowców
Analizowane kwiaty 10 okazów rdestowca japońskiego nie różniły się pod
względem morfologicznym. We wszystkich stwierdzono obecność dużego słupka
z trzema wyraźnymi znamionami. Pręcikowie było silnie zredukowane. W naturalnym
zasięgu geograficznym (Chiny, Japonia, Korea) spotykane są męskie, żeńskie oraz
hermafrodytyczne osobniki rdestowca japońskiego [Bailey 2003]. Natomiast do Europy
zostały introdukowane wyłącznie żeńskie okazy tego gatunku [Bailey i in. 2008].
Stwarza to możliwość rozprzestrzeniania się rdestowca japońskiego poza naturalnym
obszarem jedynie drogą wegetatywną. Co więcej, występujące na kontynencie
europejskim okazy Fallopia japonica nie wykazują zróżnicowania genetycznego,
wszystkie zawierają oktoploidalną liczbę chromosomów i reprezentują prawdopodobnie
ten sam genotyp. Fakt ten potwierdzają badania naukowców brytyjskich [Bailey i in.
1996; Hollingsworth i Bailey 2000] i czeskich [Mandák i in. 2005]. Na terenie
Wrocławia, podobnie jak w innych częściach Europy (Wielka Brytania, Francja,
Niemcy, Czechy, Holandia, Belgia) potwierdzono obecność wyłącznie żeńskich klonów
Fallopia japonica.
Na obszarze Wrocławia zidentyfikowano męskosterylne (żeńskie) i obupłciowe
okazy Fallopia × bohemica (tab. 9). Kwiaty żeńskie wytwarzały rośliny występujące na
stanowiskach przy ul. Grunwaldzkiej, Kamiennej, Orzechowej, Paczkowskiej,
Sanockiej i Ślicznej. Obupłciowe kwiaty rdestowca pośredniego zlokalizowano na ul.
Gnieźnieńskiej, Nasypowej, Robotniczej, Powstańców Śląskich, Swobodnej i pl. Św.
Macieja oraz nad Odrą. Żeńskie i obupłciowe okazy Fallopia × bohemica notowane są
też w innych częściach Europy i świata. Ich obecność potwierdzono w Wielkiej Brytanii
[Bailey 1989; Hart i in. 1997], Francji [Schnitzler i in. 2007], Belgii [Tiébré i in.
2007b], a także w Ameryce Północnej, Australii i Nowej Zelandii [Bailey 2003].
Kwiaty u badanego Fallopia sachalinensis były obupłciowe. Charakteryzowała
je obecność niewielkich słupków i dużych wystających z okwiatu pręcików. W Europie
notowane się głównie żeńskie osobniki tego gatunku [Bailey 1989; Bailey i Stace 1992;
Bailey 1994; Hart i in. 1997; Mandák i in. 2003], natomiast hermafrodyczne okazy
rdestowca sachalińskiego spotykane są rzadziej [Bailey 1994; Tiébré i in. 2007b]. Fakt
ten zasługuje na uwagę, gdyż współwystępowaniem na danym terenie żeńskich okazów
Fallopia japonica i obupłciowych klonów Fallopia sachalinensis zwiększa szanse na
powstanie nowych form międzygatunkowego mieszańca – Fallopia × bohemica.
69
III – Liczba chromosomów rdestowców
Rdestowce występują z natury na różnych poziomach ploidalności. Największe
zróżnicowanie liczby chromosomów wykazuje Fallopia × bohemica. Cecha ta, ze
względu na podobieństwo mieszańca do taksonów rodzicielskich umożliwia jego
ostateczną identyfikację [Hart i in. 1997].
Wyniki analiz dotyczących liczby chromosomów rdestowców zamieszczono
w tab. 10. Wszystkie badane klony Fallopia × bohemica były heksaploidalne (2n=66).
W Europie stwierdzono – jak dotąd, okto, heksa i tetraploidalne osobniki tego gatunku
[Bailey 2003]. Ploidalność klonów rdestowca pośredniego ma wpływ na jego
propagację drogą generatywną. Bailey i Stace [1992] podkreślają, że zdolne do dalszego
rozwoju nasiona produkują przede wszystkim tetra i oktoploidalne klony. Natomiast
u osobników heksaploidalnych proces wytwarzania nasion jest zaburzony ze względu
na nieregularne podziały mejotyczne. Można, więc przypuszczać, że rdestowiec
pośredni rozmnaża się w obszarze Wrocławia wyłącznie drogą wegetatywną.
Analizowany klon rdestowca sachalińskiego był tetraploidalny (2n=44), tak jak
większość przebadanych w Europie osobników tego gatunku [Hart i in. 1997; Mandák
i in. 2005; Schnitzler i in. 2007; Tiébré i in. 2007b].
70
Tab. 9. Charakterystyka kwiatów Fallopia × bohemica i Fallopia sachalinensis występujących na
terenie Wrocławia.
Ulica
N
Lokalizacja
E
Kwiaty
Fallopia × bohemica
Gnieźnieńska
51°07.308'
17°00.584'
obupłciowe
Gnieźnieńska
51°07.304'
17°00.455'
obupłciowe
Grunwaldzka
51°06.930'
17°04.261'
męskosterylne (żeńskie)
Kamienna
51°05.153'
17°02.681'
męskosterylne (żeńskie)
Nasypowa
51°06.012'
17°01.665'
obupłciowe
Odra
51°06.035'
17°04.643'
obupłciowe
Odra
51°06.030'
17°04.677'
obupłciowe
Orzechowa
51°04.676'
17°02.390'
męskosterylne (żeńskie)
Orzechowa
51°04.660'
17°02.361'
męskosterylne (żeńskie)
Paczkowska
51°05.385'
17°02.928'
męskosterylne (żeńskie)
Paczkowska
51°05.383'
17°02.932'
męskosterylne (żeńskie)
Powstańców Śląskich
51°05.739'
17°01.295'
obupłciowe
Powstańców Śląskich
51°05.774'
17°01.249'
obupłciowe
Robotnicza
51°06.710'
16°59.999'
obupłciowe
Robotnicza
51°06.699'
16°59.977'
obupłciowe
Sanocka
51°05.658'
17°01.780'
męskosterylne (żeńskie)
Sanocka
51°05.770'
17°01.874'
męskosterylne (żeńskie)
Swobodna
51°05.911'
17°01.840'
męskosterylne (żeńskie)
Św. Macieja Plac
51°07.180'
17°02.079'
obupłciowe
Śliczna
51°05.080'
17°02.378'
męskosterylne (żeńskie)
51°06.190'
17°08.635'
obupłciowe
Fallopia sachalinensis
Tatarakowa
Tab. 10. Liczba chromosomów u Fallopia × bohemica i Fallopia sachalinensis
Fallopia × bohemica
2n=66
Fallopia sachalinensis
2n=44
71
7.1.4.
DYNAMIKA WZROSTU ORAZ PRZEBIEG FAZ ROZWOJOWYCH
RDESTOWCÓW W WARUNKACH MIEJSKICH
Badania nad przebiegiem faz fenologicznych rdestowców przeprowadzono
w ciągu dwóch sezonów wegetacyjnych (w latach 2009 i 2010). Na rys. 22 i 23
przedstawiono rozkład średnich miesięcznych temperatur powietrza oraz miesięcznych
sum opadów atmosferycznych w 2009 i 2010 roku.
W roku 2009 średnia roczna temperatura powietrza wyniosła 9,4˚C, a w 2010
roku 8,2˚C. Rok 2010 w porównaniu, z rokiem poprzednim charakteryzował się niższą
temperaturą powietrza w miesiącach zimowych (styczeń, luty, grudzień) oraz wyższą w
okresie letnim (czerwiec, lipiec, sierpień). W roku 2010 średnia temperatura
w miesiącach zimowych wyniosła –4,0˚C, a w roku 2009 –0,8˚C. Średnia temperatura
powietrza w okresie letnim w 2010 roku kształtowała się w granicy 19,4˚C, rok
wcześniej – na poziomie 13,7˚C. Rok 2010 charakteryzował się większą sumą opadów,
w porównaniu z rokiem poprzednim. W 2010 roku suma opadów wyniosła 772,6 mm.
Szczególnie intensywne opady wystąpiły w kwietniu (140,7 mm – miesięczna suma
opadów), w lipcu (109,0 mm) i we wrześniu (134,1 mm). Najmniejszy średni opad
odnotowano w październiku – 5,7 mm. Dla porównana, w 2009 roku średnie opady
wyniosły 730,0 mm. Największy opad wystąpił w miesiącach letnich, w czerwcu (141,4
mm) i lipcu (134,2 mm). W 2009 roku jednym z najbardziej suchych miesięcy był
wrzesień ze średnim opadem na poziomie 12 mm, czyli ponad 11 razy mniejszym niż w
roku 2010.
72
25,0
20,0
Temperatura [C]
15,0
10,0
5,0
0,0
I
II
III
IV
V
VI
VII
VIII
IX
X
XI
XII
-5,0
Miesiące
-10,0
2009 rok
2010 rok
Rys. 22. Rozkład średnich miesięcznych temperatur powietrza we Wrocławiu w latach 2009 i 2010
(dane Katedry Agrometeorologii Uniwersytetu Przyrodniczego we Wrocławiu)
160
140
Opady [mm]
120
100
80
60
40
20
0
I
II
III
IV
V
VI
VII
Miesiące
VIII
IX
X
XI
XII
2009 rok
2010 rok
Rys. 23. Rozkład średnich sum opadów atmosferycznych we Wrocławiu w latach 2009 i 2010 (dane
Katedry Agrometeorologii Uniwersytetu Przyrodniczego we Wrocławiu)
73
W wyniku przeprowadzonych obserwacji stwierdzono 5 faz rozwojowych
rdestowców, a wśród nich 14 faz, które można skojarzyć z fenologią
I – Wzrost pędów
P1 – pojawianie się pąków pędowych (na około 50% powierzchni zajmowanej przez
dane skupisko rdestowców pojawiają się pąki pędowe)
P2 – pojawianie się i początek wzrostu elongacyjnego pędów (na około 50%
powierzchni zajmowanej przez dane skupisko pojawiają się pędy, które rozpoczynają
wzrost elongacyjny)
P3 – koniec wzrostu pędów (obserwacje wskazują, iż pędy zakończyły wzrost
i osiągnęły wysokość maksymalną)
II – Rozwój liści
L1 – początek rozchylania się pąków liściowych (około 50% pędów rozchyliło pąki
liściowe)
L2 – pojawianie się liści (około 50% pędów wytworzyło blaszki liściowe)
L3 – pierwsze liście normalnej wielkości (około 50% pędów ma liście o rozmiarze
typowy dla gatunku)
III – Przebarwianie i zrzucanie liści
L4 – przebarwianie się liści (około 50% liści jest przebarwionych)
L5 – zrzucanie liści (około 50% liści na danym skupisku opadło)
IV – Rozwój kwiatów
K1 – pojawianie się kwiatostanów (około 50% pędów wytworzyło kwiatostany)
K2 – kwitnienie (około 50% kwiatów zakwitło)
K3 – opadanie kwiatów (około 50% kwiatów opadło)
V – Rozwój owoców
O1 – formowanie się pierwszych trójgraniastych orzeszków
O2 – pełnia owocowania – około 50 % pędów owocuje
O3 – opadanie owoców (około 50% owoców występujących na pędach opadło)
74
Przebieg poszczególnych faz rozwojowych rdestowców na terenie Wrocławia
w latach 2009 i 2010 przedstawiono w tab. 11 i 12. Na wszystkich stanowiskach
rdestowca japońskiego i sachalińskiego, podczas dwóch lat obserwacji wystąpiło 14 faz
związanych z fenologią. Wśród skupisk rdestowca japońskiego najdłuższy okres
wegetacji
miały
rośliny
na
stanowisku
numer
10
zlokalizowanym
przy
ul. Tramwajowej. W roku 2009 wyniósł on 236 dni, rok później 223 dni. Spośród
wszystkich
rdestowców
najkrótszą
wegetacją
charakteryzował
się
Fallopia
sachalinensis. Na stanowisku przy ul. Tatarakowej wegetacja w roku 2009 trwała 212
dni, a w 2010 roku 207 dni. W przypadku rdestowca pośredniego na wszystkich
stanowiskach zanotowano fazy od P1 do K3. Natomiast nie wszystkie klony wytwarzały
owoce. W 2009 roku owoce obserwowano na stanowiskach numer: 12, 13, 15, 16, 17
i 18. Rok później jedynie na stanowisku numer 16. W roku 2009 najdłuższą wegetację
miały rośliny ze stanowiska numer 16 – 256 dni. W roku 2010 najdłuższy okres
wegetacji, wyniósł 224 dni ( stanowisko nr 17).
I – Wzrost pędów
Gatunki z rodzaju Fallopia są geofitami, w związku z tym ich pąki odnawiające
zimują pod powierzchnią gleby. Rozwój rdestowców rozpoczyna się od pojawienia się
na powierzchni gleby pąków pędowych (faza P1). We Wrocławiu faza ta przypadła na
okres pomiędzy marcem a kwietniem. W 2009 roku pąki pędowe pojawiły się
najwcześniej 14.III na stanowisku nr 3 (Fallopia japonica) oraz 15.III na stanowisku nr
18 (Fallopia × bohemica). Na stanowisku Fallopia sachalinensis omawiana faza
wystąpiła 17.III. W roku 2010 zaobserwowano opóźnienie fazy P1 (nawet o 14 dni),
w stosunku do roku poprzedniego. Najprawdopodobniej wpłynęły na to warunki
pogodowe. W styczniu 2010 zanotowano 29 dni z temperaturą poniżej 0˚C (średnia
dobowa temperatura wyniosła –5,9˚C), w lutym wystąpiło 18 dni z temperaturą poniżej
0˚C (średnia dobowa temperatura wyniosła -1,1˚C), w marcu odnotowano 10 dni
z ujemną temperaturą (średnia dobowa temperatura wyniosła 4,2˚ C). Dla porównania,
w styczniu 2009 roku wystąpiło 18 dni z ujemną temperaturą (średnia dobowa
temperatura wyniosła -2,3˚C), w lutym odnotowano 13 dni z temperaturą poniżej 0˚C
(średnia dobowa temperatura wyniosła 0,2˚C), w marcu ujemna temperatura wystąpiła
tylko raz (średnia dobowa temperatura wyniosła 4,6˚C). W 2010 roku fazę P1
najwcześniej odnotowano 26.III na stanowiskach: 3, 10 (Fallopia japonica) i 18
(Fallopia × bohemica). Na stanowisku rdestowca sachalińskiego faza ta wystąpiła
27.III.
75
Kolej etapem rozwoju rdestowców jest pojawianie się pędów oraz początek ich
wzrostu elongacyjnego (faza P2). We Wrocławiu faza P2 notowana jest około 5–10 dni
po pojawieniu pąków pędowych. W 2009 roku najwcześniej odnotowano ją 20.III na
stanowisku 10 (stanowisko rdestowca japońskiego), najpóźniej zaś 06.IV na stanowisku
16 (stanowisko rdestowaca pośredniego). W kolejnym roku pędy rdestowców
najwcześniej pojawiły się 01.IV (stanowiska 3 i 10 – Fallopia japonica), zaś ostatnie
pędy w fazie P2 odnotowano 10.IV (stanowisko 19 – Fallopia × bohemica). Koniec
wzrostu pędów rdestowców, czyli fazę P3 wyznaczono na podstawie obserwacji.
Zaobserwowano, że w obydwu latch obserwacji badane gatunki przestały przyrastać
w drugiej połowie czerwca.
II – Rozwój liści
W ciągu około siedmiu dni od pojawieniu się pędów notowana jest faza L1,
podczas której około 50% pędów na stanowisku rozchyliło pąki liściowe. W 2009 roku
faza L1 najwcześniej pojawiła się na stanowisku 18 (stanowisko rdestowca pośredniego
– 27.III). W następnym roku fazę L1 po raz pierwszy zanotowano 01.IV, także na
stanowisku 18. Najpóźniej w 2009 i 2010 roku omawiana faza wystąpiła na stanowisku
9 (stanowisko rdestowca japońskiego).
W drugiej połowie kwietnia 2009 i 2010 roku około 50% roślin wytworzyło
blaszki liściowe (faza L2). W pierwszym roku obserwacji faza L2 najwcześniej
wystąpiła 13.IV na stanowisku nr 3 (Fallopia japonica), najpóźniej zaś 30.IV na
stanowisku nr 15 (Fallopia × bohemica). W kolejnym roku po raz pierwszy omawianą
fazę odnotowano 18.IV na stanowisku 17 (Fallopia × bohemica). Najpóźniej natomiast
30.IV, na stanowisku rdestowca pośredniego, nr – 19.
W 2009 i 2010 roku liście rdestowca japońskiego i sachalińskiego osiągnęły
wielkości typową dla gatunku w pierwszej połowie maja (faza L3). U rdestowca
pośredniego faza L3 pojawiła się później, tzn. w drugiej połowie miesiąca. W 2009 roku
typowe liście rdestowca pośredniego pierwszy raz obserwowano 22.V (stanowiska nr
13, 14, 15, 18, 19 i 20), w roku następnym 23.V (stanowiska nr 13 i 14 ).
III – Przebarwianie i zrzucanie liści
Podczas obserwacji fazy L4 (przebarwianie liści) i fazy L5 (zrzucanie liści)
zauważono różnice pomiędzy poszczególnymi gatunkami. Najwcześniej obie fazy
wystąpiły na stanowiskach Fallopia sachalinensis i Fallopia japonica. W 2009 i 2010
roku fazę L4 po raz pierwszy odnotowano wśród kęp rdestowca sachalińskiego 30.IX,
rok później 08.X. W 2009 pierwsze przebarwione liście rdestowca japońskiego
76
zaobserwowano 14.X (stanowisko nr 5), a w 2010 roku – 17.X. (stanowisko nr 1, 2 i 6).
W 2009 roku u rdestowca pośredniego najwcześniej omawiana faza wystąpiła 21.X
(stanowisko nr 17), a w 2010 roku 27.X (stanowisko nr 11 i 13). Najpóźniej, tzn.
w pierwszej dekadzie listopada 2009 i 2010 roku fazę L4 osiągnęły pędy Fallopia
× bohemica (stanowiskach nr 15 – 2009 rok, i 16 –lata 2009, 2010). Opadanie liści
obserwowano najwcześniej u Fallopia sachalinensis. W pierwszym roku badań fazę L5
dnotowano 15.X. Natomiast, wśród skupień rdestowca japońskiego omawiana faza
wystąpiła najwcześniej 28.X (stanowiskach nr 4). W kolejnym roku badań fazę L5
zanotowano 20.X na stanowisku rdestowca sachalińskiego oraz 27.X na stanowisku
rdestowca japońskiego (nr 2). Liście Fallopia × bohemica utrzymywały się najdłużej.
W roku 2009 na stanowiskach 15, 16 i 19 faza L5 wystąpiła dopiero w ostatniej
dekadzie listopada. W 2010 roku jesienne przymrozki oraz ujemne temperatury
powietrza notowane pod koniec listopada (od – 0,6 do – 7,6˚C) spowodowały
przemarznięcie liści na sześciu stanowiskach rdestowca pośredniego (numer: 12, 13, 14,
16, 18 i 19).
IV – Rozwój kwiatów
We Wrocławiu pierwsze w pełni wykształcone kwiatostany rdestowców
w postaci wiechy zawiązywały się w połowie sierpnia. Ogólnie, faza kwitnienia trwała
od sierpnia (ostatnia dekada miesiąca) do października (ostatnia dekada miesiąca).
W 2009 roku fazę K1 po raz pierwszy zanotowano 13.VIII (stanowiska
rdestowca japońskiego – nr 5 i 10 oraz sachalińskiego – nr 21). W 2010 roku – 20.VIII
(stanowisko Fallopia japonica – nr 10), a w przypadku Fallopia sachalinensis 30.VIII.
U rdestowca pośredniego w 2009 roku faza K1 pojawiła się pierwszy raz 14.VIII
(stanowisko nr 15), rok pózniej 16.VIII (także stanowisko nr 15).
Po 11 – 21 dniach od fazy K1 na stanowiskach rdestowców zaobserwowano
około 50% kwitnących kwiatów (faza K2). W pierwszym roku obserwacji na większości
stanowisk rdestowca japońskiego fazę K2 obserwowano od 26. do 29.VIII. U rdestowca
sachalińskiego omawiana faza pojawiła się 26.VIII. Natomiast u rdestowca pośredniego
wystąpiła w okresie od 27. do 29.VIII (stanowiska nr 11, 13, 14, 15, 17,19) oraz od 06.
do 09.IX (stanowiska nr: 12,16,18). W roku kolejnym fazę K2 obserwowano od 09.IX
do 19. IX u Fallopia japonica, a w przypadku Fallopia sachalinensis 08.IX. Natomiast,
u rdestowca pośredniego omawiana faza wystąpiła w okresie od 29.VIII do 19.IX.
77
Ostatnią fazą w rozwoju kwiatów było ich opadanie (faza K3). Najwcześniej
faza K3 pojawiała się u rdestowców: sachalińskiego (20.IX – rok 2009 i 04.X – rok
2010) oraz japońskiego (19.IX – rok 2009, stanowisko 2, 8 i 9 i 13.X – 2010 rok,
stanowisko 8 i 9). Najdłużej kwiaty utrzymywały się na pędach rdestowca pośredniego.
W roku 2009 najpóźniej faza K3 wystąpiła 28.X – stanowisko Fallopia × bohemica, nr
16, a w roku 2010 02.XI (stanowisko nr 19).
V – Rozwój owoców
Rozwój owoców rdestowców obejmuje okres od formowanie się trójgraniastych
orzeszków (O1), poprzez pełnię owocowania (O2), aż do ich opadania (O3) i trwa od
października do listopada. We Wrocławiu wszystkie obserwowane kępy rdestowca
japońskiego produkowały dużą liczbę owoców. W roku 2009 pierwsze owoce Fallopia
japonica pojawiły się 05.IX (stanowisko nr 3 i 10) i utrzymywały się do końca
października (28.X – stanowisko 9). Roku później u rdestowca japońskiego fazę O1
odnotowano po raz pierwszy 12.IX (stanowisko nr: 3, 4, 7, 8), a owoce weszły w fazę
O2 pomiędzy 10–14.X. W 2009 roku na stanowisku Fallopia sachalinensis fazę O1
odnotowano 14.IX, a w roku 2010 19.IX. Pełnia owocowania rdestowca sachalińskiego
(faza O2) wystąpiła w terminie 07.X (rok 2009 i 2010). Opadanie owoców rdestowca
sachalińskiego (faza O3) odnotowano 15.X (rok 2009) i 18.X (2010 rok). Jak
wspomniano wcześniej, nie wszystkie klony rdestowca pośredniego zawiązywały
owoce. W pierwszym roku badań orzeszki pojawiły się na stanowiskach numer: 12, 13,
15, 16, 17 i 18, w okresie od września (druga połowa miesiąca – stanowiska: 12, 13, 15,
16 i 17) do października (druga dekada miesiąca – stanowisko 18). Kolony rdestowca
pośredniego (z wyjątkiem pędów na stanowisku 13 – ul.Orzechowa i 18 – ul. Ślęża)
wytwarzały niewielką liczbę owoców, co utrudniało dokładne określenie fazy O2, w
której to około 50% pędów owocuje. Ostatecznie przyjęto, że w 2009 faza ta wystąpiła
na stanowiskach w terminie od 24.IX do 28.X. Na stanowisku 12 i 13 owoce weszły
najwcześniej w fazę O3 (11.X), najpóżniej zaś 15.XI (stanowisko 16). Rok później
skąpo owocujące pędy rdestowca pośredniego odnotowano jedynie na stanowisku nr 16
(8.X). Pełnia owocowania na stanowisku 16 przypadła na 30.X, natomiast faza O3
wystąpiła 06.XI.
78
Tab. 11. Fazy fenologiczne Fallopia japonica (1–10), Fallopia × bohemica (11–20) i Fallopia sachalinensis (21) obserwowane w 2009 roku
Objaśnienia: ~ faza nie wystąpiła; − fazy nie zanotowano z powodu uszkodzenia pędów na stanowisku
Przebarwianie
Rozwój kwiatów
Wzrost pędów
Rozwój liści
Numer
i opadanie liści
stanowiska
P1
P2
P3
L1
L2
L3
L4
L5
K1
K2
K3
79
Rozwój owoców
1
18.III
27.III
15.VI
05.IV
17.IV
01.V
16.X
30.X
14.VIII 26.VIII
11.X
O1
09.IX
2
22.III
02.IV
17.VI
11.IV
23.IV
03.V
18.X
30.X
14.VIII 26.VIII 19.IX
10.IX
19.IX
24.X
3
14.III
22.III
17.VI
01.IV
13.IV
04.V
18.X
01.XI
14.VIII 27.VIII
12.X
05.IX
12.X
27.X
4
23.III
02.IV
15.VI
08.IV
22.IV
03.V
21.X
28.X
02.X
24.IX
02.X
23.X
5
22.III
03.IV
17.VI
07.IV
22.IV
03.V
14.X
30.X
13.VIII 27.VIII 21.IX
10.IX
21.IX
22.X
6
22.III
03.IV
17.VI
09.IV
22.IV
03.V
16.X
29.X
16.VIII 29.VIII 24.IX
12.IX
24.IX
23.X
7
18.III
28.III
17.VI
08.IV
22.IV
03.V
15.X
29.X
15.VII
27.VIII 28.IX
19.IX
28.IX
22.X
8
18.III
02.IV
15.VI
10.IV
22.IV
03.V
15.X
29.X
16.VIII 26.VIII 19.IX
10.IX
19.IX
22.X
9
23.III
01.IV
17.VI
11.IV
23.IV
05.V
18.X
29.X
16.VIII 25.VIII 19.IX
10.IX
16.IX
28.X
10
15.III
20.III
18.VI
02.IV
14.IV
05.V
22.X
07.XI
13.VIII 27.VIII
12.X
05.IX
12.X
27.X
11
19.III
01.IV
12.VI
05.IV
19.IV
28.V
26.X
12.XI
15.VIII 29.VIII
26.X
~
~
~
12
17.III
27.III
10.VI
05.IV
19.IV
28.V
25.X
10.XI
27.VIII
27.X
20.IX
27.IX
11.X
13
19.III
26.III
17.VI
29.III
14.IV
22.V
22.X
10.XI
16.VIII 28.VIII
23.X
19.IX
26.IX
11.X
14
19.III
26.III
18.VI
29.III
14.IV
22.V
27.X
09.XI
16.VIII 28.VIII
25.X
−
−
−
15
16.III
22.III
18.VI
14.IV
30.IV
22.V
03.XI
27.XI
14.VIII 29.VIII
26.X
17.IX
27.IX
18.X
16
18.III
06.IV
17.VI
08.IV
22.IV
28.V
03.XI
27.XI
28.VIII
28.X
21.IX
28.X
15.XI
17
22.III
01.IV
19.VI
08.IV
22.IV
28.V
21.X
12.XI
15.VIII 27.VIII
21.X
17.IX
24.IX
27.X
18
15.III
26.III
19.VI
27.III
15.IV
22.V
22.X
10.XI
25.VIII
27.X
20.X
28.IX
27.X
19
19.III
26.III
17.VI
29.III
15.IV
22.V
29.X
22.XI
16.VIII 28.VIII
23.X
−
−
−
20
19.III
28.III
06.VI
29.III
15.IV
22.V
−
−
−
−
−
−
21
17.III
27.III
17.VI
31.III
14.IV
03.V
30.IX
15.X
14.IX
07.X
15.X
08.IX
−
23.IX
06.IX
10.IX
08.IX
−
13.VIII 26.VIII 20.IX
O2
27.IX
O3
24.X
Tab. 12. Fazy fenologiczne Fallopia japonica (1–10), Fallopia × bohemica (11–20) i Fallopia sachalinensis (21) obserwowane w roku 2010 roku
Objaśnienia: ~ faza nie wystąpiła,* zaobserwowano przemarzniecie pędów, − fazy nie zanotowano z powodu uszkodzenia pędów na stanowisku
Numer
stanowiska
80
Wzrost pędów
Przebarwianie
Rozwój liści
Rozwój kwiatów
i opadanie liści
L4
L5
K1
K2
K3
17.X
28.X 21.VIII 11.IX
15.X
1
P1
28.III
P2
07.IV
P3
19.VI
L1
14.IV
L2
28.IV
L3
14.V
2
29.III
07.IV
19.VI
14.IV
28.IV
14.V
20.X
27.X
21.VIII
11.IX
3
26.III
01.IV
22.VI
08.IV
22.IV
15.V
18.X
03.XI
21.VIII
4
01.IV
09.IV
19.VI
16.IV
23.IV
15.V
30.X
10.XI
5
30.III
07.IV
21.VI
15.IV
29.IV
10.V
18.X
6
29.III
08.IV
21.VI
15.IV
29.IV
10.V
7
30.III
08.IV
20.VI
16.IV
23.IV
8
30.III
09.IV
21.VI
17.IV
9
01.IV
10.IV
21.VI
10
26.III
01.IV
11
29.III
12
Rozwój owoców
O1
13.IX
O2
10.X
O3
28.X
15.X
13.IX
10.X
23.X
12.IX
18.X
12.IX
14.X
30.X
02.IX
19.IX
18.X
12.IX
14.X
30.X
03.XI
29.VIII
12.IX
18.X
15.IX
14.X
30.X
17.X
03.XI
29.VIII
12.IX
18.X
15.IX
14.X
30.X
14.V
18.X
31.X
29.VIII
12.IX
18.X
12.IX
14.X
25.X
24.IV
13.V
18.X
31.X
29.VIII
12.IX
13.X
12.IX
13.X
23.X
18.IV
24.IV
13.V
18.X
31.X
29.VIII
12.IX
13.X
15.IX
13.X
23.X
24.VI
13.IV
27.IV
15.V
19.X
03.XI
20.VIII
09.IX
16.X
15.IX
14.X
30.X
05.IV
18.VI
09.IV
28.IV
24.V
27.X
10.XI
22.VIII
04.IX
03.X
29.III
08.IV
19.VI
14.IV
28.IV
24.V
28.X
30.VIII
13.IX
10.X
13
01.IV
06.IV
19.VI
10.IV
23.IV
23.V
27.X
14
01.IV
06.IV
20.VI
08.IV
23.IV
23.V
03.XI
~*
~*
~*
~
~
~
~
~
~*
~*
~*
15
27.III
03.IV
21.VI
08.IV
25.IV
27.V
−
−
−
16
01.IV
07.IV
21.VI
09.IV
23.IV
27.V
10.XI
~*
17
01.IV
07.IV
19.VI
10.IV
18.IV
24.V
30.X
18
26.III
02.IV
01.IV
25.IV
24.V
30.X
19
06.IV
10.IV
15.VI
21.VI
15.IV
30.IV
24.V
20
29.III
08.IV
22.VI
09.IV
28.IV
21
27.III
04.IV
20.VI
10.IV
27.IV
17.VIII 31.VIII
26.X
17.VIII 31.VIII
26.X
~
~
~
~
−
−
−
−
−
06.IX
19.IX
01.XI
8.X
30.X
06.XI
10.XI
19.VIII
01.IX
26.X
30.VIII
13.IX
10.X
08.XI
~*
~*
06.IX
18.IX
02.XI
~
~
~
~
~
~
~
~*
~*
26.V
−
−
−
−
−
−
−
−
10.V
08.X
20.X
30.VIII
08.IX
04.X
19.IX
07.X
18.X
W pierwszych tygodniach wegetacji rdestowców następuje ich gwałtowny
wzrost. W tab. 13–18 zestawiono średnie przyrosty pędów (łodyg) [cm] trzech
gatunków rdestowców odnotowane na terenie Wrocławia w latch 2009 i 2010.
Obserwacje wykonano w pierwszych czterech tygodniach rozwoju roślin.
W roku 2009 tygodniowy przyrosty pędów rdestowca japońskiego kształtowały
się w przedziałach od 2,0 do 9,5 cm (I tydzień), od 6,7 do 44,8 cm (II tydzień), od 20 do
57,2 cm (III tydzień) oraz od 16,2 do 50,9 cm (IV tydzień). Rok później w trzech
pierwszych tygodniach wegetacji zanotowano nieco mniejsze wartości przyrostów tzn.
od 2,3 do 4,9 cm (I tydzień), od 6,5 do 15,3 cm (II tydzień) oraz od 19,0 do 46,7 cm (III
tydzień). Natomiast, w ostatnim tygodniu obserwacji średni wzrost łodyg wahał się w
zakresie od 36,4 do 86,5 cm. W 2009 roku przyrosty nadziemnych pędów Fallopia
× bohemica wyniosły odpowiednio: od 2,2 do 6,0 cm (I tydzień), od 8,0 do 25,0 cm
(tydzień II), od 22,0 do 49,0 cm (III tydzień) oraz od 41,0 do 82,3 cm (IV tydzień).
W roku 2010 wystąpiły podobne średnie przyrosty długości segmentów pędowych: od
2,1 do 6,7 cm (I tydzień), od 4,3 do 24,6 cm (II tydzień) od 8,6 do 49,4 cm (III tydzień)
oraz od 9,0 do 71,2 cm (IV tydzień). Wzrost kęp rdestowca sachalińskiego w
pierwszym roku obserwacji kształtował się na poziomie 3,0 cm (I tydzień), 25,0 cm (II
tydzień), 28,0 cm (III tydzień ) i 41 cm (IV). W roku kolejnym zanotowano następujące
przyrosty pędów Fallopia sachalinensis: 6,7 cm (I tydzień), 24,6 cm (II tydzień) 32,7
cm (III tydzień) oraz 38,4 cm (IV tydzień).
Najmniejszy miesięczny przyrost pędów Fallopia japonica w 2009 roku
odnotowano na stanowiskach 9 (56,7 cm), 1 (62,7 cm) oraz 4 (63,1 cm), natomiast
największy (131,6 cm) na stanowisku nr 10. W następnym roku obserwacji uzyskano
podobne wyniki. Najmniejsze miesięczne wartość przyrostów zanotowano na
stanowiskach 4 (70,0 cm), 2 (64,7 cm), 9 (73,8 cm) oraz 1 (79,5 cm), najszybciej zaś
przyrastały pędy na stanowisku nr 10 (142,1 cm) oraz 3 (126,1 cm).
W 2009 i 2010 roku u Fallopia × bohemica najmniejszy miesięczny wzrost
łodyg wystąpił na stanowisku nr 20 (77,6 cm i 24,9 cm). Największe przyrosty pędów w
roku 2009 odnotowano na stanowiskach 15 (144,5 cm) oraz 16 (154,6 cm). W roku
2010 największe przyrosty wystąpiły na stanowisku 15 (139,7 cm).
Stwierdzone różnice we wzroście pędów rdestowców na poszczególnych
stanowiskach prawdopodobnie wynikają ze swoistych cech siedlisk oraz ze sposobu
użytkowania terenu. Duże znaczenie odgrywają tutaj warunki świetlne. Zauważono, że
gatunki z rodzaju Fallopia – zwłaszcza Fallopia japonica i Fallopia × bohemica
81
preferują obszary silnie nasłonecznione. Do takich należy m.in. stanowisko rdestowca
pośredniego przy ul. Powstańców Śląskich (nr 15), na którym w 2009 i 2010 roku
odnotowano wysokie średnie miesięczne przyrosty segmentów pędowych. Wzrost
w miejscach zacienionych przebiegał wolniej. Przykładem może być zacienione
stanowisko rdestowca japońskiego (nr 4), zlokalizowane przy ul. Robotniczej, na
którym w ciągu dwóch lat obserwacji wystąpiły jedne z najniższych średnich
miesięcznych
przyrostów
łodyg.
Szybkiemu
wzrostowi
pędów
rdestowców
w pierwszych tygodniach wegetacji sprzyja także regularne usuwanie zalegającej
ściółki. Nowe, rozwijające się rośliny pośród gęstwiny zeszłorocznych pędów mają
gorszy dostęp do światła oraz ograniczone możliwości szybkiego wykiełkowania spod
opadłych jesienią liści. Takie warunki panują m.in. na stanowiskach Fallopia japonica
– nr 1 (ul. Morwowa) oraz nr 9 (al. Wiśniowa). Natomiast w ogrodach przydomowych
(np. stanowisko przy ul. Orzeszkowej) wzrost kęp rdestowców przebiega szybciej.
Zarośla rdestowców zlokalizowane na terenach zieleni miejskiej lub przy obiektach
użyteczności publicznej były często koszone. Regularne zabiegi pielęgnacyjne
ograniczają wzrost rdestowców, co zaobserwowano na stanowisku rdestowca
pośredniego (nr 20) znajdującego się na parkingu przy ul. Ślicznej, na którym w latach
2009 i 2010 odnotowano najniższe średnie miesięczne przyrosty długości segmentów
pędowych.
82
Tab. 13. Przyrosty pędów [cm] Fallopia japonica mierzone w pierwszych czterech tygodniach
wegetacji w roku 2009
Stanowisko
I tydzień
II tydzień
III tydzień
IV tydzień
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
1
2
3
4
5
6
7
8
9
10
5,2
2,0
10,0
10,8
1,0
13,0
19,3
10,0
33,0
27,4
10,0
48,0
5,7
2,9
9,0
33,1
21,0
60,0
36,5
9,0
62,0
20,5
1,0
41,0
4,2
2,0
7,5
22,9
4,5
51,0
26,7
15,0
41,0
48,7
12,0
125,0
3,0
1,0
6,0
15,0
4,0
57,0
20,0
9,0
82,0
25,1
10,0
72,0
4,7
2,0
10,0
44,8
13,5
67,0
30,3
10,0
61,0
37,2
10,0
88,0
3,8
1,5
9,0
14,8
6,5
31,0
20,6
6,0
50,0
44,3
28,0
125,0
2,6
1,0
5,0
16,0
6,5
46,0
23,8
12,0
39,0
30,0
12,2
62,0
2,0
1,0
4,0
6,7
2,0
13,0
44,7
5,0
118,0
50,9
20,0
86,0
2,6
1,0
5,5
14,1
6,0
36,0
23,8
9,0
52,0
16,2
5,0
32,0
9,5
2,8
20,0
15,3
6,9
36,0
57,2
27,0
108,0
49,7
24,0
98,0
Tab. 14. Przyrosty pędów [cm] Fallopia japonica mierzone w pierwszych czterech tygodniach
wegetacji w roku 2010
Stanowisko
I tydzień
II tydzień
III tydzień
IV tydzień
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
1
2
3
4
5
6
7
8
9
10
2,8
2,0
4,0
11,3
8,0
15,0
27,2
10,5
45,0
38,2
19,6
58,0
2,8
1,0
5,3
6,5
1,5
15
19,0
9,5
42,5
36,4
11,5
61,0
4,7
1,5
7,0
10,9
4,0
14,0
46,7
11,0
77,8
63,8
60,0
97,0
2,4
1,0
4,0
11,9
5,0
18,0
18,2
8,0
37,9
37,5
9,5
66,3
2,6
1,5
3,5
15,3
8,5
27,0
31,9
10,6
46,0
46,5
8,5
72,0
4,9
3,0
7,0
9,8
1,4
22,2
19,0
1,5
33,0
65,6
32,0
93,0
3,0
1,0
5,5
7,6
1,0
12,7
27,0
10,2
40,8
52,2
10,2
89,0
2,3
0,5
3,5
8,1
3,0
13
22,5
11,3
45,5
60,3
47,0
79,0
1,8
0,5
4,0
11,1
4,3
24,0
23,0
7,5
46,0
37,9
10,5
59,0
3,9
2,5
11,2
11,8
8,1
14,5
39,9
27,0
49,9
86,5
70,5
93,7
Tab. 15. Całkowity przyrost pędów [cm] Fallopia japonica w latach 2009 i 2010
Grupy jednorodne wyznaczono za pomocą testu HSD Tukeya po jednoczynnikowej analizie
wariancji, liczby oznaczone tą samą literą nie różnią się istotnie na poziomie p ≤ 0,05
Stanowisko
2009
2010
1
62,7 a
79,5 a
2
95,8 abc
64,7 a
3
102,5 abc
126,1 bc
4
63,1 a
70,0 a
5
117,0 bc
96,1 ab
6
83,5 ab
99,3 ab
7
72,4 ab
89,8 ab
8
104,3 abc
93,2 ab
9
56,7 a
73,8 a
10
131,6 c
142,1 c
83
Tab. 16. Przyrosty pędów [cm] Fallopia × bohemica (stanowiska 11–20) i Fallopia sachalinensis
(stanowisko 21) mierzone w pierwszych czterech tygodniach wegetacji w roku 2009
Stanowisko
I tydzień
II tydzień
III tydzień
IV tydzień
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
średnia
min.
max.
11
2,2
1,2
3,0
8,0
0,4
18,0
31,5
13,5
45,0
72,0
39,0
98,9
12
3,4
1,5
7,4
11,3
7,4
16,0
29,2
5,0
63,0
44,5
5,0
85,0
13
5,5
3,9
8,6
15,5
5,5
30,0
34,0
10,4
61,5
57,7
39,9
99,0
14
6,0
1,1
10,0
12,1
2,2
21,5
23,9
15,8
40,2
41,2
24,3
58,2
15
2,2
1,5
4,0
15,5
8,2
23,7
44,3
22,1
70,3
82,3
60,7
117,0
16
5,5
2,0
10,0
17,2
7,0
28,4
49,0
12,8
71,1
82,9
30,0
115,0
17
2,7
2,0
3,6
13,3
5,5
20,1
42,2
10,5
70,1
68,8
32,5
105,0
18
2,2
1,0
3,0
13,1
4,7
20,9
29,6
10,9
46,0
57,8
42,9
79,7
19
5,1
1,5
10,0
17,9
6,5
40,0
44,5
15,8
61,5
53,2
33,6
88,2
20
2,0
1,5
3,5
11,9
8,0
18,3
22,0
6,5
45,0
41,7
10,0
67,0
21
3,0
1,5
7,0
25,0
13,1
38,0
28,0
17,0
43,0
41,0
28,0
67,0
Tab. 17. Przyrosty pędów [cm] Fallopia × bohemica (stanowiska 11–20) i Fallopia sachalinensis
(stanowisko 21) mierzone w pierwszych czterech tygodniach wegetacji w roku 2010
Stanowisko
11
2,7
1,0
4,0
12
13
14
15
16
17
18
19
20
21
3,0
2,0
5,0
6,2
4,0
10,0
3,7
1,5
8,3
6,4
2,5
10,4
4,0
1,1
6,7
2,1
2,0
4,5
5,2
1,5
9,0
3,2
2,0
5,0
3,0
1,8
3,7
6,7
1,2
14,1
I tydzień
średnia
min.
max.
II tydzień
średnia
min.
max.
7,1 17,9
3,2 9,8
14,1 27,0
17,0
6,5
30,0
6,0
3,9
20,0
19,2
6,4
33,0
10,9
1,0
20,6
9,8
0,6
14,0
11,5
8,0
15,0
9,7
5,9
14,9
4,3
1,6
9,1
24,6
10,5
33,6
III tydzień
średnia
min.
max.
40,5 28,8
22,8 17,2
59,1 38,0
49,4
16,0
71,2
17,0
6,5
30,0
42,9
25,2
55,3
34,0
0,5
48,4
36,2
5,0
70,0
24,0
9,8
45,0
24,3
9,8
49,0
8,6
0,5
11,9
32,7
19,9
41,0
IV tydzień
średnia
min.
max.
59,4 40,7
31,4 18,8
90,5 48,5
50,2
34,0
82,4
49,3
15,9
71,2
71,2
44,2
99,0
43,5
10,3
73,3
54,5
5,0
103,0
45,5
10,0
78,0
50,3
20,0
88,5
9,0
2,7
13,8
38,4
27,2
44,6
Tab. 18. Całkowity przyrost pędów [cm] Fallopia × bohemica (stanowiska 11–20) i Fallopia
sachalinensis (stanowiska 21) w latach 2009 i 2010
Grupy jednorodne wyznaczono za pomocą testu HSD Tukeya po jednoczynnikowej analizie
wariancji, liczby oznaczone tą samą literą nie różnią się istotnie na poziomie p ≤ 0,05
Stanowisko
2009
2010
11
113,7 abcde
109,7 abc
12
88,4 abc
90,4 ab
13
112,7 abcde
122,8 bc
14
83,2 ab
76,0 a
15
144,5 e
139,7 c
16
154,6 e
92,4 ab
17
127,0 cde
102,6 abc
18
102,6 abcd
86,2 ab
19
120,7 bcde
87,5 ab
20
77,6 a
24,9 d
21
97,0
102,4
84
7.2. WYNIKI DOŚWIADCZEŃ WAZONOWYCH
7.2.1.
WPŁYW METALI CIĘŻKICH NA PRZEBIEG WZROSTU I ROZWOJU
RDESTOWCÓW
Przedstawione rezultaty badań z trzema gatunkami rdestowców hodowanymi
w kulturach glebowych (z zastosowaniem różnych dawek Cd, Cr, Cu, Pb i Zn)
dostarczają danych na temat wpływu metali ciężkich na możliwości regeneracyjne
kłączy, wzrost i rozwój pędów oraz zmienność cech morfologicznych. Omówiono
również zagadnienie różnic w kumulacji metali ciężkich u poszczególnych gatunków
z rodzaju Fallopia.
Doświadczenie wazonowe zostało przeprowadzone w dwóch etapach.
W pierwszym, wcześniejszym testowano reakcję jednego gatunku – Fallopia japonica
w odniesieniu do pięciu metali: Cd, Cr, Cu, Pb i Zn, które zaaplikowano do gleby
w trzech dawkach: Cd – 20, 100, 200 mg·kg-1, Cr – 10, 20, 100 mg·kg-1, Cu – 100, 200,
300 mg·kg-1, Pb – 50, 100, 200 mg·kg-1 oraz Zn
– 100, 200, 300 mg·kg-1.
W drugim, późniejszym eksperymencie badano wpływ wyłącznie Cd – 200 mg·kg-1
i Cr – 100 mg·kg-1 na wzrost i rozwój trzech gatunków rdestowców: Fallopia japonica,
Fallopia × bohemica i Fallopia sachalinensis. Wybór metali oraz dawek przyjętych w
drugim doświadczeniu oparto na wynikach uzyskanych w doświadczeniu pierwszym
oraz na wcześniejszych badaniach [Sołtysiak i in. 2011].
Badania potwierdziły dużą zdolność rdestowców do regeneracji – także
w obecności nadmiaru metali ciężkich w podłożu (tab. 19 i 20). W pierwszym
doświadczeniu z udziałem rdestowca japońskiego zregenerowało 90% posadzonych
kłączy, a pędy nadziemne pojawiły się już w czwartym dniu eksperymentu. Największą
zdolność do regeneracji (100%) miały kłącza umieszczone w glebie z dodatkiem Cd
(20, 100, 200 mg·kg-1), Cr (10, 20, 100 mg·kg-1), Zn (100, 200 mg·kg-1) oraz Cu (100
mg·kg-1). Natomiast najmniej kłączy (75%) wykazało regenerację w wazonach
z dodatkiem 300 mg Zn ·kg-1, 200 i 300 mg Cu ·kg-1 oraz 50, 100 i 200 mg Pb·kg-1.
W późniejszym, drugim eksperymencie (z udziałem trzech gatunków: Fallopia
japonica, Fallopia × bohemica i Fallopia sachalinensis) pędy nadziemne zaczęły
pojawiać się także po czterech dniach od umieszczenia fragmentów kłączy
w glebie. Szczególnie duże zdolności do regeneracji wykazał rdestowiec pośredni,
którego pędy pojawiły się we wszystkich wazonach już siedem dni po posadzeniu.
85
Najniższą regenerację z fragmentów kłączy wykazał rdestowiec sachaliński.
W wazonach kontrolnych oraz w glebie z dodatkiem 200 mg Cd ·kg-1 aktywnie rosło
25% pędów podziemnych. W wazonach z dodatkiem 100 mg Cr ·kg-1 zdolności
regeneracyjne Fallopia sachalinensis wyniosły 100%.
Na podstawie pomiarów wysokości pędów rdestowców sporządzono wykresy
obrazujące dynamikę ich wzrostu w obecności metali ciężkich (rys. 24 i 25).
Zaaplikowane dawki Cr – 10, 20, 100 mg·kg-1 i Pb – 50, 100, 200 mg·kg-1, które
przyjęto w pierwszym eksperymencie nie działały hamująco na regenerację kłączy oraz
wzrost i rozwój badanych roślin. Uzyskane w tym zakresie wyniki odpowiadają
wariantowi kontrolnemu. Natomiast dawki Cd – 20, 100, 200 mg·kg-1, Cu –100, 200,
300 mg·kg-1 oraz Zn –100, 200, 300 mg·kg-1 wykazały inhibicyjne działanie na
dynamikę wzrostu wszystkich testowanych gatunków. Szczególnie silne zahamowanie
wzrostu pędów stwierdzono u rdestowca japońskiego pod wpływem 100 i 200 mg·kg-1
Cd. W drugim doświadczeniu wazonowym wzrost rdestowców japońskiego
i pośredniego w wazonach z dodatkiem 100 mg Cr ·kg-1 nie różnił się znacząco od
wariantu kontrolnego. Natomiast u rdestowca sachalińskiego nastąpiło spowolnienie
wzrostu w porównaniu z kontrolą. Kadm w dawce 200 mg·kg-1 spowodował
zahamowanie wzrostu u wszystkich badanych gatunków rdestowców. Najsilniejszą
reakcję zaobserwowano u rdestowca sachalińskiego, u którego nastąpiło całkowite
zahamowanie wzrostu i rozwoju po pięciu tygodniach. Nieco późniejsza reakcja
wystąpiła u rdestowca japońskiego (brak przyrostu po siedmiu tygodniach). Największą
odporność na obecność 200 mg·kg-1 Cd wykazał rdestowiec pośredni, gdyż całkowita
inhibicja wzrostu pędów nastąpiła dopiero po dziewięciu tygodniach wegetacji.
86
Tab. 19. Regeneracja kłączy Fallopia japonica [%] w I doświadczeniu wazonowym
Gatunek
Metal
Dawka
[mg·kg-1]
20
100
4
50
0
25
7
75
25
50
10
100
50
50
13
100
75
100
16
100
75
100
19
100
100
100
200
0
25
50
75
75
100
10
50
75
100
100
100
100
20
50
75
100
100
100
100
100
50
100
100
100
100
100
100
50
75
100
100
100
100
Kontrola
Cd
Cr
Fallopia
japonica
Cu
Pb
Zn
Dzień
200
0
25
50
75
75
75
300
25
75
75
75
75
75
50
50
50
50
75
75
75
100
25
50
50
50
75
75
200
0
25
50
50
75
75
100
25
50
75
75
100
100
200
50
100
100
100
100
100
300
0
50
75
75
75
75
Tab. 20. Regeneracja kłączy Fallopia japonica, Fallopia × bohemica i Fallopia sachalinensis [%]
w II doświadczeniu wazonowym
Gatunek
Fallopia
japonica
Fallopia
× bohemica
Fallopia
sachalinensis
Metal
Dawka
[mg·kg-1]
Dzień
Cd
200
4
25
50
Cr
100
50
100
100
100
100
100
200
50
50
100
100
100
100
100
100
100
100
100
100
50
100
100
100
100
100
Kontrola
Kontrola
Cd
Cr
100
Kontrola
7
75
75
10
100
75
13
100
100
16
100
100
19
100
100
Cd
200
25
25
25
25
25
25
25
25
25
25
25
25
Cr
100
50
100
100
100
100
100
87
wysokość pędów roślin
[cm]
Cr
60
40
20
0
1
2
3
4
5
6
7
8
9
10 11
12 13 14
czas [tygodnie]
K
10
20
100
Cu
wysokosć pędów roślin
[cm]
60
40
20
0
1
2
3
4
5
6
7
8
9
10 11 12 13 14
czas [tygodnie]
K
100
200
300
88
Pb
wysokość pędów roślin [cm]
60
40
20
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
9
10 11 12 13 14
czas [tygodnie]
K
50
100
200
wysokość pędów roślin
[cm]
Zn
60
40
20
0
1
2
3
4
5
6
7
8
czas [tygodnie]
K
100
200
300
Rys. 24. Przebieg wzrostu pędów nadziemnych Fallopia japonica hodowanego w kulturach
glebowych z dodatkiem metali ciężkich; K – wariant kontrolny
89
wysokość pędów roślin
[cm]
a)
60
40
20
0
1
K
2
3
4
200 Cd
5
100 Cr
6
7
8
9
10 11 12 13 14
czas [tygodnie]
wysokość pędów roślin [cm]
b)
80
60
40
20
0
1
2
K
3
4
5
6
7
8
9
10
11
12
13
10
11
12
13
14
czas [tygodnie]
100 Cr
200 Cd
wysokość pędów roślin
[cm]
c)
120
100
80
60
40
20
0
1
2
3
4
5
6
7
8
9
14
czas [tygodnie]
K
200 Cd
100 Cr
Rys. 25. Przebieg wzrostu trzech gatunków rdestowców hodowanych w kulturach glebowych
z dodatkiem Cd – 200 mg·kg-1 i Cr – 100 mg·kg-1; K – wariant kontrolny; a) Fallopia japonica,
b) Fallopia × bohemica, c) Fallopia sachalinensis,)
90
W badaniach morfologicznych rdestowców hodowanych w kulturach glebowych
uwzględniono następujące cechy: I – wysokość pędów [cm], II – liczba liści na pędzie
[sz.], III – długość blaszki liściowej [cm], IV – szerokość blaszki liściowej [cm] oraz
V– świeżą i VI – suchą masę pędów nadziemnych [g] .
Na rys. 26 i 27 przedstawiono średnie arytmetyczne, przedziały błędów
standardowych oraz zakres minimalnych i maksymalnych wartości badanych cech
rdestowców hodowanych w wazonach z różnymi dawkami metali ciężkich.
Średnie wyniki pomiarów cech Fallopia japonica z wazonów z dodatkiem
trzech różnych dawek Cr i Pb (I doświadczenie) odpowiadały wariantowi kontrolnemu.
Pierwszą analizowaną cechą była wysokość pędów (łodyg). Rdestowiec japoński
z próby kontrolnej osiągnął 52,0 cm długości. Najbardziej zbliżoną do wariantu
kontrolnego średnią długość miały rośliny hodowane na glebie z dodatkiem 20 mg Cr
·kg-1 (50,1 cm) i 50 mg Pb ·kg-1 (50,5 cm). Najmniejszą wysokość – niespełna 8 cm
osiągnęły pędy hodowane na podłożu z dodatkiem 200 mg Cd ·kg-1. Kolejną badaną
cechą była liczba liści na pędzie. Wartości tej cechy kształtowały się w podobnych
zakresach, zarówno w kontroli, jak i w następujących wariantach: 20 mg Cd ·kg-1, 10
mg Cr ·kg-1 oraz 50, 100 i 200 mg Pb ·kg-1. Najwięcej liści wytworzyły pędy z
wazonów z dodatkiem 200 mg Zn ·kg-1, najmniej zaś z wazonów, do których
zaaplikowano 200 mg Cd ·kg-1 i 300 Cu ·kg-1. Liście roślin w próbie kontrolnej miały
10,7 cm długości i 7,1 cm szerokości (wartości średnie). Zbliżone wymiary miały liście
rdestowca japońskiego z wazonów z dodatkiem Cr, Pb (wszystkie testowane dawki)
i 100 mg Zn ·kg-1. Najmniejsze blaszki liściowe, o średnich wymiarach 2,3 cm
(długość)
i
2,0
cm
(szerokości)
wykształciły
pędy
hodowane
na
glebie
z 200 mg Cd ·kg-1. Świeża i sucha masa nadziemnych części roślin z wariantu
kontrolnego wyniosła odpowiednio 119,0 g i 37,7 g (wartości średnie). Podobną świeżą
masę miały rośliny z wazonów, do których zaaplikowano 20 mg Cd ·kg-1, 10 mg Cr ·kg1
oraz 50, 100 mg Pb ·kg-1. Największy spadek świeżej i suchej masy pędów względem
próby kontrolnej zanotowano w wariantach z Cd (200 mg·kg-1), Cu (300 mg·kg-1) oraz
Zn (300 mg·kg-1).
W drugim doświadczeniu wazonowym Fallopia japonica, Fallopia × bohemica
i Fallopia sachalinensis hodowane w wazonach z dodatkiem Cr (100 mg·kg-1) pod
względem morfologicznym były zbliżone do kontroli. Natomiast dawka 200 Cd mg·kg-1
znacząco wpłynęła na zmianę cech morfologicznych wszystkich gatunków. Łodygi
rdestowca japońskiego osiągnęły w wariancie kontrolnym 54,0 cm (wartość średnia).
91
Natomiast w wazonach z dodatkiem 200 mg Cd były ponad 3 razy krótsze (średnia
długość – 15,5 cm). W przypadku rdestowca sachalińskiego rośliny z próby kontrolnej
miały 99,9 cm wysokości, a w wariancie z Cd zaledwie 10,7 cm. Pędy rdestowca
pośredniego osiągnęły w warunkach kontrolnych 67,5 cm długość. Natomiast średnia
długość łodyg roślin hodowanych w wazonach z 200 mg Cd ·kg-1 była
prawie
trzykrotnie mniejsza niż u roślin z próby kontrolnej (24,8 cm). U wszystkich gatunków
zanotowano podobny (około półtorakrotny) spadek liczby liści w stosunku do próby
kontrolnej. Długość i szerokości blaszek liściowych zmniejszyła się od 1,5 do 2,4 razy.
W wazonach z dodatkiem Cd (200 mg·kg-1) odnotowano duży spadek świeżej i suchej
masy nadziemnych części roślin. Największy ubytek świeżej i suchej masy wystąpił
w przypadku rdestowca sachalińskiego. Masy pędów rdestowca sachalińskiego
wyniosły 148 g (świeża masa) i 54,9 g (sucha masa), natomiast w wariancie testowym
(200 mg Cd ·kg-1)13,0 g (świeża masa) i 3,4 g (sucha masa).
92
0
93
-1
Metal i dawka [mg kg ]
Metal i dawka [mg kg
-1
80
60
40
20
5
0
0
]
Rys. 26. Cechy morfologiczne pędów Fallopia japonica hodowanych z dodatkiem metali ciężkich (Cd, Cr, Cu, Pb i Zn)
Metal i dawka [mg kg
-1
]
Zn 300
100
Zn 200
35
Zn 100
120
-1
Pb 200
Metal i dawka [mg kg
Pb 100
40
Pb 50
140
Cu 300
8
Cu 200
45
Cr 100
-1
Cu 100
Metal i dawka [mg kg ]
Cr 20
Zn 300
Zn 200
Zn 100
Pb 200
Pb 100
Pb 50
Cu 300
Cu 200
Cu 100
0
Cr 100
0
Cr 20
2
Cr 10
20
Cr 10
40
Cd 200
60
Cd 200
80
Cd 100
12
Cd 100
140
Cd 20
100
Długość liści [cm]
120
Kontrola
Zn 300
Zn 200
Zn 100
Pb 200
Pb 100
Pb 50
Cu 300
Cu 200
Cu 100
Cr 100
Cr 20
Cr 10
Cd 200
14
Cd 20
160
Sucha masa pędów [g]
Cd 20
160
Kontrola
Zn 300
Zn 200
Zn 100
Pb 200
Pb 100
1
Pb 50
2
Cu 300
3
Cu 200
4
Cu 100
5
Cr 100
-1
Cr 20
Metal i dawka [mg kg ]
Cr 10
6
Cd 200
7
Cd 100
10
Cd 100
20
Kontrola
30
Liczba liści na pędzie [szt.]
40
Cd 20
9
Świeża masa pędów [g]
Zn 300
Zn 200
Zn 100
Pb 200
Pb 100
Pb 50
Cu 300
Cu 200
Cu 100
Cr 100
Cr 20
Cr 10
Cd 200
Cd 100
Cd 20
Kontrola
Wysokość pędów roślin [cm]
50
Kontrola
Zn 300
Zn 200
Zn 100
Pb 200
Pb 100
Pb 50
Cu 300
Cu 200
Cu 100
Cr 100
Cr 20
Cr 10
Cd 200
Cd 100
Cd 20
0
Kontrola
Szerokość liści [cm]
60
10
8
6
4
]
30
25
20
15
10
94
0
Metal i dawka [mg kg ]
-1
F.s. Cr 100
F.s. Cd 200
F.s. Kontrola
F.x b. Cr 100
F.x b. Cd 200
F.x b. Kontrola
F.j. Cr 100
F.j. Cd 200
F.j. Kontrola
0
Metal i dawka [mg kg ]
80
60
40
20
0
-1
.
F.s. Cr 100
100
F.s. Cd 200
120
F.s. Kontrola
140
F.x b. Cr 100
70
F.x b. Cd 200
-1
F.x b. Kontrola
Metal i dawka [mg kg ]
F.j. Cr 100
160
F.j. Cd 200
80
Sucha masa pędów [g]
180
F.j. Kontrola
F.s. Cr 100
2
F.s. Cd 200
4
F.s. Kontrola
6
F.x b. Cr 100
-1
F.x b. Cd 200
10
F.s. Cr 100
F.s. Cd 200
F.s. Kontrola
F.x b. Cr 100
F.x b. Cd 200
F.x b. Kontrola
F.j. Cr 100
F.j. Cd 200
F.j. Kontrola
F.s. Cr 100
F.s. Cd 200
F.s. Kontrola
F.x b. Cr 100
F.x b. Cd 200
F.x b. Kontrola
Liczba liści na pędzie [szt.]
20
18
16
14
12
10
8
6
4
2
0
F.x b. Kontrola
Metal i dawka [mg kg ]
F.j. Cr 100
0
F.j. Cr 100
20
F.j. Cd 200
40
F.j. Kontrola
60
Długość liści [cm]
80
F.j. Cd 200
8
Świeża masa pędów [g]
F.s. Cr 100
F.s. Cd 200
F.s. Kontrola
F.x b. Cr 100
F.x b. Cd 200
F.x b. Kontrola
F.j. Cr 100
F.j. Cd 200
F.j. Kontrola
Wysokość pędów roślin [cm]
100
F.j. Kontrola
Szerokość liści [cm]
120
180
160
140
120
100
80
60
40
20
0
Metal i dawka [mg kg -1]
60
50
40
30
20
10
-1
Metal i dawka [mg kg ]
Rys. 27. Cechy morfologiczne pędów Fallopia japonica (F. j.), Fallopia × bohemica (F. b.) i Fallopia sachalinensis (F. s.) hodowanych z dodatkiem Cd i Cr
W trakcie doświadczeń szklarniowych notowano również objawy uszkodzeń
i zmian morfologicznych liści i pędów badanych roślin.
W przypadku rdestowców japońskiego i pośredniego hodowanych w wazonach
z dodatkiem Cr (I i II doświadczenie wazonowe) nie odnotowano żadnych objawów
zewnętrznych świadczących o toksycznym działaniu tego pierwiastka. Niewielkie
zmiany w postaci purpurowo–czerwonych przebarwień liści wystąpiły u rdestowca
sachalińskiego. Dodanie do gleby 50, 100 i 200 mg Pb ·kg-1 także nie spowodował
żadnych widocznych objawów na pędach Fallopia japonica. Zmiany na blaszkach
liściowych w postaci chloroz oraz czerwono– purpurowych przebarwień pojawiły się
u roślin hodowanych w wazonach z dodatkiem Cd (20, 100, 200 mg·kg-1 – I i 200
mg·kg-1 – II doświadczenie wazonowe), Cu (200 i 300 mg·kg-1) oraz Zn (100, 200 i 300
mg·kg-1). Ponadto, we wszystkich wariantach z udziałem Cd oraz w wariantach, gdzie
zastosowano 200 i 300 mg Zn ·kg-1stwierdzono deformacje blaszek liściowych,
zasychanie i przedwczesne opadanie liści oraz karłowacenie pędów. W pierwszym
doświadczeniu, w wazonach z najwyższymi dawkami Cd i Zn obserwowano zasychanie
i obumieranie pędów Fallopia japonica. Jednak w drugim doświadczeniu przy tej samej
dawce Cd, u rdestowca japońskiego nie zanotowano wyżej wymienionych objawów.
Materiał roślinny (kłącza Fallopia japonica) w I i II doświadczeniu szklarniowym mógł
się różnić, ponieważ pobrano go z dwóch odmiennych stanowisk.
95
7.2.2.
AKUMULACJA METALI CIĘŻKICH W NADZIEMNYCH I PODZIEMNYCH
CZĘŚCIACH RDESTOWCÓW
Wyniki dotyczące kumulacji metali ciężkich w nadziemnych i podziemnych
częściach rdestowców hodowanych w kulturach glebowych z dodatkiem wybranych
metali ciężkich zawarto w tab. 21 i 23. Korelacje pomiędzy wzrastającymi dawkami
metali w glebie, a zawartością metali ciężkich w tkankach roślin przedstawiono w tab.
22 i 24.
W
pierwszym
doświadczeniu
wazonowym
średnia
zawartość
kadmu
w nadziemnych i podziemnych częściach rdestowca japońskiego rosnącego w wariancie
kontrolnym kształtowała się w zbliżonym zakresie (1,3 mg·kg-1 – cz. podziemne i 1,1
mg·kg-1 – cz. nadziemne). Wzrost stężenia Cd w glebie spowodował akumulację tego
pierwiastka, przede wszystkim w liściach. W wariancie, gdzie zastosowano dawkę 100
mg Cd ·kg-1 rośliny zgromadziły w częściach nadziemnych średnio 700,3 mg Cd ·kg-1.
Uzyskane wyniki są istotne statystycznie, a dodatnie wartości współczynnika korelacji
linowej Persona wskazują na silną zależność pomiędzy wzrastającymi dawkami Cd w
glebie, a jego koncentracją w materiale roślinnym. Do metali akumulowanych w
liściach
należał
także
Zn.
Średnie
zawartości
tego
pierwiastkach
w roślinach kontrolnych wyniosły 25,5 mg·kg-1 (kłącza i korzenie ) oraz 52,4 mg·kg-1
(liście). W tkankach Fallopia japonica rosnącego na glebie z dodatkiem
200 mg Zn ·kg-1 stwierdzono średnio 194,5 mg·kg-1 (cz. podziemne) oraz 563,5 mg·kg-1
(cz. nadziemne). Prezentowane wyniki są istotne statystycznie, a dodatnie wartości
współczynnika
korelacji
Spermana
potwierdzają
dużą
zależność
pomiędzy
analizowanymi parametrami. U rdestowca japońskiego chrom, miedź oraz ołów były
akumulowane głównie w kłączach i korzeniach. W wariancie kontrolnym średnia
zawartość Cr w częściach podziemnych wyniosło 4,4 mg·kg-1, w nadziemnych zaś 2,1
mg·kg-1. Zaaplikowanie do gleby 100 mg Cr ·kg-1 spowodowało wzrost stężenia chromu
w częściach podziemnych do 18,25 mg·kg-1 oraz do 9,3 mg·kg-1 w liściach.
Analiza statystyczna potwierdza wysoką korelację pomiędzy zawartością Cr w glebie,
a jego koncentracją w badanych częściach roślin. Nadziemne i podziemne organy
rdestowca japońskiego z wariantów kontrolnych zawierały zbliżone ilości miedzi
(średnio 7,9 mg Cu ·kg-1 – części podziemne i 7,2 mg Cu ·kg-1 – części nadziemne).
W roślinach z wazonów z dodatkiem 300 mg Cu ·kg-1 stwierdzono średnio 48,5 mg
Cu ·kg-1 (cz. nadziemne) i 112,8 mg Cu ·kg-1 (cz. podziemne). Uzyskane wyniki były
96
istotne statystycznie, a wartości współczynnika korelacji świadczą o wysokiej
zależności pomiędzy dawką metali, a ich zawartością w liściach oraz kłączach
i korzeniach Fallopia japonica. Ostatnim testowanym pierwiastkiem był ołów.
Rdestowiec japoński z wazonów kontrolnych zawierał średnio 2,5 mg Pb ·kg-1
w kłączach i korzeniach oraz 1,0 mg Pb ·kg-1 w liściach. W roślinach z gleby
zanieczyszczonej 200 mg Pb ·kg-1 stwierdzono odpowiednio 28,5 mg Pb ·kg-1
w częściach podziemnych i 8,6 mg Pb ·kg-1 w częściach nadziemnych. Analizy
statystyczne wykazały wysoki poziom istotności oraz silną korelacje pomiędzy
zawartością ołowiu w glebie i w tkankach rdestowca japońskiego.
Wyniki drugiego eksperymentu (z zastosowaniem Cd i Cr) potwierdzają
zdolności trzech badanych gatunków rdestowców do akumulacji kadmu, przede
wszystkim w liściach. Najwyższe stężania tego pierwiastka (zarówno w roślinach
kontrolnych, jak i hodowanych na glebie z dodatkiem 200 mg Cd ·kg-1) stwierdzono
u Fallopia japonica. Podziemne pędy rdestowca japońskiego pobrane z wazonów
kontrolnych zawierały średnio 1,3 mg Cd ·kg-1. W częściach nadziemnych stwierdzono
średnio 0,6 mg Cd ·kg-1. Rdestowiec japoński hodowany w glebie z dodatkiem 200 mg
Cd ·kg-1 zgromadził średnio 487,3 mg Cd ·kg-1 (części podziemne) oraz 1761,8 mg Cd
·kg-1 (części nadziemne). Nieco niższe stężenia kadmu odnotowano w tkankach
Fallopia sachalinensis. Analizom poddano jednak tylko po jednej próbie z wazonów
kontrolnych i zanieczyszczonych 200 mg Cd ·kg-1. Kłącza rdestowca sachalińskiego
wykazały niską zdolność do regeneracji, ograniczając tym samym liczbę badanych
prób. Podziemne pędy Fallopia sachalinensis rosnące w próbie kontrolnej zawierały
średnio 0,7 mg Cd ·kg-1, części nadziemne zgromadziły 0,5 mg Cd ·kg-1. Rośliny z
wazonów z dodatkiem 200 mg Cd ·kg-1 zgromadziły 697,0 mg Cd ·kg-1 (pędy
podziemne)
i 1068,0 mg·kg-1 (liście). Najniższą zawartość kadmu stwierdzono w organach Fallopia
× bohemica. Średnia zawartość Cd w częściach podziemnych pochodzących
z wazonów kontrolnych wyniosło 0,43 mg·kg-1, natomiast w częściach nadziemnych
stwierdzono średnio 0,33 mg Cd ·kg-1. Rośliny z wazonów, do których zaaplikowano
200 mg Cd ·kg-1 zawierały 390,00 mg Cd ·kg-1 w częściach podziemnych oraz 547,8 mg
Cd ·kg-1 w częściach nadziemnych (wartości średnie).
Uzyskane wynik dotyczące kumulacji Cd u rdestowców japońskiego i pośredniego były
istotne statystycznie. Ponadto, wykazano bardzo wysoką korelacjię pomiędzy
zawartością kadmu w glebie, a jego kumulacją w tkankach roślin.
97
Badane gatunki rdestowców akumulowały chrom przede wszystkim w pędach
podziemnych. Kłącza i korzenie u Fallopia japonica z wazonów kontrolnych zawierały
średnio 5,61 mg Cr ·kg-1, a części nadziemne 3,34 mg Cr ·kg-1. W tkankach Fallopia
sachalinensis odnotowano średnio 6,22 mg Cr ·kg-1 (części podziemne) oraz 3,58 mg
·kg-1 (części nadziemne). Rdestowiec pośredni zawierał 4,55 mg Cr ·kg-1 w liściach
oraz 2,82 mg·kg-1 w organach podziemnych. Rośliny hodowane w wazonach
z dodatkiem 100 mg Cr ·kg-1 zawierały w pędach podziemnych 39,65 mg·kg-1 (Fallopia
sachalinensis), 13,23 mg·kg-1 (Fallopia × bohemica) i 10,78 mg·kg-1 (Fallopia
japonica). Średnia zawartość chromu w liściach kształtowała się na poziomie 5,47
mg·kg-1 w przypadku rdestowca sachalińskiego, 5,92 mg·kg-1 u rdestowca pośredniego
oraz 7,07 mg·kg-1 u rdestowca japońskiego. Wyniki uzyskane w tym zakresie dla
Fallopia × bohemica i Fallopia japonica zostały potwierdzone statystycznie.
98
Tab. 21. Średnie zawartości metali ciężkich [mg·kg-1] w nadziemnych i podziemnych częściach
Fallopia japonica
Grupy jednorodne wyznaczone za pomocą testu HSD Tukeya po jednoczynnikowej analizie
wariancji, liczby oznaczone tą samą literą nie różnią się istotnie przy p ≤ 0,05
Metal
Dawka [mg·kg-1]
Cd
Kontrola
1,3 a
1,1 a
20
6,9 a
17,0 a
100
301,8 b
700,3 b
200
n.o
n.o
Kontrola
4,4 a
2,1 a
10
5,5 a
3,3 a
20
15,05 b
3,8 a
100
18,25 b
9,3 b
Kontrola
7,9 a
7,2 a
100
19,0 a
12 a
200
37,9 b
36,3 b
300
112,8 c
48,5 b
Kontrola
2,5 a
1,0 a
50
3,1 a
2,1 a
100
7,8 a
4,0 a
200
28,5 b
8,6 b
Kontrola
25,5 a
52,4 a
100
115,4 b
360,5 ab
200
194,5 c
563,5 c
300
n.o
n.o
Cr
Cu
Pb
Zn
Części podziemne
Części nadziemne
Objaśnienie: n.o – nie oznaczono z powodu braku materiału badawczego, zastosowana dawka metalu
spowodowała zamieranie pędów
Tab. 22. Współczynniki korelacji Persona (r) i Spearmana (Rs) pomiędzy zastosowanymi dawkami
metali, a zawartością metali ciężkich w podziemnych i nadziemnych częściach Fallopia japonica (I
doświadczenie)
Fallopia japonica
Cd
Cr
Cu
Pb
Zn
Części podziemne
r = 0,8981
p = 0,000
Rs = 0,5400
p = 0,03
Rs = 0,7420
p = 0,001
r = 0,8843
p = 0,000
Rs = 0,8278
p = 0,000
Części nadziemne
r = 0,8744
p = 0,000
r = 0,7601
p = 0,002
r = 0,9030
p = 0,000
r = 0,8101
p = 0,000
Rs = 0,9059
p = 0,000
99
Tab. 23. Średnie zawartości metali ciężkich [mg·kg-1] w nadziemnych i podziemnych częściach
Fallopia japonica, Fallopia x bohemica i Fallopia sachalinensis.
Grupy jednorodne wyznaczono za pomocą testu HSD Tukeya po jednoczynnikowej analizie
wariancji, liczby oznaczone tą samą literą nie różnią się istotnie przy p ≤ 0,05
Metal
Dawka [mg·kg-1]
Części podziemne
Części nadziemne
Fallopia japonica
Cd
Cr
Kontrola
1,3 a
0,6 a
200
487,3 b
1761,8 b
Kontrola
5,6 a
3,3 a
100
10,8 a
7,1 b
Kontrola
0,4 a
0,3 a
200
390 b
547,8 b
Kontrola
4,5 a
2,8 a
100
13,2 b
5,9 b
Kontrola
0,7
0,5
200
697
1068
Kontrola
6,2
3,6
100
39,6
5,5
Fallopia x bohemica
Cd
Cr
Fallopia sachalinensis
Cd
Cr
Tab. 24. Współczynniki korelacji Persona (r) i Spearmana (Rs) pomiędzy zastosowanymi dawkami
metalu, a zawartością metali ciężkich w podziemnych i nadziemnych częściach Fallopia japonica,
Fallopia x bohemica i Fallopia sachalinensis
Fallopia japonica
Cd
Cr
Części podziemne
r = 0,8832
p = 0,04
Rs = 0,6301
p = 0,03
Części nadziemne
r = 0,9760
p = 0,000
Rs = 0,9657
p = 0,000
Fallopia x bohemica
Cd
Cr
Części podziemne
r = 0,9214
p = 0,001
Rs = 0,8728
p = 0,004
Części nadziemne
r = 0,8258
p = 0,012
Rs = 0,8728
p = 0,004
Fallopia sachalinensis
Cd
Cr
Części podziemne
n.o
n.o
Części nadziemne
n.o
n.o
Objaśnienie: n.o – nie oznaczono
100
8. DYSKUSJA WYNIKÓW
Rdestowce to jedne z najbardziej ekspansywnych roślin występujące obecnie na
obszarze niemal całej Europy (Wielka Brytania, Czechy, Niemcy, Francja, Słowenia,
Szwecja, Norwegia), a także w Ameryce Północnej, Australii oraz w Nowej Zelandii
[Beerling 1993; Beerling i in. 1994; Weston i in. 2005; Alberternst i Bőhmer 2006;
Bailey i Wisskirchen 2006; Bailey i in. 2007; Bailey i in. 2008].
Przedstawiciele z rodzaju Fallopia są częstym elementem fitocenoz w miastach,
gdzie szybko zwiększają swój areał występowania, stając się nieodłącznym elementem
lokalnej flory. Jak podają Fojcik i Tokarska-Guzik [2000] obecność rdestowców
odnotowano między innymi na terenie Katowic, Poznania i Warszawy. Wrocław jako
zurbanizowane, stale rozwijające się miasto stanowi dogodne miejsce do bytowania
i rozprzestrzeniania się inwazyjnych gatunków roślin, również z rodzaju Fallopia.
W latach 2009–2011 na terenie miasta odnotowano 310 skupień rdestowców,
zajmujących powierzchnię 1,1343 ha. Dla porównania w 1960 roku na obszarze
Dolnego Śląska odnotowano 342 stanowiska rdestowców [Tokarska-Guzik 2005].
Obecna liczba dolnośląskich stanowisk przedstawicieli z rodzaju Fallopia oraz ich
aktualny zasięg nie są znane.
Spośród wszystkich gatunków najliczniej na terenie Wrocławia reprezentowany
jest rdestowiec japoński, który stanowi ponad 73,2% ich liczby ogólnej. Fallopia
sachalinensis występuje sporadycznie obejmując zaledwie 5,2% ogółu skupisk
rdestowców. Podobne tendencje dotyczące rozmieszczenia badanych gatunków
zaznaczają się w innych częściach Europy (Wielka Brytania, Czechy, Niemcy), gdzie
dominującym gatunkiem jest Fallopia japonica var. japonica [Jalas i Suominen 1988
cyt. za: Bailey i in. 2007]. Rdestowiec sachaliński spotykany jest znacznie rzadziej
[Sukopp i Starfinger 1995]. Dla przykładu w Czechach na ogólną liczbę 1982
odnalezionych stanowisk rdestowców 68% ogółu stanowił Fallopia japonica, a 13%
Fallopia sachalinensis [Mandák i in. 2004]. Rdestowiec japoński notowany jest obecnie
na 41% terytorium Europy, a w Wielkiej Brytanii występuje aż na 99%
niezurbanizowanego obszaru [Fabiszewski i Brej 2005].
We Wrocławiu odnaleziono także klony międzygatunkowego mieszańca –
Fallopia × bohemica. Obecność rdestowca pośredniego na danym terenie stanowi
poważne zagrożenie dla lokalnej flory. Gatunek ten posiada najwyższe ze wszystkich
101
rdestowców zdolności do regeneracji [Bimová i in. 2003; Pyšek i in. 2003],
charakteryzuje się wyższą ekspansywnością niż gatunki rodzicielskie [Mandák i in.
2004], jest także najtrudniejszy do zwalczania [Bimová i in. 2001]. Udział rdestowca
pośredniego w ogólnej liczbie zlokalizowanych we Wrocławiu skupień wynosi 21,6%.
Z doniesień literaturowych wynika, że w innych częściach Europy hybryda ta występuje
rzadziej niż przeważający rdestowiec ostrokończysty, lecz częściej, niż rdestowiec
sachaliński [Bailey i in. 2007; Bailey i in 2008]. We wschodniej części Europy notuje
się wzrastający udział Fallopia × bohemica w ogólnej liczbie stanowisk rdestowców
[Bailey i Wisskirchen 2006].
Badania własne pozwoliły na określenie procentowego udziału powierzchni
zajmowanej przez poszczególne gatunki. We Wrocławiu kępy rdestowca japońskiego
zajmowały 54,8% ogółu, podczas gdy rdestowiec sachaliński pod względem
powierzchni stanowił zaledwie 4,6%. Na uwagę zasługuje stosunkowo duży udział
powierzchni Fallopia × bohemica. Liczba stanowisk rdestowca pośredniego była ponad
trzykrotnie niższa od dominującego na terenie Wrocławia rdestowca japońskiego,
pomimo to kępy Fallopia × bohemica zajmowały aż 40,6% powierzchni wszystkich
zlokalizowanych skupisk. Obecne proporcje dotyczące występowania gatunków z
rodzaju Fallopia na obszarze ich wtórnego zasięgu wynikają między innymi z różnic w
zdolnościach do regeneracji, które zostały stwierdzone przez Bimovą i in. [2003].
Wszystkie trzy gatunki – o czym już wspominano wcześniej, rozmnażają się droga
wegetatywną z fragmentów pędów podziemnych lub łodyg, przy czym kłącza wykazują
największą zdolność do regeneracji [Brock i Wade 1992; cyt. za: Brock i in. 1995].
Wśród przedstawicieli z rodzaju Fallopia najmniejszą zdolność odrastania z pędów
podziemnych ma Fallopia sachalinensis, co odpowiada niewielkiej liczebności tego
gatunku na terenie Europy w porównaniu z pozostałymi taksonami [Mandák i in. 2004].
Analizę przestrzennego rozmieszczenie rdestowców na terenie Wrocławia
przeprowadzono w oparciu o metodę kartowania, wyznaczając jako podstawowe pole
badawcze kwadraty o boku 1 km. We Wrocławiu wyznaczono łącznie 340 kwadratów.
Obecność wszystkich przedstawili z rodzaju Fallopia stwierdzono na 79 polach
badawczych, które stanowią ponad 23% powierzchni miasta. Najwięcej skupisk
rdestowców odnaleziono w silnie zurbanizowanych częściach miasta. Natomiast na
terenach niezabudowanych, obszarach leśnych lub użytkowanych rolniczo rdestowce
występowały zdecydowanie rzadziej. Podobny model rozmieszczenia rdestowców na
obszarze Katowic podają Fojcik i Tokarska-Guzik [2000]. Również Żołnierz i Antczak
102
[2005] badając inwazję rdestowców w dolnym biegu Bystrzycy i Ślęzy (w granicach
administracyjnych Wrocławia) stwierdzili, że najsilniej postępuje ona w rejonach
zurbanizowanych, w pobliżu osiedli i ogródków działkowych. Natomiast wzdłuż
brzegów rzeki ciągnących się pośród obszarów leśnych, pól uprawnych i łąk
obserwowano zdecydowanie mniej stanowisk tego gatunku.
We Wrocławiu Fallopia japonica zlokalizowany został w 53 kwadratach, czyli
na ponad 15,5% powierzchni badanego terenu. Skupiska tego gatunku rozproszone były
w niemal wszystkich częściach miasta, za wyjątkiem północnych i skrajnie zachodnich
terenów. Najczęściej w polu badawczym występowało od 2 do 4 skupisk rdestowca
japońskiego. Pod względem powierzchniowym dominowały kępy w przedziale od 10
do 40 m2. W Polsce najliczniejsze jak dotąd stanowiska rdestowca japońskiego opisano
na terenie Katowic, gdzie zajmował on aż 106 pól badawczych [Fojcik i TokarskaGuzik 2000]. Obecność rdestowca japońskiego odnotowano także w Poznaniu w 12
kwadratach badawczych, w Jaworzynie w 62 polach badawczych oraz w Warszawie
w 84 kwadratach, gdzie za podstawowe pole badawcze przyjęto kwadrat o boku 1,5 km
[Fojcik i Tokarska-Guzik 2000].
Drugi z rdestowców – rdestowiec sachaliński (Fallopia sachalinensis) został
odnotowany w zaledwie 3 z 340 kwadratów badawczych. W zachodniej i południowej
części miasta w dwóch polach badawczych występowały kępy w zagęszczeniu od 2– 4
na 1 km2, o powierzchni w przedziale od 40 do 200 m2. Najwięcej kęp Fallopia
sachalinensis (5–10 skupisk na 1 km2), których powierzchnia przekraczała 2000 m2
odnotowano w południowo– wschodniej części Wrocławia. Rdestowiec sachaliński
spotykany był rzadko także w innych miastach Polski. Fojcik i Tokarska-Guzik [2000]
podają, że w Katowicach odnotowano go w 11 kwadratach, w Poznaniu w 1 kwadracie,
zaś w Warszawie w 3 polach badawczych, a w Jaworzynie nie występował.
Współwystępowanie na danym obszarze rdestowców ostrokończystego i sachalińskiego
ma istotny wpływa na liczbę stanowisk ich mieszańca. Z uwagi na pospolite
występowanie rdestowca japońskiego czynnikiem ograniczającym rozprzestrzenianie
się rdestowca pośredniego może być mniejsza częstotliwość występowania rdestowca
sachalińskiego [Zając 1989; Jackowiak 1993; Urbisz 1996; Tokarska-Guzik i Rostański
1998; Studnik-Wójcikowska 1998; Tokarska-Guzik 1999 cyt. za: Fojcik i TokarskaGuzik 2000]. Z drugiej zaś strony znane są przypadki obecności na danym obszarze
Fallopia × bohemica pomimo braku jego gatunków rodzicielskich. Taki stan rzeczy
zanotowano m.in. na Węgrzech [Balogh 1999 cyt. za: Fojcik i Tokarska-Guzik 2000].
103
Klony międzygatunkowego mieszańca stwierdzono także w śródziemnomorskiej części
Francji, w której nie odnotowano rdestowca japońskiego [Bailey i Wisskirchen 2006].
We Wrocławiu kępy Fallopia × bohemica występowały stosunkowo często
pomimo niewielkiej liczby stanowisk Fallopia sachalinensis. Skupiska rdestowca
pośredniego odnotowano w 23 polach badawczych, czyli na około 6,8% powierzchni
miasta. Przypuszczalnie fragmenty kłączy Fallopia × bohemica zostały przeniesione
wraz z zanieczyszczoną glebą z jednej do drugiej części miasta. Świadczyć o tym może
częste występowanie młodych pędów rdestowca pośredniego w pobliżu zwałowisk,
gruzowisk i śmietnisk. Mieszaniec ten spotykany był głównie w centralnej i zachodniej
części Wrocławia. Skupiska rdestowca pośredniego, podobnie jak japońskiego
występowały najczęściej w zagęszczeniu od 2 do 4 na 1km2. Najmniejsze pod
względem powierzchniowym skupiska (poniżej 10 m2 na 1 km2) stanowiły 30% ogółu
skupisk rdestowców i występowały zwłaszcza w silnie zabudowanych częściach miasta.
Na niezabudowanych obszarach rdestowiec pośredni szybko powiększał swój areał,
w związku, z czym skupienia powyżej 200 m2 spotykane były równie często i stanowiły
26% wszystkich notowanych skupisk. Niestety brak jest danych literaturowych
dotyczących występowania Fallopia × bohemica na terenie Polski. Informacje na ten
temat pochodzą jedynie z Katowic, gdzie obecność rdestowca pośredniego
potwierdzono w 35 kwadratach badawczych [Fojcik i Tokarska-Guzik 2000].
W trakcie badań terenowych zwrócono uwagę na sposób zagospodarowania
terenu, na którym odnaleziono skupiska rdestowców.
Zarówno w obrębie pierwotnego, jak i wtórnego zasięgu występowania
rdestowce wykazują preferencje do siedlisk antropogenicznych [Mandák i in. 2004;
Bailey i in. 2008] oraz do rozprzestrzeniania się na obszarach ruderalnych [Sukopp
i Sukopp 1988]. Najczęściej występują wzdłuż dróg, autostrad, kompleksów
kolejowych oraz porastają brzegi rzek.
W warunkach miejskich Wrocławia najwięcej skupień Fallopia japonica
odnotowano na obszarach zabudowy mieszkaniowej (jedno lub wielokondygnacyjnej),
na terenach niezagospodarowanych (do których zaliczono także dzikie śmietniska,
zwałowiska i gruzowiska) oraz na terenach nadwodnych, na których występowały
największe pod względem powierzchni kępy. Najmniej skupisk Fallopia japonica
zlokalizowano na terenach zieleni miejskiej.
Agregacje
rdestowca
pośredniego
notowano
najczęściej
na
terenach
niezagospodarowanych (głównie w sąsiedztwie dzikich śmietnisk, zwałowisk
104
i gruzowisk). Na terenach nadwodnych Fallopia × bohemica spotykany był rzadziej.
Skupiska rdestowca pośredniego tworzyły tam duże płaty stanowiąc tym samym 45,4%
jego powierzchni ogólnej. Podobnie, jak w przypadku rdestowca japońskiego najmniej
stanowisk Fallopia × bohemica odnotowano na terenach zieleni miejskiej.
Obecność rdestowca sachalińskiego stwierdzono w zaledwie trzech z sześciu
wyróżnionych typów siedlisk: na terenach niezagospodarowanych, na poboczach dróg
i torów kolejowych oraz na terenach nadwodnych. Największą powierzchnię,
stanowiącą 43,6% powierzchni wszystkich skupisk Fallopia sachalinensis zajmowały
kępy rosnące wzdłuż dróg i torów kolejowych. Najmniejsze pod względem
powierzchniowym stanowiska zlokalizowano na obszarach zabudowy mieszkaniowej.
Badane okazy Fallopia japonica były zbliżone pod względem morfologicznym
do notowanych na terenie Europy i Ameryki Północnej oktoploidalnych okazów
żeńskich. Analizowany klon rdestowca sachalińskiego był obupłciowy, o tetraploidalnej
liczbie chromosomów. Fakt ten ma znaczenie, gdyż współwystępowanie na danym
obszarze oktoploidalnych żeńskich klonów Fallopia japonica i tetraploidalnych
obupłciowych
okazów
Fallopia
sachalinensis
zwiększa
ryzyko
powstawania
międzygatunkowego mieszańca – Fallopia × bohemica na drodze hybrydyzacji
(krzyżowania). Ponadto, jak podkreślają Bailey i Stace [1992] skuteczna hybrydyzacja
pomiędzy spokrewnionymi taksonami prowadzi do formowania się nowych genotypów
roślin, które wykazują wyższe zdolności do inwazji niż ich taksony rodzicielskie.
Wśród występujących we Wrocławiu klonów Fallopia × bohemica odnotowano
okazy żeńskie i obupłciowe, wszystkie były heksaploidalne (2n=66). Stopień
poliploidalność klonów rdestowca pośredniego wpływa na sukces reprodukcyjny
gatunku na drodze generatywnej. Bailey i Stace [1992] informują, że zdolne do
dalszego rozwoju nasiona tworzą przede wszystkim tetra i oktoploidalne klony Fallopia
× bohemica. Przy czym w warunkach laboratoryjnych największą liczbę płodnych
nasion zawiązują tetraploidalne osobniki żeńskie [Bailey 1994]. Obecnie na terenie
Europy tetra i oktoploidalne osobniki rdestowca pośredniego notowane są sporadycznie.
O sukcesie roślin inwazyjnych decyduje szeroka skala tolerancji w odniesieniu
do warunków życiowych oraz możliwości szybkiego dostosowania się do zachodzących
w środowisku zmian [Kornaś 1990; Bradley i in. 2010]. Wymienione cechy posiadają
gatunki z rodzaju Fallopia. W naturalnej ojczyźnie rdestowce, a zwłaszcza japoński
mają dużą amplitudę ekologiczną [Sukopp i Sukopp 1988]. Na przykład Maruta [1994]
oraz Adachi [1996] opisują Fallopia japonica (var. compacta) jako pionierski gatunek
105
porastający wulkaniczną glebę góry Fudżi. Podobnie, we wtórnym zasięgu
występowania tolerancja ekologiczna rdestowców jest szeroka. Świadczyć o tym może
choćby fakt odnalezienia skupień rdestowców na silnie zasolonych siedliskach
[Richards i in. 2008].
Badania chemiczne gleby wykazały, że we Wrocławiu rdestowce występują na
glebach o odczynie: od kwaśnego (pH w KCl – 5,4 oraz w H2O – 6,0) do zasadowego
(pH w KCl 7,9 oraz 8,0 w H2O). Jeszcze szerszy zakres pod względem pH gleby,
podaje [Beerling i in. 1994] z obszaru Anglii. Obecność rdestowca japońskiego
stwierdzono na glebach o pH w zakresie od 3,0 do 8,5. Gleby pobrane z Wrocławia
charakteryzowały się bardzo wysoką zawartością przyswajalnych form fosforu, potasu
i magnezu (do 129,5 mg P2O5·100g-1, 127,0 mg K2O ·100g-1 oraz 35,0 mg Mg ·100
g-1). Badania nad składem chemicznym gleb w Japonii wykazały, że rdestowce mogą
porastać także gleby ubogie w składniki pokarmowe oraz o niskiej pojemności wodnej
[Beerling i in. 1994]. Najwieksze zawartość C organicznego i N ogólnego stwierdzono
w glebach pochodzących ze stanowisk Fallopia × bohemica. Zawartość węgla
organicznego kształtowała się tu na poziomie od 1,10% aż do 14,48%, a zawartości N
ogólnego od 0,03% do 0,42%. Równie wysokie zawartości materii organicznej
stwierdzono w Anglii, gdzie zawartość C organicznego w glebach porośniętych przez
rdestowce sięgała 18,6% [Beerling i in. 1994].
Gatunki
z
rodzaju
Fallopia
dobrze
znoszą
obecność
w
środowisku
zanieczyszczeń. Rozprzestrzenianie się w pobliżu wulkanów górskiej odmiany
rdestowca japońskiego – Fallopia japonica var. compacta sugeruję tolerancje gatunku
na podwyższone zawartości dwutlenku siarki. Ponadto, w obrębie naturalnego zasięgu
występowania rdestowce zasiedlają tereny zanieczyszczone metalami ciężkimi. Na
przykład, Nishizono i in. [1989] informują o stanowiskach rdestowca ostrokończystego
na glebach o wysokich koncentracjach Cd, Cu oraz Zn.
W materiale glebowym pobranym z obszaru Wrocławia stwierdzono wyższe
w porównaniu z naturalnymi zawartości Cd, Cu, Pb oraz Zn. Na najwyższym poziomie
koncentracji występował Pb i Zn, których koncentracja w glebach przekraczała
dopuszczalną zawartość dla gruntów zabudowanych i zurbanizowanych określoną
w Rozporządzeniu Ministra Środowiska w sprawie standardów jakości gleb oraz
standardów jakości ziem [2002].
Ważnym dla roślin czynnikiem ekologicznym jest temperatura, której rozkład
warunkuje rozmieszczenie i rozprzestrzenianie się gatunków na kuli ziemskiej
106
[Kacperska 2002]. Występujące powszechnie w ekosystemach miejskich zjawisko
miejskiej wyspy ciepła dodatkowo proteguje rozprzestrzenianie się gatunków obcych
[Kowarik 1995]. Zauważono, że w miastach przestrzenny wzór rozmieszczenia
niektórych inwazyjnych gatunków roślin pokrywa się z rozkładem miejskiej wyspy
ciepła. Na przykład, rozmieszczenie inwazyjnego Ailanthus altissima w Berlinie
odpowiada strukturze miejskiej wyspy ciepła [Kowarik i Böcker 1984 cyt. za: Kowarik
1995].
Przedstawiciele z rodzaju Fallopia występują w różnych strefach klimatycznych
(od chłodnej, poprzez umiarkowaną aż do pustynnej). Dobrze znoszą warunki związane
z ostrym klimatem górskim [Fabiszewski i Brej 2007]. Dowiedziono, iż kłącza
rdestowców są w stanie przetrwać temperatury sięgające nawet do –42˚C [Beerling
1993]. Badania prowadzone przez Mariko i in. [1993] oraz Yamaguchi i in. [2000]
potwierdzają także wysoką żywotność i możliwość przetrwania siewek rdestowców
w
ekstremalnych
warunkach
klimatu
górskiego.
Natomiast
przeprowadzone
w warunkach miejskich Wrocławia badania wskazują na preferencje gatunków
z rodzaju Fallopia, zwłaszcza Fallopia japonica i jego mieszańca do ciepłych rejonów
miasta,
gdzie
odnotowano
najwięcej
skupisk
tych
gatunków.
W najzimniejszych obszarach Wrocławia nie stwierdzono obecności przedstawicieli
z rodzaju Fallopia.
Podczas dwóch lat badań stanowisk rdestowca japońskiego i pośredniego
obserwowano 5 faz rozwojowych oraz 14 faz, które można skojarzyć z fenologią.
Okazy rdestowca japońskiego produkowały znaczną liczbę owoców. W przypadku
rdestowca pośredniego na części stanowisk nie zanotowano faz rozwojowych owoców.
W pierwszym roku obserwacji owoce zaobserwowano na 6 z 10 badanych stanowisk.
Rok później skąpo owocujące kępy Fallopia × bohemica wystąpiły na zaledwie
1 stanowisku. Bailey i in. [2008] podaje, że w Wielkiej Brytanii rdestowce nie zawsze
związywały owoce. Według Conolly [1977] owoce u Fallopia japonica pojawiały się
sporadycznie, głównie po ciepłym i suchym lecie. Bailey i in. [2008] wskazał czynniki
prawdopodobnie odpowiedzialne za ten stan. Należy do nich duża wrażliwość
rdestowca japońskiego na wczesne przymrozki jesienne oraz mało atrakcyjne dla
owadów zapylających (głównie pszczół) kwiaty. W ostatnich latach na terenie Wielkiej
Brytanii obserwuje się bogato owocujące okazy Fallopia japonica var. japonica.
Omawiane zjawisko wynika ze zmieniających się warunków klimatycznych (ocieplanie
klimatu) oraz ze wzrastającej liczby stanowisk Fallopia baldschuanica [syn. Fallopia
107
aubertii], który na terenie Anglii jest głównym donorem pyłku dla klonów rdestowca
japońskiego [Bailey 2001; Bailey i in. 2008]. Wynikiem krzyżowania się wyżej
wymienionych taksonów jest powstawanie na terenie Wielkiej Brytanii Fallopia
× conollyana – nowych hybryd w obrębie rodzaju Fallopia [Bailey i in. 2008].
Brak owoców u żeńskich i obupłciowych klonów rdestowca pośredniego w II
roku obserwacji mógł wynikać z przyczyn temperaturowych (występowanie jesiennych
przymrozków) lub ze spadku aktywności zapylaczy, spowodowanej przez duże opady
deszczu. We wrześniu 2010 roku suma opadów była 11 razy wyższa w porównaniu
z rokiem ubiegłym. Zagadnienie to wymaga dalszych obserwacji.
Znamienną cechą rdestowców jest ich szybki przyrost biomasy, zwłaszcza
w pierwszych tygodniach wegetacji. W USA przyrost pędów podczas wczesnej wiosny
określono 4,65 cm/dzień, w Anglii zaś obliczono, że tempo wzrostu rdestowca
japońskiego wynosi średnio na 4,3 cm/dzień [Beerling i in. 1994]. Sukopp i Starfinger
[1995] podają, że według Numata i Yoshizawa [1975] dzienne przyrosty pędów
rdestowca sachalińskiego w okresie wczesnego lata dochodzą do 15 cm. Natomiast
Hartmann i in. [1995] informują, że na terenie Badenii - Wirtembergii pędy rdestowców
wykazywały przyrost nawet do 30 cm na dobę. We Wrocławiu największe średnie
miesięczne przyrost pędów Fallopia japonica wyniosły: 131,6 cm (2009 rok)
i 126,1 cm (2010 rok). W 2009 i 2010 roku wśród stanowisk Fallopia × bohemica
odnotowano wzrost na poziomie 144,5 cm i 154,6 cm. Miesięczne tempo wzrostu łodyg
Fallopia sachalinensis wynosiło 97,0 cm (2009 rok) i 102,4 cm (2010 rok).
Zanotowane różnice w przebiegu faz rozwojowych i we wzroście pędów
rdestowców na poszczególnych stanowiskach wynikały prawdopodobnie ze swoistych
cech siedlisk oraz ze sposobu użytkowania terenu. Duże znaczenie odgrywają tutaj
warunki świetlne. Zauważono, że gatunki z rodzaju Fallopia – zwłaszcza Fallopia
japonica i Fallopia × bohemica preferują obszary silnie nasłonecznione. Szybkiemu
wzrostowi łodyg rdestowców w pierwszych tygodniach wegetacji sprzyja także
regularne usuwanie zalegającej ściółki. Nowe, rozwijające się rośliny pośród gęstwiny
zeszłorocznych pędów mają gorszy dostęp do światła oraz ograniczone możliwości
szybkiego wykiełkowania spod opadłych jesienią liści. Zarośla rdestowców
zlokalizowane na terenach zieleni miejskiej lub przy obiektach użyteczności publicznej
są często koszone, co ogranicza wzrost rdestowców na tych stanowiskach.
Obecność wysokich stężeń metali ciężkich jest bezpośrednim czynnikiem
ograniczającym kolonizację terenów bogatych w metale [Ernest 1999; Schwartz i in.
108
2001 cyt. za: Siwek 2008a]. Zanieczyszczenie gleb metalami ciężkimi to także jedna ze
znamiennych cech ekosystemów miejskich. Głównymi źródłami metali ciężkich
w środowisku miejskim są różne gałęzie przemysłu, energetyka, komunikacja, a także
gospodarka komunalna. Do znacznego zanieczyszczenia gleb metalami dochodzi
wzdłuż szlaków komunikacyjnych; odnosi się to przede wszystkim do ołowiu, cynku,
kadmu i chromu [Gorlach i Gambuś 2000]. Do częstych zanieczyszczeń należy także
miedź. Wyniki doświadczenia wazonowego wskazują na wysoką zdolność Fallopia
japonica i Fallopia × bohemica do regeneracji z pędów podziemnych w warunkach
stresu jonowego związanego z obecnością w glebie wysokich koncentracji metali
ciężkich. W pierwszym etapie eksperymentu, w którym testowano reakcje rdestowca
japońskiego na toksyczne działanie pięciu metali ciężkich (Cd, Cr, Cu, Pb i Zn)
największą regenerację (100%) kłączy wykazano w wazonach z dodatkiem 20, 100
i 200 mg Cd ·kg-1 oraz 10, 20, 100 mg Cr·kg-1. Nieco mniejszą zdolność do regeneracji
miały kłącza w glebie z dodatkiem 100, 200, 300 mg Cu ·kg-1 oraz 100, 200, 300 mg Zn
·kg-1.
Najmniej
podziemnych
pędów
(75%)
zregenerowało
w
wazonach
zanieczyszczonych przez 50, 100 i 200 mg Pb ·kg-1. W drugiej części doświadczenia
wazonowego badano reakcje wszystkich trzech gatunków rdestowców na kadm (200
mg·kg-1) i chrom (100 mg·kg-1). Badania wykazały tu niższą w porównaniu
z pozostałymi gatunkami zdolność regeneracyjną rdestowca sachalińskiego. Natomiast
regeneracja rdestowców japońskiego i pośredniego we wszystkich wazonach wyniosła
100%.
Rośliny wyższe wykształciły dwie strategie umożliwiające im bytowanie
w glebach z wysokimi koncentracjami metali ciężkich: strategię unikania metali
ciężkich (ang. avoidance) oraz strategię tolerancji metali ciężkich (ang. tolerance)
[Cumming i Tomsett 1992; Punz i Sieghardt 1993; Hall 2002]. Pierwsza z nich
występuje na poziomie komórkowym lub może dotyczyć całego organizmu. Oparta jest
na mechanizmach umożliwiających ograniczenie pobierania toksycznych metali ze
środowiska glebowego lub ich eliminacje [Punz i Sieghardt 1993]. O prawdopodobnych
mechanizmach wykluczania lub ograniczania pobierania ołowiu z gleby przez
inwazyjny Solidago canadensis informują Yang i in. [2007]. Autorzy porównali reakcje
Solidago canadensis na ołów z dwoma innymi, nieinwazyjnymi gatunkami (Festuca
arundinacea i Kummerowia striata). Rośliny hodowano w glebie z dodatkiem 300 i 600
mg Pb ·kg-1. Badania wykazały wysoką zawartość ołowiu w korzeniach Solidago
canadensis w porównaniu z pozostałymi gatunkami. Pomimo wysokich dawek ołowiu
109
w glebie pędy Solidago canadensis wykazywały duży przyrost biomasy oraz
intensywne pobieranie składników pokarmowych.
Tolerancja roślin na metale ciężkie jest wynikiem ewolucji na poziomie
genetycznym, fizjologicznym lub ekologicznym, która zachodzi na glebach naturalnie
wzbogaconych w metale ciężkie [Ernest 2006], choć jak podają [Hall 2002 i Ernest
2006] w niektórych przypadkach wykształcenie tolerancji na glebach antropogenicznie
zanieczyszczonych metalami ciężkimi jest także możliwe. Rośliny o wysokiej tolerancji
na metale ciężkie mogą gromadzić toksyczne pierwiastki z jednoczesnym ich
neutralizowaniem, zapewniając tym samym ochronę procesów metabolicznych oraz
błon biologicznych przed uszkodzeniami [Siwek 2008a]. Tolerancja Polygonum
cuspidatum (Fallopia japonica) na miedź była badana przez Kubota i in. [1988].
Analizy chemiczne wykazały obecność w korzeniach i kłączach rdestowca kompleksów
białkowych wchodzących w reakcje z jonami miedzi. Co więcej, poziom tych
kompleksów wzrastał wraz ze wzrostem stężenie metalu w cytoplazmie. Obecność
w cytozolu kompleksów białkowych łączących się z metalami ciężkimi jest ważnym
mechanizmem detoksykacji i tolerancji roślin na metale ciężkie [Hall 2002].
Akumulacja metali ciężkich w roślinach zależy od właściwości gleby, mobilności
metalu
oraz
od
gatunku/ekotypu
[Siwek
2008b].
W
zależności
od
ilości
akumulowanego metalu i miejsca akumulacji wyróżniono trzy grupy roślin: 1. Rośliny
akumulujące metale ciężkie w korzeniach i ograniczające ich transport do części
nadziemnych (ang. excluders) [Punz i Sieghardt 1993]. 2. Rośliny akumulujące metale
ciężkie w ilościach odzwierciedlających zawartość metalu w glebie (ang. indicators)
[Punz i Sieghardt 1993; Memon i in. 2001]. 3. Rośliny akumulujące znaczne ilości
metali ciężkich w częściach nadziemnych, zwłaszcza w liściach (ang. accumulators)
[Punz i Sieghardt 1993], które utrzymują niskie zawartości metali w cytoplazmie dzięki
obecności mechanizmów detoksykacyjnych [Siwek 2008a]. Akumulacja metali ciężkich
(Cu, Cd i Zn) w tkankach Polygonum cuspidatum (Fallopia japonica) została zbadana
przez Nishizono i in. [1989]. Autorzy porównywali zawartość metali ciężkich
w roślinach pobranych z zanieczyszczonych i niezanieczyszczonych przez metale
ciężkie gleb. W obu przypadkach większość metali ciężkich była akumulowana
w korzeniach, przy czym w największych ilościach gromadzona była miedź.
We własnych doświadczeniach wazonowych do pierwiastków kumulowanych
w kłączach i korzeniach rdestowców należał chrom, miedź oraz ołów. Zawartość metali
ciężkich w tkankach roślin wielokrotnie przewyższała ich stężenia naturalne.
110
Średnia zawartość Cr w podziemnych pędach roślin hodowanych w wazonach
zanieczyszczonych 100 mg Cr ·kg-1 wyniosła: 39,65 mg·kg-1 – Fallopia sachalinensis,
13,23 mg·kg-1 – Fallopia × bohemica i 10,78 mg·kg-1 – Fallopia japonica, natomiast w
liściach kształtowała się następująco: 5,47 mg·kg-1 w przypadku rdestowca
sachalińskiego, 5,92 mg·kg-1 u rdestowca pośredniego oraz 7,07 mg·kg-1 u rdestowca
japońskiego. Chrom jest pierwiastkiem słabo pobieranym przez rośliny. Według Allena
[1989] naturalna koncentracja Cr w tkankach roślin kształtuje się w przedziale od 0,05
do 0,50 µg·g-1 (mg·kg-1). Porównując dane literaturowe, całkowita zawartość chromu w
tkankach roślin może kształtować się w przedziale od 0,20 do 0,30 mg·kg-1 (np. Citrus
sinensis) oraz od 10,20 do 14,80 mg·kg-1 (np.Triticum spp) [Samantaray i in. 1998].
Natomiast Kabata-Pendias i Pendias [1999] podają, że zawartość tego pierwiastka
w pędach roślin na poziomie 5,0 mg·kg-1 jest szkodliwa dla większości gatunków. Jak
dotąd, stwierdzono, że niewiele gatunków roślin gromadzi znaczne ilości Cr. Jako
dobrego akumulatora Cr uważa się Polygonum hydropiperoides [Qiu i in. 1999 cyt. za:
Mei i in. 2002].
Rośliny hodowane w wazonach z dodatkiem 200 mg Pb ·kg-1 zgromadziły średnio
28,5 mg Pb ·kg-1 w korzeniach i kłączach oraz 8,6 mg Pb ·kg-1 w liściach. Jak podaje
Konstantinou i Babalonas [1996] naturalna zawartość ołowiu waha się w przedziale od
0,05–3,0 µg·g-1 [mg·kg-1]. Koncentracja w tkankach roślin powyżej 30 mg Pb ·kg-1 sm
jest toksyczna dla roślin [Kabata-Pendias i Pendias 1999]. Pomimo to, niektóre gatunki
roślin mogą kumulować znaczne ilości ołowiu. Przykładem jest pleszczotka górska
(Biscutella laevigata). Gatunek ten występuje na glebach o podwyższonej zawartości
metali ciężkich, między innymi w Tatrach oraz na hałdach galmanowych w okolicach
Olkusza, gdzie zawartość Pb dochodzi do 1500 mg Pb ·kg-1 sm gleby [Godzik 1991].
Badania wykazały, że populacja hałdowa Biscutella laevigata kumuluje od 1 do nawet
420 µg Pb ·g-1 (mg·kg-1) [Godzik 1991].
Według Burkhead i in. [2009] zawartość Cu w roślinach waha się w przedziale
od 2 do 50 µg·g-1 (mg·kg-1). Metal ten jest głównie gromadzony w korzeniach. Średnie
zawartość Cu w tkankach rdestowca japońskiego z wazonów, do których zaaplikowano
300 mg Cu ·kg-1wyniosły: 112,8 mg·kg-1 – kłącza i korzenie oraz 48,5 mg·kg-1 – liście.
Znanych jest niewiele gatunków gromadzących znaczne ilości miedzi. Najwyższe
odnotowane zawartości tego pierwiastka dochodziły do 6000 mg·kg-1 w pędach
[Burkhead i in. 2009].
111
Badania wykazały zdolności rdestowców do akumulowania w częściach
nadziemnych kadmu oraz cynku. Najwięcej kadmu – 1761,8 mg·kg-1 stwierdzono w
liściach rdestowca japońskiego hodowanego w glebie, zanieczyszczonej przez 200
mg·kg-1
tego
sachalińskiego
pierwiastka
zawierały
(II
średnio
doświadczenie
1068,0
wazonowe).
mg·kg-1, a
Liście
rdestowca
rdestowca
pośredniego
-1
547,8 mg·kg . Dla porównania, wspomniane już wcześniej populacje pleszczotki
górskiej występujące w podłożu zwierającym 180 mgCd ·kg-1 zawierały od 0,4 do 26,0
µg·g-1 (mg·kg-1) [Godzik 1991]. Przytoczone wynik badań wskazują na duże
właściwości rdestowców do akumulacji Cd. Kadm należy on do pierwiastków łatwo
pobieranych przez rośliny, na ogół akumulowany jest w korzeniach [Kabata-Pendias
i Pendias 1999]. Naturalna zawartość Cd w roślinach kształtuje się zaledwie w zakresie
od 0,01 do 0,30 µg·g-1 (mg·kg-1) [Allen 1989]. Natomiast rośliny gromadzące
w tkankach organów nadziemnych więcej niż więcej niż 100 mg Cd ·kg-1 uważane są za
hiperakumulatory (ang. hyperaccumulators) [Brooks 1989 cyt. za: Kirkham 2006].
Hiperakumulacja jest procesem powstałym na drodze ewolucji, prawdopodobnie
poprzez presję selekcyjną i wykształcenie u roślin mechanizmów adaptacji [Siwek
2008b]. Potencjalne zdolności roślin do gromadzenia metali ciężkich można indukować
w warunkach laboratoryjnych, o czym infomuje Siwek [2008a], powołując się na
badania Mesjasz–Przybyłowicz i in. [2004] oraz Pielichowskiej i Wierzbickiej [2004].
W pierwszym doświadczeniu szklarniowym stwierdzono także zdolności Fallopia
japonica do gromadzenia Zn. Średnie stężenia tego metalu w liściach rdestowca
japońskiego rosnącego na glebie z dodatkiem 300 mg Zn ·kg-1 wyniosło 2509,0 mg·
kg-1. Normalna zawartość tego pierwiastka w roślinach kształtuje się – według Allena
[1989] w przedziale od 15 do 100 µg·g-1 (mg·kg-1). Hiperalumulatory gromadzą
w częściach nadziemnych więcej niż 10000 ppm (mg·kg-1) cynku [Baker i Brooks 1989;
Brooks 1998 cyt. za: Brej i Fabiszewski 2006]. Do roślin gromadzących znaczne ilości
cynku należy pleszczotka górska. Populacje tego gatunku mogą zgromadzić nawet do
2800,0 µg·g-1 (mg·kg-1) [Godzik 1991]. Cynk i kadm to pierwiastki podobne pod
względem chemicznym, dlatego rośliny akumulujące Zn gromadzą często duże ilości
Cd [Kirkham 2006]. Na przykład, Thlaspi caerulescens i Thlaspi praecox znane jako
hiperakumulatory Zn kumulują także znaczne ilości kadmu [Rascio i Navari–Izzo
2011].
Do symptomów związanych z toksycznym działeniem metali ciężkich na rośliny
należą: zahamowanie wzrostu, chlorozy i nekrozy liści, czerwone i purpurowe
112
przebarwienia liści, brunatne brzegi liści, spadek liczby liści, przedwczesne starzenie
[Kabata-Pendias i Pendias 1999].
Podczas
eksperymentów
szklarniowych
wymienione
wyżej
objawy
obserwowano wśród roślin hodowanych w wazonach z dodatkiem Cd, Cu oraz Zn.
W przypadku testowanych dawek Cr i Pb nie stwierdzono żadnego z wyżej
wymienionych symptomów. Pędy rdestowców w wazonach z dodatkiem Cd (20 ,100
mg·kg-1 – I doświadczenie wazonowe, 200 mg·kg-1 – I i II doświadczenie wazonowe),
Cu (100, 200, 300 mg·kg-1) oraz Zn (100, 200, 300 mg·kg-1) miały mniejszą
w porównaniu z kontrolą intensywność wzrostu. W wariancie z 200 mg Cd ·kg-1
nastąpiło zahamowanie wzrostu u wszystkich gatunków. Analiza morfologiczna
rdestowców z doświadczeń wazonowych potwierdziła negatywne oddziaływanie Cd,
Cu i Zn na wzrost pędów oraz rozmiary liści (długość i szerokości blaszki liściowej).
Zanotowano także znaczne spadki świeżej i suchej masy pędów. W II doświadczeniu
szklarniowym największy ubytek masy stwierdzono u rdestowca sachalińskiego.
Zmiany na liściach w postaci chloroz oraz czerwono– purpurowych przebarwienia
pojawiły się wśród roślin hodowanych w glebie zanieczyszczonej przez Cd (20, 100,
200 mg·kg-1 – I i 200 mg·kg-1 – II doświadczenie wazonowe), Cu (200 i 300 mg·kg-1)
oraz Zn (100, 200 i 300 mg ·kg-1). Niewielkie purpurowo–czerwone przebarwienia liści
wystąpiły u rdestowca sachalińskiego rosnącego na glebie z dodatkiem 100 mg Cr ·kg-1.
W wazonach z najwyższymi dawkami Cd i Zn obserwowano zasychanie i obumieranie
pędów Fallopia japonica.
W literaturze zagranicznej rozważano wykorzystanie rdestowców, a zwłaszcza
rdestowca sachalińskiego do oczyszczanie gleb z metali ciężkich [Sukopp i Starfinger
1995]. Alberternst i Böhmer [2006] podają, że badania nad zastosowaniem Fallopia
sachalinensis do fitoremediacji prowadzono między innymi w Niemczech i Czech.
Należy pamiętać, że przedstawiciele z rodzaju Fallopia to gatunki silnie inwazyjne
stwarzające
współcześnie
poważne
zagrożenie
dla
bioróżnorodności
flory
poszczególnych regionów. Wyróżnia je szeroka amplituda ekologiczne, szybkie
dostosowywanie się do zmieniających warunków środowiska oraz wysokie zdolności
do regeneracji.
Nawet niewielki fragment kłącza rdestowców może być początkiem nowej,
niekontrolowanej pod względem rozmiaru inwazji biologicznej, tak, więc należy
przestrzec przed próbami zastosowania rdestowców do fitoremediacji.
113
9. PODSUMOWANIE WYNIKÓW BADAŃ I WNIOSKI
Przeprowadzone badania terenowe i laboratoryjne pozwalają na następujące
stwierdzenia:
1.
Podczas prac terenowych wykonanych w latach 2009–2011 we Wrocławiu
odnotowano 310 skupień rdestowców, reprezentujących trzy różne taksony
(Fallopia japonica, Fallopia × bohemica i Fallopia sachalinensis), zajmujących
powierzchnię 1,1343 ha. Najwięcej agregacji zlokalizowano w zabudowanych
częściach miasta. Na obszarach zieleni miejskiej oraz na terenach użytkowanych
jako ogródki działkowe, chwasty z rodzaju Fallopia występowały bardzo rzadko.
2.
Spośród trzech gatunków badanych rdestowców na terenie miasta najliczniej
reprezentowany jest rdestowiec japoński, który stanowi ponad 73,2% notowanych
skupisk. Najwięcej kęp Fallopia japonica zlokalizowano na obszarach zabudowy
mieszkaniowej, terenach niezagospodarowanych oraz nad brzegami rzek i rowów
melioracyjnych, gdzie stwierdzono największe pod względem powierzchniowym
skupiska tego gatunku. Drugi z rdestowców – rdestowiec sachaliński (Fallopia
sachalinensis) występuje sporadycznie, obejmując zaledwie 5,2% ogółu skupisk
rdestowców. Najczęściej spotykany jest on na terenach niezagospodarowanych
oraz w pobliżu cieków wodnych.
3.
Pomimo niewielkiej liczby stanowisk Fallopia sachalinensis – jako donora pyłku
dla wyłącznie żeńskich klonów Fallopia japonica, okazy międzygatunkowego
mieszańca – Fallopia × bohemica występują na terenie badań stosunkowo często,
stanowiąc 21,6% ogółu skupisk rdestowców. Najwięcej agregacji rdestowca
pośredniego odnotowano na terenach niezagospodarowanych (w sąsiedztwie
dzikich śmietnisk, zwałowisk i gruzowisk). Sugeruje to, iż ekspansja Fallopia
× bohemica we Wrocławiu odbywa się głównie drogą wegetatywną, a działalność
człowieka proteguje rozprzestrzenianie się mieszańca.
114
4.
We Wrocławiu zidentyfikowano jedynie żeńskie okazy Fallopia japonica. Na
podstawie wyników analiz wybranych cech morfologicznych liści rdestowca
japońskiego – zbieżnych z danymi uzyskanymi przez badaczy z innych krajów
europejskich – potwierdzono, wysuniętą przez naukowców brytyjskich, hipotezę
o obecności na terenie Europy wyłącznie żeńskiego, i prawdopodobnie
genetycznie niezróżnicowanego, klonu Fallopia japonica. Natomiast badane w
obszarze Wrocławia okazy rdestowca pośredniego (Fallopia × bohemica)
wytwarzały kwiaty żeńskie lub obupłciowe, a pod względem liczby chromosomów
okazały się heksaploidalne (2n=66). Obecność na terenie miasta heksaploidalnych
okazów
rdestowca
pośredniego
zmniejsza
ryzyko
powstawania
nowych
mieszańców w obrębie rodzaju Fallopia, gdyż według badaczy zdolne do dalszego
rozwoju nasiona wytwarzają głównie tetra i oktoploidalne klony tego gatunku.
5.
Analizy chemiczne gleby z obszaru Wrocławia wykazały, że rdestowce porastają
siedliska o szerokim zakresie odczynu: od kwaśnego do zasadowego. Ponadto,
gleby te charakteryzują się bardzo wysoką zawartością przyswajalnych form P, K
i Mg oraz Corg i Nog. W materiale glebowym stwierdzono wyższe w porównaniu
z naturalnymi zawartości kadmu, chromu, miedzi, ołowiu oraz cynku. Najwyższy
poziom koncentracji stwierdzono dla cynku i ołówu, których średnie zawartości
kształtowały się od 448,8 mg Zn ·kg-1 i 216,3 mg Pb ·kg-1 (stanowiska Fallopia
× bohemica), do 413,7 mg Zn ·kg-1 i 105,9 mg Pb ·kg-1 (stanowiska Fallopia
japonica) oraz 237,7 mg Zn ·kg-1 i 45,1 mg Pb · kg-1 (stanowiska Fallopia
sachalinensis). Zawartości cynku i ołowiu w większości badanych prób
przekraczały stężenia dopuszczalne określone dla gleb obszarów zabudowanych
i zurbanizowanych.
6.
Istotny wpływ na rozprzestrzenianie się i wzorzec rozmieszczenia chwastów
z rodzaju Fallopia w mieście może mieć zjawisko tzw. miejskiej wyspy ciepła.
Rdestowce, a zwłaszcza rdestowiec japoński i pośredni – pomimo szerokiej
amplitudy termicznej, wykazują preferencje do cieplejszych rejonów Wrocławia.
W
najzimniejszych
obszarach
Wrocławia
nie
stwierdzono
obecności
przedstawicieli z rodzaju Fallopia, co potwierdzają dane klimatyczne z okresu
wegetacji.
115
7.
Stwierdzone różnice w przebiegu faz rozwojowych oraz we wzroście pędów
rdestowców na poszczególnych stanowiskach we Wrocławiu wynikały ze
swoistych cech siedlisk (nasłonecznienie, warunki glebowe) oraz ze sposobu
użytkowania terenu. I tak np. zarośla rdestowców zlokalizowane na terenach
zieleni miejskiej lub przy obiektach użyteczności publicznej są często koszone, co
ogranicza wzrost i zagęszczanie się kęp na tych stanowiskach, wpływając tym
samym na przebieg zjawisk fenologicznych u badanych roślin.
8.
Wyniki doświadczenia wskazują na wysoką zdolność Fallopia japonica
i
Fallopia
×
bohemica
do
regeneracji
z
pędów
podziemnych
w warunkach stresu jonowego, związanego z obecnością w glebie wysokich
koncentracji metali ciężkich. Dawki 200 mg Cd ·kg-1, jak też 100 mg Cr ·kg-1 nie
zahamowały w żadnym stopniu możliwości regeneracji rdestowca pośredniego
i
japońskiego
z
ich
części
podziemnych.
Niższą
w
porównaniu
z pozostałymi gatunkami regenerację stwierdzono u rdestowca sachalińskiego.
9.
Do pierwiastków kumulowanych w częściach podziemnych rdestowców należał
chrom, miedź i ołów. Natomiast kadm i cynk gromadzone były głównie
w nadziemnych częściach roślin. Zawartość metali ciężkich w tkankach
rdestowców wielokrotnie przewyższała stężenia naturalne.
10.
Stwierdzone duże zdolności badanych gatunków do kumulacji w pędach
nadziemnych cynku (563,5 mg Zn·kg-1 – Fallopia japonica) oraz kadmu (547,8 mg
Cd ·kg-1 – Fallopia × bohemica, 1068,0 mg Cd ·kg-1 – Fallopia sachalinensis oraz
1761,8 mg Cd ·kg-1 – Fallopia japonica) wskazują, iż wszystkie badane gatunki
rdestowców można uznać za potencjalne akumulatory wymienionych metali
ciężkich.
To
jedyna
ich
pozytywna
rola
w
środowisku
miejskim.
Ten interesujący wniosek wymaga jednak dalszych badań.
116
11.
Środowisko miejskie sprzyja rozprzestrzenianiu się gatunków z rodzaju Fallopia.
Rdestowce wykazują właściwości odpowiadające gatunkom urbanofilnym.
Preferują centralne, silnie przekształcone rejony miasta o podwyższonej
temperaturze powietrza. Tolerują także lokalne zanieczyszczenia środowiska.
Zwłaszcza obecność metali ciężkich w glebie nie ogranicza ekspansji tych
gatunków, a wprost przeciwnie – czyni je silnymi konkurentami wobec innych
gatunków, unikających wyższych koncentracji metali ciężkich, szczególnie
toksycznych (np. kadmu).
12.
Wrocław jako dynamiczna, stale rozwijająca się aglomeracja jest szczególnie
narażony na inwazję rdestowców. Niepokój powinna budzić wzrastająca liczba
stanowisk rdestowców, związana między innymi z rozbudową sieci szlaków
komunikacyjnych oraz wysokie ryzyko transportu kłączy podczas prowadzenia
prac budowlanych w zakresie infrastruktury miejskiej.
117
10. LITERATURA
1.
ADACHI N., TERASHIMA I., TAKAHASHI M. 1996.
Central die–back of monoclonal
stands of Reynoutria japonica in an early stage of primary succession on
Mount Fuji. Annals of Botany 77: 477–486.
2.
ALBERTERNST B., BŐHMER H. J.
2006. Nobanis – Invasive Alien Species Fact
Sheet – Fallopia japonica. Online Database of the North European and Baltic
Network in Invasive Alien Species – Nobanis, www.nobanis.org. (11.07.2010).
3.
ALLEN S.E.
1989. Chemical Analysis of Ecological Materials. Blackwell
Scientific Publications, 368 pp.
4.
BAILEY J.P.
1989. Cytology and breeding behaviour of gigant alien Polygonum
species in Britain. Maszynopis pracy doktorskiej, Uniwersytet w Leciester,
Wielka Brytania.
5.
BAILEY J. P., STACE C. A.
1992. Chromosome number, morphology, pairing and
DNA values of species and hybrids in the genus Fallopia (Polygonaceae).
Plant Systematics and Evolution 180: 29–52.
6.
BAILEY, J.P.
1994. The reproductive biology and fertility of Fallopia japonica
(Japanese Knotweed) and its hybrids in the British Isles. [In:] Waal L.C., Child
L.E., Wade P.M. and Brock J.H. (eds). Ecology and Management of Invasive
Riparian Plants, John Wiley and Sons. Chichester, p.141–158.
7.
BAILEY J.P., CHILD L.E., CONOLLY A.
1996. A survey and dystribution of
Fallopia x bohemica (Chrtek et Chrtková) J. Bailey (Polygonaceae) in the
British Isles. Watsonia 21: 187–198.
8.
BAILEY J. P., CONOLLY A. P.
2000. Prize–winners to pariahs – A history of
Japanese Knotweed s.l. (Polygonaceae) in the British Isles. Watsonia 23: 93–
110.
9.
BAILEY, J. P.
2001. Fallopia × conollyana The Railway–yard Knotweed.
Watsonia 23: 539–541.
10.
BAILEY J.
2003. Japanese Knotwees s.l. at home and abroad. [In:] Child L.,
Brock J. H., Brundu G., Prach K., Pyšek P., Wade P.M., Williamson M. (eds).
Plant Invasions: Ecological Threats and Management Solutions, p. 183–196.
11.
BAILEY J. P., WISSKIRCHEN R.
2006. The distribution and ogius of Fallopia x
bohemica in Europe. Nordic Journal of Botany 24: 173–200.
118
12.
BAILEY J. P., BIMOVÁ K., MANDÁK B.
2007. The potential role of polyploidy and
hybridisation in the further evolution of the highly invasive Fallopia taxa in
Europe. Ecological Research 22: 920–928.
13.
BAILEY J. P., BIMOVÁ K., MANDÁK
B. 2008. Asexual spread versus sexual
reproduction and evolution in Japanese Knotweed s.l. sets the stage of “Battle
of the Clones”. Biological Invasions 11: 1189–1203.
14.
BAILEY J.
2010. Opening Pandora's seed packet. The Horticulturist 19(2): 21–
24.
15.
BARNEY J. N., THARAYIL N., DI TOMMASO A. BHOWMIK P.C.
2006. The biology of
invasive alien plants in Canada. 5. Polygonum cuspidatum Sieb. & Zucc.
[=Fallopia japonica (Houtt.) Ronse Decr.]. Canadian Journal of Plant Science
86: 887–905.
16.
BAUER M.
1994. Verbreitung neophytischer Knötericharten an Fließgewässern
in Baden-Württemberg. [In:] Böcker R., Gebhardt H, Konold W., Schmidt–
fischer S. (eds). Gebietsfremde Pflanzenarten. Auswirkungen auf einheimische
Arten, Lebensgemeinschaften und Biotope. Kontrollmöglichkeiten und
Management, Landsberg, p. 105–111.
17.
BEERLING D.J.1993.
The impact of temperature on the northern distribution
limits of the incroduced species Fallopia japonica and Impatiens glandulifera
in north–west Europe. Journal of Biogeography 20:45–53.
18.
BEERLING D.J., BAILEY J.P., CONOLLY A.P.
1994. Fallopia japonica (Houtt.)
Ronse Decraene (Reynoutria japonica Houtt.; Polygonum cuspidatum Sieb.
and Zucc.). Journal of Ecology 82: 9599–79.
19.
BEERLING D.J., HUNTLEY B., BAILEY J.P.
1995. Climate and the distribution of
Fallopia japonica: use of an introduced species to test the predictive capacity
of response surfaces. Journal of Vegetation Science 6: 2692– 82.
20.
BIMOVÁ K., MANDÁK B., PYŠEK P.
2001. Experimental control of Reynoutria
congeners: a comparative study of a hybryd and its parents.[In:] Brundu G.,
Brock J., Camarda I., Child L., Wade M. (eds). Plant Invasions: Species
Ecology and Ecosystem Management, Backhuys Publisher, Leiden, The
Netherlands, p. 283–290
21.
BIMOVÁ K., MANDÁK B., PYŠEK P.
2003. Experimental study of vegetative
regeneration in four invasive Reynoutria taxa (Polygonaceae). Plant Ecology
166: 11–1.
119
22.
BIMOVÁ K., MANDÁK B., KASPAROVA
2004. How does Reynoutria invasion fit
the various theories of invasibility? Journal of Vegetation Science 15: 495–
504.
23.
BRADLEY B.A., BLUMENTHAL D.M., WILCOVE D.S. ZISKA L.H.
2010. Predicting
plant invasions in an era of global change. Trends in Ecology and Evolution
25: 310–318.
24.
BREJ T., FABISZEWSKI J.
2006. Plants accumulating heavy metals in the Sudety
Mts. Acta Societatis Botanicorum Poloniae 75: 61–68.
25.
BROCK J. H.
1994. Technical note: standing crop of Fallopia japonica in the
autumn of 1991 in the United Kingdom. Preslia 66: 337–343.
26.
BROCK J. H., CHILD L. E., WAAL L. C., WADE M.
1995. The invasive nature of
Fallopia japonica is enhanced by vegetative regeneration from stem tissues.
[In:] Pyšek P., Prach K., Rejmánek M., Wade M. (eds). Plant Invasions:
General Aspect and Special Problems. Academic Publishing, (Amsterdam), p.
131–139.
27.
BURKHEAD J. L., GOGOLIN REYNOLDS K. A., ABDEL-GHANY S. E., COHU C. M. AND
PILON M.
2009. Copper homeostasis in plant cells. New Phytologist 182 (4):
799– 816.
28.
CHILD L., WAAL.
1997. The use of GIS in the management of Fallopia japonica
in the urban environment. [In:] Brock J.H., Wade M., Pyšek P, Greek D.(eds).
Plant Invasions:Studies from North America and Europe. Backhuys Publishers,
Leiden, The Netherlands, p. 207–220.
29.
CHILD L., WADE M.
2000. The Japanese Knotweed Manual– The Management
and Control of an Invasive Alien Weed. Packard Publishing Limited,
Chichester, UK, 123 pp.
30.
CONOLLY A.P.
1977. The distribution and history in the British Isles some alien
species of Polygonum and Reynoutria. Watsonia 11: 291–311.
31.
CRUTZEN P. J.
2004. New directions: the growing urban heat and pollution
“island” effect – impact on chemistry and climate. Atmospheric Environment
38 (21): 3539–3540.
32.
CUMMING J.R., TOMSETT A. B.
1992. Metal tolerance in plants: Signal
transduction and acclimation mechanisms. [In:] Adriano D. C. (ed.)
Biogeochemistry of trace Metals. Lewis Publishers, p. 329–364.
120
33.
DAVIS M., A., GRIME P., J., THOMSON K.
2000. Fluctuating resources in plant
communities: a general theory of invasibility. Journal of Ecology, 88: 528–534.
34.
Di CASTRI F.
1990. On invading species and invaded ecosystems: the interplay
of historical chance and biological necessity. [In:] Di Castri F., Hansen A. J.,
Debussche M. (eds).Biological Invasions in Europe and the Mediterranean
Basin. Kluwer Academy Publishere, p. 3– 16.
35.
DRZENIECKA-OSIADACZ A., KRYZA M., SZYMANOWSKI M.
2010. Klimat
Wrocławia. [In:] Lewicki Z. (ed.) Środowisko Wrocławia – Informator 2010.
Lemitor, Wrocław, p. 25– 38.
36.
DUBICKI A., DĘBICKA M., SZYMANOWSKI M.
2002. Klimat Wrocławia. [In:]
Smolnicki K., Szykasiuk M. (eds) Środowisko Wrocławia – Informator 2002.
Dolnośląska Fundacja Ekorozwoju, Wrocław, p. 9– 25.
37.
ELLSTRAND N. C.
2009. Evolution of invasiveness in plants following
hybridization. Biological Invasions 11: 1089– 1091.
38.
ERNST W. H. O.
2006. Evolution of metal tolerance in higher plants. Forest
Snow and Landscape Research 80(3): 251–274.
39.
EUROPEJSKA BAZA DANYCH O GATUNKACH OBCYCH
(Delivering Alien Invasive
Species In Europe) (http://www.europe–aliens.org (11.11.2011).
40.
FABISZEWSKI J., BREJ T.
2005. Agresywni przedstawiciele kenofitów w
Karkonoszach. Annales Silesiae 34: 115– 120.
41.
FABISZEWSKI J., BREJ T.
2007. Agresywni przedstawiciele kenofitów w
Karkonoszach. Cz. II. Inwazje na tle odmiennych siedlisk. Annales Silesiae 35:
97–103.
42.
FALIŃSKI J. B.
2004. Inwazje w świecie roślin: mechanizmy, zagrożenia, projekt
badań. Phytocoenosis 11 (N.S.), Seminarium Geobotanicum 10: 1– 32.
43.
FOJCIK B., TOKARSKA-GUZIK B.
2000. Reynoutria x bohemica (Polygonaceae)–
nowy takson we florze Polski. Fragmenta Floristica et Geobotanica Polonica 7:
63– 71.
44.
„GATUNKI
OBCE
W
POLSCE”.
INSTYTUT
OCHRONY
ŚRODOWISKA
PAN.
http://www.iop.krakow.pl/ias/Default.aspx. (11.11.2011).
45.
GAMMON M.A., KESSELI R.
2010. Haplotypes of Fallopia introduced into the
US. Biological Invasions 12: 421–427.
46.
GNIAZDOWSKA A.
2005. Oddziaływanie allelopatyczne – „nowa broń” roślin
inwazyjnych. Kosmos 54 (3): 221– 226.
121
47.
GODZIK B.
1991. Accumulation of heavy metals in Biscutella laevigata
(Cruciferae) as a function of their concentration in substrate. Polish Botanical
Studies 2: 241–246.
48.
GORLACH E., GAMBŚ F.
2000. Potencjalnie toksyczne pierwiastki śladowe w
glebach (nadmiar, szkodliwość i przeciwdziałanie). Zeszyty Problemowe
Postępów Nauk Rolniczych 472: 275– 296.
49.
HALL J. L.
2002. Cellular mechanisms for heavy metal detoxification and
tolerance. Journal of Experimental Botany 53: 1–11.
50.
HARTMANN E., SCHULDES U., KÜBLER R., KONOLD W.
1995. Neophyten Biologie,
Verbreitung und Kontrolle ausgewählter Arten. Ecomed – Verlag, Landsberg,
p. 79– 97.
51.
HART M.L., BAILEY J., HOLLINGSWORTH P.M., WATSON K., J.1997.
Sterile species
and fertile hybrids of Japanese knotweeds along the river Kelvin.Glasgow.
Naturalist 23: 18–22.
52.
HEGER T., TREPL L.
2003. Predicting biological invasions. Biological Invasions
5: 313– 321.
53.
HIERRO L. J., CALLAWAY R.
2003. Allelopathy and exotic plant invasion. Plant
and Soils 256: 29– 39.
54.
HOLLINGSWORTH M. L., HOLLINGSWORTH P. M., JENKINS G. I., BAILEY J. P., FERRIS
C.
1998. The use of molecular markers to study patterns of genotypie diversity
in some invasive alien Fallopia spp. (Polygonaceae). Molecular Ecology
7: 1681– 1691.
55.
HOLLINGSWORTH M. L., HOLLINGSWORTH P. M.,
FERRIS C. 1999. Chloroplast
DNA variation and hybridization between invasive populations of Japanese
knotweed and gigant knotweed (Fallopia, Polygonaceae). Botanical Journal of
the Linnean Society 129: 139– 154.
56.
HOLLINGSWORTH M. L., BAILEY J. P.
2000 Evidence for massive clonal growth in
the invasive weed Fallopia japonica (Japanese Knotweed). Botanical Journal
of the Linnean Society 133: 463– 472.
57.
JACKOWIAK
B.
1999.
Modele
ekspansji
roślin
synantropijnych
i transgenicznych. Phytocoenosis, Seminarium Geobotanicum 6: 1–24.
58.
JÄGER E.J.
1995. Die Gesamtareale von Reynoutria japonica Houtt. und R.
sachalinensis (F. Schmidt) Nakai, ihre klimatische Interpretation und Danen
122
zur Ausbreitungsgeschichte. Schr.-R. f. Vegetationskde, Sukopp-Festschrift,
Bonn-Bad Godesberg 27: 395–403.
59.
KABATA-PENDIAS A., PENDIAS P.
1999. Biogeochemia pierwiastków śladowych.
Wydawnictwo Naukowe PWN. Warszawa, 363 pp.
60.
KACPERSKA A.
2002. Reakcje roślin na abiotyczne czynniki stresowe.
[In:] Kopcewicz J., Lewak S. Fizjologia roślin. PWN Warszawa, p. 612–678.
61.
KARCZEWSKA A., KABAŁA C.
2008. Metodyka analiz laboratoryjnych gleb
i roślin. Uniwersytet Przyrodniczy we Wrocławiu, Instytut Nauk o Glebie
i Ochrony Środowiska Zakład Ochrony Środowiska
http://karnet.up.wroc.pl/~kabala/Analizy2008v4.doc (19.01.2010).
62.
KIM J. Y. C., PARK C.-W.
2000. Morphological and chromosomal variation in
Fallopia section Reynoutria (Polygonaceae) in Korea. Brittonia, 52: 34–48.
63.
KIRKHAM M. B.
2006. Cadmium in plants on polluted soils: Effects of soil
factors hyperaccumulation and amendments. Geoderma 137: 19 – 32.
64.
KNOX A.S., GAMERDINGER A.P., ADRIANO D.C., KOLKA R.K., KAPLAN D.I.
1999.
Sources and Practices Contributing to Soil Contamination. Agronomy
Monograph 37: 53–87.
65.
KONSTANTINOU M., BABALONAS D.
1996. Metal uptake by Caryophyllaceae
species from metalliferous soils in northern Greece. Plant Systematic and
Evolution 203: 1– 10.
66.
KORABIEWSKI B., LEWICKI P.
2010. Gleby Wrocławia. [In:] Lewicki Z. (ed.)
Środowisko Wrocławia – Informator 2010. Lemitor, Wrocław, p. 22–25.
67.
KORNAŚ J.
1972. Wpływ człowieka i jego gospodarki na szatę roślinną Polski,
flora synantropijna. [In:] Szafer W., Zarzycki K. (eds). Szata roślinna Polski,
tom I. PWN, Warszawa, p. 95–128.
68.
KORNAŚ J.
1990. Plants invasion in Central Europe: historical and ecological
aspects. [In:] Di Castri F., Hansen A.J., Debussche M. (eds). Biological
Invasions in Europe and the Mediterranean Basin. Kluwer Academy
Publishere, p. 19–36.
69.
KWIATKOWSKA-SZYKULSKA B., MIKOŁAJCZYK A., ŻYNIEWICZ Ś.
Powietrze. [In:]
Smolnicki K., Szykasiuk M. (eds). Środowisko Wrocławia – Informator 2002.
Dolnośląska Fundacja Ekorozwoju, Wrocław, p. 26–37.
123
70.
KOWARIK I.
1995. The role of alien species in urban flora and vegetation.[In:]
Pyšek P., Prach K., Rejmánek M., Wade M. Plant Invasions: General Aspects
and Special Problems, Academic Publishing, Amsterdam, p. 85–103.
71.
KUBOTA K., NISHIZONO H., SHIYUO S., ISHII F.
1988. A Cooper – binding proteins
in root cytoplasm of Polygonum cuspidatum growing in a metalliferous habitat.
Plant Cell Physiology 29(6): 1029–1033.
72.
KUROSE D., RENELS T., SHAW R., FURUYA N., TAKAGI M., EVANS H.
2006.
Fallopia japonica, an increasingly intractable weed problem in the UK: Can
fungi help cut through this Gordian knot? Mycologist 20: 126–129.
73.
LEE C.E.
2002. Evolutionary genetics of invasive species. Trends in Ecology
and Evolution 17(8): 386–391.
74.
MACK R. N., SIMBERLOFF D.S., LONSDALE W.M., EVANS H., CLOUT M., BAZZAZ F.A.
2000. Biotic invasions: causes, epidemiology, global consequences and control.
Ecological Applications 10: 689–710.
75.
MANDÁK B., PYŠEK P., LYSAK M., SUDA J., KRAHULCOVÁ A., BIMOVÁ K.
2003
Data Variation in DNA–ploidy Levels of Reynoutria taxa in the Czech
Republic. Annals of Botany 92(2): 265–272.
76.
MANDÁK B., PYŠEK P., BIMOVÁ K.
2004. History of the invasion and distribution
of Reynoutria taxa in the Czech Republic: a hybrid spreading faster than its
parents. Preslia 76:15–64.
77.
MANDÁK B., BIMOVÁ K., PYŠEK P., ŠTĚPÁNEK J., PLAČKOVÁ I.
2005. Isoenzyme
diversity in Reynoutria (Polygonaceae) taxa: escape from sterility by
hybridization. Plant Systematics and Evolution 253: 219–230.
78.
MARIGO G., PAUTOU G.
1998. Phenology, growth and ecophysiological
characteristics of Fallopia sachalinensis. Journal of Vegetation Science 9:
179–386.
79.
MARIKO S., KOIZUMI H., SUYUKI J., FURUKAWA A.
1993. Altitudinal variation in
germination and growth responses of Reynoutria japonica populations on Mt.
Fuji to a controlled thermal environment. Ecological Research 8: 27–34.
80.
MARUTA E.
1994. Seedling establishment of Polygonum cuspidatum and
Polygonum weyrichii var. alpinum at high altitudes of Mt Fuji. Ecological
Research 9: 205–213.
124
81.
MCDONNELL M. J., PICKETT S. T. A., GROFFMAN P., BOHLEN P., POUYAT R. V.,
ZIPPERER W. C.
1997. Ecosystem processes along an urban – to– rural gradient.
Ubran Ecosystems 1: 21–36.
82.
MCKINNEY M.
2006. Urbanization as a major couse of biotic homogenization.
Biological Conservation 127: 247 –260.
83.
MEI B., PURYEAR J. D., NEWTON R. J.
2002. Assessment of Cr tolerance and
accumulation in selected plant species. Plant and Soils 247: 223–231.
84.
MEMON A. R., AKTOPRAKLGIL D., ÖYDEMIR A.,VERTII A.
2001. Heavy metal
accumulation and detoxification mechanisms in plants. Turkish Journal of
Botany 25: 111–121.
85.
MIREK Z.
et al. 1995. Vascular Plants of Poland. A Checklist. Polish Academy
of Sciences.W. Szafer Institute of Botany, Kraków, 442 pp.
86.
NISHIZONO H., KUBOTA K., SUZUKI S., ISHII F.
1989. Accumulation of heavy
metals in cell walls of Polygonum cuspidatum roots from metalliferous
habitats. Plant and Cell Physiolgy 30(4): 595–598.
87.
PASHLEY C.H., BAILEY J.P., FERRIS C.
2007. Clonal diversity in British
populations of the alien invasive Giant Knotweed, Fallopia sachalinensis (F.
Schmidt) Ronse Decraene, in the context of European and Japanese plants.
Watsonia 26: 359–371.
88.
PIEROŃSKI Z., TARKA Z.
2010. Zasoby wodne na terenie Wrocławia. [In:]
Lewicki Z. (ed.) Środowisko Wrocławia –Informator 2010. Lemitor, Wrocław,
p. 40–46 .
89.
PIMENTEL D., PIMENTEL M., WILSON A.
2007. Plant, animal and microbe invasive
species in the United States and World. [In:] Nentwig W. (ed.) Biological
Invasions, Ecological Studies. Springer, 193: 315–330.
90.
PUNZ W.F., SIEGHARDT H.
1993.The response of roots of herbaceous plant
species to heavy metals. Environmental Botany 33 (1): 85–98.
91.
PYŠEK P.
1998. Alien and native species in Central European urban floras: a
quantitative comparison. Journal of Biogeography 24: 155–163.
92.
PYŠEK, P., J. H. BROCK, K. BÍMOVÁ, B. MANDÁK, V. JAROŠÍK, I. KOUKOLÍKOVÁ, J.
PERGL, AND J. ŠTĚPÁNEK.
2003. Vegetative regeneration in invasive Reynoutria
(Polygonaceae) taxa: the determinant of invasibility at the genotype level.
American Journal of Botany 90: 1487–1495.
125
93.
PYŠEK P., PERGL J., JAHODOVÁ Š., MORAVCOVÁ L., MÜLLEROVÁ J., PERGLOVÁ I. &
WILD J.
2010: The hogweed story: invasion of Europe by large Heracleum
species. [In:] Settele J., Penev L., Georgiev T., Grabaum R., Grobelnik V.,
Hammen V., Klotz S., Kotarac M., Kühn I. (eds). Atlas of Biodiversity Risk.
Pensoft, Sofia & Moscow, p. 150– 151.
94.
RADECKI W.
2009. Prawne aspekty ochrony przed gatunkami obcymi.
Maszynopis, 6 pp.
95.
RAPORT O STANIE ŚRODOWISKA W WOJEWÓDZTWIE DOLNOŚLĄSKIM W 2010
ROKU.
Wojewódzki Inspektorat Ochrony Środowiska
http://www.wroclaw.pios.gov.pl/index.php?id=publikacje&sub=raporty
(12.11.2010).
96.
RASCIO N., NAVARI-IZZO F.
2011. Heavy metal hyperaccumulating plants: how
and why do they do it? And what makes them so interesting? Plant Science
180: 169–81.
97.
REJMÁNEK M.
1995. What makes a species invasive? [In:] Pyšek P., Prach K.,
Rejmánek M., Wade M.(eds). Plant Invasions – General Aspects and Special
Problems,Academic Publishing, Amsterdam, p. 3–13.
98.
RICHARDS C. H. L., WALLS R.L., BAILEY J.P., PARAMESWARAN R., GEORGE T.,
PIGLIUCCI M.
2008. Plasticity in salt tolerance traits allows for invasion of novel
habitat by Japanese knotweed s. l. (Fallopia japonica and F. x bohemica,
Polygonaceae). American Journal of Botany 95: 931–942.
99.
RICHARDSON D. M., PYŠEK P., REJMÁNEK M., BARBOUR M. G., PANETTA F. D.,
WEST C. J.
2000. Naturalization and invasion of alien plants: concepts and
definitions. Diversity and Distributions 6: 93– 107.
100. RONSE DECRAENE L.-P., AKEROYD J.R. 1988. Generic limits in Polygonum and
related genera (Polygonaceae) on the basis of flora characters. Botanical
Society of the Linnean Society 98: 321– 371.
101. ROZPORZĄDZENIE MINISTRA ŚRODOWISKA Z DNIA 9 WRZESNIA 2002 ROKU W
SPRAWIE STANDARDÓW JAKOŚCI GLEBY ORAZ STANDARDÓW JAKOŚCI ZIEMI.
Dz.
U. 2002 nr 165 poz. 1359 – http://www.abc.com.pl/serwis/du/2002/1359.htm
(06.12.2011).
102. SAMANTARAY S., ROUT G. R., DAS P. 1998. Role of chromium on plant growth
and metabolism. Acta Physiologiae Plantarum 20(2): 201–212.
126
103. SCALERA R. 2010 How much is Europe spending on invasive alien species?
Biological Invasions 12: 173–177.
104. SCHNITZLER A., BAILEY J.P.,
HANSEN C.N.
2007. Genotypic and phenotypic
variation in a Fallopia x bohemica population in north–eastern France. [In:]
Tokarska-Guzik B., Brock J.H., Brundu G., Child L., Daehler C.C. & Pyšek P.
Plant Invasions: Human Perception, Ecological Impacts and Management.
Backhuys Publishers, Leiden, The Netherlands, p. 133–144.
105. SEIGER L. A. 1997. The status of Fallopia japonica (Reynoutria japonica;
Polygonum cuspidatum) in North America. [In:] Brock J. H., Wade M., Pyšek
P., Green D. Plant Invasions: Studies from North America and Europe.
Backhuys Publishers, Leiden, p. 95–102.
106. SHARMA G.P., SINGH J.S., RAGHUBANSHI A.S. 2005. Plant invasion: emerging
trends and future implications. Current Science 88: 726–734.
107. SIEMENS T., BLOSSEY B. 2007. An evaluation of mechanisms preventing growth
and survival of two native species in invasive Bohemian Knotweed (Fallopia x
bohemica, Polygonaceae). American Journal of Botany 94 (5): 776–783.
108. SIWEK M. 2008a. Rośliny w skażonym metalami ciężkimi środowisku
poprzemysłowym. Część I . Pobieranie, transport i toksyczność metali ciężkich
(śladowych). Wiadomości Botaniczne 52: 7–22.
109. SIWEK M. 2008b. Rośliny w skażonym metalami ciężkimi środowisku
poprzemysłowym.
Część
II.
Mechanizmy
detoksykacji
i
strategie
przystosowania roślin do wysokich stężeń metali ciężkich. Wiadomości
Botaniczne 52: 7–23.
110. SOLARZ W. 2007. Inwazje biologiczne jako zagrożenie dla przyrody. Postępy w
Ochronie Roślin 47(1): 128– 133.
111. SOŁTYSIAK J., BERCHOVÁ-BIMOVÁ K.,VACH M., BREJ T. 2011. Heavy metals
content in the Fallopia genus in Central European cities – Study from Wrocław
and Prague. Acta Botanica Silesiaca 7 :209–218.
112. SUKOPP H., SUKOPP U. 1988. Reynoutria japonica Houtt. in Japan und in
Europa. Veröff. Geobot. Inst. ETH, Stiftung Rübrl, Zürich, 98: 354– 372.
113. SUKOPP H., STARFINGER U. 1995. Reynoutria sachalinensis in Europe and in the
Far East: A comparison of the species' ecology in its native and adventive
distribution range. [In:] Pyšek P., Prach K., Reymánek M., Wade M. (eds).
127
Plant Invasion: General Aspects and Special Problems. SPB Academic
Publishing, Amsterdam, p. 151–159.
114. STUDNIK-WÓJCIKOWSKA B.
2002. Flora miasta–chaos i przypadek czy
prawidłowości w bioróżnorodności?. Kosmos 51: 213–219.
115. SZYMANOWSKI M. 2004. Miejska wyspa ciepła we Wrocławiu. Studia
Geograficzne. Wydawnictwo Uniwersytetu Wrocławskiego, 229 pp.
116. ŚWIATOWA BAZA DANYCH NA TEMAT GATUNKÓW INWAZYJNYCH (The global
invasive species database) – http://www.issg.org/database/welcome/
(11.11.2011).
117. TIÉBRÉ MARIE-S., BIZOUX JEAN-P., HARDY OLIVIER J., BAILEY JOHN P., MAHT
GRÉGORY.
2007a. Hybridization and Morphogenetic variation in the invasive
alien Fallopia (Polygonaceae) Complex in Belgium. American Journal of
Botany 94(11): 1900–1910.
118. TIÉBRÉ MARIE-S., VANDERHOEVEN S., SAAD L., MAHY G. 2007b. Hybridization
and sexual reproduction in the invasive alien Fallopia (Polygonaceae) complex
in Belgium. Annals of Botany 99: 193–203.
119. TOKARSKA-GUZIK B. 2002. “ Zielone Widmo” i “ Natrętny Mongoł” – czyli o
przybyszach i przybłędach we florze [In:] Nakonieczny M., Migula P. (eds).
Problemy środowiska i jego ochrony. Centrum studiów nad człowiekiem i
środowiskiem, Uniwersytet Śląski, Katowice, p. 101–127.
120. TOKARSKA-GUZIK B. 2003. The expansion of some alien plant species
(neophytes) in Poland.[In:] Child L., Brock J. H., Brundu G., Prach K., Pyšek
P., Wade P. M., Williamson M. (eds). Plant Invasions: Ecological Threats and
Management Solutions. Backhuys Publishers, Leiden, The Netherlands, p.
147–167.
121. TOKARSKA-GUZIK B. 2005. The Establishment and Spread of Alien Plant
Species (Kenophytes) in the Flora of Poland. Wydawnictwo Uniwersytetu
Śląskiego, Katowice, 192 pp.
122. VAN DER VELDE G., RAJAGOPAL S., KUYPER- KOLLENAAR M., BIJ DE VAATE A.,
THIELTGES D.W., MAC ISAAC H.J.
2006. Biological invasions: concepts to
understand and predict a global threat. [In:] Bobbink R., Beltman B.,
Verhoeven J. T. A., Whigham D. F. (eds). Wetlands: Functioning, Biodiversity
Conservation and Restoration. Ecological Studies Springer-Verlag, Berlin,
Heidelberg, 191: 61–90.
128
123. VICHOTOVÁ N., ŠERÁ B. 2008. Alleopathic properties of knotweed rhizome
extracts. Plant Soil and Environment 54: (7) 301–303.
124. VILÁ M., CORBIN J.D., DUKES J.S., PINO J., STANLEY S.D. 2007. Linking plant
invasion to global enviromental change. [In:] Canadell J. G. Pataki D. E.,
Pitelka F L. (eds). Terrestrial Ecosystems in a Changing World. Springer,
Berlin, Heidelberg, 8: 93–102.
125. VITOUSEK P. M., D’ANTONIO C. M., LOOPE L. L., REJMÁNEK M., WESTBROOKS R.
1997. Introduced species: a significant component of human–caused global
change. New Zealand Journal of Ecology 21: 1–16.
126. WAYNE P., FOSTER S., CONNOLLY J., BAZZAZ F., EPSTEIN P. 2002. Production of
allergenic pollen by ragweed (Ambrosia artemisiifolia L.) is increased in CO2 –
enriched atmospheres. Annals of Allergy, Asthmma and Immunology 8: 279–
282.
127. WESTON, L. A., BARNEY, J. N., & DITOMMASO, A. 2005. A review of the biology
and ecology of three invasive perennials in New York State: Japanese
knotweed (Polygonum cuspidatum), mugwort (Artemisia vulgaris) and pale
swallow–wort (Vincetoxicum rossicum). Plant Soil and Environment 277:
53– 69.
128. WILLIAMSON M. 1993. Invaders, weeds and risk from genetically modified
organisms. Experientia 49: 219–224.
129. WILLIAMSON M. 1996. Biological Invasions. Chapman – Hall, London, 244 pp.
130. WITTIG R. 2004. The origin and development of the urban flora of Central
Europe.Urban Ecosystems 7: 323–339.
131. YANG RU-YI, TANG JIAN-JUN, YANG YI-SONG, CHEN XIN. 2007. Invasive and
non–invasive plants differ in response to soil heavy metal lead contamination.
Botanical Studies 48: 453–458.
132. YAMAGUCHI F., NOZUE M., YASUDA H., KUBO H. 2000. Effects of temperature on
the pattern of anthocyanin accumulation in seedlings of Polygonum
cuspidatum. Journal of Plant Research 13 (1109): 71–77.
133. ZAJĄC A., ZAJĄC M., TOKARSKA-GUZIK B. 1998. Kenophytes in the flora of
Poland: list, status and origin. – Phytocoenosis, Suplementum Cartographiae
Geobotanicae Warszawa–Białowieża, 9: 107– 115.
129
134. ZHOU Z., MIWA M., NARA K., WU B., NAKAYA H., LIAN C., MIYASHITA N., OISHI R.,
MATURA E.
2003. Patch establishment and development of clonal plant,
Polygonum cuspidatum on Mount Fuji. Molecular Ecology 12: 1361–1373.
135. ZIKA P.F., JACOBSON A.L. 2003. An overlooked hybrid Japanese knotweed
(Polygonum cuspidatum x sachalinense; Polygonaceae) in North America.
Rhodora 105: 143–152.
136. ŻOŁNIERZ L., ANTCZAK M. 2005. Aktualny stan inwazji gatunków z rodzaju
Reynoutria wzdłuż lewobrzeżnych dopływów Odry w zachodniej części
Wrocławia. Annales Silesiae 34: 27–37.
137. ŻURBICKI
Z.
1974. Metodyka doświadczeń wazonowych. Państwowe
Wydawnictwo Rolnicze i Leśne, Warszawa, 402 pp.
130
11. ZAŁĄCZNIKI
131
Fot. 1. Jedno ze stanowisk Fallopia × bohemica – kępy rdestowca pośredniego
były tu regularnie wypalane, co ograniczało wzrost i rozwój roślin
Fot. 2. Zwarte agregacje Fallopia × bohemica i Fallopia japonica
132
Fot. 4. Komórki ze stożka wzrostu korzenia Fallopia × bohemica (66 chromosomów)
Fot. 5. Komórki ze stożka wzrostu korzenia Fallopia sachalinensis (44 chromosomów)
133
Kontrola
I
II
III
Fot. 6. Inhibicyjny wpływ kadmu na wzrost i rozwój Fallopia japonica
(I – 20, II – 100, III – 200 mg·kg–1)
Kontrola
I
II
III
Fot. 7. Inhibicyjny wpływ cynku na wzrost i rozwój Fallopia japonica
(I – 100, II – 200, III – 300 mg·kg–1)
134
Kontrola
I
II
III
Fot. 8. Wzrost i rozwój Fallopia japonica z dodatkiem ołowiu
(I – 50, II – 100, III – 200 mg·kg–1)
Kontrola
I
II
III
Fot. 9. Inhibicyjny wpływ miedzi na wzrost i rozwój Fallopia japonica
(I – 100, II – 200, III – 300 mg·kg–1)
135
Kontrola
I
II
III
Fot. 10. Wzrost i rozwój Fallopia japonica z dodatkiem chromu
(I – 10, II – 20, III – 100 mg·kg–1)
I
II
III
Fot. 11. Wzrost i rozwój trzech gatunków rdestowców (I – Fallopia × bohemica,
II – Fallopia japonica, III – Fallopia sachalinensis) z dodatkiem chromu (100 mg ·kg–1)
136
II
II
III
Fot. 12. Inhibicyjny wpływ kadmu (200 mg·kg–1) na wzrost i rozwój trzech gatunków rdestowców
(I – Fallopia × bohemica, II – Fallopia japonica, III – Fallopia sachalinensis)
Fot. 13. Zmiany morfologiczne liści Fallopia japonica pod wpływem kadmu (200 mg·kg–1)
137
Kontrola
Fot. 14. Zmiany morfologiczne liści Fallopia japonica pod wpływem
kadmu (200 mg·kg–1)
Kontrola
Fot. 15. Zmiany morfologiczne liści Fallopia sachalinensis pod wpływem
kadmu (200 mg·kg–1)
138
Fot. 16. Zmiany morfologiczne liści Fallopia japonica
pod wpływem cynku (300 mg·kg–1)
Fot. 17. Zmiany morfologiczne liści Fallopia sachalinensis
pod wpływem chromu (100 mg·kg–1)
139